Устройство атома. Уровни 1 и 2. Орбитали s, p, d, f. Устройство атома
Устройство атома. Уровни 1 и 2. Орбитали s, p, d, f
Этот пост — снова про устройство атома.Для того, чтобы понимать в общих чертах разные генетические штуки, слишком детально представлять себе устройство атома, конечно, не обязательно, но если ты хочешь более глубоко разобраться в межмолекулярных взаимодействиях, на которых и строится собственно вся биохимия, то без хотя бы поверхностного понимания того, как устроен атом, уже совершенно точно не обойтись.Поэтому я предлагаю тебе сначала пролистать/прочесть наши предыдущие три статьи про устройство атома, а потом пойти дальше. На самом деле это совсем несложно.
Итак, мы знаем, что первый электронный уровень любого атома выглядит очень просто. Конфигурация его может быть представлена сферой, в центре которой находится ядро, а находиться на первом уровне может максимум 2 электрона. Картинка со сферой — первая. Нет ничего проще:) По этой сфере вокруг ядра «размазан» либо один электрон, либо два, но никак не больше. Что значит «размазан»? Значит электрон можно обнаружить в любой точке этой сферы с одинаковой вероятностью.
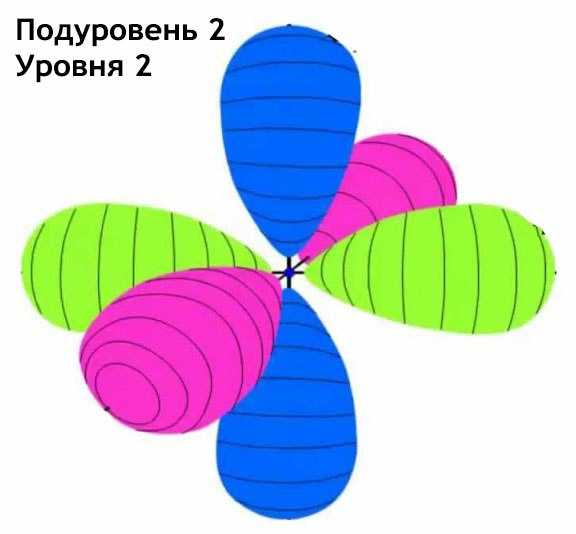
А теперь рассмотрим второй уровень. Главное, что тут нужно понять, это то, что второй уровень состоит из двух под-уровней. Первый подуровень — это такая же сфера, но побольше диаметром. А второй подуровень имеет форму трех гантелей — см. вторую картинку. При этом на каждой такой гантеле может находиться максимум 2 электрона.
Подуровень, являющийся сферой, обозначается латинской буквой «s», а подуровень, являющийся тройной гантелей, обозначается как «p». Соответственно сферический подуровень первого уровня обозначается 1s, а сферический подуровень второго уровня — 2s. Гантельный подуровень 2-го уровня обозначается как 2p.
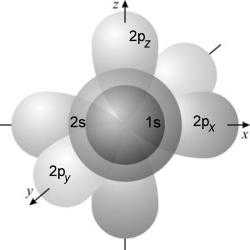
Теперь, если мы одновременно представим себе оба уровня, то понятно, что там будет три подуровня: два S-подуровня и один P-подуровень — см. третью картинку. Если мы увидим обозначение «2s», то поймем, что речь идет о сферическом подуровне второго уровня.
Рассматривая картинки с гантелями можно подумать, что есть вероятность найти электрон также и в ядре атома, но это не так — это просто недостаток таких картинок.
Как видишь, все просто. Теперь давай немного посчитаем электроны. На первом уровне — максимум два. На 2s-подуровне — тоже максимум 2. На 2p-подуровне — максимум 6 электронов, так как на каждой гантельной орбите может находиться одновременно максимум два электрона.Итак, сколько максимум электронов будет находиться на первых двух уровнях? 2+2+6=10. Десять.
Отсюда и получается, что тот атом, в ядре которого 10 протонов (и соответственно на первых двух уровнях у него будет максимум 10 электронов), будет последним из тех, кто обходится двумя уровнями. Атому с порядковым номером 11 уже не хватит двух уровней, и один из его электронов будет вынужден поместиться на третий уровень. Так что натрий (Na) с его 11 протонами в ядре — это первый химический элемент, которому двух уровней уже не хватает для размещения на них всех своих электронов.
Третий электронный уровень устроен еще сложнее, чем второй, но мы легко разберемся и в нем, потому что тут очень простая логика: если первый уровень имеет только один подуровень (1s), а второй — два подуровня (2s, 2p), то третий уровень содержит уже три подуровня: 3s, 3p и 3d.
Есть и еще одна простая закономерность: на s-подуровне размещается максимум 2 электрона, потому что s-подуровень — это лишь одна сфера. На p-подуровне размещается максимум 6 электронов, потому что p-подуровень — это уже три гантели, на каждой из которых максимально может быть 2 электрона. Соответственно на d-подуровне есть целых 5 усложненных гантелей, на каждой из которых опять-таки может поместиться максимум по 2 электрона.
Давай потренируемся и попробуем подсчитать — сколько всего может быть электронов на третьем уровне? На сфере 3s — максимум 2 электрона. На трех гантелях 3p — максимум 6. На пяти сложных траекториях 3d — максимум 10. Итого: на третьем уровне максимум может быть 2+6+10=18 электронов.
Давай еще ответим на один простой вопрос: сколько максимум может быть электронов на всех первых трех уровнях? На первом (сфера): 2. На втором (сфера + 3 гантели): 8. На третьем: 18. Итого: 2+8+18=28Всё просто.
Удобно ввести термин «ОРБИТАЛЬ», которым мы будем обозначать любую электронную конфигурацию некоторого подуровня, будь то сфера, или гантель, или что-то еще более сложное более высоких подуровней.
Термином ЭЛЕКТРОННОЕ ОБЛАКО называется общая совокупность всех орбиталей всех уровней данного атома.
Вернувшись к уровням и подуровням, мы можем заметить простую закономерность. Каждый новый уровень имеет на один подуровень больше, чем предыдущий. Можно это объяснить так, что чем дальше от ядра, тем более свободно, тем больше там пространства, и уже можно не толпиться и образовывать больше и больше разных подуровней. Так что четвертый уровень уже имеет 4 подуровня, и этот новый четвертый подуровень обозначается буквой «f». Он уже имеет 7 орбиталей.
Давай подытожим и перечислим все подуровни первых 4-х уровней:
1: s2: s, p3: s, p, d4: s, p, d, f
Теперь в скобках еще укажем количество орбиталей, каждое из которых вмещает в себя максимум 2 электрона:
1: s (1)2: s (1), p (3)3: s (1), p (3), d (5)4: s (1), p (3), d (5), f (7)
Поскольку каждая орбиталь вмещает в себя максимум 2 электрона, мы теперь можем переписать эту таблицу еще раз, в скобках уже указывая максимальное количество электронов, находящихся на данном подуровне:
1: s (2)2: s (2), p (6)3: s (2), p (6), d (10)4:s (2), p (6), d (10), f (14)
Просуммировав эти электроны, мы теперь можем очень легко написать таблицу с указанием того — сколько максимум электронов помещается на каждом уровне в атоме:
1 уровень: 2 электрона2 уровень: 8 электронов3 уровень: 18 электронов4 уровень: 32 электрона
Если мы знаем, что в каком-то атоме заполнены первые два уровня, а на более высоких уровнях электронов нет, то это значит, что в нем находится (2+8) 10 электронов, и значит в его ядре 10 протонов, а значит в периодической таблице он находится под номером 10 — это неон (Ne).
Больше всего неона во Вселенной мы сможем найти там же, где находится больше всего водорода и гелия — внутри звезд, в газовых туманностях, в атмосфере газовых гигантов типа Юпитера и Сатурна. Как и гелий, неон не вступает в химические реакции, и поэтому совершенно неинтересен ни биохимии, ни генетике.
Все электроны в атоме идентичны, если их оттуда вытащить и рассмотреть по-отдельности. Между ними нет никакой разницы, но при этом каждый электрон ведет себя несколько по-своему в зависимости от того, на каком подуровне и на какой орбитали он находится. Для того, чтобы было легче говорить про электроны в атоме, ввели добавочные простые термины: «s-электрон» — это электрон, находящийся на орбитали типа «s», «p-электрон» — это электрон, находящийся на орбитали типа «p», и так далее — это вполне логично.
Да, это большой пост, но его проще понять целиком, чем частями. В следующих постах про атомное устройство мы еще более приблизимся к пониманию того — что такое «химическая связь».

bodhi.name
Строение атома
Строение атома интересовало ученых еще задолго до того, как существование его было доказано научно. Еще тысячи лет назад Демокрит, древнегреческих философ и мудрец, высказал предположение о том, что любое вещество состоит из мельчайших частиц. И именно он первым употребил слово «атом». После его смерти возникла группа греческих философов, члены которой пытались развить его взгляды. Их называли атомистами. Все эти взгляды изложил римлянин Лукреций Кар в своем известном труде «О природе вещей». Однако в более поздние времена, вплоть до начала эпохи Возрождения, преобладали взгляды другого греческого мудреца, Аристотеля, который категорически отрицал существование атомов.
Первым, кто сделал попытку возродить учение Демокрита, был англичанин Бойль, который обосновывал свою теорию «неделимых частиц». Ему вторил Ньютон. Однако научно обосновал это учение Дальтон, учитель математики. Проводя опыты с газами, он заметил, что соотношение тех частиц водорода и кислорода, которые участвовали в химической реакции, всегда соответствует определенной пропорции. Последние, как правило, представляют собой соотношение небольших чисел. Это дало возможность английскому учителю математики сформулировать свой закон «кратных соотношений», а со временем – и закон «постоянных отношений», исходя из которого, в каждом химическом соединении соотношение масс исходных веществ всегда одинаковое. Его исследования были продолжены Берцеллиусом и Авогадро.
То, что строение атома достаточно сложное, было доказано физиками еще столетие назад. Вклад в такое большое открытие внесли: Томсон, доказавший существование катодных лучей, Складовская-Кюри и ее муж Пьер Кюри, открывшие естественную радиоактивность веществ, Резефорд, который заявил о наличии в центре атома положительно заряженного ядра и о возможности искусственного превращения одного элемента в другой, Чедвик, обнаруживший наличие нейтральных элементов, или нейтронов. Строение атома первым всерьез начал изучать Томпсон, который и открыл электрон в 1897 году. Он смог доказать существование еще более микроскопических тел. Благодаря его деятельности строение атома стало во многом понятным. Он открыл, что данная частица представлена сферическим распределением положительных зарядов, которые полностью компенсируются отрицательными. По этой причине атом является электрически нейтральным.
В результате ряда исследований, проведенных этими и другими учеными, было выяснено, что атом не является однородным телом, а состоит из таких частиц, как нейтроны, протоны и электроны.
В ядре атома протонов столько же, сколько и электронов в его оболочке, кроме того, количество протонов соответствует номеру элемента в таблице Менделеева. Массы протона и нейтрона практически идентичны. Эти элементы удерживаются в ядре атома особыми силами, которые еще называются ядерными; эти силы очень мощные, но действуют на сверхкоротких расстояниях, при этом многократно превосходя силы отталкивания частиц. Вес электронов весьма незначителен. Практически вся масса атома заключается в его ядре, строение ядра атома включает нейтроны и протоны. Свойства этой его части определяются его основными компонентами, указанными выше. Среди атомов встречаются так называемые изотоны. Эти частицы одного и того же вещества имеют разную массу из-за того, что количество их нейтронов может различаться. Количество же их протонов, однако, всегда одно и то же. К примеру, строение атома углерода обычно предполагает наличие в его ядре шести положительно заряженных частиц и шести нейтральных – всего 12, то есть так называемое массовое число углерода чаще всего - 12. Однако имеются и изотопы этого элемента, в которых число протонов стабильно соответствует 6, а число нейтронов может отличаться.
Оболочка атома является достаточно сложной системой. Состоит она из различных подоболочек с разными энергетическими уровнями, которые, в свою очередь, делятся на подуровни, а подуровни – на орбитали. Последние различаются по форме и своему размеру.
fb.ru
КАК УСТРОЕНЫ АТОМЫ
АТОМНАЯ ЭНЕРГИЯ
Атомы так малы, что их нельзя увидеть даже с помощью самых сильных увеличительных приборов. Вместе с тем, они имеют довольно сложное строение.
Большую роль в изучении строения атомов сыграли работы английского физика Резерфорда и датского физика Бора.
По современным представлениям в центре любого атома находится маленькое тяжёлое тело — атомное ядро. Поперечник ядра примерно в 100 000 раз меньше поперечника атома. Но именно в этом очень маленьком ядре и заключена основная доля массы атома. Ядро имеет положительный электрический заряд, величина которого различна у атомов разных элементов.
Вокруг ядра, на расстояниях, в десятки и сотни тысяч раз превосходящих его размеры, с огромной скоростью движутся мельчайшие частицы, несущие заряд отрицательного электричества — электроны. Каждый электрон примерно в 1840 раз легче атома водорода и поэтому на их долю приходится лишь небольшая часть массы атома. Число электронов в каждом атоме равно числу положительных зарядов, заключённых в его ядре. Например, атом кислорода, газа, которым мы дышим, имеет 8 зарядов в ядре и 8 электронов. Так как одинаковое число положительных и отрицательных зарядов друг друга нейтрализует, то атомы в обычных состояниях являются электрически незаряженными или, как принято говорить, нейтральными.
Между номером (положением) элемента в периодической системе, от которого зависят химические свойства элемента, и зарядом ядра его атомов существует очень простая связь: заряд ядра, а следовательно, и число обращающихся вокруг него электронов, равны порядковому номеру элемента в периодической системе Менделеева. Например, химический элемент гелий стоит на втором месте в периодической системе; это значит, что каждый атом гелия имеет 2 положительных заряда з ядре, и вокруг ядра обращаются 2 электрона. Кислород, имея 8 зарядов в ядре и 8 электронов, занимает в системе Менделеева восьмое место. Атом урана, занимающий в периодической системе девяносто второе место, имеет 92 положительных заряда в ядре и столько же электронов.
Электроны в атомах располагаются несколькими слоями. Например, 92 электрона атома урана располагаются так: 2 образуют ближайший к ядру слой; в следующий, более отдалённый от ядра слой, входит 8 электронов; затем опять 8, далее 18, 18, 32. Последние 6 электронов образуют наиболее далёкий от ядра внешний слой и удерживаются ядром с наименьшей силой. Они легче всего могут объединяться с электронами других атомов. Основные химические свойства атомов, их способность к различным химическим превращениям определяются главным образом именно этими внешними электронами.
ИСПОЛЬЗОВАНИЕ НЕЙТРОНОВ И ГАММА-ИЗЛУЧЕНИЯ
Большую ценность представляют и последние два продукта атомного котла — нейтроны и гамма-лучи. Котёл производит их в огромных количествах. Например, из котла, мощностью в 10 ООО киловатт, через площадку в …
ГДЕ И КАК ПРИМЕНЯЮТСЯ МЕЧЕНЫЕ АТОМЫ
В жизни растений важную роль играет фосфор, извлекаемый ими из почвы в виде солей фосфорной кислоты — фосфатов. Как узнать, каким частям растения он более нужен, где он накапливается в …
МЕЧЕНЫЕ АТОМЫ
Большинство процессов, происходящих в природе, связано с движением атомов и молекул. Растворение соли в воде, выплавка металла в доменной печи, дыхание и питание живых организмов — всё это сопровождается движением …
msd.com.ua
Строение атома и все что с этим связано
Содержание:
История строения атома
Еще с давних времен мыслители, философы и первые ученые мужи предполагали, что все сущее, материя, воздух, вода, все состоит из неких мельчайших частиц — атомов. Основоположником атомарной теории строения мира был древнегреческий философ и ученый Демокрит, хотя, скорее всего не он был первым автором этой идеи – Демокрит много путешествовал по тогдашней ойкумене и учение о строении атомов мог перенять у халдейских и/или египетских жрецов, по совместительству блестящих ученых древнего мира.
Согласно учению Демокрита даже человеческая душа состоит из атомов. Он также объяснял многие особенности разных веществ, например, огонь, согласно Демокриту, потому печет, что атомы из которых он состоит острые, а твердые тела именно потому твердые, что атомы из которых они состоят крепко сцеплены между собой.
Учение Демокрита вызвало многие споры среди античных философов (в целом охочих к этому занятию), в частности частым предметом дискуссий и рассуждений был вопрос о делимости/неделимости атома и если атом таки делится, рассуждали философы, то делятся ли в свою очередь его мельчайшие частицы, и до каких пор происходит это деление? Некоторые же мудрецы считали атом мельчайшей неделимой частицей, ведь само название этого слова «atomos» на древнегреческом означало «неделимый».
Правда античные мудрецы дальше теоретических дискуссий так и не зашли, затем на смену античности пришло мрачное средневековье и стало не до атомов. Новый интерес к атомам, основным сведениям об их строении уже возник в XIX веке, времени нового расцвета науки и техники. Так уже с практическими опытами ученым стало понятно, что атом не является неделимым, а в 1860 году было сформулировано академическое понятие атома и молекулы.
XX век стал подлинным временем прорыва наших знаний об атоме, в том числе блестящие ученые физики Нильс Бор и Эрнест Резерфорд предложили так званую планетарную модель атома, сравнив его с планетной системой, где подобно тому как планеты вращаются вокруг Солнца, электроны в атоме вращаются вокруг атомного ядра, состоящего из протонов и нейтронов. Любопытно, что подобные рассуждения перекликаются с представлениями древних, ведь еще легендарный Гермес Трисмегист говорил «что вверху, то внизу», или другими словами строение планетных систем и галактик подобно строению мельчайшей частицы – атома.
Модели строения атома
Помимо модели Бора/Резерфорда были и другие, например, модель Томпсона, полагавшего, что атом является положительно заряженным телом, внутри которого располагаются электроны. Эту модель опроверг Резерфорд.
Также стоит отметить планетарную модель атома Нагаоки, предполагавшего, что строение атома подобно планете Сатурн, у которого вокруг ядра вращаются объединенные в кольца электроны.
Закономерным развитием общепризнанной планетарной модели Бора/Резерфорда стала квантовая модель строения атома, утверждающая, что в ядре атома находятся не имеющие заряда нейтроны, положительно заряженные протоны, а вокруг летают отрицательно заряженные электроны. При этом траектории движения электронов согласно законам квантовой механики наперед не заданы.
Разумеется, все модели строение атомы являются весьма упрощенными вариантами, подлинное строение атома куда более сложное.
Периодический закон Менделеева и строение атомов
Строение и свойства атомов различных химических элементов прямо связаны с местом последних в знаменитой таблице Менделеева. Там они расположены согласно электрическим зарядам своих ядер, зависящего от количества протонов (как помним заряженных положительно) и электронов, летающих вокруг ядра и заряженных отрицательно.
Электронная оболочка атомов
Электронная оболочка атомов имеет ровно столько электронов, сколько есть в его ядре протонов, именно благодаря этому атом является нейтрально заряженным – количество положительно и отрицательно заряженных частиц уравнивают друг друга.
Формула строения атома
Наряду с появлением планетарной теории строения атома появились и формулы, описывающие это самое строение для атомов разных химических элементов. Например, формулу строения атома азота можно описать как — 1s22s22p3, строение атома натрия — 1s22s22p63s1. Эти формулы показывают, какое количество электронов движется по каждой из орбит того или иного химического элемента.
Современная модель строения атома
В наше время физика не стоит на месте и с момент создания канонической планетарной модели атома Бора/Резерфорда было сделано много интересных открытий относительно устройства атома. Так, например, мы уже знаем что протоны, из которых состоит атомное ядро, сами в свою очередь состоят из еще более мелких элементарных частиц – кварков. Но кварки, также далеко не самые мелкие частицы, меньше их открытые загадочные нейтрино, о которых на нашем сайте есть интересная статья.
Строение атома, видео
И в завершение познавательное видео про электронное строение атома и атомного ядра.
www.poznavayka.org
Строение атома
1. Ядро и электроны
Развитие естествознания на границе XIX-XX веков показало, что помимо химических превращений существует целый ряд процессов, в которых атомы выступают как сложные объекты, состоящие из положительно заряженной части - ядра и отрицательно заряженных электронов, суммарный заряд которых в точности компенсирует заряд ядра. В результате работ английского физика Дж. Дж. Томсона и американского физика Р.С. Малликена было установлено, что электрон имеет массу 9,1•1031 кг, или 1/1837 массы атома водорода, и заряд 1,6•10 19 Кл. Основная масса атома сосредоточена в ядре, которое занимает очень малую часть его объема: диаметр ядра порядка 1СГ14 м, он составляет лишь около 10 4 диаметра атома. Наглядно это соотношение размеров можно представить себе, если увеличить атом в 1011 раз: тогда ядро диаметром 1 мм разместится внутри атома диаметром 10 метров!
Позднее было показано, что атомные ядра состоят из положительно заряженных частиц - протонов и незаряженных частиц - нейтронов. Протон имеет заряд, равный заряду электрона, но со знаком плюс, его масса практически равна массе нейтрона. Отметим, что в химии принято выражать заряды ионов в единицах заряда электрона с соответствующим знаком, например Н+ , Mg2+ , СГ.
Таким образом, число протонов в ядре определяет его заряд и порядковый номер, а сумма чисел протонов и нейтронов - округленную общую массу ядра в атомных единицах, или массовое число атома. Очевидно, что в электронейтральном атоме число протонов в атомном ядре равно числу электронов в электронной оболочке атома.
2. Атомный номер элемента. изотопы
Порядковый номер элемента принято называть его атомным номером и обозначать буквой Z. Атомный номер лежит в основе систематизации химических элементов и определяет их положение в периодической системе.
При определенном атомном номере, т.е. при определенном числе протонов, в ядре могут находиться разные числа нейтронов, поэтому могут существовать отличающиеся по массе разновидности атомов одного и того же элемента - изотопы.
Например, природный водород представляет собой смесь изотопов с массовыми числами 1 и 2, а.
Клетка периодической таблицы
В ядре атома урана 92 протона, а в его электронной оболочке - 92 электрона
В периодической таблице, элементы расположены в порядке увеличения заряда ядра, а в отдельных клеточках таблицы принято приводить средневзвешенные атомные массы, поэтому они часто сильно отличаются от целочисленных.
Рис. 2.3, а. Масс-спектрометр.
Газ вводится в вакуумированный прибор через трубку (i) и подвергается ионизации потоком электронов из электронной пушки (2). Заряженные пластины (3) и (4) разгоняют поток полученных положительных ионов, который проходит через щель в пластине (4) и попадает в поле магнита (5), отклоняющее отдельные ионы в соответствии с отношением заряд: масса. За второй щелью (в) расположен детектор (7), который регистрирует число частиц, прошедших через щель. Меняя напряженность магнитного поля, можно последовательно регистрировать относительное количество ионов с различной массой, получая масс-спектр.
В масс-спектрометре молекулы газа превращаются в ионы. Показана часть масс-спектра, соответствующая нонам ТЮ+ и ТЮ2 . Отдельные полосы отвечают пяти изотопам титана с массой 46, 47, 48, 49, 50 значений масс атомов и разделение изотопов стало возможным в результате создания масс-спектрометрии - метода, основанного на воздействии магнитного поля на направленные пучки заряженных частиц.
3. Ядерная модель атома
Первая модель атома была предложена в начале XX века Э. Резерфордом, новозеландцем, работавшем в Англии. Она предполагала, что электроны движутся с большой скоростью по круговым орбитам вокруг ядра, подобно планетам по отношению к Солнцу. По представлениям классической электромагнитной теории в таком атоме электрон должен приближаться по спирали к ядру, непрерывно излучая энергию. Через короткое время электрон неизбежно должен упасть на ядро. Это очевидное несоответствие фактам было не единственным недостатком модели Резерфорда: плавное изменение энергии электронов в атоме не согласовывалось с появившимися наблюдениями над спектрами атомов. Одним из достижений второй половины XIX века была разработка атомного спектрального анализа - точного и чувствительного метода, сыгравшего важнейшую роль в открытии новых элементов и послужившего экспериментальной основой изучения строения атомов. Метод основан на испускании света свободными атомами, получающимися при сильном нагреваний вещества; при этом атомы переходят из основного состояния с минимальной энергией в возбужденные состояния с более высокими энергиями.
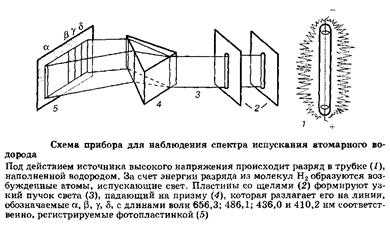
Возвращаясь в основное состояние, атомы излучают свет. Оказалось, что атомные спектры излучения состоят из отдельных линий, отвечающих только определенным длинам волн.
Чтобы объяснить линейчатый характер атомных спектров и устойчивость атомов, знаменитый датский физик Нильс Бор предложил два постулата, выходящие за рамки классической физики:
Из бесконечного числа орбит, возможных с точки зрения классической механики, допустимы лишь определенные орбиты, по которым электрон движется не излучая.
Частота поглощаемого или испускаемого атомом излучения при переходе из одного разрешенного состояния в другое определяется разностью энергий этих состояний.
При этом Бор опирался на идею Макса Планка о квантовании энергии. Планк установил, что, хотя свет, испускаемый раскаленным телом, кажется сплошным, световая энергия поглощается или излучается отдельными порциями - квантами Е = hv, пропорциональными частоте светового электромагнитного колебания. Коэффициент пропорциональности h = 6,6252 • 10 34 Дж • с был назван постоянной Планка. Таким образом в науку было введено понятие кванта света, или некоторого светового пакета - фотона, отражающее не только волновую, но и корпускулярную природу света.
Модель Бора позволила рассчитать точные значения энергии атома водорода и любых одноэлектронных ионов, но оказалась непригодной для объяснения наблюдаемых энергетических характеристик атомов с двумя и более электронами; главный же ее недостаток заключался в том, что она не давала логического обоснования природы квантования и устойчивости не меняющихся во времени состояний атома. Однако, несмотря на эти недостатки, сами идеи Бора о квантовании и стационарных состояниях легли в основу современного описания строения атома с позиций квантовой механики.
4. Волновые свойства электрона
Вскоре после 1920 г. был сделан следующий важный шаг в познании микромира: было установлено, что не только световые кванты, но и любые микрочастицы, в том числе электроны, обладают двойственной природой - частицы как таковой и волны.
Например, электрону при скорости 3 • 10е м/с отвечает длина волны
В частности, удалось обнаружить дифракцию электронов на периодической решетке кристаллов и на молекулах газов. Частице с массой покоя т, движущейся со скоростью v, соответствует длина волны X, которая может быть найдена из уравнения де Бройля: сопоставимая с размерами атома. В то же время можно говорить и об импульсе и даже о массе движущегося фотона, хотя, конечно, его масса покоя равна нулю. Это обстоятельство существенным образом влияет на характер информации, которую дает спектроскопия. При столкновении фотона с электроном меняются импульс фотона и частота света, тем самым давая экспериментатору информацию об импульсе электрона. Однако, поскольку импульсы фотона и электрона сопоставимы, при этом меняется и импульс электрона, который надо определить. Ситуация в какой-то степени подобна попытке измерить скорость бегуна с помощью наблюдателя, который прыгает ему на плечи с разбега. Математически эти соображения описываются принципом неопределенности Гейзенберга, согласно которому возможность одновременного определения положения микрочастицы в пространстве и ее импульса ограничена постоянной Планка. Это, в частности, означает, что если мы хотим определить с большой точностью энергию электрона в атоме, то мы не сможем столь же точно определить его положение по отношению к ядру.
5. Квантово-механическая модель атома
Представления о стационарных состояниях атома и двойственной природе электрона, а также требования принципа неопределенности были использованы австрийским физиком Эрвином Шредингером, который в 1926 г. предложил модель, описывающую электрон в атоме как своего рода стоячую волну, причем вместо точного положения электрона в пространстве рассматривалась вероятность его пребывания в определенном месте.
Для того чтобы представить себе электрон в виде трехмерной стоячей волны, остановимся сначала на более простой одномерной модели стоячей волны, в качестве которой можно взять струну, закрепленную на концах. Струна способна издавать звуки только определенных частот, так как на ее длине может уложиться лишь целое число полуволн - это и есть квантование энергии колебаний струны. Для описания характера стоячих волн одномерной системы достаточно одного числа п, которое однозначно определяет длину волны и число узловых точек, в которых струна неподвижна, как и на закрепленных концах.
Моделью двумерной системы, испытывающей стационарные колебания, может служить круглая мембрана, закрепленная по периметру, например, в телефонной трубке. Здесь также возможны лишь определенные, квантованные колебания, для описания которых необходимы уже два числа.
mirznanii.com
Каков диаметр атома? Размер атома
Атом – уникальная частица мироздания. Эта статья постарается донести до читателя информацию об этом элементе материи. Здесь мы рассмотрим такие вопросы: каков диаметр атома и его размеры, какие он имеет качественные параметры, в чем заключается его роль во Вселенной.
Знакомство с атомом
Атом – составная частица веществ, имеющая микроскопические размер и массу. Это наименьшая часть элементов химической природы с невероятно малыми размерами и массой.
Атомы строятся из двух основных структурных элементов, а именно из электронов и атомного ядра, которое, в свою очередь, образуется протонами и нейтронами. Число протонов может отличаться от количества нейтронов. Как в химии, так и в физике атомы, в которых величина протонов соизмерима с количеством электронов, называют электрически нейтральными. Если число электронов выше или ниже числа протонов, то атом, приобретая положительный или отрицательный заряд, становится ионом.
Атомы и молекулы в физике долгое время считались мельчайшими «кирпичиками», из которых строится Вселенная, и даже после открытия еще меньших составных компонентов остаются среди важнейших открытий в истории человечества. Именно атомы, связанные при помощи межатомных связей, образуют молекулы. Основная масса атома сосредоточена в ядре, а именно, в весе его протонов, которые составляют около 99,9 % от значений общей величины.
Исторические данные

Благодаря достижениям науки в области физики и химии было совершено множество открытий относительно природы атома, его строения и возможностей. Были произведены многочисленные опыты и расчеты, в ходе которых человек смог ответить на такие вопросы: каков диаметр атома, его размер, и многое другое.
Впервые понятие атома было открыто и сформулировано философами древней Греции и Рима. В XVII–XVIII веках химики смогли при помощи экспериментов доказать идею об атоме как наименьшей частице вещества. Они показали, что множество веществ можно расщеплять многократно при помощи химических методов. Однако в дальнейшем открытые физиками субатомные частицы показали, что даже атом можно разделить, а строится он из субатомных компонентов.
Международный съезд ученых по химии в Карлсруэ, расположенном на территории Германии, в 1860 г. принял решение относительно понятия об атомах и молекулах, где атом рассматривается как самая маленькая часть химических элементов. Следовательно, он также входит в состав веществ простого и сложного типа.
Диаметр атома водорода был изучен одним из самых первых. Однако его расчеты были произведены множество раз и последние из них, опубликованные в 2010 г., показали, что он на 4 % меньше, чем предполагалось ранее (10-8). Показатель общего значения величины атомного ядра соответствует числу 10-13-10-12, а порядок величины всего диаметра равен 10-8. Это вызвало множество противоречий и проблем, поскольку сам водород по праву относится к основным составным частям всей обозримой Вселенной, а подобная несостыковка вынуждает совершать множество перерасчетов по отношению к фундаментальным утверждениям.
Атом и его модель
В настоящее время известно пять основных моделей атома, отличающиеся между собой, прежде всего, временными рамками представлениями об его устройстве. Рассмотрим непосредственно модели:
- Кусочки, из которых состоит материя. Демокрит считал, что любое свойство веществ должно определяться его формами, массой и другим рядом практических характеристик. Например, огонь может обжечь, потому что его атомы острые. Согласно мнению Демокрита, даже душа образована атомами.
- Атомная модель Томсона, созданная в 1904 г., самим Дж. Дж. Томсоном. Он предположил, что атом можно принимать в качестве положительно заряженного тела, заключенного внутри электронов.
- Ранняя планетарная атомная модель Нагаоки, созданная в 1904 году, полагала, что устройство атома аналогично системе Сатурна. Ядро маленьких размеров и имеющее положительный показатель заряда окружено электронами, которые двигаются по кольцам.
- Атомная планетарная модель, открытая Бором и Резерфордом. В 1911 г. Э. Резерфорд, после того как провел целый ряд экспериментов, стал полагать, что атом схож с планетарной системой, где у электронов есть орбиты, по которым они двигаются вокруг ядра. Однако это предположение шло в разрез с данными классической электродинамики. Чтобы доказать состоятельность этой теории, Нильс Бор ввел понятие о постулатах, утверждающих и показывающих, что электрону не требуется расходовать энергию, так как он находится в определенном, специальном энергетическом состоянии. Изучение атома в дальнейшем привело к тому, что появилась квантовая механика, которая смогла объяснить множество противоречий, которые можно было наблюдать.
- Квантово-механическая атомная модель утверждает, что центральная основа рассматриваемой частицы состоит из ядра, образующегося из протонов, а также нейтронов и электронов, движущихся вокруг него.
Особенности строения
Размер атома ранее предопределял, что это неделимая частица. Однако множество опытов и экспериментов показали нам, что он строится из субатомных частиц. Любой атом состоит из электронов, протонов и нейтронов, за исключением водорода – 1, который не включает в себя последние.
Стандартная модель показывает, что протоны и нейтроны образованы посредством взаимодействия между кварками. Они относятся к фермионам, наряду с лептонами. В настоящее время различают 6 видов кварков. Протоны своим образованием обязаны двум u-кварками и одному d-кварку, а нейтрон – одному u-кварку и двум d-кварками. Ядерное взаимодействие сильного типа, которым связываются кварки, передается при помощи глюонов.
Движение электронов в атомном пространстве предопределяется их «желанием» быть ближе к ядру, другими словами, притягиваться, а также кулоновскими силами взаимодействия между ними. Эти же типы сил удерживают каждый электрон в потенциальном барьере, окружившем ядро. Орбита движения электронов обуславливает величину диаметра атома, равную прямой линии, проходящей от одной точки в окружности к другой, а также через центр.
У атома имеется его спин, который представлен собственным импульсным моментом и лежит вне понимания общей природы материи. Описывается при помощи квантовой механики.
Размеры и масса
Каждое ядро атома с одинаковым показателем числа протонов относится к общему химическому элементу. К изотопам относятся представители атомов одного элемента, но имеющие различие в нейтронном количестве.
Поскольку в физике строение атома указывают на то, что основную их массу составляют протоны и нейтроны, то общую сумму данных частиц имеют массовым числом. Выражение атомной массы в состоянии спокойствия происходит посредством использования атомных единиц массы (а. е. м.), которые по-другому именуются дальтонами (Да).
Размер атома не имеет четко выраженных границ. Потому определяется он при помощи измерения расстояния между ядрами одинакового типа атомов, химически связанных между собой. Другой способ измерения возможен при расчете длительности пути от ядра до дальнейшей из имеющихся электронных орбит стабильного типа. Периодическая система элементов Д. И. Менделеева располагает в себе атомы по размеру, от меньших к большим, в направлении столбца сверху вниз, движение по направлению слева направо также основано на уменьшении их размеров.

Время распада
Все хим. элементы имеют изотопы, от одного и выше. Они содержат в себе нестабильное ядро, подверженное радиоактивному распаду, вследствие чего происходит испускание частиц или электромагнитного излучения. Радиоактивным называют тот изотоп, у которого величина радиуса сильного взаимодействия выходит за пределы дальних точек диаметра. Если рассмотреть на примере аурума, то изотопом будет атом Au, за пределы диаметра которого во всех направлениях "вылетают" излучающиеся частицы. Изначально диаметр атома золота соответствует величине двух радиусов, каждый из которых равен 144 пк, а частицы, выходящие за пределы этого расстояния от ядра, будут считаться изотопами. Существует три типа распада: альфа-, бета- и гамма излучение.
Понятие о валентности и наличии энергетических уровней
Мы уже ознакомились с ответами на такие вопросы: каков диаметр атома, его размер, ознакомились с понятием распада атома и т. д. Однако, помимо этого, существуют и такие характеристики атомов, как величина энергетических уровней и валентность.
Электроны, двигающиеся вокруг атомного ядра, обладают потенциальной энергией и пребывают в связанном состоянии, располагаясь на возбужденном уровне. В соответствии с квантовой моделью, электрон занимает только дискретное количество энергетических уровней.

Валентность – это общая способность атомов, у которых на электронной оболочке имеется свободное место, устанавливать связи химического типа с другими атомными единицами. Посредством установления химических связей атомы стараются заполнить свой слой внешней валентной оболочки.
Ионизация
В результате воздействия высокого значения напряженности на атом он может подвергаться необратимой деформации, которая сопровождается электронным отрывом.
Это приводит к ионизации атомов, в ходе которой они отдают электрон(ы) и претерпевают превращение из стабильного состояния в ионы с положительным зарядом, иначе именуемые катионами. Этот процесс требует определенной энергии, которую называют потенциалом ионизации.
Подводя итоги

Изучение вопросов о строении, особенностях взаимодействия, качественных параметрах, о том, каков же диаметр атома и какие он имеет размеры, все это позволило человеческому разуму совершить невероятный труд, помогающий лучше осознать и понять устройство всей материи вокруг нас. Эти же вопросы позволили открыть человеку понятия об электроотрицательности атома, его дисперсном притяжении, валентных возможностях, определить длительность радиоактивного распада и многое другое.
fb.ru
строение атома и атомного ядра
Атом является наименьшей частицей элемента, сохраняющей его характеристики.
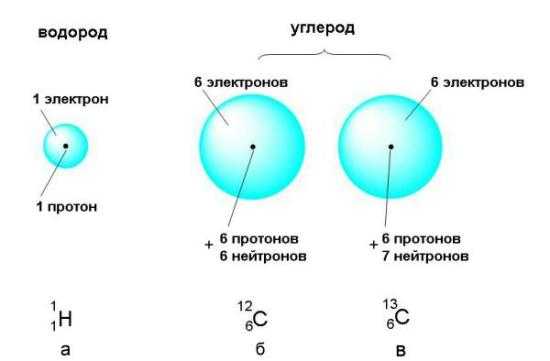
Строение атомного ядра.
Атомы различных элементов отличаются друг от друга. Поскольку существует свыше 100 различных элементов, то существует и свыше 100 различных видов атомов.
Рис 1-2. Части атома.
Каждый атом имеет ядро, расположенное в центре атома. Оно содержит положительно заряженные частицы – протоны и незаряженные частицы – нейтроны.
Электроны, отрицательно заряженные частицы, вращаются вокруг ядер (см. Рис. 1-2).
Количество протонов в ядре атома называется атомным номером элемента.
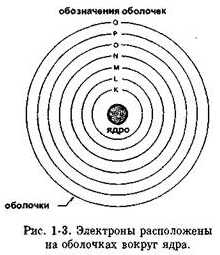
Рис. 1-3. Электроны, расположенные на оболочках вокруг ядра.
Атомные номера позволяют отличить один элемент от другого. Каждый элемент имеет атомный вес. Атомный вес — это масса атома, которая определяется общим числом протонов и нейтронов в ядре. Электроны практически не дают вклада в общую массу атома, масса электрона составляет только 1/1845 часть массы протона и ею можно пренебречь.
Электроны вращаются по концентрическим орбитам вокруг ядра. Каждая орбита называется оболочкой. Эти оболочки заполняются в следующей последовательности: сначала заполняется оболочка К, затем L, М, N и т.д. (см. Рис. 1-3). Максимальное количество электронов, которое может разместиться на каждой оболочке, показано на Рис. 1-4.
Внешняя оболочка называется валентной, и количество электронов, содержащееся в ней, называется валентностью. Чем дальше от ядра валентная оболочка, тем меньшее притяжение со стороны ядра испытывает каждый валентный электрон. Таким образом, потенциальная возможность атома присоединять или терять электроны увеличивается, если валентная оболочка не заполнена и расположена достаточно далеко от ядра.
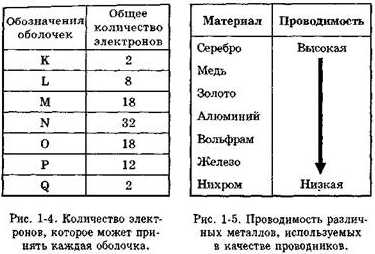
Рис. 1-4 и 1-5. Состав атома.
Электроны валентной оболочки могут получать энергию. Если эти электроны получат достаточно энергии от внешних сил, они могут покинуть атом и стать свободными электронами, произвольно перемещающимися от атома к атому. Материалы, содержащие большое количество свободных электронов, называются проводниками.
Рис. 1-6. Валентность меди.
На Рис. 1-5 сравниваются проводимости различных металлов, используемых в качестве проводников. В таблице серебро, медь и золото имеют валентность, равную единице (см. Рис. 1-6). Однако серебро является лучшим проводником, поскольку его валентные электроны слабее связаны.
Изоляторы, в противоположность проводникам, препятствуют протеканию электричества. Изоляторы стабильны благодаря тому, что валентные электроны одних атомов присоединяются к другим атомам, заполняя их валентные оболочки, препятствуя, таким образом, образованию свободных электронов.

Рис. 1-7. Диэлектрические свойства различных материалов, используемых в качестве изоляторов.
Материалы, классифицируемые как изоляторы, сравниваются на Рис. 1-7. Слюда является наилучшим изолятором, потому что она имеет наименьшее число свободных электронов на своих валентных оболочках.
Промежуточное положение между проводниками и изоляторами занимают полупроводники.Полупроводники не являются ни хорошими проводниками, ни хорошими изоляторами, но они важны, потому что их проводимость можно изменять от проводника до изолятора. Кремний и германий являются полупроводниковыми материалами.
Об атоме, который имеет одинаковое число электронов и протонов, говорят, что он электрически нейтрален. Атом, получающий один или более электронов, не является электрически нейтральным. Он становится отрицательно заряженным и называется отрицательным ионом. Если атом теряет один или более электронов, то он становится положительно заряженным и называется положительным ионом. Процесс присоединения или потери электронов называется ионизацией. Ионизация играет большую роль в протекании электрического тока.
Поделитесь полезной статьей:
Topfazaa.ru
Видеоматериалы
Опыт пилотных регионов, где соцнормы на электроэнергию уже введены, показывает: граждане платить стали меньше
Подробнее...С начала года из ветхого и аварийного жилья в республике были переселены десятки семей
Подробнее...Более 10-ти миллионов рублей направлено на капитальный ремонт многоквартирных домов в Лескенском районе
Подробнее...Актуальные темы
ОТЧЕТ о деятельности министерства энергетики, ЖКХ и тарифной политики Кабардино-Балкарской Республики в сфере государственного регулирования и контроля цен и тарифов в 2012 году и об основных задачах на 2013 год
Подробнее...Предложения организаций, осуществляющих регулируемую деятельность о размере подлежащих государственному регулированию цен (тарифов) на 2013 год
Подробнее...
КОНТАКТЫ
360051, КБР, г. Нальчик
ул. Горького, 4
тел: 8 (8662) 40-93-82
факс: 8 (8662) 47-31-81
e-mail:
Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.