Свойства алюминия – материала на все времена. Электропроводность у алюминия
физические свойства, получение, применение, история :: ТОЧМЕХ
Физические свойства алюминия
Алюминий — мягкий, легкий, серебристо-белый металл с высокой тепло- и электропроводностью. Температура плавления 660°C.
По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния среди всех атомов и 1-е место — среди металлов.
К достоинствам алюминия и его сплавов следует отнести его малую плотность (2,7 г/см3), сравнительно высокие прочностные характеристики, хорошую тепло- и электропроводность, технологичность, высокую коррозионную стойкость. Совокупность этих свойств позволяет отнести алюминий к числу важнейших технических материалов.
Алюминий и его сплавы делятся по способу получения на деформируемые, подвергаемые обработке давлением и литейные, используемые в виде фасонного литья; по применению термической обработки — на термически не упрочняемые и термически упрочняемые, а также по системам легирования.
Получение
Впервые алюминий был получен Гансом Эрстедом в 1825 году. Современный метод получения разработали независимо друг от друга американец Чарльз Холл и француз Поль Эру. Он заключается в растворении оксида алюминия Al2O3 в расплаве криолита Na3AlF6 с последующим электролизом с использованием графитовых электродов. Такой метод получения требует больших затрат электроэнергии, и поэтому оказался востребован только в XX веке.
Применение
Алюминий широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — легкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной пленкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки.
Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий).
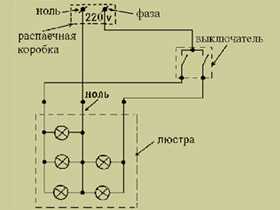
Электропроводность алюминия сравнима с медью, при этом алюминий дешевле. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Правда, у алюминия как электротехнического материала есть неприятное свойство — из-за прочной оксидной пленки его тяжело паять.
Благодаря комплексу свойств широко распространен в тепловом оборудовании.
Внедрение алюминиевых сплавов в строительстве уменьшает металлоемкость, повышает долговечность и надежность конструкций при эксплуатации их в экстремальных условиях (низкая температура, землетрясение и т.п.).
Алюминий находит широкое применение в различных видах транспорта. На современном этапе развития авиации алюминиевые сплавы являются основными конструкционными материалами в самолетостроении. Алюминий и сплавы на его основе находят все более широкое применение в судостроении. Из алюминиевых сплавов изготовляют корпусы судов, палубные надстройки, коммуникацию и различного рода судовое оборудование.
Идут исследования по разработке пенистого алюминия как особо прочного и легкого материала.
Драгоценный алюминий
В настоящее время алюминий является одним из самых популярных и нашедших широкое применение металлов. С самого момента открытия в середине XIX века его считали одним из ценнейших благодаря удивительным качествам: белый как серебро, легкий по весу и не подверженный воздействию окружающей среды. Стоимость его была выше цен на золото. Не удивительно, что в первую очередь алюминий нашел свое применение в создании ювелирных изделий и дорогих декоративных элементов.
В 1855 г. на Универсальной выставке в Париже алюминий был самой главной достопримечательностью. Изделия из алюминия располагались в витрине, соседствующей с бриллиантами французской короны. Постепенно зародилась определенная мода на алюминий. Его считали благородным малоизученным металлом, используемым исключительно для создания произведений искусства.
Наиболее часто алюминий использовали ювелиры. При помощи особой обработки поверхности ювелиры добивались наиболее светлого цвета металла, из-за чего его часто приравнивали к серебру. Но в сравнении с серебром, алюминий обладал более мягким блеском, чем обуславливалась еще большая любовь к нему ювелиров.
Так как химические и физические свойства алюминия сначала были слабо изучены, ювелиры сами изобретали новые техники его обработки. Алюминий технически легко обрабатывать, этот мягкий металл позволяет создавать отпечатки любых узоров, наносить рисунки и создавать желаемой формы изделия. Алюминий покрывался золотом, полировался и доводился до матовых оттенков.
Но со временем алюминий стал падать цене. Если в 1854-1856 годах стоимость одного килограмма алюминия составляла 3 тысячи старых франков, то в середине 1860-х годов за килограмм этого металла давали уже около ста старых франков. Впоследствии из-за низкой стоимости алюминий вышел из моды.
В настоящее время самые первые алюминиевые изделия представляют большую редкость. Большинство из них не пережило обесценивания металла и было заменено серебром, золотом и другими драгоценными металлами и сплавами. В последнее время вновь наблюдается повышенный интерес к алюминию у специалистов. Этот металл стал темой отдельной выставки , организованной в 2000 году Музеем Карнеги в Питсбурге. Во Франции расположен Институт истории алюминия, который в частности занимается исследованием первых ювелирных изделий из этого металла.
В Советском союзе из алюминия делали общепитовские приборы, чайники и т.д. И не только. Первый советский спутник был выполнен из алюминиевого сплава. Другой потребитель алюминия — электротехническая промышленность: из него делаются провода высоковольтных линий передач, обмотки моторов и трансформаторов, кабели, цоколи ламп, конденсаторы и многие другие изделия. Кроме того, порошок алюминия применяют во взрывчатых веществах и твердом топливе для ракет, используя его свойство быстро воспламеняться: если бы алюминий не покрывался тончайшей оксидной пленкой, то мог бы вспыхивать на воздухе.
Последнее изобретение — пеноалюминий, т.н. «металлический поролон», которому предсказывают большое будущее.
tochmeh.ru
Ответы@Mail.Ru: сравнить медь и алюминий
Медь обладает высокой тепло- и электропроводностью (занимает второе место по электропроводности среди металлов после серебра) . Удельная электропроводность при 20 °C: 55,5-58 МСм/м [Из-за низкого удельного сопротивления (уступает лишь серебру, удельное сопротивление при 20 °C: 0,01724-0,0180 мкОм·м [5]), медь широко применяется в электротехнике для изготовления силовых кабелей, проводов или других проводников, например, при печатном монтаже. Медные провода, в свою очередь, также используются в обмотках энергосберегающих электроприводов (быт: электродвигателях) и силовых трансформаторов. Для этих целей металл должен быть очень чистый: примеси резко снижают электрическую проводимость. Например, присутствие в меди 0,02 % алюминия снижает её электрическую проводимость почти на 10 % Алюминий Металл серебристо-белого цвета, лёгкий плотность — 2,7 г/см³ температура плавления у технического алюминия — 658 °CШироко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — лёгкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной плёнкой Al2O3, которая препятствует его дальнейшему окислению) , высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки. Первые же три свойства сделали алюминий основным сырьем в авиационной и авиакосмической промышленности (в последнее время медленно вытесняется композитными материалами, в первую очередь, углеволокном) . Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому для упрочнения его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий) . Электропроводность алюминия всего в 1,7 раза меньше, чем у меди, при этом алюминий приблизительно в 4 раза дешевле [12] за килограмм, но, за счёт в 3,3 раза меньшей плотности, для получения равного сопротивления его нужно приблизительно в 2 раза меньше по весу. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Меньшую электропроводность алюминия (37 1/ом) по сравнению с медью (63 1/ом) компенсируют увеличением сечения алюминиевых проводников. Недостатком алюминия как электротехнического материала является наличие прочной оксидной плёнки, затрудняющей пайку.
touch.otvet.mail.ru
Свойства алюминия – материала на все времена
Часто первые названия чего-либо – устройства, материала или изделия - наиболее точно и понятно отражают их сущность. А потом наступает период осмысления и приходит новое название, научное, в котором понятный “житейский” смысл уходит в небытие. Когда-то алюминий имел название глинозем, т.е. “глина земли”, а глина, как известно, первичная суть земли. Теперь так называют оксид алюминия. А на смену бытовавшему ранее названию “глинозем” пришло новое имя - “алюминиум” – красиво, загадочно и по-научному. Легенда о первом пришествии алюминия имеет печальный конец: мастеру, подарившему императору Тиберию удивительную чашу из доселе неизвестного металла, чтобы сохранить подарок в единственном экземпляре, на всякий случай, отрубили голову – нашел кому дарить. В те времена, в начале нашей эры, вопросы секретности решались кардинально, а благодарность за мастерство также была своеобразной. Как бы там ни было, но только через пятнадцать столетий Парацельс установил, что глинозем (квасцы), применяемый для закрепления красок в тканях и кожах, содержит окись неизвестного металла.
Чистый металл удалось получить только в 1825 г. Датский ученый Эрстед в качестве побочного эффекта своих исследований получил «кусок металла, похожий на олово», но продолжать работы не стал. Тем не менее, к середине XIX века алюминий - серебристый, легкий, простой в обработке металл - ценился больше золота. Свойства алюминия в первую очередь оценили ювелиры. На него была мода, а на выставке в Париже в 1855 году изделия из алюминия демонстрировались рядом с бриллиантами французской короны. Как известно, спрос приводит к росту предложений, поэтому технологии производства получили толчок к развитию. И к середине ХХ века алюминий стал обычным широко применяемым в технике материалом, а физические свойства алюминия были уже достаточно хорошо изучены.
Технологии промышленного производства алюминия
Основой производства алюминия является электролиз, а сырьем служит растворенный в расплаве криолита оксид алюминия Al2O3. Для электролиза применяют ванны, рабочая температура которых чуть меньше 1000°С. Жидкий алюминий собирается на дне ванны - это катод установки. Разливают его в формы и получают слитки или чушки - сырье для дальнейшей переработки.
Свойства алюминия изменяют в нужном ключе при помощи легирующих добавок. При этом добиваются повышения прочности, твердости, жаропрочности и т.д. с ориентацией на конкретное применение. Легирующие материалы для различных сплавов - медь, марганец, цинк, магний, а также (в небольших количествах) кремний, железо, никель и др. добавляют в расплав при окончательном изготовлении нужного вида готовой продукции.
Основные физические свойства алюминия
Любой материал характеризуется набором физико-химических свойств, которые и определяет его последующее использование. Свойства алюминия — пластичность, небольшой удельный вес, хорошая тепло- и электропроводность — известны всем.
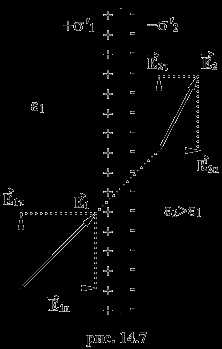
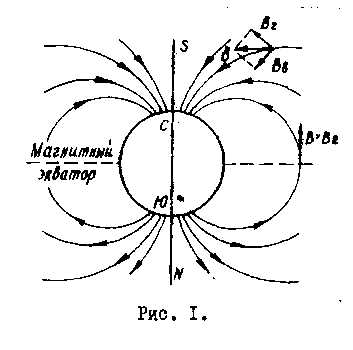
С точки зрения применения в электротехнике безусловный интерес представляют магнитные свойства алюминия, по которым он относится к слабомагнитным веществам группы парамагнетиков. Этот класс материалов характерен тем, что его магнитное поле при действии внешнего поля совпадает с ним по направлению, и, хоть и очень незначительно, но усиливается.
Применение алюминия
Ценность материала определяет востребованность изделий из него. Алюминий востребован в первую очередь как конструкционный материал. Легкость обработки и коррозионная стойкость позволяют использовать изделия из алюминия в строительстве, машиностроении, для изготовления теплового, пищевого и других видов оборудования. Алюминий – это основной конструкционный материал авиации. Все более широкое применение находят алюминиевые сплавы в судостроении - корпуса судов, коммуникации, палубные надстройки, различное судовое оборудование. Широко применяются в промышленности и быту дюралюминий и силумин - некорродирующие сплавы алюминия с медью – до 7% или кремнием – до 14%.
Электропроводность алюминия незначительно уступает меди, но алюминий намного легче и дешевле, чем и обусловлено его широкое применение в электротехнике. При этом основные свойства алюминия для такого применения – малое электрическое сопротивление, вес и невысокая стоимость. Все чаще в электрооборудовании, где совсем недавно безраздельно господствовали исключительно медные проводники, применяют алюминиевые обмотки трансформаторов, катушек индуктивности, реакторов, “жилы” кабелей и др. Магистральные линии электропередач также во многом обязаны именно алюминию.
Нет сомнений, что этот удивительный металл еще не раскрыл всех своих возможностей – это предстоит сделать в будущем.
fb.ru
Свойства алюминия
Свойства алюминия
Алюминий-самый распространненый металл в земной коре. Его содержание оценивают в 7.45 % (больше, чем железа, которого только 4.2 %). Алюминий как элемент открыт недавно-в 1825 г., когда были получены первые небольшие комочки этого металла. Начало его промышленного освоения относится к концу прошлого столетия. Толчком к этому послужила разработка в 1886 г. способа его получения путем электролиза глинозема, растворенного в криолите. Принцип способа лежит в основе современного промышленного извлечения алюминия из глинозема во всех странах мира.
По внешнему виду алюминий представляет собой блестящий серебристый белый металл. На воздухе он быстро окисляется, покрываясь тонкой белой
матовой пленкой Al O . Эта пленка обладает высокими защитными свойствами, поэтому, будучи покрытым такой пленкой, алюминий является коррозионностойким.
Алюминий достаточно легко разрушается растворами едких щелочей, соляной и серной кислот. В концетрированной азотной кислоте и органических кислотах он обладает высокой стойкостью.
Наиболее характерными физическими свойствами алюминия является его малая относительная плотность, равная 2.7, а также сравнительно высокие тепло- и электропроводность. При 0 C удельная электропроводность алюминия, т.е. электропроводность алюминиевой проволоки сечением 1 мм и длиной 1 м равна 37 1 ом.
Коррозионная стойкость и особенно электропроводность алюминия тем выше, чем он чище, чем меньше в нем примесей.
Температура плавления алюминия невысокая, она равна приблизительно 660 C. Однако скрытая теплота плавления его очень большая-около 100 кал г, поэтому для расплавления алюминия требуется большой расход тепла, чем для расплавления такого же количества, например, тугоплавкой меди, у которой температура плавления 1083 C, скрытая теплота плавления 43 кал г.
Для механических свойств алюминия характерна большая пластичность и малая прочность. Прокатанный и отожженный алюминий имеет =10 кГ мм, а твердость НВ25, =80% и =35%.
Кристаллическая решетка алюминия представляет собой гранецентрированный куб, имеющий при 20 C параметр (размер стороны) 4.04 . Аллотропических превращений алюминий не имеет.
В природе аллюминий находится в виде алюминиевых руд: бокситов, нефелинов, алунитов и каолинов. Важнейшей рудой, на которой базируется большая часть мировой алюминиевой промышленности, являются бокситы.
Получение алюминия из руд состоит из двух последовательно проводимых этапов-сначала производят глинозем (Al O ), а затем из него получают алюминий.
Известные в настоящее время методы получения глинозема можно разбить на три группы: щелочные, кислотные и электротермические. Наиболее широкое применение получили щелочные методы.
В одних разновидностях щелочных методов боксит, обезвоженный при 1000 C, измельчают в шаровых мельницах, смешивают в определенных пропорциях с мелом и содой и спекают для получения растворимого в воде твердого алюмината натрия по реакции
Al O + Na CO = Al O Na O + CO .
Спекшуюся массу измельчают и выщелачивают водой, алюминат натрия при этом переходит в раствор.
В других разновидностях щелочного метода глинозем, содержащийся в боксите, связывают в алюминат натрия путем непосредственной обработки руды щелочами. При этом сразу получается раствор алюмината в воде.
В обоих случаях образование водного раствора алюмината натрия приводит к отделению его от нерастворимых компонентов руды, представляющих собой в основном окиси и гидроокиси кремния, железа и титана. Отделение раствора от нерастворимого осадка, называемого красным шламом, осуществляют в отстойниках.
В полученный раствор при 125 C и давлении 5 ам добавляют известь, что приводит к обескремниванию-CaSiO уходит в осадок, образуя белый шлам. Очищенный от кремния раствор после отделения его от белого шлама обрабатывают углекислым газом при 60-80 C, в результате чего в осадок выпадает кристаллический гидрат окиси алюминия:
Al O Na O + 3H O + CO = 2Al(OH) + Na CO .
Его промывают, просушивают и прокаливают. Прокаливание приводит к образованию глинозема:
2Al(OH) = Al O + 3H O .
Описанный способ обеспечивает довольно полное извлечение глинозема из боксита-около 80%.
Получение металлического алюминия из глинозема заключается в его электролитическом разложении на составные части-на алюминий и кислород. Электролитом в этом процессе является раствор глинозема в криолите (AlF 3NaF). Криолит, обладая способностью растворять глинозем, одновременно снижает его температуру плавления. Глинозем плавится при температуре около 2000 C, а температура плавления раствора, состоящего, например, из 85 % криолита и 15 % глинозема, равна 935 C.
Схема ээлектролиза глинозема достаточно проста, но технологически этот процесс сложный и требует больших затрат электроэнергии.
В поду ванны с хорошей теплоизоляцией 1 и угольной набивкой 2 заложены катодные шины 3, соединенные с отрицательным полюсом источника электрического тока. К анодной шине 4 присоединены электроды 5. Перед началом электролиза на дно ванны насыпают тонкий слой кокса, электроды опускают до соприкосновения с ним и включают ток. Когда угольная набивка накалится, постепенно вводят криолит. При толщине слоя расплавленного криолита, равной 200-300 мм, загружают глинозем из расчета 15% к количеству криолита. Процесс происходит при 950-1000 C.
Под действием электрического тока глинозем разлагается алюминий и кислород. Жидкий алюминий 6 скапливается на угольной подине (дно угольной ванны), являющейся катодом, а кислород соединяется с углеродом анодов, постепенно сжигая их. Криолит расходуется незначительно. Глинозем периодически добавляют, электроды для компенсации сгоревшей части постепенно опускают вниз, а накопившийся жидкий алюминий через определенные промежутки времени выпускают в ковш 8.
При электролизе на 1 т алюминия расходуется около 2 т глинозема,
0.6 т угольных электродов, служащих анодами, 0.1 т криолита и от
17000 до 18000 квт ч электроэнергии.
Полученный при электролизе глинозема алюминий-сырец содержит металлические примеси (железо, кремний, титан и натрий), растворенные газы, главным из которых является водород, и неметаллические включения, представляющие собой частицы глинозема, угля и криолита. В таком состоянии он непригоден для применения, так как имеет низкие свойства, поэтому его обязательно подвергают рафинированию. Неметаллические и газообразные примеси удаляют путем переплавки и продувки металла хлором. Металлические примеси можно удалить только сложными электролитическими способами.
После рафинирования получают торговые сорта алюминия.
Чистота алюминия является решающим показателем, влияющим на все его свойства, поэтому химический состав положен в основу классификации алюминия.
Неизбежными примесями, получающимися при производстве алюминия, являются железо и кремний. Обе они в алюминии вредны. Железо не растворяется в алюминии, а образует с ним хрупкие химические соединения FeAl и Fe Al . С кремнием алюминий образует эвтектическую механическую смесь при 11.7% Si. Поскольку растворимость кремния при комнатной температуре очень мала (0.05%), то даже при его незначительном количестве он образует эвтетику Fe+Si и включения очень твердых (НВ 800) хрупких кристалликов кремния, которые снижают пластичность алюминия. При совместном присутствии кремния и железа образуется тройное химическое соединение и тройная эвтектика, тоже понижающие пластичность.
У нас в стране в зависимости от количества примесей установлены тринадцать марок алюминия, выпускаемых промышленностью.
______________________________________________________________
| Чистота алюминия разных марок |
Контролируемыми примесями в алюминии являются железо, кремний, медь и титан.
Алюминий всех марок содержит более 99 % Al. Количественное же превышение этой величины в сотых или десятых долях процента указывают в названии марки после начальной буквы А. Так, в марке А85 содержится
99.85 % Al. Исключение из этого принципа маркировки составляют марки А
АЕ, в которых содержание алюминия такое же, как в марках А0 и А5, но другое соотношение входящих в состав примесей железа и кремния.
Буква Е в марке АЕ означает, что алюминий данной марки предназначается для производства электропроводов. Дополнительным требованием к свойствам алюминия является низкое электросопротивление, которое для проволоки, изготовленной из него, должно быть не более 0.0280 ом мм м при 20 C.
Алюминий применяют для производства из него изделий и сплавов на его основе, свойства которых требуют большой степени его чистоты.
В зависимости от назначения алюминий можно производить в различном виде. Алюминий всех марок (высокой и технической чистоты), предназначенный для переплавки, отливают в виде чушек массой 5; 15 и 1000 кг. Их предельные величины следущие: высота от 60 до 600 мм, ширина от 93 до 800 мм и длина от 415 до 1000 мм.
Если же алюминий предназначается для проката листа и ленты, то непрерывным или полунепрерывным методом отливают плоские слитки семнадцати размеров. Толщина их колеблется в пределах от 140 до 400 мм, ширина-от 560 до 2025 мм, а масса 1 м длины слитка-от 210 до 2190 кг. Длину слитка согласовывают с заказчиком.
Основным видом контроля алюминия как в чушках, так и в плоских слитках, является проверка химического состава и его соответсвие марочному. К чушкам и слиткам, предназначенным для обработки давлением, предьявляют дополнительные требования, такие, например, как отсутсвие раковин, газовых пузырей, трещин, шлаковых и других посторонних включений.
mirznanii.com
Алюминий — Знаешь как
Содержание статьи
(Aluminium; от лат. alumen (aluminis) — квасцы], Al — хим. элемент III группы периодической системы элементов; ат. н. 13,ат. м. 26,98154. Серебристо-белый металл, при обычных условиях покрыт тонкой окисной пленкой. Во всех устойчивых соединениях алюминий трехвалентен, но при высоких т-рах может быть одновалентным (образуя субсоединения) и, значительно реже, двухвалентным. Состоит из стабильного изотопа 27Al . Впервые алюминий в свободном виде выделил в 1825 датский ученый X. К. Эрстед. Первый пром. способ произ-ва А. предложил в 1854 франц. химик А. Э. Сент-Клер Девиль. По распространенности в природе алюминий занимает первое место среди металлов. Его содержание в земной коре составляет 8,8%. В свободном состоянии в природе не встречается из-за высокой хим. активности. Главная масса алюминия сосредоточена в боксит, нефелин, алунит, каолин и др. Наиболее ценная алюминиевая руда — бокситы, где содержится около 50% окиси алюминия. Кристаллическая решетка алюминия гранецентрированная кубическая с периодом а = 4.0414А (т-ра 20° С), плотность (т-ра 20° С) 2,7 г/см³, tпл 660° С, tкип 2327° С, температурный коэфф. линейного расширения (т-ра 25° С) 24,3 X 10-6 град-1, удельная теплопроводность (т-ра 20° С) 0,538 кал/см • сек • град, удельная теплоемкость (т-ра 20° С) 0,215 кал/г, удельное электрическое сопротивление (т-ра 20° С) 2,66•10-6 ом • см, электрическое сопротивление проводникового алюминия не более 0,028 ом • мм2/м, температурный ко-эфф. электрического сопротивления А.— 0,004 градˉ¹. А. слабо парамагнитен. Отличается пластичностью, легко поддается прессованию, прокатке, ковке, штампованию и волочению.Предел прочности на растяжение 8—10 кгс/мм2, предел текучести при растяжении 3 кгс/мм2, относительное удлинение 35 %, относительное сужение 80 %, твердость по Бринеллю 25, модуль норм, упругости 7100 кгс/мм2, модуль сдвига 2600 кгс/мм2. После холодной прокатки предел прочности возрастает до 18—25 кгс/мм2, твердость по Бринеллю — до 45 —60, относительное удлинение уменьшается до 3—5%. Алюминий отличается высокой электропроводностью (четвертое место среди металлов — после серебра, меди и золота).
Примеси и легирующие добавки снижают электропроводность алюминия, особенно марганец, ванадий, хром и титан, в меньшей степени — никель, кремний, цинк, железо и медь. Так, электропроводность алюминия чистотой 99,997% составляет 65,5% электропроводности меди, а электропроводность А. чистотой 99,5% снижается до 62,5%. Алюминий относится к химически активным металлам. На воздухе быстро покрывается тонкой прочной окисной пленкой толщиной 50—100 А, защищающей от дальнейшего окисления.Пленка имеет высокое электр. сопротивление (напряжение пробоя превышает 500 в) и, в отличие от органических изоляторов, выдерживает высокие т-ры. Алюминий образует соединения почти со всеми элементами, растворяется в к-тах и щелочах. Однако он может успешно использоваться в коррозионных средах, в к-рых поверхностная защитная пленка окиси алюминия нерастворима. Алюминий отличается высокой коррозионной стойкостью в воде, в том числе кипящей и морской. Он устойчив в уксусной, лимонной, винной и др. органических к-тах.
Алюминий практически не взаимодействует с концентрированной азотной к-той, мн. органическими веществами и пищевыми продуктами, Быстро растворяется в растворах едких щелочей (образуя алюминаты), соляной, плавиковой и бромистоводородной к-тах. Слабо взаимодействует с борной к-той. При обычных т-рах не взаимодействует с водой, парами воды, окисью и двуокисью углерода; при достаточно высоких т-рах способен реагировать с ними. А. устойчив в растворах сернокислых нейтральных солей магния, натрия, а также гипосульфита. Мало влияют на А. сернистый газ, аммиак и сероводород. Добавление к воде щелочей, солей, ртути, меди и ионов хлора увеличивает его коррозию. Водород растворяется в твердом алюминии, с повышением т-ры растворимость увеличивается (при т-ре 350° С она составляет 0,002 см3/100 г, а при т-ре 660° С — 0,036 см3/100 г). Компактный А. в среде азота покрывается тонкой пленкой нитрида. С галогенами, серой и фосфором А. взаимодействует при высоких т-рах. С более электроположительными элементами образует алюминиды. При нагревании алюминий восстанавливает большинство окислов др. металлов, что используется в алюмотермии. Производство алюминия заключается в получении окиси алюминия из алюминиевых руд щелочным, кислотным, электротермическим или комбинированными способами, получении первичного металла электролизом окиси алюминия (в спец. аппаратах — электролизерах), растворенной в расплавленном криолите при т-ре около 950° С, и рафинировании этого металла.Небольшие добавки фторидов кальция, магния и натрия улучшают физико-хим. св-ва электролита, повышая эффективность электролизеров. Макс, содержание окиси алюминия в электролите — 6—8%.
В производстве используют электролизеры с непрерывными самообжигающимися анодами и боковым или верхним подводом тока, электролизеры с обожженными анодами. Катодом служит подина ванны, анодом — погруженные в электролит угольные обожженные блоки или набивные самообжигающиеся электроды. Ванну эксплуатируют при напряжении 4,0—4,5 в. Сила тока, подводимая к электролизерам,— 130—160 ка. Плотность тока на аноде 0,7—0,8 а/см², на катоде 0,4—0,5а/см².. Расход электроэнергии на произ-во 1mA. составляет 14 000— 15000квт-ч. Черновой алюминий содержит примеси от к-рых его очищают продуванием расплава хлором при т-ре 750—770 С в течение 10—15 мин, после чего разливают в чушки.
Чистоте первичного А, 99,7—99,5%. Перспективен хлоридный способ получения алюминия позволяющий уменьшить затраты энергии и слизать загрязнение окружающей среды. В зависимости от способа получения и хим. состава различают: Алюминий особой чистоты, А. высокой чистоты и А. технической чистоты. А. особой чистоты (марки А999) содержит не более 0,001% примесей. Получают его зонной плавкой и дистилляцией через субгалогениды электролитически рафинированного металла. Для более глубокой очистки эти способы комбинируют. Применяется для научно-исследовательских целей, в полупроводниковой и ядерной технике. Алюминий высокой чисто-т ы (марок А995, А99, А97, А95) содержит от 0,005 до 0,05% примесей.
Получают алюминий из первичного металла технической чистоты дополнительным рафинированием по трехелойному способу, снижающему содержание примесей железа, кремния, титана, меди и др. Используется в основном при произ-ве специальной хим. аппаратуры, электр. конденсаторов и др. Алюминий технической чистоты (марок А85, А8, А7, А6, А5, АО, А и АЕ) содержит от 0,15 до 1,00% примесей. А. марок А85 и А8 применяют для произ-ва алюминиевого прока та, А. ма рок А 7, А6 и А5 — для получения алюминиевых сплавов, фольги, произ-ва кабельных и токопроводящих изделий, алюминиевого порошка, для плакирования и пр.
Для изготовления сплавов на алюминиевой и др. основах, спец. лигатур, кабельных и токопроводящих изделии применяют металл марки ДО, для подших-товки алюминиевых сплавов, изготовления лигатур, в алюмотер-мни — металл марки А, для произ-ва алюминиевой катанки — металл марки АЕ. А. высокой и технической чистоты выпускают в чушках массой 5; 15 и 1000 кг. Осн. виды алюминиевых полуфабрикатов — листы, проволока и полосы.
Поставляют полуфабрикаты и изделия в горячекатаном, нагартованном и отожженном состоянии. Малая плотность металла, высокая электропроводность, достаточная механическая прочность и высокая коррозионная стойкость по отношению к некоторым хим. реагентам, а также низкая себестоимость обусловливают широкое применение А. в различных областях техники.
Относительно низкое сечение поглощения тепловых нейтронов, малая чувствительность структуры и мех. св-в к радиационному воздействию, а также значительная коррозионная стойкость в некоторых средах-теплоносителях позволяют использовать А. как конструкционный материал ядерных реакторов, гл. обр. с водяным охлаждением. А. применяют также для изготовления защитных оболочек тепловыделяющих элементов, трубопроводов. Алюминий служит основой для алюминия сплавов, легирующим элементом в магниевых, цинковых, медных, титановых и других сплавах.
На основе алюминия методом порошковой металлургии созданы спеченные алюминиевые сплавы, отличающиеся высокой жаропрочностью. А. используют для раскисления стали, получения некоторых металлов методом алюмотермии, взрывчатых веществ, а также в композиционных материалах на различной основе. См. также Алюминиевая бронза, Алюминиевая латунь. Алюминиевый чугун, Алюми-нирование, Алитирование.Природный алюминий
Это стабильный изотоп 27Al
Несколько радиоактивных изотопов алюминия получены искусственно , из них … применяется как меченый атом .
По распространённости в литосфере алюминий занимает первое место среди металлов и общее третье место ( после кислорода и кремния ) . в следствие большой химической активности он не встречается в свободном состоянии .
Важные руды алюминия — бокситы Al2O3 · nh3O ( содержащего 32 — 60% Al2O3 ) , алунит K2SO4 · Al2( SO4 )3 · 2Al2O3 · 6h3O , каолин Al2O3 · 2SiO2 · 2h3O , нефелин Na2O · Al2O3 · 2SiO2 , залегающий совместно с апатитом .Алюминий входит также в состав многочисленных полевых шпатов : ортоклаза K[AlSiO8] , альбита Na[AlSi3O8] , цеолита , слюда и др .
Сложность получения алюминия обусловливается тем , что оксид алюминия не проводит электрический ток и отличается высокой температурой плавления 2050°C . Поэтому электролизу подвергают расплавленную смесь , содержащую 6 — 8% Al2O3 и 92 — 94% криолита Na3[AlF6] . Кроме того , в расплав добавляют фториды кальция , магния или алюминия для понижения температуры плавления электролита и улучшения хода процесса . В результате всего этого удаётся вести процесс при температуре 960°C . Дно электролизёра , собранное из блоков спрессованного угля , служит катодом . Алюминиевые каркасы , расположенные сверху и заполненные угольными брикетами , играют роль анодов :
Al2O3 ⇄ Al³⁺+ AlO3³ˉ
На катоде выделяется металлический алюминий :
Al³⁺+ 3eˉ = Al
2AlO — 6e = ³/2O2↑+ Al2O3
По мере накопления на дне электролизёра расплавленного алюминия его выпускают , а расплав добавляют новые порции полутораокиси алюминия . Выделяющийся кислород взаимодействует с углём анода , который выгорает с выделением окиси и двуокиси углерода .
Металлические свойства выражены у алюминия гораздо сильнее , чем у бора , но химические связи алюминия с другими металлами ещё в основном ковалентного характера .
В отличие от бора атом алюминия имеет свободные d- подуровни на внешнем электронном уровне .
Кроме того, ион Al³⁺ отличается небольшим радиусом при довольно высоком заряде и поэтому является комплексообразователем с координационными числами четыре ( как у бора ) и шесть .
Химически чистый алюминий — серебристо- белый металл плотность 2,7 г / см³ c температурой плавления 660,1°C , имеет гранецентрированную кубическую решетку , отличается хорошей пластичностью в холодном и горячем состояниях .
Алюминий — активный металл с большим сродством к кислороду . На воздухе быстро покрывается защитной оксидной плёнкой , а в воде — защитной плёнкой гидроксида . Разрушение защитной плёнки ( путём амальгамации ) приводит к быстрой коррозии алюминия на воздухе и к активному взаимодействию его с водой :
2Al + 6h3O = 2Al( OH )3 +3h3↑
Холодная концентрированная азотная кислота пассивирует алюминий , но в разбавленных серной кислоте и соляной кислоте он легко растворяется :
2Al + 3h3SO4 = Al2( SO4 ) + 3h3↑
С водными растворами щелочей алюминий взаимодействует , образуя тетрагидроксодиаквааюминат :
2Al + 2NaOH + 10h3O = 2Na[Al( OH )4( h3O )2] + 3h3↑
но могут получатся и гидроксоалюминаты Na[Al( OH )5] или Na3[Al( OH )6] .
Взаимодействие с галогенами при обычной температуре , алюминий образует галиды — летучие и гигроскопичные вещества , дымящие на воздухе вследствие гидролиза :
AlCl3 + h3O ⇄ AlOHHCl2 + HCl
Непосредственная реакция с неметаллами , алюминий образует нитрид AlN ( при 800°C ) , сульфид Al2S3 ( при 1000°C ) , карбид Al4C3 ( при 2000°C ) . С водородом алюминий не реагирует , а полимерный гидрид его ( Alh4 )n получают косвенным путём .
Оксид Al2O3 — единственный для алюминия — может получен при нагревании на воздухе мелкораздробленного металла или алюминиевой фольги :
2Al +³/2 O2 = Al2O3
Это белое тугоплавкое , нерастворимое в воде вещество . Встречается в виде минерала корунда , занимающего по плотности 2 место после алмаза . Прозрачные кристаллы корунда бывают окрашены в красный или синий цвет ( рубин и сапфир ) . В настоящее время рубины получают искусственно для технических целей . Кристаллы рубинов приобрели значение как квантовые усилители ( генераторы ) электромагнитных излучений ; усилителями радиоволн называют мазерами , а усилителями световых волн — лазерами .
Непрозрачные , содержащие много примесей кристаллы корунда , известны как наждак , применяемый для шлифовки и обработки металлов .
Оксид алюминия амфотерен . При сплавлении его с едкими щелочами получаются соли мета алюминиевой кислоты HAlO2 например мета алюминат калия :
Al2O3 + 2KOH = 2KAlO2 + h3O
Он взаимодействует и с кислотами :
Al2O3 + 6HCl = 2AlCl3 + 3h3O
Но сильно прокаленный оксид алюминия не растворяется ни в кислотах , ни в щелочах .
Измельченный и активированный метаалюминатом натрия оксид алюминия используют как минеральный ионообменник под названием ( окись алюминия для хроматографии )
Гидроксид алюминия Al( OH )3 осаждают , действуя щелочами на растворы солей :
AlCl3 + 3NaOH = Al( OH )3 + 3NaCl
Белый студенистый осадок гидроксида алюминия растворяется в кислотах :
Al( OH )3 + 3HCl = AlCl3 + 3h3O
Растворяется в избытке растворов щелочей :
Al( OH )3 + NaOH = Na[Al( OH )4]
то есть проявляет амфотерность .
Формула Na[Al( OH )4] не вполне соответствует составу продукта реакции , в действительности у алюминия координационное число равно шести и получается тетрагидрооксодиакваалюминат натрия :
Al( OH )3 + OH⁻ + 2h3O = [Al( OH )4( h3O )2]⁻
Но при сплавлении со щелочами гидроксид алюминия образует соли метаалюминиевой или ортоалюминиевой кислот :
Al( OH)3 + NaOH = NaAlO2 + 2h3O
или ортоалминат натрия :
Al( OH )3 + 3NaOH = Na3AlO3 + 3h3O
У гидроксида алюминия основные и кислотные свойства выражены приблизительно одинаково .
Соли алюминия хорошо растворимы в воде , легко гидролизуются и некоторые из них ( Al2S3 ) то есть на основание и кислоту .Хлорид алюминия AlCl3 известен как катализатор в органическом синтезе .
Сульфат алюминия Al2( SO4 )3 · 18h3O применяется для очистки природных вод от коллоидных частиц , которые захватываются гидроксидом алюминия , образующимся при гидролизе соли .
Сульфат калия — алюминия ( алюмокалиевые квасцы ) KAl( SO4 )2 · 12h3O применяется в кожевенной промышленности , служит протравой при крашении хлопчатобумажных тканей .
Применение
Малая плотность , пластичность и устойчивость к коррозии обеспечили алюминию применение в авиа — и автопромышленности . Он входит в состав лёгких сплавов : дуралюмина ( сплав алюминия , меди , магния и марганца ) , силумина ( сплава алюминия и кремния ) и некоторых других . Из алюминиевых сплавов изготовляют корпуса искусственных спутников Земли и космических кораблей .
В электротехнике алюминий заменил медь как материал для изготовления проводов . Используется как восстановитель при выплавке металлов ( алюминотермия ) :
Cr2O3 + 2Al = 2Cr + Al2O3
Алюминотермию , открыл Н.Н. Бекетовым в 1859 г. применяют и для сварки металлических деталей . При этом смесь порошкообразных алюминия и оксида железа ( II , III ) Fe3O4 называемую термитом :
8Al + 3Fe3O4 = 9Fe + 4Al2O3
в результате реакции развивается температура около 3000°C , получившееся железо плавится , стекая вниз и сваривает детали .
Помимо технического алюминий имеет также большое биологическое значение . Низкие концентрации ионов алюминия стимулируют некоторые процессы жизнедеятельности растений , например прорастание семян . Но более высокие концентрации ( > 2 мг/л раствора ) , снижают интенсивность фотосинтеза , нарушают фосфорный обмен , задерживают рост корневой системы .
Присутствие катионов Al в почве отчасти обусловливает вредную для растений обменную кислотность почвенного раствора . Ионы алюминия обычно поглощаются почвенными коллоидами , но под действием нейтральных солей ( например , хлорид калия ) они вытесняются из почвенного поглощающего комплекса .
В результате катионообменного процесса ионы алюминия переходят в почвенный раствор . Получившаяся при этом соль гидролизуется :
AlCl3 + h3O ⇄ HCl + Al( OH )Cl2
В результате гидролиза происходит нежелательное повышение концентрации водородных ионов в почвенном растворе ( понижение величины pH ) .
Вы читаете, статья на тему алюминий
znaesh-kak.com
У чего электропроводность больше? у алюминия или у меди?
Ответ. Удельное сопротивление меди 1,7*10^-8, а у алюминия- 2,8*10^-8.
Электропроводность алюминия всего в 1,7 раза меньше, чем у меди
электропроводность величина обратная удельному сопротивлению привет
У меди блин! в таблицах смотри!!!!
touch.otvet.mail.ru
электропроводность меди лучше , чем у алюминия.Почему же провода высокого напряжения делают из алюминия?
Во-первых, он существенно дешевле. Во-вторых, легче (особенно актуально для ЛЭП) . Вообще, у алюминия один недостаток: очень легко ломается. Посему тонкие и низковольтные провода - из меди (чтобы не сломали) , толстые, высоковольтные, магистральные - алюминий.
дешевле а провода высокого напряжения делают из стали
потому что дешевле
Сопротивление меди больше, а значит, медные провода могут расплавиться
Вероятно он дешевле меди?
Дешевле! Сейчас стали делать омеднёные! так как он бежит по наружности провода !
более толстые алюминиевые провода проводят не хуже а стоят дешевле. золото кстати проводник намного лучше меди. А почему-то не используется массово
touch.otvet.mail.ru
Видеоматериалы
Опыт пилотных регионов, где соцнормы на электроэнергию уже введены, показывает: граждане платить стали меньше
Подробнее...С начала года из ветхого и аварийного жилья в республике были переселены десятки семей
Подробнее...Более 10-ти миллионов рублей направлено на капитальный ремонт многоквартирных домов в Лескенском районе
Подробнее...Актуальные темы
ОТЧЕТ о деятельности министерства энергетики, ЖКХ и тарифной политики Кабардино-Балкарской Республики в сфере государственного регулирования и контроля цен и тарифов в 2012 году и об основных задачах на 2013 год
Подробнее...Предложения организаций, осуществляющих регулируемую деятельность о размере подлежащих государственному регулированию цен (тарифов) на 2013 год
Подробнее...
КОНТАКТЫ
360051, КБР, г. Нальчик
ул. Горького, 4
тел: 8 (8662) 40-93-82
факс: 8 (8662) 47-31-81
e-mail:
Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.