Метан, структурная формула, химические, физические свойства
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Алканы
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Метан физические свойства — Справочник химика 21
Углеводородные газы резко отличаются друг от друга по температурам кипения. Метан может перейти в жидкое состояние лишь при очень низких температурах. Жидкий метан кипит и превращается в газ лишь при температуре —161° С. Критическая температура метана —82° С. Следовательно, в толщах горных пород, где температура выше 0° С, ни при каком давлении метан не перейдет в жидкое состояние. Этан кипит при довольно низкой температуре (—88° С), но его критическая температура 32° С, поэтому при температуре более низкой чем 32° С и при достаточном давлении этан может перейти в жидкое состояние. Еще легче переводят в жидкое состояние пропан, бутан и изобутан. Например, для того чтобы при комнатной температуре перевести эти углеводороды в жидкое состояние, требуется давление для пропана 7—8 ат, для изобутана около 3 ат и для бутана около 2 ат. В табл. 6 приведены основные физические свойства углеводородных и некоторых других газов. [c.235]
В табл. 6 приведены основные физические свойства углеводородных и некоторых других газов. [c.235]
Рассматривая физические свойства углеводородных газов, следует отметить большое различие их плотностей. Метан является наиболее легким из углеводородных газов, его плотность составляет 0,55 по отношению к атмосферному воздуху. Плотность этана близка к плотности воздуха. Пропан и бутан уже значительно тяжелее. Пары жидких углеводородов имеют плотность в 3—4 раза большую, чем плотность воздуха. [c.235]
Изотермические емкости для хранения сжиженных газов. Метан, этан, этилен в виде жидкой фазы в силу их физических свойств практически невозможно хранить в емкостях под давлением. Для этой цели применяют изотермические резервуары, в которых эти продукты хранятся под атмосферным давлением при температуре кипения. В ряде случаев пропан, бутан или их смеси (ПБФ, ШФЛУ) целесообразно хранить также в изотермических емкостях. Температура хранения для каждого [c.278]
Температура хранения для каждого [c.278]
В трех запаянных ампулах находятся три разных газа метан, углекислый газ, ацетилен. Опишите, как, основываясь на различии в химических и физических свойствах, можно надежно определить, где какой газ находится. Приведите необходимые уравнения реакции. [c.61]
Гомологические ряды неразветвленных алканов обнаруживают плавное изменение физических свойств (см. табл. 2.3 и рис. 2.1.1) [12]. Метан, этан, пропан и бутан в обычных условиях — газы, углеводороды С5—С17 — жидкости, высшие углеводороды — твердые вещества. Все алканы легче воды и не растворяются в ней. [c.71]
Раздел 2. Метан Основные физические свойства метана [c.9]
Метан — бесцветный газ, в жидком состоянии его плотность меньше плотности воды (уд. вес. 0,4). В соответствии с правилом подобное растворяется в подобном он очень плохо растворим в воде, но хорошо растворим в органических жидкостях, таких, как бензин, эфир и спирт. Физические свойства метана сходны со свойствами других членов ряда алканов. [c.41]
Физические свойства метана сходны со свойствами других членов ряда алканов. [c.41]
Некоторые физические свойства используемых в настоящее время геттеров приведены в табл. 7. Из всех геттеров, указанных в таблице, наибольшее распространение получил титановый, который при распылении сорбирует значительные количества кислорода, азота, двуокиси и окиси углерода, водорода и паров воды. Инертные газы, а также метан и другие углеводороды сорбируются титаном слабо. В атмосфере поверхность титана быстро покрывается прочной и непроницаемой пленкой окислов, нитридов и карбидов, которые предотвращают дальнейшую реакцию газов с металлом. Высокая активность титана наряду со сравнительно высокой скоростью испарения и низкой стоимостью предопределили его широкое использование как геттера. [c.55]
Относительно других физических свойств предельных углеводородов следует упомянуть/ что газообразные члены ряда (метан, этан) не обладают запахом легко летучие низшие парафины имеют запах бензина , а высшие углеводороды вследствие слишком малой летучести не вызывают уже никакого ощущения запаха. [c.37]
[c.37]
Безопасность работы с метаном требует знаний не тельно правил техники безопасности, но и физических свойств метана [c.220]
Физические свойства веществ находятся в определенной зависимости от их состава и строения. Так, типичные соединения водорода с неметаллами представляют собой или газы (как НС1, HjS, NHj и др.), или низкокипящие жидкости (как Н2О). Метан, этан, пропан и бутан также представляют собой газы (табл. I). [c.23]
Важную роль в структурообразовании играют газовые компоненты нефти азот, метан и этан. Растворенные в нефти, эти газы в зависимости от их количества изменяют ее физические свойства вязкость, объемную упругость, теплоемкость и т. д. [c.8]
Отсутствие неподеленных пар в молекуле СН4, во-первых, приводит к заметному упрочнению связей и, во-вторых, делает метан гораздо менее реакционноспособным по сравнению с соединениями элементов 15-17 й групп. Высокая симметрия sp -гиб-ридных орбиталей приводит к тому, что тетраэдрические молекулы метана лишены дипольного момента и поэтому межмолекулярные силы слабы, а отсутствие неподеленных пар на атомах углерода делает невозможным образование водородных связей в жидком СН4, что сразу же сказывается на его физических свойствах. [c.305]
Высокая симметрия sp -гиб-ридных орбиталей приводит к тому, что тетраэдрические молекулы метана лишены дипольного момента и поэтому межмолекулярные силы слабы, а отсутствие неподеленных пар на атомах углерода делает невозможным образование водородных связей в жидком СН4, что сразу же сказывается на его физических свойствах. [c.305]
Физические свойства и распростр нение в природе. Метан — бесцветный газ, почти вдвое легче воздуха, мало растворимый в воде, но хорошо в нефти и других органических растворителях. Его иначе называют болотным, или рудничным, газом, так как он выделяется со дна болот и нередко содержится в воздухе угольных шахт и рудников. В болотах он образуется при разложении растительных и животных остатков без доступа воздуха. Много его растворено в нефти. В нефтеносных районах метан с небольшой примесью других газов выделяется иногда из земли. Эту смесь называют природным газом. Некоторые месторождения природного газа содержат громадные количества метана (до 80—90%). В СССР крупные газоносные районы расположены в Поволжье (Саратов и др.), на Северном Кавказе (Ставрополь), Украине (Прикарпатье и др.), в Зауралье (Березовское) и в других местах. [c.194]
В СССР крупные газоносные районы расположены в Поволжье (Саратов и др.), на Северном Кавказе (Ставрополь), Украине (Прикарпатье и др.), в Зауралье (Березовское) и в других местах. [c.194]
Природные и нефтяные газы — это источники ценного углеводородного сырья для нефтехимической и химической промышленности. Основной компонент этих газов — метан, по физическим свойствам он резко отличается от других компонентов газа. На различии физических констант компонентов основаны процессы, применяемые для извлечения из газа целевых компонентов и их разделения. [c.212]
Примером влияния водородной связи на химические и физические свойства веществ является повышенная растворимость различных веществ в растворителях, содержащих электронодонорные атомы азота и кислорода (амины, эфиры). Причем растворимость растет по мере замещения водорода в метане или этане на галоген, например, от СНзС1 до СНС1з- Но при переходе к ССЬ растворимость резко падает. Это объясняется тем, что при увеличения числа атомов галогена повышается подвижность оставшихся в молекуле атомов водорода. При замещении же последнего из них на галоген исключается самая возможность возникновения водородной связи. [c.23]
При замещении же последнего из них на галоген исключается самая возможность возникновения водородной связи. [c.23]
На рис. 5.6 показана принципиальная технологическая схема станции, на которой слив сжиженного газа осуществляют с помощью газов под необходимым давлением. Например, при сливе хлора используют сжатый воздух, окиси этилена — азот, сжиженных углеводородных газов — природный газ, технологические газы е химико-физическими свойствами, аналогичными транспортируемому продукту, а также метан, азот, двуокись углерода. [c.77]
Физические свойства. Метан — бесцветный газ, лишенный запаха, мало растворим в воде (в 100 объемах воды при 20°С растворяется 9 объемов метана), легче воздуха. [c.27]
Для выяснений той роли, которую вода играет в нашем природном окружении, важно знать ее физические свойства в твердом, жидком и газообразном состояниях. Поэтому полезно начать с напоминания о некоторых особых свойствах воды, описанных в предыдущих главах. Для вещества с такой небольшой молекулярной массой вода обладает необычно высокими температурами плавления и кипения (см. разд. 11.5, ч. 1). Метан СН , имеющий приблизительно такую же молекулярную массу, как и вода, кипит при 89 К, в то время как вода кипит при 373 К. Вода обладает необьино высокой удельной теплоемкостью, равной 4,184 Дж/(г град). Удельная теплоемкость большинства простых органических жидкостей составляет лишь приблизительно половину указанной величины. Это означает, что при поглощении определенного количества теплоты температура воды повышается на меньшую величину, чем у многих других жидкостей. Теплота испарения воды тоже необычно высока, т.е. для испарения одного грамма воды требуется больше теплоты, чем для испарения [c.143]
Для вещества с такой небольшой молекулярной массой вода обладает необычно высокими температурами плавления и кипения (см. разд. 11.5, ч. 1). Метан СН , имеющий приблизительно такую же молекулярную массу, как и вода, кипит при 89 К, в то время как вода кипит при 373 К. Вода обладает необьино высокой удельной теплоемкостью, равной 4,184 Дж/(г град). Удельная теплоемкость большинства простых органических жидкостей составляет лишь приблизительно половину указанной величины. Это означает, что при поглощении определенного количества теплоты температура воды повышается на меньшую величину, чем у многих других жидкостей. Теплота испарения воды тоже необычно высока, т.е. для испарения одного грамма воды требуется больше теплоты, чем для испарения [c.143]
При радиолизе алканов образуются не только метан и водород, но и насыщенные углеводороды с низким молекулярным весом — продукты с содержанием углеродных атомов, большим, чем в исходной молекуле, и ненасыщенные углеводороды с различным молекулярным весом. В основном выход разложения алканов находится между 6 и 10. Для алканов с прямой цепью количество продуктов радиолиза (см. табл. 9.1) с числом атомов углерода меньше, чем в материнском соединении, уменьшается по мере возрастания длины цепи и одновременно повышается доля высокомолекулярных продуктов. Таким образом, излучение в данном случае увеличивает средний молекулярный вес углеводородов, что легко заметить по изменению физических свойств облучаемого материала. Например, в жидких системах появляются нерастворимые гели, а у твердых соединений возрастает температура плавления. Эти явления хорошо изучены при сшивании цепей облучаемого полиэтилена (см. гл. И). [c.277]
В основном выход разложения алканов находится между 6 и 10. Для алканов с прямой цепью количество продуктов радиолиза (см. табл. 9.1) с числом атомов углерода меньше, чем в материнском соединении, уменьшается по мере возрастания длины цепи и одновременно повышается доля высокомолекулярных продуктов. Таким образом, излучение в данном случае увеличивает средний молекулярный вес углеводородов, что легко заметить по изменению физических свойств облучаемого материала. Например, в жидких системах появляются нерастворимые гели, а у твердых соединений возрастает температура плавления. Эти явления хорошо изучены при сшивании цепей облучаемого полиэтилена (см. гл. И). [c.277]
При изучении процессов фиксации азота обычно приходится иметь дело с шестью газами, а именно с водородом, азотом, аммиаком, метаном, окисью углерода, двуокисью углерода и их смесями. Настоящая глава представляет сводку наиболее важных физических свойств этих шести газов и их смесей. [c.194]
[c.194]
Физические свойства. Метан СН4 — первый член ряда предельных углеводородов. Бесцветный, не имеющий запаха газ, плотность его по отношению к воздуху 0,554 (20°С) 1 г метана занимает объем 1520 мл (25°С, 101,3 кПа) в воде растворим очень мало. Объясняется это тем, что химические связи в молекуле метана имеют неполярный ковалентный характер и молекулы метана тоже неполярны, поэтому они не взаимодействуют с полярными молекулами воды. [c.238]
В органической химии парафинами называются предельные углеводороды алканового (алифатического, или жирного) ряда, имеющие формулу СпНгп+з, вне зависимости от их места, занимаемого в этом ряду, а также от физических свойств и химической структуры. Так, парафинами в органической химии считаются в равной степени и газообразный метан СН4, и н-гептаконтан С7оН]42, плавящийся при 105,2 °С. [c.7]
В гомологическом ряду наблюдается постепенное изменение физических свойств углеводородов повышаются температуры кипения и плавления, возрастает плотность. При обычных условиях (температура 22°С) первые четыре члена ряда (метан, этан, пропан, бутан) — газы, с СбНха до С1вНз4 — жидкости, а с С Нд, — твердые вещества. [c.281]
При обычных условиях (температура 22°С) первые четыре члена ряда (метан, этан, пропан, бутан) — газы, с СбНха до С1вНз4 — жидкости, а с С Нд, — твердые вещества. [c.281]
Как видно из табл. 3.1, удельная массовая теплота сгорания у одорода выше в 2,4 раза, а объемная — ниже в 3,3 раза, чем у втана. Температура кипения у водорода на 86,7 К ниже, чем у ме-Водород более пожароопасен и взрывоопасен, чем метан, олее подробно физические свойства водорода рассмотрены в Де книг и обзоров [14 46]. [c.151]
Физические свойства. Низшие тиолы — жидкости (за исключением метан-тиола) с сильным неприятным запахом. Обоняние человека обнаруживает в воздухе ничтожные количества тиола (1 часть метантиола на 5-10 частей воздуха). Поэтому некоторые тиоспирты (например, пентантиол) добавляют к природному газу в качестве одоранта (от лат. odoratio — запах) для обнаружения его утечки в газопроводах. [c.185]
Неполярные соединения. Физические свойства рассматриваемых в этом разделе неполярных соединений зависят от межмолекулярной ассоциации молекул в жидком и твердом состояниях. Силы иритяження (силы Ван-дер-Ваальса) растут с поляризуемостью этих молекул. Повышение температуры плавления и кипения при переходе от соединений с более низким молекулярным весом к соединениям с более высоким молекулярным весом в гомологических рядах обусловлено наконлением слабых ван-дер-ваальсовых взаимодействий. Две молекулы метана могут вступать во взаимодействие только посредством двух пар водородных атомов, между тем как две виолне вытянутые молекулы /(-декана имеют пять точек контакта, подобных одной паре в метане. Две вполне вытянутые молекулы к-декана изображены на рис. 7.5. [c.162]
Силы иритяження (силы Ван-дер-Ваальса) растут с поляризуемостью этих молекул. Повышение температуры плавления и кипения при переходе от соединений с более низким молекулярным весом к соединениям с более высоким молекулярным весом в гомологических рядах обусловлено наконлением слабых ван-дер-ваальсовых взаимодействий. Две молекулы метана могут вступать во взаимодействие только посредством двух пар водородных атомов, между тем как две виолне вытянутые молекулы /(-декана имеют пять точек контакта, подобных одной паре в метане. Две вполне вытянутые молекулы к-декана изображены на рис. 7.5. [c.162]
Первые четыре представителя гомологического ряда—метан, этан, пропан, бутан и изобутан —это газы, входящие в состав природных горючих газов, а также растворенные в нефти. Следующие представители — жидкости, начиная с С16Н34 —твердые вещества. Формула каждого следующего члена гомологического ряда метана отличается от предыдущей на СНг. Нужно подчеркнуть, что это отличие выражается в изменениях физических свойств членов гомологического ряда, например в повышении температуры кипения, т. е. наблюдается переход количественных изменений в качественные. [c.49]
е. наблюдается переход количественных изменений в качественные. [c.49]
Если рассмотреть два органических вещества — СН4 (метан)и СН3ОН (метиловый спирт), то, кроме бросающихся в глаза различий в физических свойствах (газ и жидкость), можно заметить глубокие различия в химических свойствах реакции спирта с Na, H l и т. д. показывают, что один атом кислорода, введенный в молекулу, преображает ее. Кислород в молекуле — это не прос- [c.80]
Для образования большого количества полимера требуется легкодоступный и дешевый источник углерода. Ферментация позволяет культивировать организм-продуцент в строго определенных условиях среды, контролируя, таким образом, процесс биосинтеза и влияя на тип продукта и его свойства. Специфи- чески изменяя условия роста, можно менять молекулярную массу и структуру образующегося полимера, В ряде случаев максимальная скорость синтеза полисахарида достигается в логарифмической стадии роста, в других — в поздней логарифмической или в начале стационарной. Обычно углеводными субстратами служат глюкоза и сахароза, хотя полисахариды могут образовываться и при росте микроорганизмов на н-алка-,яах( С12-61), керосине, метаноле, метане, этаноле, глицероле и этиленгликоле. Недостатком проведения процесса в ферментерах является то, что среда часто становится очень вязкой, поэтому культура быстро начинает испытывать недостаток кислорода мы все еще не умеем рассчитывать соотношение между скоростью перемешивания неньютоновских жидкостей и подачей кислорода. Необходимо также контролировать быстрые изменения pH среды. И все же упомянутый метод позволяет быстро синтезировать полимер для того, чтобы определить его физические свойства, а также дает возможность оптимизировать состав среды, главным образом в отношении эффективно- сти различных углеводных субстратов. Часто в качестве лимитирующего фактора применяют азот (соотношение углерод азот — 10 1), хотя можно использовать и другие (серу, магний, калий и фосфор). Природа лимитирующего фактора способна определять свойства полисахарида, например его вяз- костные характеристики и степень ацилирования.
Обычно углеводными субстратами служат глюкоза и сахароза, хотя полисахариды могут образовываться и при росте микроорганизмов на н-алка-,яах( С12-61), керосине, метаноле, метане, этаноле, глицероле и этиленгликоле. Недостатком проведения процесса в ферментерах является то, что среда часто становится очень вязкой, поэтому культура быстро начинает испытывать недостаток кислорода мы все еще не умеем рассчитывать соотношение между скоростью перемешивания неньютоновских жидкостей и подачей кислорода. Необходимо также контролировать быстрые изменения pH среды. И все же упомянутый метод позволяет быстро синтезировать полимер для того, чтобы определить его физические свойства, а также дает возможность оптимизировать состав среды, главным образом в отношении эффективно- сти различных углеводных субстратов. Часто в качестве лимитирующего фактора применяют азот (соотношение углерод азот — 10 1), хотя можно использовать и другие (серу, магний, калий и фосфор). Природа лимитирующего фактора способна определять свойства полисахарида, например его вяз- костные характеристики и степень ацилирования. Так, многие оолисахариды, синтезируемые грибами, фосфорилированы. При недостатке фосфора степень фосфорилирования может уменьшаться или становиться равной нулю в этих условиях может даже измениться соотношение моносахаридов в конечном по- [c.219]
Так, многие оолисахариды, синтезируемые грибами, фосфорилированы. При недостатке фосфора степень фосфорилирования может уменьшаться или становиться равной нулю в этих условиях может даже измениться соотношение моносахаридов в конечном по- [c.219]
Эти гидриды во всех агрегатных состояниях существуют в виде одних и тех же молек л. Когда твердый метан превращается последовательно в жидкость и газ, то не происходит никаких перестановок атомов углерода и водорода относительно друг друга структура молекулы СН4 сохраняется во всех этих состояниях. Между молекулами действуют только слабые ван-дер-ваальсовские силы это Идмеет. место для всех молекулярных гидридов, за исключением гидридов самы.ч электроотрицательных эле.ментов первого короткого периода (азот, кислород и фтор . Физические свойства МН.,, ОН., и РН во многих отношениях отклоняются от нормы, особенно в жидком и твердом состоянии, вследствие образования междумолеку.тярных водородных связей. В одном из следующих разделов мы вернемся к рассмотрению гидридов с этой точки зрения. Во многих случаях твердые вещества образуют плотно упакованные структуры, в которых вращаются молекулы (например, кубические плотно упакованные структуры СН , РНл, АзНд, ЗНг, ЗеН, и т. д.). [c.282]
Во многих случаях твердые вещества образуют плотно упакованные структуры, в которых вращаются молекулы (например, кубические плотно упакованные структуры СН , РНл, АзНд, ЗНг, ЗеН, и т. д.). [c.282]
Методы получения и некоторые простые реакции присоединения альдегидов и кетонов Ч.1 (0) — [
c.90
,
c.385
]
Начала органической химии Книга первая (1969) — [
c.62
,
c.63
]
Органическая химия Том1 (2004) — [
c.139
]
Основы органической химии (1968) — [
c.72
]
Основы органической химии 1 Издание 2 (1978) — [
c.86
,
c.87
]
Основы органической химии Часть 1 (1968) — [
c. 72
72
]
Основные начала органической химии Том 1 Издание 6 (1954) — [
c.162
,
c.170
]
Холодильная техника Кн. 1 (1960) — [
c.444
]
Общая химическая технология Том 1 (1953) — [
c.288
,
c.308
]
Методы органической химии Том 2 Издание 2 (1967) — [
c.798
]
Методы органической химии Том 2 Методы анализа Издание 4 (1963) — [
c.798
]
Начала органической химии Кн 1 Издание 2 (1975) — [
c.58
,
c.59
]
ICSC 0291 — МЕТАН
ICSC 0291 — МЕТАН
| МЕТАН | ICSC: 0291 (Февраль 2000) |
| CAS #: 74-82-8 |
| UN #: 1971 |
| EINECS #: 200-812-7 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Чрезвычайно легковоспламеняющееся. Смеси газа с воздухом взрывоопасны. Смеси газа с воздухом взрывоопасны. | НЕ использовать открытый огонь, НЕ допускать образование искр, НЕ КУРИТЬ. Замкнутая система, вентиляция, взрывозащищенное электрическое оборудование и освещение. Использовать ручной инструмент, не образующий искры. | Перекрыть поступление; если невозможно и нет риска для окружения, дать огню прогореть. В других случаях тушить распыленной водой, порошком, двуокисью углерода. В случае пожара: охлаждать баллон распыляя воду. Бороться с огнем из укрытия. |
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
|---|---|---|---|
| Вдыхание | Удушье. См. примечания. | Применять вентиляцию. Применять средства защиты органов дыхания. | Свежий воздух, покой. Может потребоваться искусственное дыхание. Обратиться за медицинской помощью. Обратиться за медицинской помощью. |
| Кожа | ПРИ КОНТАКТЕ С ЖИДКОСТЬЮ: ОБМОРОЖЕНИЕ. | Перчатки для защиты от холода. | ПРИ ОБМОРОЖЕНИИ: промыть большим количеством воды, НЕ удалять одежду. обратиться за медицинской помощью . |
| Глаза | ПРИ КОНТАКТЕ С ЖИДКОСТЬЮ: ОБМОРОЖЕНИЕ. | Использовать защитные очки. | Прежде всего промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений), затем обратится за медицинской помощью. |
| Проглатывание | |||
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
Покинуть опасную зону! Индивидуальная защита: автономный дыхательный аппарат. Проконсультироваться со специалистом! Вентилировать. Удалить все источники воспламенения. НИКОГДА не направлять струю воды на жидкость. Проконсультироваться со специалистом! Вентилировать. Удалить все источники воспламенения. НИКОГДА не направлять струю воды на жидкость. |
Согласно критериям СГС ООН
Транспортировка |
| ХРАНЕНИЕ | |
| Обеспечить огнестойкость. Прохладное место. Вентиляция вдоль пола и потолка. | |
| УПАКОВКА | |
Исходная информация на английском языке подготовлена группой международных экспертов, работающих от имени МОТ и ВОЗ при финансовой поддержке Европейского Союза. |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
|
Агрегатное Состояние; Внешний Вид
Физические опасности
Химические опасности
|
Формула: CH4 |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
|
Пути воздействия
Эффекты от кратковременного воздействия
|
Риск вдыхания
Эффекты от длительного или повторяющегося воздействия
|
| Предельно-допустимые концентрации |
|---|
|
|
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| ПРИМЕЧАНИЯ |
|---|
| Density of the liquid at boiling point: 0.42 kg/l. Высокие концентрации в воздухе вызывают дефицит кислорода с риском потери сознания или смерти. Проверьте содержание кислорода перед тем, как войти.  Поверните протекающий цилиндр местом протечки вверх, чтобы предотвратить утечку газа в жидком состоянии. After use for welding, turn valve off; regularly check tubing, etc., and test for leaks with soap and water. The measures mentioned in section PREVENTION are applicable to production, filling of cylinders, and storage of the gas. Other UN number: 1972 (refridgerated liquid), Hazard class: 2.1. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
|
Классификация ЕС Символ: F+; R: 12; S: (2)-9-16-33 |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Все об угарном газе — Новости
В домашнем хозяйстве в Эстонии используется два типа газа – природный газ и сжиженный газ. Природный газ поступает к нам из России по длинным газопроводам, и в Эстонии распределяется по разным потребителям. Сжиженный газ, однако, хранится в баллонах и его распределение происходит баллонами.
В больших районах установлены специальные подземные газохранилища, откуда газ поступает пользователям по трубам. Поэтому стоит знать, что хозяйственный газ, который находится в баллонах – это сжиженный газ, а газ, который мы получаем по трубам, в зависимости от района, может быть, как природный, так и сжиженный.
Что такое природный газ?
- Основной составляющей природного газа является метан – это газ без цвета и запаха. Для того чтобы обнаружить утечку газа к нему добавлено немного веществ для усиления запаха.
- Природный газ легче воздуха, поэтому в случае утечки, перемешавшись с воздухом, он поднимается наверх. Всегда стоит помнить, что вентиляция или иные потоки воздуха могут направить газ и в сторону.
 Это означает, что обычно в случае утечки газа в опасности находятся квартиры сверху, но газ может и двигаться в соседние квартиры.
Это означает, что обычно в случае утечки газа в опасности находятся квартиры сверху, но газ может и двигаться в соседние квартиры. - Природный газ оказывает на людей удушающее воздействие. Это не очень ядовитый газ. Скорее он обладает наркотическими свойствами. Если газом наполнено приблизительно 10% помещения, то он вызывает сонливость, головную боль и плохое самочувствие. Если содержание газа в квартире поднимается до 20-30%, то происходит нехватка кислорода, что может вызвать удушение.
Что такое сжиженный газ?
- Основной составляющей сжиженного газа является пропан. Как и метан, пропан бесцветный и не имеет запаха. Чтобы человек обнаружил в хозяйстве утечку газа, то к нему добавляется немного веществ для усиления запаха. Из-за таких веществ у газа появляется четко выраженный запах.
- Пропан не ядовитый газ, но попав в воздух в больших количествах и в условиях уменьшения кислорода, может возникнуть удушение. Вдыхая такой газ, может возникнуть головокружение, сонливость, тошнота и слабость.

- Пропан тяжелее воздуха и поэтому, в случае утечки, газ оседает на пол, в подвал, в канализации и прочие углубления. Поэтому в случае утечки газа в опасности находятся квартиры на низких этажах и подвалы.
Что такое угарный газ?
- Даже обычное пригорание еды дома может вызвать угарный газ, а как следствие этого — отравление. Однако, в домах и квартирах основной причиной возникновения угарного газа является рано закрытая печная заслонка, плохо отрегулированная газовая плита или газовый бойлер с плохой тягой.
- По своим свойствам угарный газ, или монооксид углерода (CO), представляет собой не имеющий цвета, запаха и вкуса отравляющий газ и распространяется совершенно незаметно для человека. Чаще всего при пожарах люди погибают именно вследствие вдыхания отравляющего дыма.
- Из-за попадания угарного газа в организм человека, кровь теряет возможность переносить кислород. Гемоглобин, который должен переносить кислород в крови, наоборот, начинает переносить угарный газ.
 В следствии этого в организме человека образуется опасное вещество – карбоксигемоглобин.
В следствии этого в организме человека образуется опасное вещество – карбоксигемоглобин. - Количество кислорода в различных частях тела снижается, так как гемоглобин больше не доставляет туда кислород. Человек начинает задыхаться. Одним разом сердце выбрасывает в организм почти один стакан крови, и угарный газ попадает через легкие в другие части тела очень быстро.
- Отравившись угарным газом, мы не понимаем масштаб ситуации. Человек находится в замешательстве и не может себе помочь, хотя и чувствует, что с ним что-то не так. Человек может и не сопоставить эти симптомы с отравлением угарным газом, а находясь во сне и вовсе ничего не почувствовать.
- Симптомы зависят от количества газа. От маленького количества может возникнуть пульсация в висках, сонливость, слабость, головная боль, потеря равновесия, шум в ушах, слабость в ногах, тошнота и рвота. Позднее могут возникнуть галлюцинации, учащение пульса, поднятие давления, может возникнуть слабость, сонливость, потеря давления, осложнения при дыхании.
 При сильном отравлении человек теряет сознание и наступает смерть.
При сильном отравлении человек теряет сознание и наступает смерть. - Человек может умереть от отравления угарным газом без имеющегося возгорания. Например, когда печную заслонку закрывают слишком рано, или газовый прибор работает в условиях кислородного голодания и как следствие этого образуется угарный газ. Также угарный газ может к вам просочится из соседних квартир.
- Дымовой датчик не способен обнаружить угарный газ. Чтобы на ранних стадиях обнаружить угарный газ необходим датчик угарного газа.
Типичные случаи
- Газовые установки бывают разных типов. Обычно несчастные случаи случаются с такими котлами, работа которых зависит от воздуха. Это означает, что для работы они получают необходимое количество воздуха с комнаты. Часто устанавливали такие котлы в закрытые шкафы.
- Также причиной может быть и утепление дома. Многие дома, в которых изначально имелась естественная вентиляция, уже утеплили, поменяли окна, сделали беспечную перестройку.
 Например, газовые установки соединили друг с другом в неподходящие дымоходы. Часто устанавливали такие газовые установки в закрытые шкафы. Со временем дымоходы забивались, а сгораемый воздух оставался в квартире.
Например, газовые установки соединили друг с другом в неподходящие дымоходы. Часто устанавливали такие газовые установки в закрытые шкафы. Со временем дымоходы забивались, а сгораемый воздух оставался в квартире. - Каждая газовая установка нуждается в регулярном контроле и обслуживании. Важно следить за тем чтобы из соединений труб не было утечки, а дымоход не был бы забитым.
- Газовое пламя обычно синего цвета. Если пламя зеленое, то это определенно указывает на опасность.
Кто несет ответственность?
- В квартирах и частных домах ответственность за работу и исправность газовых установок несет владелец. Необходимо проверять и обслуживать домашние газовые установки раз в год.
- За газовые трубы на лестничных площадках в многоквартирных домах ответственность несут члены товарищества.
- За строительство, контроль и обслуживание газовых приборов отвечает фирма, осуществляющая данные услуги. Человеческие жизни зависят от качества таких услуг.

- Государство осуществляет надзор над владельцами домов и квартир, а также предприятий за соблюдением данных предписаний.
Датчик угарного газа
- С 1 января 2018 года установка датчика угарного газа является обязательной во всех жилых помещениях, в которых находится подсоединенная к трубе газовая установка.
- Прежде всего к таким установкам относятся работающие на газе водонагреватели. Датчик угарного газа становится обязательным при наличии газового отопления, однако разумно установить соответствующий датчик во всех жилых помещениях, в которых находится связанное с процессами горения оборудование, например, печь на древесном топливе, камин, плита или газовый бойлер. Установка датчика является добровольной в том случае, если предприняты технические меры, исключающие утечку угарного газа и его попадание в жилое помещение, например, если забор воздуха для горения газовой установки осуществляется непосредственно из наружного воздуха и выделяемые при горении газы также выводятся непосредственно через предназначенную для этого трубу в наружный воздух.

- Датчик угарного газа дает сигнал только тогда, когда концентрация угарного газа в воздухе приближается к уровню, опасному для здоровья человека.
- Один датчик угарного газа предназначен для использования в одном помещении, так как устройство показывает только уровень СО, распространяющегося вблизи датчика.
Где установить датчик угарного газа?
- При установке датчика угарного газа необходимо в первую очередь следовать инструкциям производителя.
- В отличие от датчика дыма датчик угарного газа крепят на стену помещения, на высоте приблизительно 0,5-1,5 метра от пола. Опытные специалисты рекомендуют устанавливать датчик, так сказать, на уровне дыхательных путей человека, или на том уровне, на котором находится лицо человека, когда он сидит на диване, а в спальной комнате ‒ примерно на высоте подушки.
- Устройство устанавливают на расстоянии 1-3 метра от источника угарного газа, также не следует устанавливать датчик вблизи вентиляционных систем и воздуховодов.

- В доме из нескольких этажей рекомендуется установить датчики угарного газа на каждом этаже. По возможности также в каждой спальной комнате.
- Если газовый бойлер находится в ванной комнате, необходимо убедиться, что датчик угарного газа подходит для установки во влажных помещениях. Для этого датчик должен иметь обозначение IP, которое должно соответствовать уровню IP44.
- Датчики угарного газа не устанавливают в гаражах, на кухнях, в котельных, в ванных комнатах и в других местах, в которых температура опускается ниже 10°C или поднимается выше 40°C.
Как осуществлять уход?
- Проверять, находится ли датчик угарного газа в рабочем состоянии, необходимо раз в месяц, нажимая тестовую кнопку. Звуковой сигнал подтверждает, что устройство находится в рабочем состоянии.
- Датчик угарного газа необходимо регулярно очищать от пыли. Для этого можно использовать как пылесос, так и тряпку.
- Источником питания датчика угарного газа являются батарейки – прерывистый регулярный звуковой сигнал датчика свидетельствует об опустошении батареек.
 Это значит, что батарейку следует немедленно заменить.
Это значит, что батарейку следует немедленно заменить. - Дополнительную информацию о газовой безопасности для бытовых потребителей найдете
Что делать если сработал датчик угарного газа?
- Быстро открыть окна и двери и тщательно проветрить комнату.
- Выключить все отопительные системы или потушить огонь в печке или плите.
- Вызовите на место профессионального техника, который поможет разрешить проблему. До приезда техника сами не включайте отопительные приборы.
- Если заметили у кого-то симптомы отравления угарным газом, то немедленно выведите человека на свежий воздух, вызовите скорую
Статистика
Выезды Спасательного департамента на случаи, связанные с газом:
2015 – 291
2016 – 403
2017 – 421
2018* – 356
*По состоянию на 14 октября
Основные регионы, откуда часто поступают вызовы — Харьюмаа и Ида-Вирумаа. Города Таллинн, Кохтла-Ярве, Тарту и Нарва.
71% случаев происходит в жилых помещениях
60% в квартирах
25% на лестничных площадках
Возьмите на заметку!
- Никогда не осуществляйте ремонт газовых установок сами!
- Установите датчик угарного газа – он обязателен с 1 января 2018 года!
- Домашние газовые установки должен проверять и обслуживать специалист один раз в год! Дополнительные требования могут возникнуть из устройства по эксплуатации устройства.
- Дымоход газового устройства необходимо прочищать согласно инструкции. Если в инструкции по эксплуатации совет отсутствует, тогда это необходимо делать один раз в год. Дымоход может чистить только квалифицированный трубочист, который имеет соответствующее удостоверение.
- Строительство, ремонт и обслуживание могут производить только лица, имеющие необходимые для работы с газом навыки.
- Список фирм и их контактов на страничке Департамента технического надзора
- Наличие профессиональных навыков можно проверить по название предприятия на сайте
Плотность метана.
 Свойства газов метанового ряда Cnh3n+2
Свойства газов метанового ряда Cnh3n+2
В таблице указана плотность метана при различных температурах, включая плотность этого газа при нормальных условиях (при 0°С). Также приведены его теплофизические свойства и характеристики других газов метанового ряда.
Представлены следующие теплофизические свойства газов метанового ряда: коэффициент теплопроводности λ, динамическая вязкость η, число Прандтля Pr, кинематическая вязкость ν, массовая удельная теплоемкость Cp, отношение теплоемкостей (показатель адиабаты) k, коэффициент температуропроводности a и плотность газов метанового ряда ρ. Свойства газов даны при нормальном атмосферном давлении в зависимости от температуры — в интервале от 0 до 600°С.
К газам метанового ряда относятся углеводороды с брутто-формулой CnH2n+2 такие, как: метан CH4, этан C2H6, пропан C3H8, бутан C4H10, пентан C5H12, гексан C6H14, гептан C7H16, октан C8H18. Их еще называют гомологический ряд метана.
Их еще называют гомологический ряд метана.
Плотность газов метанового ряда при увеличении их температуры снижается из-за теплового расширения газа. Такой характер зависимости плотности от температуры свойственен и многим другим газам. Следует также отметить, что плотность газов метанового ряда растет по мере увеличения количества атомов углерода и водорода в молекуле газа (числа n в формуле CnH2n+2).
Наиболее легким газом из рассмотренных в таблице является метан — плотность метана при нормальных условиях равна 0,7168 кг/м3. Метан при нагревании расширяется и становиться менее плотным. Так, например при температуре 0°С и 600°С, плотность метана отличается приблизительно в 3 раза.
Теплопроводность газов метанового ряда снижается при увеличении числа n в формуле CnH2n+2. При нормальных условиях она изменяется в диапазоне от 0,0098 до 0,0307 Вт/(м·град). По данным в таблице следует, что наибольшей теплопроводностью обладает такой газ, как метан — его коэффициент теплопроводности, например при 0°С, равен 0,0307 Вт/(м·град).
Наименьшая теплопроводность (0,0098 Вт/(м·град) при 0°С) свойственна газу октану. Следует отметить, что при нагревании газов метанового ряда их теплопроводность увеличивается.
Удельная массовая теплоемкость газов, входящих в гомологический ряд метана при нагревании увеличивается. Также увеличивают свои значения такие их свойства, как вязкость и температуропроводность.
Источник:
Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
Измеряемые газы — НПЦ АТБ
Измеряемые газы
Метан (CH4)
Метан (Ch5) имеет относительную плотность 0,554. Характерными свойствами этого газа являются горючесть и способность давать взрывчатую смесь с воздухом.
Температура воспламенения метана равна 650-750°C, однако эта температура может быть выше и ниже указанных пределов в зависимости от рода воспламенителя, способа воспламенения, содержания метана в воздухе и др.
Для метана характерным является свойство воспламеняться при соприкосновении с источником высокой температуры не сразу, а через некоторый промежуток времени, величина которого зависит от температуры воспламенения: при 650°C время запаздывания составляет 10 с, при 1000°C оно падает до 1 с и ниже.
Взрывы метана в шахтах всегда сопровождаются двумя ударными волнами — прямой и обратной. Прямая волна образуется под действием раскаленных продуктов взрыва, обладающих чрезвычайно высоким давлением. Обратная волна образуется в результате последующего понижения давления в месте взрыва, что объясняется остыванием продуктов химической реакции и конденсацией содержащихся в них паров воды. Сила обратного удара несколько меньше, чем прямого. Однако в связи с тем, что он следует по тому пути, на котором прямая волна уже оказала определенное разрушительное действие, механические эффекты, вызванные обратной волной, могут быть сильнее, чем прямой.
При концентрации метана свыше 9,5% после первичного пламени, распространяющегося с огромной скоростью и сжигающего весь кислород воздуха, может наблюдаться вторичное пламя, проходящее вследствии дожигания оставшегося метана притекающим извне кислородом воздуха. Вторичное пламя движется в направлении, обратном пути прохождения первичного пламени, и имеет меньшую скорость.
Выработка, в которой произошел взрыв, заполняется раскаленной смесью газов, полностью лишенной кислорода или содержащей его в весьма малых количествах. Эта смесь в основном содержит азот и углекислый газ, а во многих случаях — примесь оксида углерода. Оксид углерода в такой смеси содержится в больших количествах в тех случаях, когда взрыв газа происходит в присутствии угольной пыли. Причем большое количество пыли может быть вызвано при распространении ударных волн.
Газы, непригодные для дыхания, из выработки, в которой произошел взрыв, распространяются по вентиляционной сети и являются главной причиной опасности пребывания в это время людей в шахте. Расследование последствий взрывов показывает, что не менее двух третей пострадавших шахтеров бывают поражены в результате отравления оксидом углерода или кислородного голодания и накопления углекислого газа в организме.
Оксид углерода (СО)
Оксид углерода или угарный газ (СО) — газ без цвета и запаха, относительная плотность 0,97.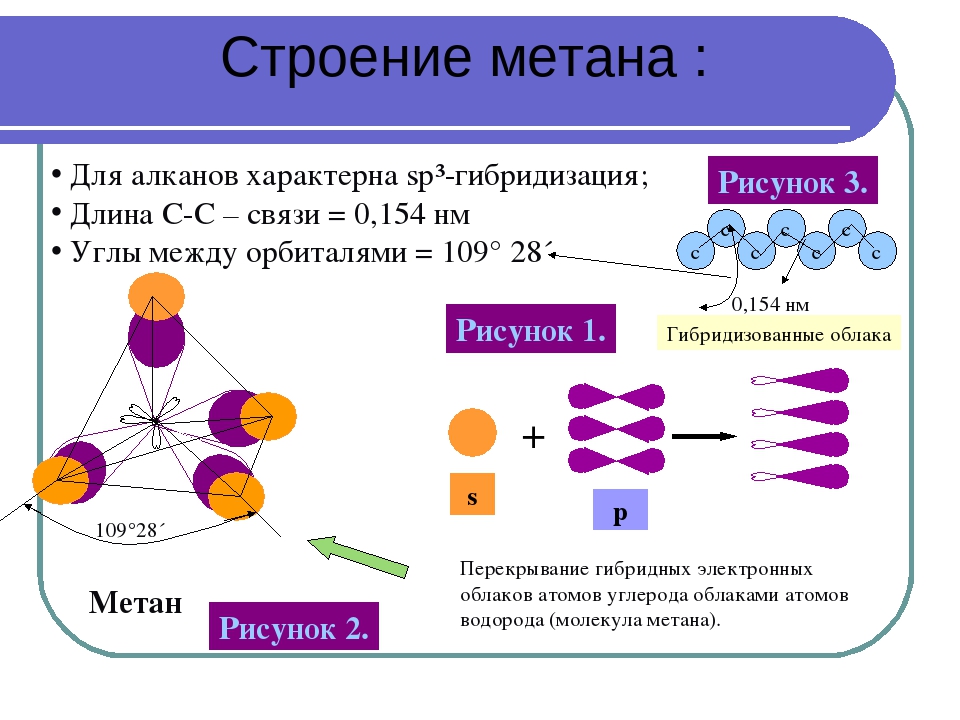 Слабо растворимый в воде, горит и при содержании в воздухе от 13 до 75% образует взрывчатые смеси с температурой воспламенения 630-810°C (наибольшая сила взрыва при 30% СО).
Слабо растворимый в воде, горит и при содержании в воздухе от 13 до 75% образует взрывчатые смеси с температурой воспламенения 630-810°C (наибольшая сила взрыва при 30% СО).
Главные источники образования СО в шахтах — низкотемпературное окисление угля, пожары, взрывы метана и пыли, взрывные работы и двигатели внутреннего сгорания.
Оксид углерода или угарный газ (СО) ядовит.
Сероводород (H2S)
Сероводород (h3S) — газ без цвета, с резким характерным запахом (тухлых яиц) и сладковатым вкусом, относительная плотность 1,17. Легко растворим в воде, образует с воздухом взрывчатую смесь, сильно ядовит.
Основными источниками сероводорода в шахтах являются гниение органических веществ, разложение водой серного колчедана, выделение из трещин и минеральных источников, эндогенные пожары, взрывные работы, взаимодействие сульфатных вод с метаном.
Кислород (О2)
Кислород (О2) — газ без цвета, вкуса и запаха, слабо растворим в воде, относительная плотность 1,105. По правилам безопасности в шахтах содержание кислорода в воздухе должно быть не менее 20%. Известно, что при содержании кислорода 18% у человека наступает сонливость, при 17% начинаются отдышка и усиленное сердцебиение, а при 12% и менее — возникает смертельная опасность.
По правилам безопасности в шахтах содержание кислорода в воздухе должно быть не менее 20%. Известно, что при содержании кислорода 18% у человека наступает сонливость, при 17% начинаются отдышка и усиленное сердцебиение, а при 12% и менее — возникает смертельная опасность.
В шахту кислород поступает с атмосферным воздухом. Основными причинами уменьшения содеожания кислорода в рудничном воздухе являются выделение различных газов из окружающего массива горных пород, а также выбросы, взрывы и подземные пожары.
Горючие газы (CxHy)
Промышленные месторождения горючих природных газов встречаются в виде обособленных скоплений, не связанных с каким-либо др. полезным ископаемым; в виде газонефтяных месторождений, в которых газообразные углеводороды полностью или частично растворены в нефти или находятся в свободном состоянии и заполняют повышенную часть залежи (газовые шапки) или верхние части сообщающихся между собой горизонтов газонефтяной свиты; в виде газоконденсатных месторождений, в которых газ обогащен жидкими, преимущественно низкокипящими углеводородами.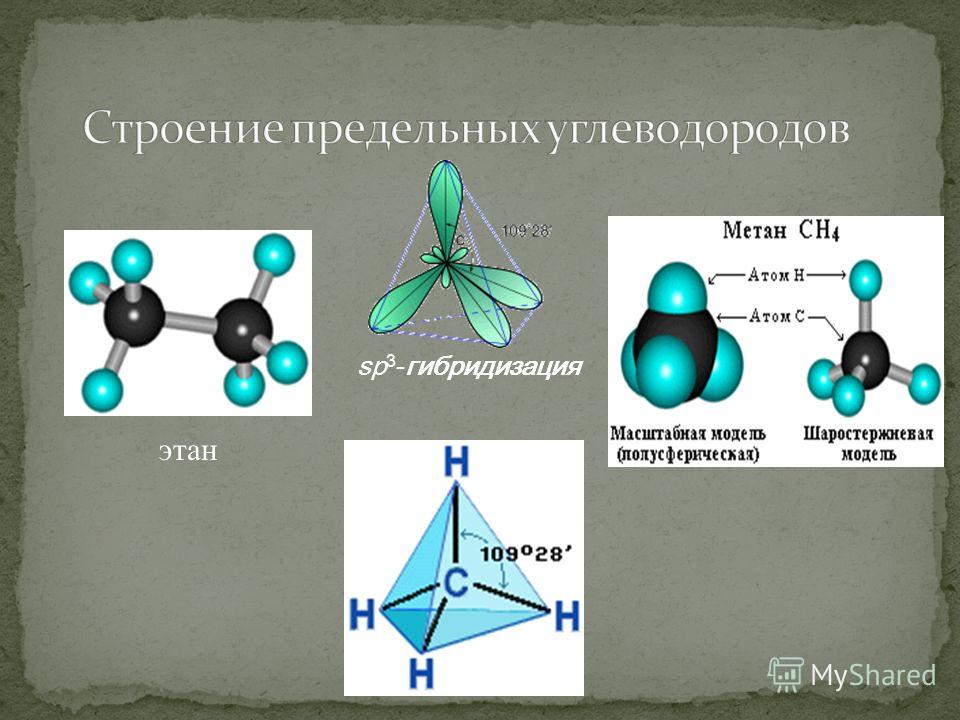
Горючие природных газы состоят из метана, этана, пропана и бутана, иногда содержат примеси легкокипящих жидких углеводородов — пентана, гексана и др.; в них присутствуют также углекислый газ, азот, сероводород и инертные газы. Многие месторождения горючих газов, залегающие на глубине не более 1,5 км, состоят почти из одного метана с небольшими примесями его гомологов (этапа, пропана, бутана), азота, аргона, иногда углекислого газа и сероводорода; с глубиной содержание гомологов метана обычно растет. В газоконденсатных месторождениях содержание гомологов метана значительно выше, чем метана. Это же характерно для газов нефтяных попутных. В отдельных газовых месторождениях наблюдается повышенное содержание углекислого газа, сероводорода и азота.
Газ метан — источник, формула, структура, свойства, использование
Что такое газ метан?
Метановый газ (CH 4 ) , также называемый болотным газом, представляет собой простейшее углеводородное соединение группы алканов или парафинов с правильной тетраэдрической химической структурой. Природный газ является основным источником молекул метана. Молекула CH 4 является важным химическим продуктом органического распада болот и топей. Органическое соединение, газообразный метан, образуется в результате действия бактерий на болотах в нашей среде.Ферментация осадка сточных вод бактериями дает около 70% газообразного метана, а также 40% по объему угольного газа. Он используется в качестве жидкого топлива в нашей повседневной жизни. Газ метан является частью парниковых газов, которые вызывают глобальное потепление, улавливая тепло.
Природный газ является основным источником молекул метана. Молекула CH 4 является важным химическим продуктом органического распада болот и топей. Органическое соединение, газообразный метан, образуется в результате действия бактерий на болотах в нашей среде.Ферментация осадка сточных вод бактериями дает около 70% газообразного метана, а также 40% по объему угольного газа. Он используется в качестве жидкого топлива в нашей повседневной жизни. Газ метан является частью парниковых газов, которые вызывают глобальное потепление, улавливая тепло.
Структурная формула метана
Четырехвалентный атом углерода в молекуле метана имеет следующую структурную формулу. Атом углерода в CH 4 имеет электронную конфигурацию 2s 1 2p x 1 2p y 1 2p z 1 90.Смешивание этих четырех атомных орбиталей дает четыре эквивалентных sp 3 -гибридных орбиталей. Эти гибридные орбитали направлены к углу правильного тетраэдра, показанного на рисунке выше. Каждая из этих полузаполненных гибридных орбиталей атома углерода химически связывается с полузаполненными атомными орбиталями атома водорода. Следовательно, молекула метана имеет тетраэдрическую форму с валентным углом C-H-C 109,5°.
Каждая из этих полузаполненных гибридных орбиталей атома углерода химически связывается с полузаполненными атомными орбиталями атома водорода. Следовательно, молекула метана имеет тетраэдрическую форму с валентным углом C-H-C 109,5°.
Четыре атома водорода в молекуле CH 4 эквивалентны без дипольного момента.Следовательно, валентный угол, энергия связи и длина связи всех углерод-водородных связей эквивалентны в молекуле CH 4 .
Как производить метан?
Метан является основной частью природного болотного газа, синтезируемого путем прожигания электрического разряда между угольными электродами в атмосфере водорода или при нагревании смеси углерода и никеля при 475°С в присутствии водорода.
Сабатье и Сендеренс в 1897 г. изобрели уравнение образования метана путем пропускания смеси водорода и моноксида или диоксида углерода над мелкодисперсными элементами, такими как никель, при температуре около 300°C.
CO + 3H 2 → CH 4 + H 2 O
CO 2 + 4H 2 → CH 4 + 2H 2
Лабораторный препарат CH
4
В лаборатории его обычно готовят путем нагревания химического состава 1:3 ацетата натрия и натронной извести. Его также получают восстановлением йодистого метила растворяющими металлами или сильноосновным алюмогидридом лития. CH 3 COONa + (NaOH + CaO) → CH 4 + Na 2 CO 3 .
Его также получают восстановлением йодистого метила растворяющими металлами или сильноосновным алюмогидридом лития. CH 3 COONa + (NaOH + CaO) → CH 4 + Na 2 CO 3 .
CH 4 получают путем гидролиза неорганических соединений, таких как карбид алюминия или реактив Гриньяра (йодистый метилмагний), молекулой воды. Al 4 C 3 + 12H 2 O → 3CH 4 + 4Al(OH) 3 .
Свойства газообразного метана
Болотный газ, имеющий общее название метан, представляет собой простейшее природное непредельное углеводородное соединение из ряда алкенов с молекулярной формулой CH 4 . При нормальной температуре метан (CH 4 ) представляет собой бесцветное, не имеющее запаха, неядовитое газообразное легковоспламеняющееся вещество.
| Свойства газообразного метана | |
| Химическая формула | СН 4 |
| Молярная масса | 16,043 г·моль−1 |
| Внешний вид | Бесцветный газ |
| Плотность | 0,657 кг·м−3 при 25 °C, 1 атм |
| Температура плавления | –182,456 °C или –296,421 °F |
| Точка кипения | −161. 5 °C или −258,7 °F 90 105 5 °C или −258,7 °F 90 105 |
| Критическая температура | 190,56 К |
| Сопряженная пара кислот и оснований | метаний и метил-анион |
Химические свойства
Этот газ менее растворим в воде, но более растворим в органических растворителях (спирте и эфире). Таким образом, 100 мл воды используются для растворения около 5 мл газа CH 4 при 20°C. В химии термодинамическое сгорание метана дает несветящееся пламя в воздухе или кислороде за счет образования углекислого газа и воды.
Химические реакции
- Природный газ сильно взрывается при смешивании с воздухом, что вызывает взрыв в угольных шахтах, где метан известен как рудничный газ.
- В присутствии подходящего химического катализатора образуется метанол и формальдегид.
- Но при прохождении смеси метана и кислорода через медную трубку при давлении 100 атм и температуре 200°С образуется химическое соединение метанол.

Использование газообразного метана
- Метан при нагревании до 1000°C или при неполном сгорании газа образует углерод или очень мелкодисперсное состояние сажи, которая используется в производстве красок, чернил для принтеров и резиновой промышленности для изготовления автомобильных шин.
- также используется в качестве органического топлива в нашей повседневной жизни.
- Он используется для получения органических соединений, таких как метилхлорид, ацетилен, формальдегид и метанол, которые в основном используются на химических предприятиях.
- Синтез-газ образуется при пропускании смеси метана и пара над нагретым никелем, нанесенным на глинозем, который используется в химической промышленности для приготовления различных химикатов. Он в основном используется в качестве природного источника газообразного водорода в химической промышленности.
Газообразный метан
Метан как парниковый газ
В настоящее время серьезная озабоченность по поводу увеличения использования метана, двуокиси углерода, фреонов, озона, закиси азота и водяного пара в атмосфере вызывает повышение глобальной температуры, и этот эффект известен как парниковый эффект. А вот теплица используется для содержания в зимних уездах за счет искусственного обогрева. Вклад газа CH 4 в глобальное потепление составляет от 16 до 20 процентов. Таким образом, CH 4 нагревает атмосферу Земли за счет улавливания излучения электромагнитного спектра (ИК) солнечного света или тепла, отраженного от поверхности Земли.
А вот теплица используется для содержания в зимних уездах за счет искусственного обогрева. Вклад газа CH 4 в глобальное потепление составляет от 16 до 20 процентов. Таким образом, CH 4 нагревает атмосферу Земли за счет улавливания излучения электромагнитного спектра (ИК) солнечного света или тепла, отраженного от поверхности Земли.
Воздействие метана на окружающую среду
В последнее время из-за многих глобальных событий, таких как промышленная революция и использование природного газа, увеличивается концентрация парниковых газов (CFC, двуокись углерода, метан и т. д.). Средняя температура земной атмосферы повысится примерно на 2,5°C в течение следующих 30 лет, что приведет к серьезному изменению климата в мире.
Полярные ледяные шапки будут таять косвенно из-за парниковых газов метана или углекислого газа. Следовательно, они повышают уровень моря.Поэтому многие приморские местности, в том числе и большая Исландия, оказались полностью затоплены. Поэтому для спасения нашей цивилизации используйте неископаемые виды топлива, возобновляемые источники энергии, такие как солнечная, ветровая, гидроэлектроэнергия и ядерная энергия.
Поэтому для спасения нашей цивилизации используйте неископаемые виды топлива, возобновляемые источники энергии, такие как солнечная, ветровая, гидроэлектроэнергия и ядерная энергия.
Что такое метан? | Факты о парниковом газе метан
- Метан — это бесцветный, легковоспламеняющийся газ без запаха и основной компонент природного газа, который используется для выработки электроэнергии и обогрева домов по всему миру.
- На долю метана приходится примерно 10 процентов всех антропогенных выбросов парниковых газов в США.С. в 2017 году, по данным EPA.
- В августе 2019 года Агентство по охране окружающей среды объявило об отмене правил в отношении метана.
В прошлом году Агентство по охране окружающей среды (EPA) объявило, что начнет отменять правила эпохи Обамы в отношении метана, мощного парникового газа. В соответствии с действующими правилами нефтегазовые предприятия должны установить средства контроля, предотвращающие утечку метана из их оборудования.
ПОГРУЖАЙТЕСЬ ГЛУБЖЕ ➡ Ознакомьтесь с лучшими в своем классе материалами по науке о Земле и получите неограниченный доступ к набору Pop Mech уже сейчас.
Администрация Трампа утверждает, что Агентство по охране окружающей среды не имеет полномочий регулировать выбросы метана в соответствии с Законом о чистом воздухе. Но этот шаг идет вразрез с рекомендацией некоторых крупных игроков нефтегазовой отрасли, таких как Shell, BP и Exxon, которые поддержали правила 2016 года и недавно публично заявили о своем намерении сократить выбросы метана.
Так почему же это так важно? Давайте сломаем это.
Что такое
Метан?
Метан (Ch5) представляет собой бесцветный легковоспламеняющийся газ без запаха, состоящий из одного атома углерода и четырех атомов водорода.Он может быть получен естественным и синтетическим путем, а при сжигании в присутствии кислорода образует углекислый газ и водяной пар.
Метан является основным компонентом природного газа и используется для производства тепла и электроэнергии во всем мире. Метан также используется в химических реакциях для производства других важных газов, таких как водород, монооксид углерода и сажа, химическое соединение, которое содержится в некоторых типах резины, используемой в автомобильных шинах.
Газ также вносит значительный вклад в изменение климата.По данным Агентства по охране окружающей среды США, в 2017 году на метан приходилось примерно 10 процентов всех выбросов парниковых газов в США, вызванных деятельностью человека. Хотя это не самый распространенный парниковый газ в атмосфере, он является одним из самых мощных.
Где встречается метан и как он выделяется?
Существует два основных способа естественного производства метана.
Во-первых, метан может быть получен в результате серии химических реакций, когда органическое вещество разлагается на небольшой глубине в средах с низким содержанием кислорода, таких как болота и топи. Когда растения умирают и опускаются на дно этой водной среды, бактерии начинают их разрушать. Согласно исследованию , опубликованному в Proceedings of the National Academy of Sciences , водно-болотные угодья являются крупнейшим естественным источником выбросов метана. Кроме того, метан может вытекать из грязевых вулканов, рисовых полей и, как ни странно, термитов.
Когда растения умирают и опускаются на дно этой водной среды, бактерии начинают их разрушать. Согласно исследованию , опубликованному в Proceedings of the National Academy of Sciences , водно-болотные угодья являются крупнейшим естественным источником выбросов метана. Кроме того, метан может вытекать из грязевых вулканов, рисовых полей и, как ни странно, термитов.
Метан также можно найти в подземных месторождениях ископаемого топлива, которые подвергались воздействию высокого давления и температуры на протяжении миллионов и миллионов лет.Поскольку эти виды топлива собираются, добываются и выбрасываются, то же самое происходит и с метаном. Метан трудно транспортировать, а легко вытекает при добыче нефти, угля и природного газа — отсюда и правила.
«Если вы пытаетесь повлиять на климатическую политику в ближайшие 10 лет, метан — действительно хорошее химическое вещество», — говорит Даниэль Варон, атмосферный ученый из Гарвардского университета, Popular Mechanics .
Форма метана, смешанного со льдом, называемая газогидратами метана, может быть обнаружена в слоях отложений на дне океана, под вечной мерзлотой и замерзшими озерами в Арктике.Эти твердые, похожие на лед отложения рекламировались как потенциальный источник энергии, но они вызывают особую тревогу, поскольку они могут выбрасывать в атмосферу большие концентрированные количества метана .
Согласно EPA , примерно от 50 до 65 процентов выбросов метана в США связаны с деятельностью человека, а около 30 процентов выбросов метана, связанных с деятельностью человека, высвобождаются в газовой и нефтяной промышленности.
Этот контент импортирован из {embed-name}.Вы можете найти тот же контент в другом формате или найти дополнительную информацию на их веб-сайте.
Около 27 процентов выбросов метана образуется в результате процесса, называемого кишечной ферментацией — коровы отрыгивают и время от времени пукают, переваривая пищу, в основном — и 16 процентов глобальных выбросов метана образуются в результате разложения органических отходов на свалках.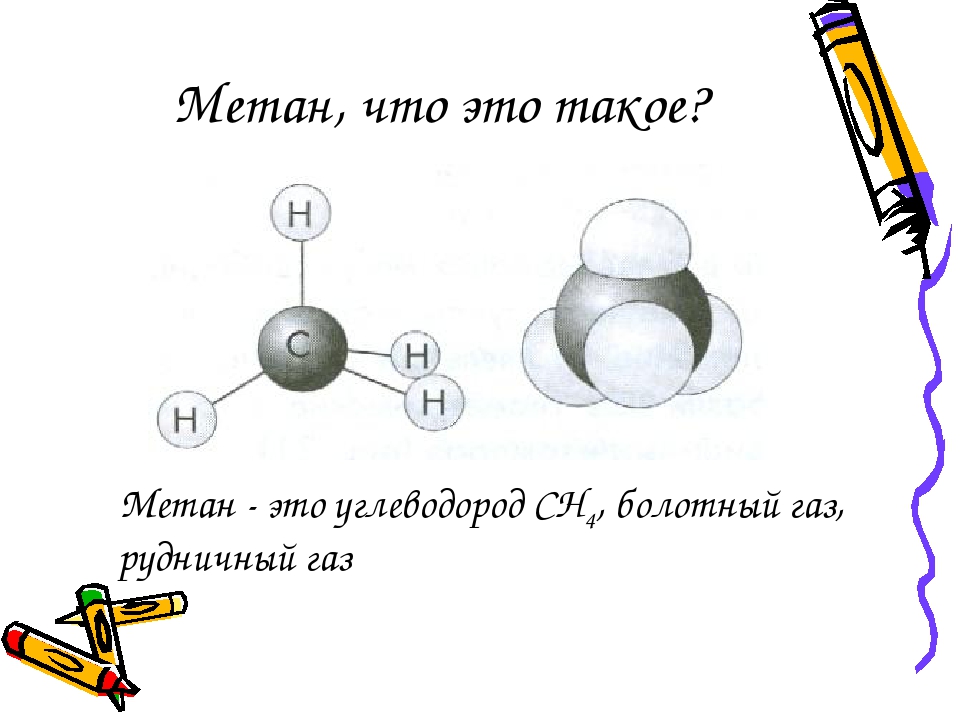 Метан также может выделяться при хранении и использовании навоза в качестве топлива (9 процентов) и при добыче угля (8 процентов).
Метан также может выделяться при хранении и использовании навоза в качестве топлива (9 процентов) и при добыче угля (8 процентов).
Агентство по охране окружающей среды
Что касается отрыжки крупного рогатого скота, недавнее исследование , опубликованное в журнале Science Advances , определило группы микробов в кишечнике коров, которые вызывают кишечное брожение, и предположило, что селективное разведение коров для производства меньшего количества газа может снизить выбросы.
Так почему метан так важен?
Из всех парниковых газов метан является одним из самых мощных из-за его способности эффективно поглощать тепло в атмосфере Земли.Исследования показали, что за 20-летний период килограмм метана согревает планету в 80 раз сильнее, чем килограмм углекислого газа .
Метан сохраняется в атмосфере Земли примерно десять лет, прежде чем он начнет реагировать со свободным радикалом, называемым гидроксилом, и превратиться в углекислый газ, где он может оставаться там веками.
Следовательно, большую часть времени метан в атмосфере в виде молекулы проводит в виде молекулы CO2, говорит Варон. В воздух выбрасывается гораздо меньше метана, чем углекислого газа.«Простое сокращение выбросов метана без сокращения выбросов CO2 не будет столь полезным в долгосрочной перспективе», — говорит он. Тем не менее, метан оставляет неизгладимые следы.
Например, одним из таких воздействий является явление, называемое тепловым расширением. Парниковые газы, такие как метан, нагревают атмосферу, и до 90 процентов этого избыточного тепла поглощается океанами. Это тепло заставляет морскую воду расширяться в объеме. Этот эффект, наряду с таянием ледников, вызывает повышение уровня моря.
Ученые давно знали, что углекислый газ нагревает атмосферу и океаны Земли, заставляя их расширяться, но только недавно они обнаружили, что короткоживущие парниковые газы, такие как метан и фреоны (газы, содержащие хлор или фтор), также вызывают тепловое расширение.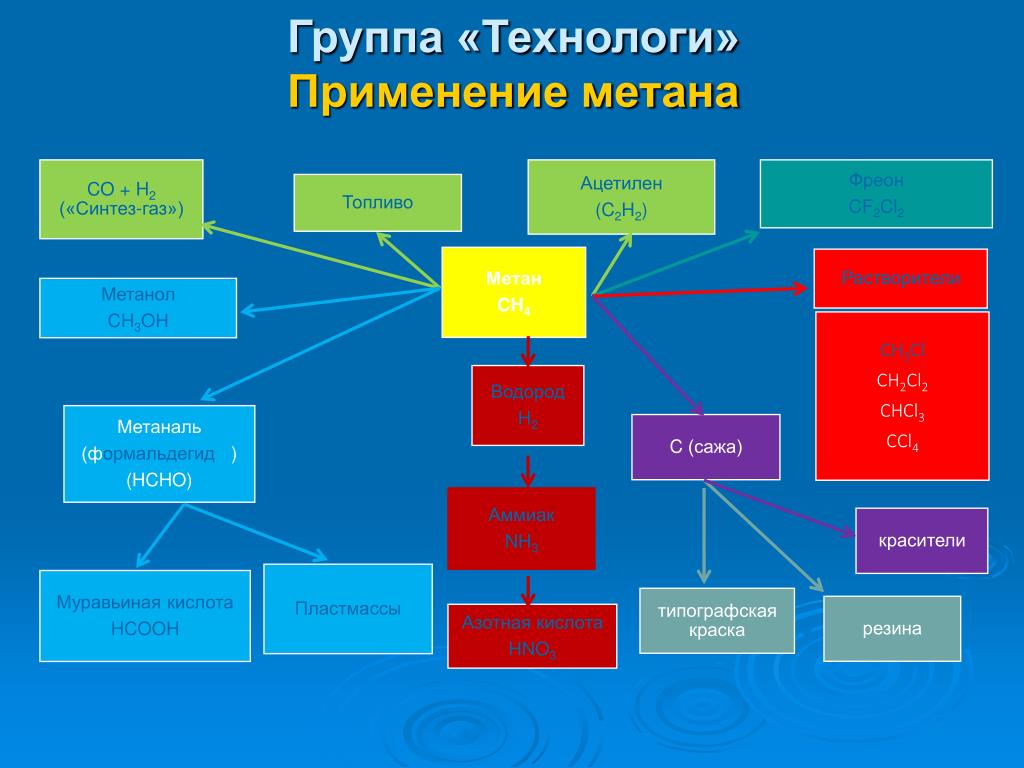 .В 2017 году ученые провели 90 248 компьютерных симуляций, которые показали, что тепловое расширение 90 249, вызванное метаном, продолжается столетиями даже после того, как газ рассеялся из атмосферы.
.В 2017 году ученые провели 90 248 компьютерных симуляций, которые показали, что тепловое расширение 90 249, вызванное метаном, продолжается столетиями даже после того, как газ рассеялся из атмосферы.
И, наконец, регулирование содержания метана полезно для здоровья. По словам Варона, выброс газа может привести к повышению уровня озона в атмосфере. По данным EPA, озон может вызвать ряд проблем со здоровьем, таких как одышка, и усугубить заболевания легких, такие как астма, эмфизема и хронический бронхит.
«Люди уже давно измеряют содержание метана в атмосфере самолетами и наземными приборами, — говорит Варон. Он и его коллеги работают с государственными учреждениями, которые используют спутники, чтобы точно определить, где выбросы самые высокие. Эта информация может помочь определить объекты, на которых происходит утечка метана, и привести к лучшему мониторингу и, следовательно, к регулированию операций с нефтью и природным газом по всему миру.
Понимание того, откуда берется метан, может помочь нам смягчить последствия изменения климата, но это все еще тяжелая битва. Последний откат Агентства по охране окружающей среды может сделать этот холм намного круче.
Последний откат Агентства по охране окружающей среды может сделать этот холм намного круче.
Первоначальная версия этой статьи утверждала, что из-за химической реакции большая часть времени жизни метана в атмосфере проходит в виде молекулы CO2. С тех пор мы уточнили утверждение, чтобы отразить, что химическая реакция происходит в конце жизни метана в атмосфере. Мы сожалеем об ошибке.
Дженнифер Леман
Дженнифер Леман — научный журналист и редактор новостей Popular Mechanics, где она пишет и редактирует статьи о науке и космосе.
Этот контент создается и поддерживается третьей стороной и импортируется на эту страницу, чтобы помочь пользователям указать свои адреса электронной почты. Вы можете найти дополнительную информацию об этом и подобном контенте на сайте piano.io.
Метан: важная возможность в борьбе с изменением климата
Как решить проблему с метаном?
До недавнего времени мало что было известно о том, где происходят утечки и как лучше всего их устранять. В 2012 году мы начали серию исследований, чтобы лучше выявлять утечки и находить решения. Это самый большой объем рецензируемых исследований по этому вопросу.
В 2012 году мы начали серию исследований, чтобы лучше выявлять утечки и находить решения. Это самый большой объем рецензируемых исследований по этому вопросу.
Синтез исследования показал, что нефтегазовая промышленность США выбрасывает не менее 13 миллионов метрических тонн метана в год — примерно на 60% больше, чем оценивало Агентство по охране окружающей среды в то время. Объем представляет собой достаточно природного газа для топлива 10 миллионов домов.
Сегодня у нас гораздо больше данных о том, откуда берется метан и как его предотвратить.Наземные средства измерения наряду с растущим числом спутников, включая один, запущенный нашей дочерней компанией MethaneSAT, позволяют быстрее и дешевле, чем когда-либо, обнаруживать, измерять и сокращать выбросы.
На самом деле, по оценкам Международного энергетического агентства, нефтегазовая промышленность во всем мире может достичь 75-процентного сокращения выбросов, используя доступные сегодня технологии, причем две трети этого сокращения будут бесплатными.
Видение лидерства из Белого дома
Являясь крупнейшим в мире производителем нефти и газа, Соединенные Штаты имеют возможность и обязаны возглавить процесс сокращения выбросов метана.Хорошая новость: 30 июня 2021 года президент Байден подписал закон о восстановлении правил эпохи Обамы, которые сокращают загрязнение метаном от нефтегазовой промышленности.
Это не только отменило один из разрушительных климатических откатов администрации Трампа — оно немедленно восстановило критически важные меры защиты для сообществ по всей стране. Этот шаг также требует от Агентства по охране окружающей среды (EPA) расширить свои амбициозные меры по защите метана следующего поколения, чтобы добиться еще более глубокого сокращения этого вредного загрязнения.
Пристальный взгляд: изучение локальных утечек
Повышение осведомленности о масштабах и воздействии утечек метана имеет важное значение для разработки эффективной политики.
Наш пилотный проект с Google Earth Outreach помог визуализировать опасные для климата утечки, обнаруженные в местных сообществах.
Метан — Энергетическое образование
Рисунок 1. Модель заполнения пространства метаном; белые сферы представляют атомы водорода, а черные сферы представляют атомы углерода. [1]
Метан представляет собой алкан с химической формулой CH 4 . Как углеводород, он может подвергаться горению углеводородов с выделением тепла. Метан является основным углеводородным компонентом природного газа, который является одним из видов ископаемого топлива. [2]
При обычных температурах и давлениях это газ, составляющий около 95% содержания сжиженного природного газа и около 80-90% природного газа. [3] Метан также является парниковым газом, как и двуокись углерода (CO 2 ). Он имеет более короткое время жизни в атмосфере, чем CO 2 , 12 лет, [4] , но это «сбалансировано» тем фактом, что он более эффективно удерживает тепло, чем CO 2 , поскольку у метана ПГП ( потенциал глобального потепления) из 21. [5]
[5]
Сжигание метана (см. моделирование внизу страницы) обеспечивает значительную долю мировой первичной энергии и используется для отопления домов, приготовления пищи, нагрева воды и выработки электроэнергии. Он может даже обеспечить энергию для транспорта. Однако это означает, что он также вносит значительный вклад в изменение климата, поскольку этот метан производит значительное количество углекислого газа, который люди выбрасывают в атмосферу.
Свойства
Ниже приведена таблица некоторых основных свойств метана.
Анимация горения
Метан высвобождает свою химическую энергию при сгорании углеводородов. Ниже представлена анимация горения углеводородов, показывающая результирующую реакцию, происходящую при соединении метана с кислородом.
CH 4 + 2O 2 → CO 2 + 2H 2 O Тепловая энергия (энтальпия)
Реакция горения углеводородов высвобождает тепловую энергию и является примером экзотермической реакции. Реакция также имеет отрицательное значение изменения энтальпии (ΔH).
Реакция также имеет отрицательное значение изменения энтальпии (ΔH).
Для дальнейшего чтения
Ссылки
Авторы и редакторы
Семаа Амин, Итан Бохлер, Эллисон Кэмпбелл, Джордан Ханания, Джеймс Дженден, Кайлин Стенхаус, Луиза Варгас Суарес, Дэниел Суше, Джейсон Донев | Энбридж Газ
Природный газ — это метан, получаемый из захороненных растений и животных, которые разлагались и образовывали крошечные пузырьки газа, который собирают, очищают и используют в качестве источника энергии.
Химический состав природного газа
Природный газ представляет собой природную газовую смесь, состоящую в основном из метана, полученного из бассейнов поставок в западной Канаде, США и производителей Онтарио.
Состав представляет собой общее среднее значение для системы и может отличаться от типичного значения, указанного ниже, в зависимости от местоположения.
| Компонент | Типичный анализ (мол.  %) %) | Диапазон (мол. %) |
|---|---|---|
| Метан | 94.7 | 87,0 — 98,0 |
| Этан | 4,2 | 1,5 — 9,0 |
| Пропан | 0,2 | 0,1 — 1,5 |
| изо-бутан | 0,02 | след — 0,3 |
| нормальный — бутан | 0,02 | след — 0,3 |
| изо-пентан | 0.01 | след — 0,04 |
| обычный — пентан | 0,01 | след — 0,04 |
| Гексаны плюс | 0,01 | след — 0,06 |
| Азот | 0,5 | 0,2 — 5,5 |
| Двуокись углерода | 0,3 | 0. 05 — 1.0 05 — 1.0 |
| Кислород | 0,01 | трассировка — 0,1 |
| Водород | 0,02 | след — 0,05 |
| Удельный вес | 0,58 | 0,57 — 0,62 |
| Теплотворная способность (МДж/м 3 ), в сухом состоянии * | 38,8 | 36.0 — 40,2 |
| Число Воббе (МДж/м 3 ) | 50,9 | 47,5 — 51,5 |
* Полная теплотворная способность – это общее количество теплоты, полученное при полном сгорании при постоянном давлении единицы объема газа в воздухе, включая теплоту, выделяющуюся при конденсации водяного пара в продуктах сгорания (газ, воздух, горение продукты, взятые при стандартной температуре и давлении).
Сера: В системе Enbridge Gas типичное содержание серы составляет от 3 до 6 мг/м3.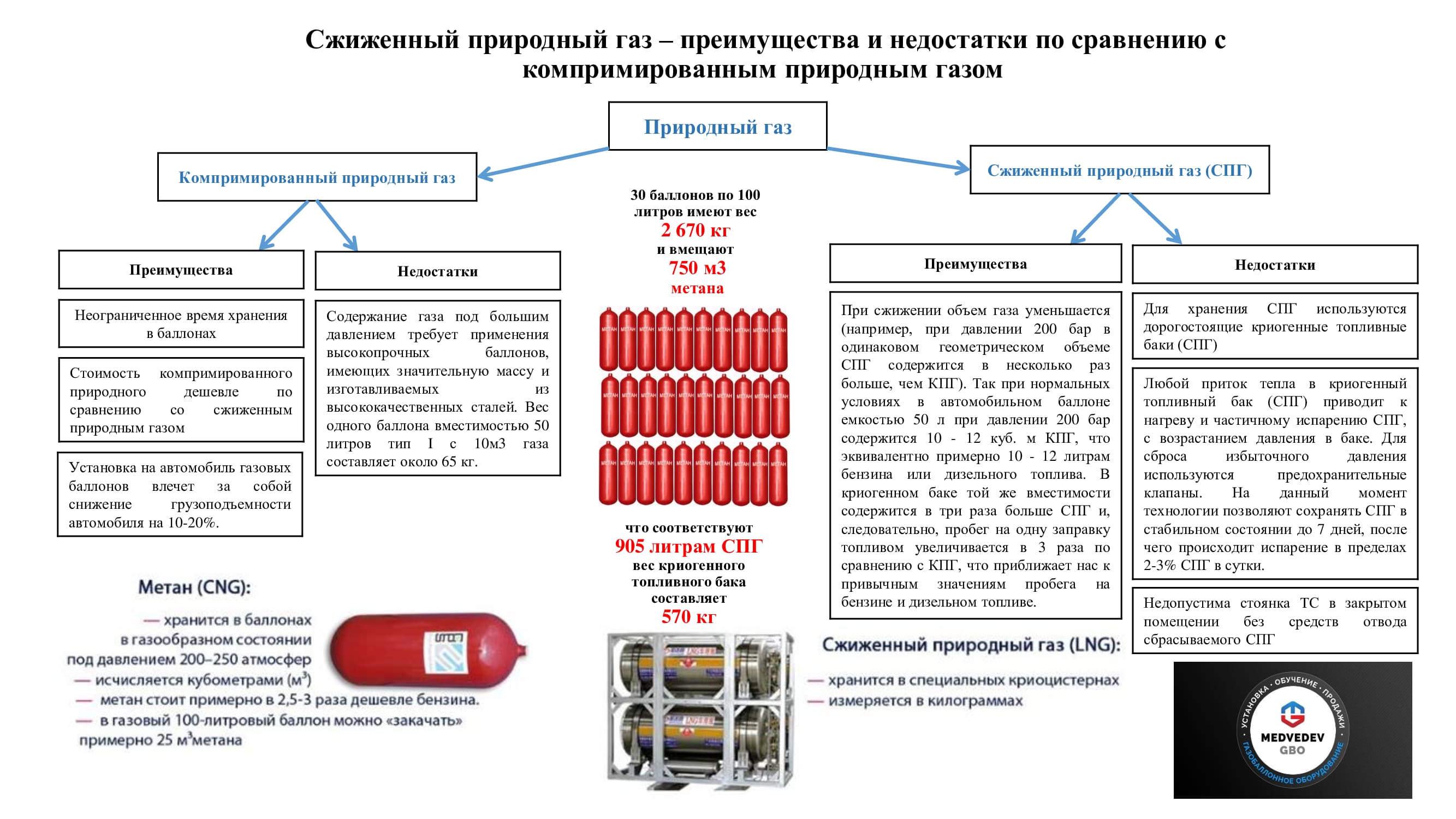
Водяной пар: Содержание водяного пара в природном газе в системе Enbridge Gas составляет менее 65 мг/м3 и обычно составляет 16–32 мг/м3.
Типичные свойства горения природного газа:
- Температура воспламенения: 564 oC *
- Пределы воспламеняемости: 4% — 15% (объемные % в воздухе) *
- Теоретическая температура пламени (стехиометрическое соотношение воздух/топливо): 1953 oC *
- Максимальная скорость пламени: 0,36 м/с *
* Показанные характеристики являются средними для системы Enbridge Gas и могут отличаться в зависимости от вашего местонахождения.Предоставленная информация взята из отчета Ortech № 26392 «Расчеты свойств горения для типичного состава газа Union», 2017 г.
Метан: менее известный парниковый газ, играющий ключевую роль в решении проблемы изменения климата
В своем домашнем офисе в Аризоне Райли Дюрен одновременно с несколькими делами рассказывал мне о пугающе мощных парниковых газах, одновременно наблюдая за самолетами своей команды. Самолет летел на высоте 20 000 футов, чтобы измерить выбросы метана из колодцев в Пермском бассейне Техаса.Аэрофотоснимок на экране его компьютера оживил измерения: десятки красных зон представляли собой невидимые шлейфы метана над нефтяными и газовыми месторождениями.
Самолет летел на высоте 20 000 футов, чтобы измерить выбросы метана из колодцев в Пермском бассейне Техаса.Аэрофотоснимок на экране его компьютера оживил измерения: десятки красных зон представляли собой невидимые шлейфы метана над нефтяными и газовыми месторождениями.
«Это как смотреть фейерверк. Они просто появляются повсюду», — сказал Дюрен, ученый из Университета Аризоны, возглавляющий некоммерческую организацию Carbon Mapper, у которой есть государственные и частные партнеры, включая НАСА, штат Калифорния и компанию Planet.
В публичных дискуссиях об изменении климата метану слишком долго уделялось слишком мало внимания.Многие люди могут не знать, что люди выбрасывают в атмосферу парниковый газ, который является даже более мощным, чем углекислый газ, со скоростью, невиданной по крайней мере 800 000 лет. Он наносит вред качеству воздуха и поступает из самых разных источников, от нефте- и газопроводов до свалок и коров. Но метан и другие парниковые газы, в том числе гидрофторуглероды, озон, оксиды азота и оксиды серы, наконец-то получают то внимание, которого они заслуживают, во многом благодаря достижениям науки.
До последних нескольких лет относительная неизвестность метана имела смысл.Углекислый газ (CO2), безусловно, является самым большим фактором изменения климата, и он поступает из узнаваемых источников ископаемого топлива, таких как выхлопные трубы автомобилей, угольные дымовые трубы и сжигание газа и нефти. Самое тревожное заключается в том, что он остается в атмосфере сотни лет, что делает изменение климата проблемой не только для нас сейчас, но и для будущих поколений.
Но мир больше не может позволить себе роскошь игнорировать метан. А на 26-й международной климатической конференции в Глазго, которая продлится до 12 ноября, была выдвинута новая крупная инициатива по прямому решению проблемы метана.Более 100 стран, на долю которых приходится почти половина глобальных уровней загрязнения метаном, взяли на себя добровольное Глобальное обязательство по сокращению выбросов метана как минимум на 30 процентов к концу десятилетия. Президент Джо Байден, который вместе с Европейским союзом возглавляет эту инициативу, объявил о наборе регулирующих мер, направленных на то, чтобы привести Соединенные Штаты в соответствие с этой глобальной целью.
Некоторые из крупнейших загрязнителей метана, в том числе Россия и Китай, не присоединились к глобальному обязательству.Это всего лишь один из признаков того, что мир до сих пор не в полной мере прислушался к тревожным звонкам ученых о метане.
Хотя метан изучен не так хорошо, как углекислый газ, он играет огромную роль в климатическом кризисе. Он по крайней мере в 80 раз эффективнее удерживает тепло, чем углекислый газ за 20 лет, но он начинает рассеиваться в атмосфере в течение нескольких лет. Если это «решающее десятилетие» для принятия мер, как заявила администрация Байдена, то метановая стратегия должна быть в центре любой политики по борьбе с глобальным потеплением.
Метан может означать разницу между быстро нагревающейся планетой, которая меняется слишком быстро и резко, чтобы человечество могло с ней справиться, и выигрышем планеты столь необходимого времени, чтобы справиться с долгосрочной проблемой ископаемого топлива и загрязнения углекислым газом.
Загрязнение метаном сводит на нет выгоды от отключения угля
Дрю Шинделл, один из ученых, которые рано забили тревогу по поводу метана, изучал загрязнение воздуха в конце 2000-х, когда обнаружил странную тенденцию.Уровень приземного озона, загрязнителя, образующего туманный смог, в США повышался, что удивило его после десятилетий прогресса в соответствии с Законом о чистом воздухе. Он понял, что виноват «неустанный рост метана», который ускоряет образование озона у земли. С тех пор он пытается предупредить мир, чтобы он не упускал из виду этот опасный загрязнитель и его последствия как для климата, так и для здоровья человека.
Определить миллионы источников метана по всему миру не так просто.Крупный рогатый скот выделяет метан, как и разлагающийся органический материал. Все пищевые отходы, попадающие на свалки, выделяют метан. А природный газ почти полностью состоит из метана.
Если вы слышали, как политики называют природный газ «переходным топливом», они имеют в виду, что природный газ выделяет меньше углекислого газа, чем уголь. Его неправильно называть чистым, потому что при сжигании метана все равно выделяется углерод, а метан, улетучившийся без сжигания, является мощным обогревателем.
Его неправильно называть чистым, потому что при сжигании метана все равно выделяется углерод, а метан, улетучившийся без сжигания, является мощным обогревателем.
В климатическом отчете, опубликованном в понедельник Межправительственной группой экспертов Организации Объединенных Наций (ООН) по изменению климата (МГЭИК), прогнозируется, что, если люди не предпримут немедленных изменений для ограничения выбросов метана, углекислого газа и других удерживающих тепло газов, земля будет продолжать нагреваться с разрушительными последствиями. на жизнь человека и животных. Спенсер Платт / Getty Images
Нефтегазовая промышленность утверждала, что она не виновата в загрязнении метаном, но защитники и ученые доказывали обратное. Фонд защиты окружающей среды, который заказал полеты для мониторинга метана над нефтяными и газовыми месторождениями Техаса, обнаружил, что нефтяные месторождения в США выделяют на 60 процентов больше метана, чем оценивает Агентство по охране окружающей среды. Ученый из Мичиганского университета Эрик Корт обнаружил, что выброс метана из морских скважин происходит гораздо быстрее, чем считалось ранее.Экологическая группа Earthworks, используя дорогостоящее оборудование для наземных камер, помогла отследить некоторые участки, которые были рецидивистами выброса метана в атмосферу.
Ученый из Мичиганского университета Эрик Корт обнаружил, что выброс метана из морских скважин происходит гораздо быстрее, чем считалось ранее.Экологическая группа Earthworks, используя дорогостоящее оборудование для наземных камер, помогла отследить некоторые участки, которые были рецидивистами выброса метана в атмосферу.
Количество научных статей увеличилось: с 2013 года не менее 45 научных статей подчеркивали непропорциональную роль нефтегазовых операций, согласно обзору, проведенному правозащитной группой Climate Nexus. Такие ученые, как Дюрен, также создали яркие изображения метана, понятные неспециалистам, как и изображения ниже, сделанные в апреле этого года.
По словам Дьюрена, Carbon Mapper обнаружил более 3000 метановых шлейфов в Пермском бассейне с помощью аэрофотосъемки, все они исходят от целого ряда нефтегазовой инфраструктуры, включая скважины, резервуарные парки, компрессорные станции, трубопроводы и многое другое.
В совокупности эти данные свидетельствуют о мрачной перспективе минимального прогресса, достигнутого до сих пор в борьбе с углеродным загрязнением: рост загрязнения метаном фактически сводит на нет некоторые успехи, достигнутые США в очистке угольного энергетического сектора.
Метан быстро растет с 2007 года, что обусловлено сочетанием сельского хозяйства (из Восточной и Западной Азии, Бразилии и Северной Африки) и ископаемого топлива, особенно из Северной Америки. Другими словами, ученые уверены, что люди являются основной причиной увеличения загрязнения метаном.
Тем не менее, данные нужно улучшить. Администрация Байдена, по сути, начинает с нуля с предложенными правилами EPA, которые требуют, чтобы нефтяные компании отслеживали и устраняли свои собственные утечки.Администрация Трампа потратила впустую критические годы, отменив правила, нацеленные на новые скважины, и установила базовые стандарты практики самоотчетности.
Чтобы мир мог бороться с метаном, страны должны лучше понимать, из каких секторов и источников он поступает.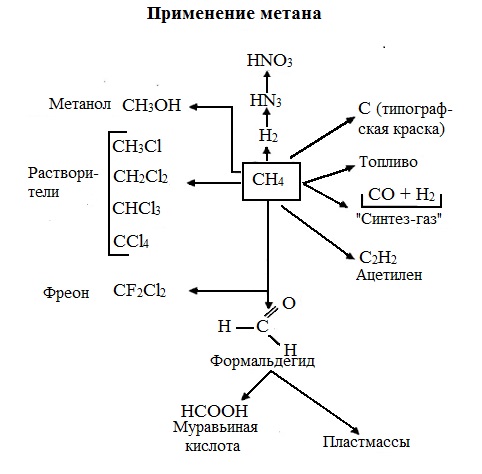 Немногие крупные экономики даже измеряют метан. Китай запустил рынок торговли углеродом для борьбы с выбросами углекислого газа, но меньше сделал для контроля над метаном, который поступает не только из газа, но и из угля.
Немногие крупные экономики даже измеряют метан. Китай запустил рынок торговли углеродом для борьбы с выбросами углекислого газа, но меньше сделал для контроля над метаном, который поступает не только из газа, но и из угля.
Ученые много знают об CO2 и гораздо меньше о других газах
Впервые в августе МГЭИК уделила значительное внимание важной роли газов, отличных от CO2.Шестая оценка ООН науки об изменении климата, в которой делается вывод о том, что доказательства антропогенного потепления «недвусмысленны» и многие воздействия на климат будут необратимыми, посвящает целую главу отчета «короткоживущим загрязнителям», таким как метан. . Одним из наиболее распространенных их источников является ископаемое топливо.
Данные NOAA показывают рост концентрации метана в атмосфере и необходимость резкого сокращения, начиная с 2020-х годов, если есть надежда ограничить потепление до 1.5 градусов Цельсия. Глобальная оценка метана ООН, 2021 г.
Глобальная оценка метана ООН, 2021 г.
Поскольку эти газы составляют такую крошечную часть атмосферы по сравнению с тем, сколько углекислого газа мы выбрасываем в воздух, метан «всегда занимает второе место» в дискуссиях об изменении климата, сказал Шинделл, который возглавлял первую в мире Организацию Объединенных Наций. Глобальная оценка метана, выпущенная в этом году. По словам Шинделла, до сих пор он находился «между трещин» в глобальных исследованиях.
До сих пор метан буквально проваливался сквозь трещины: часть его просачивается из-под земли в местах вроде нефтяных месторождений и вечной мерзлоты, и ученые до сих пор пытаются понять, откуда все это берется.Отчет МГЭИК отражает эти неопределенности. Авторы отчета, например, не называют доминирующий источник антропогенных выбросов метана, будь то ископаемое топливо или сельское хозяйство. Но то, что мы теперь знаем, представляет собой одно из величайших достижений в исследованиях климата с тех пор, как в 2013 году была опубликована последняя оценка МГЭИК. Работа таких ученых, как Дюрен, помогает миру понять главных виновников метанового кризиса в надежде, что правительства и корпорации примут меры. срочное действие.
Работа таких ученых, как Дюрен, помогает миру понять главных виновников метанового кризиса в надежде, что правительства и корпорации примут меры. срочное действие.
Помимо CO2 и метана существуют и другие парниковые газы.Закиси азота, черный углерод и галогенсодержащие газы (категория, в которую входят химические вещества, используемые для хладагентов, гидрофторуглероды) также способствуют изменению климата.
График из сводки МГЭИК для политиков дает представление о том, как все эти газы взаимодействуют, что в сумме составляет не менее 1,1 градуса Цельсия среднего глобального потепления с 1850-х годов. Как показано на графике ниже, CO2 и метан составляют большую часть потепления, но другие загрязняющие вещества также оставляют свой след. Некоторые аэрозоли ископаемого топлива, такие как диоксид серы, на самом деле обладают охлаждающим эффектом (но опасны для наших легких).
Другие загрязняющие вещества, помимо углерода, оказывают нагревающее воздействие на атмосферу. Резюме ДО6 МГЭИК для политиков
Резюме ДО6 МГЭИК для политиков
Когда речь идет о второй по значимости причине глобального потепления, есть и хорошие, и плохие новости.
Сначала о плохом: уровень метана растет, и мы многого о нем не знаем. Даже если мы выявим главных виновников в нефти и газе, другие источники все равно потребуют масштабных социальных изменений, таких как сокращение поголовья коров, выращиваемых для еды.(Были некоторые эксперименты с кормом для крупного рогатого скота, чтобы уменьшить выбросы метана, или, что более странно, с рюкзаками для сбора газов для коров).
Пищевые отходы, которые при разложении выделяют метан, также являются проблемой. Во всем мире самые богатые экономики выбрасывают половину своей еды. Свалки могут улавливать часть метана, но это тоже энергоемкий процесс.
Хотя метан изучен не так хорошо, как углерод, он играет огромную роль в климатическом кризисе. Патрисия Монтейро / Bloomberg через Getty Images
Остаются нефть, уголь и газ. Уголь — худший преступник; он выщелачивает как углекислый газ, так и метан, что делает его приоритетом номер один для поэтапного отказа. Добыча нефти также представляет собой серьезную проблему, отчасти потому, что производители не сталкиваются с серьезным нормативным или экономическим давлением, требующим возврата излишков газа. Даже когда промышленность пытается улавливать и продавать природный газ, производители теряют метан при его добыче и транспортировке.Он просачивается, когда производители направляют газ на компрессорные станции, обрабатывают его для отправки, отправляют по трубопроводу на сотни миль на нефтеперерабатывающий завод и доставляют потребителю в виде сжиженного природного газа, пластика, нефтехимических продуктов или газа, который освещает печи в домах и квартирах.
Уголь — худший преступник; он выщелачивает как углекислый газ, так и метан, что делает его приоритетом номер один для поэтапного отказа. Добыча нефти также представляет собой серьезную проблему, отчасти потому, что производители не сталкиваются с серьезным нормативным или экономическим давлением, требующим возврата излишков газа. Даже когда промышленность пытается улавливать и продавать природный газ, производители теряют метан при его добыче и транспортировке.Он просачивается, когда производители направляют газ на компрессорные станции, обрабатывают его для отправки, отправляют по трубопроводу на сотни миль на нефтеперерабатывающий завод и доставляют потребителю в виде сжиженного природного газа, пластика, нефтехимических продуктов или газа, который освещает печи в домах и квартирах.
Вся система очень негерметична, но самые негерметичные части не совсем чистые. «Было очень сложно точно определить источник и объяснить его степень детализации, которая позволила бы нам решить эту проблему», — сказала Фрэн Ройланд, исследователь метана в нефтегазовой промышленности в Think.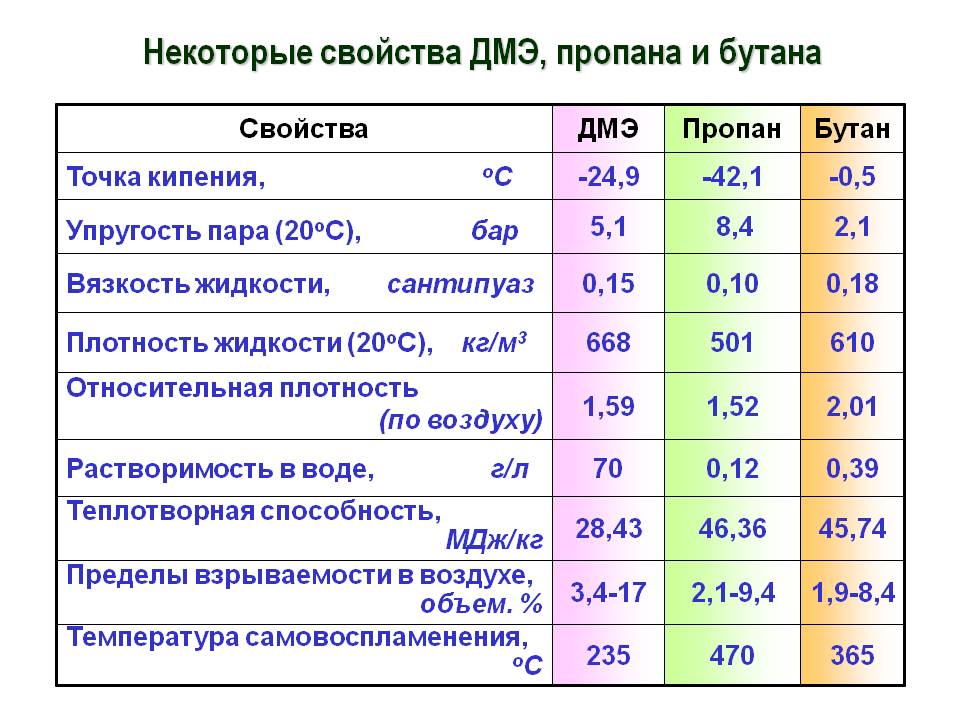 танк РМИ.«Поскольку это происходит на такой большой территории, осознание того, сколько всего выходит, является одной из основных проблем».
танк РМИ.«Поскольку это происходит на такой большой территории, осознание того, сколько всего выходит, является одной из основных проблем».
Еще одна неприятная проблема заключается в том, что выбросы метана колеблются. Carbon Mapper собрал воедино временной ряд участка Пермского бассейна на юго-западе США, в котором точки соответствуют выбросам метана. Примерно в половине случаев, по оценкам Дюрена, некоторые из самых серьезных нарушителей могут выбрасывать метан непосредственно в атмосферу для снижения давления, а другая половина, вероятно, связана с постоянными утечками и неисправностями.
Экологи утверждают, что мы должны как можно быстрее отказаться от угля, газа и нефти, но прекращение загрязнения не может ждать, пока переход завершится. Коалиция из 134 экологических и медицинских групп объединилась вокруг определенной цели — сократить к 2025 году выбросы метана в нефтегазовой отрасли на 65 процентов — и оказала давление на администрацию Байдена, чтобы она поставила ту же цель, используя существующие технологии.
Выгоды от сдерживания метана будут иметь решающее значение, поскольку мир продолжает играть со своим климатом.Исследование ученых EDF, опубликованное в рецензируемом журнале Environmental Research Letters, показало, что борьба с выбросами метана в нескольких секторах, включая нефть и газ, сельское хозяйство и мусорные свалки, может замедлить нынешние темпы безудержного потепления на ошеломляющие 30 процентов. Может показаться, что четверть градуса Цельсия к 2050 году не так уж и много, но небольшие изменения глобальных средних значений содержат ряд экстремальных воздействий, которые будут ухудшаться по всему миру.
Есть и хорошие новости: миру не нужно ждать улучшения науки.Действие возможно уже сейчас.
Оценки крупнейших источников метана в результате деятельности человека во всем мире. В Северной Америке крупнейшим источником является ископаемое топливо. Глобальная оценка метана ООН, 2021 г.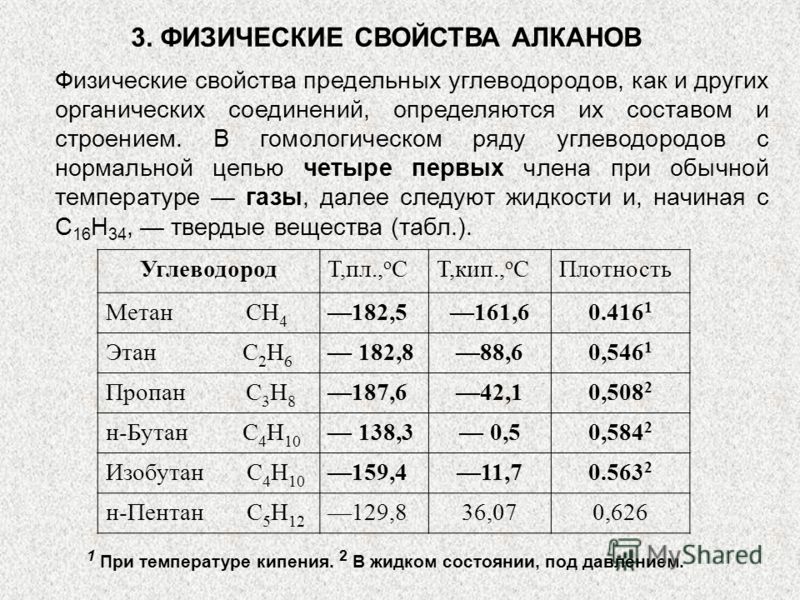
Вот что можно сделать с выбросами метана уже сейчас
Когда 9 августа был опубликован отчет МГЭИК, Лиза ДеВиль, член Совета по ресурсам Дакоты, проживающая в индейской резервации Форт-Бертхольд, была воодушевлена тем, что ученые «вторят тому, что большинство из нас может видеть своими глазами», основываясь на о том, что она видит на передовой нефтедобычи в Северной Дакоте.
«Земля рядом с моим домом испещрена нефте- и газопроводами, буквально усеяна буровыми установками», — сказал ДеВиль в разговоре с журналистами. Она сказала, что ее дом был разрушен необычно сильными дождями и наводнениями, и ей и ее мужу пришлось дышать дымом от лесных пожаров. «Я живу менее чем в миле от кустовых площадок, которые выбрасывают и сжигают метан и засоряют нашу атмосферу, от чего местные жители, такие как мой муж и я, болеют. Это означает, что земля, которая является частью моей идентичности как коренной женщины, превратилась в загрязненную промышленную зону.
Под давлением защитников климата Агентство по охране окружающей среды в ноябре предложило новый свод правил по метану. После окончательной доработки правила потребуют от нефтегазовых компаний отслеживать и устранять утечки метана из существующих и будущих скважин с использованием датчиков и регулярных проверок оборудования. Администрация заявляет, что новое правило распространяется на 75 процентов всех выбросов метана в США.
Предложение является лишь первым шагом на долгом пути к серьезному сокращению выбросов метана из нефти и газа. Правила могут столкнуться с длительными задержками, поскольку EPA собирает комментарии общественности, а противники подают иски.Они также рискуют потерпеть неудачу, если республиканец возьмет Белый дом на следующих двух выборах.
Существует широко распространенное мнение, даже среди представителей отрасли ископаемого топлива, что начинать следует с устранения утечек. Это станет проще, поскольку ученые соберут более точные данные о том, где происходит утечка метана.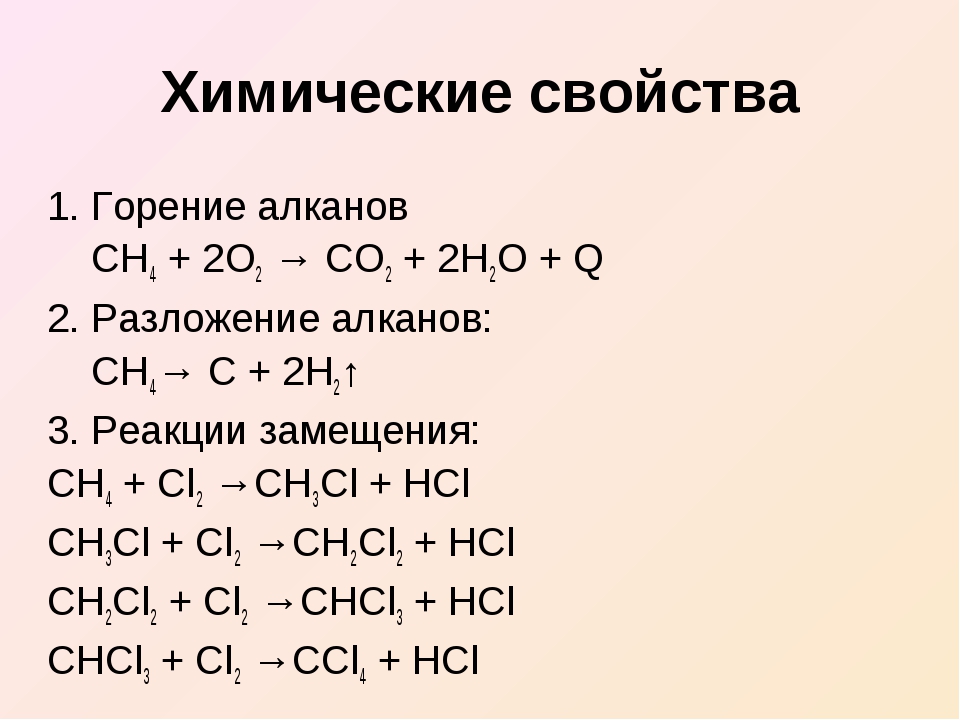 С точки зрения отрасли компании теряют продукт и доллары. Для активистов устранение утечек — это еще один шаг на пути к окончательному отказу от газа.
С точки зрения отрасли компании теряют продукт и доллары. Для активистов устранение утечек — это еще один шаг на пути к окончательному отказу от газа.
Несмотря на все разговоры отрасли об сдерживании утечек метана, нефтяные компании остаются одним из самых больших препятствий на пути ужесточения ограничений на метан в США.Конгресс обсуждает важную часть предложенного законопроекта «Восстановить лучше, чем было» — установить плату за выбросы метана, не только обеспечив лучший мониторинг метана, но и финансово побудив производителей нефти исправить наиболее проблемные области. Лобби нефтяной промышленности, Американский институт нефти, официально выступило против этой меры, которая считается одной из наиболее эффективных мер политики в области климата, которые все еще находятся на столе в повестке дня «Восстановить лучше, чем было».
Проблема, которая лежит в основе всех действий по борьбе с изменением климата, заключается в том, что человечество вынуждено обменивать краткосрочную прибыль на долгосрочную. Углекислый газ влияет на мир в долгосрочной перспективе, а метан значительно усугубляет кризис в ближайшей перспективе.
Углекислый газ влияет на мир в долгосрочной перспективе, а метан значительно усугубляет кризис в ближайшей перспективе.
Положительным моментом является то, что борьба с метаном и другими опасными загрязнителями принесет «немедленную отдачу», считает Шинделл из Глобальной оценки метана. Это может изменить нашу опасную климатическую траекторию в течение следующих 30 лет.
«Каждое действие имеет значение», — сказала Джейн Любченко, старший научный советник администрации Байдена, в августовском интервью Vox. «Каждая уклоненная десятая градуса имеет значение.
Доли градусов могут привести к диким колебаниям в экстремальных погодных условиях или к переломным моментам, которые мы даже не до конца понимаем. В усилиях по предотвращению климатической катастрофы большое значение будет иметь метан.
Обновление, 3 ноября, 16:00: . Эта история была обновлена, чтобы включить события на COP26 и объявление администрации Байдена о том, что она будет регулировать выбросы метана из новых и существующих нефтегазовых месторождений.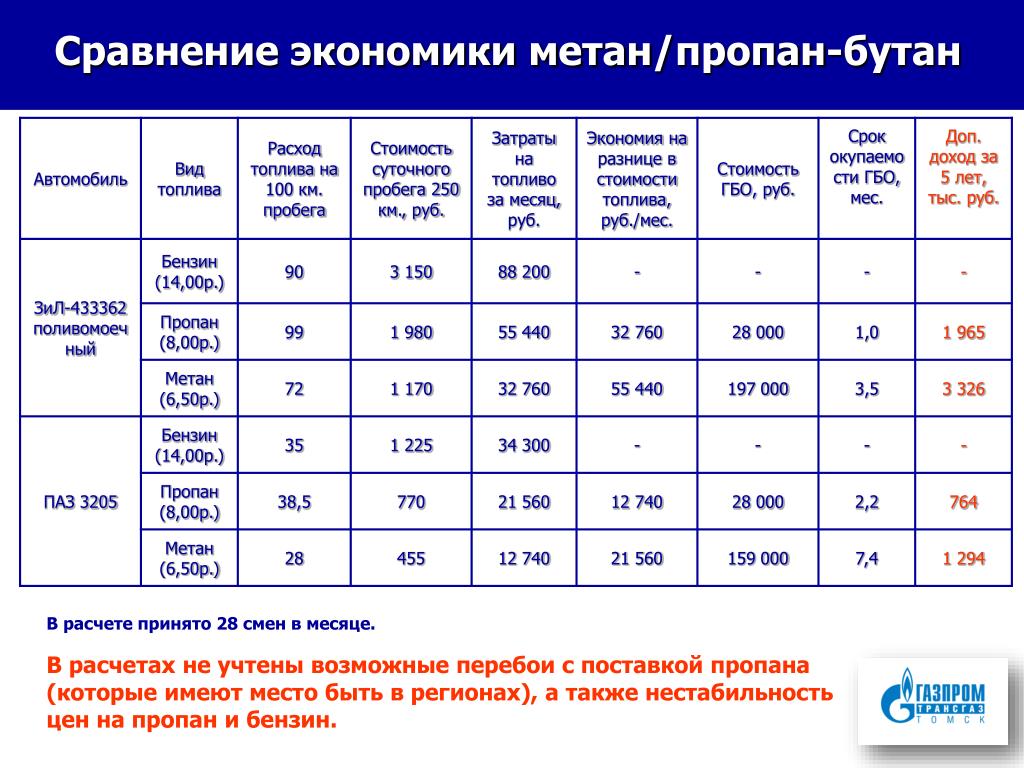
Исправление, 4 ноября, 12:45: Ранее в этой статье загрязняющий диоксид азота (NO2) ошибочно идентифицировали как парниковый газ.Закись азота (N2O) является парниковым газом.
Деревья выделяют легковоспламеняющийся метан — вот что это означает для климата
Эта статья была создана в сотрудничестве с Национальным географическим обществом.
В 1907 году Фрэнсис У. Бушонг, профессор химии Канзасского университета, сообщил о новом открытии в журнале Chemical and Physical Papers . Он нашел метан, основной компонент природного газа, в дереве.
Несколько лет назад, писал он, он срубил несколько тополей и «наблюдал образование пузырей в соке на свежесрубленном стволе, пне и щепках.Когда он чиркнул спичкой, газ воспламенился голубым пламенем. В университете он воспроизвел испытание пламенем на тополе кампуса и на этот раз взял образцы газа. Концентрация метана была ненамного ниже уровня, измеренного в пробах с месторождений природного газа в Канзасе.
О находке сообщалось в основном как о новинке, но затем она канула в Лету.
Метан с деревьев вернулся, причем с размахом.
Расширяющаяся сеть исследователей обнаружила, что метан вытекает из деревьев из обширных затопленных лесов бассейна Амазонки в заболоченные торфяники Борнео, из горных лесов умеренного пояса в Мэриленде и Венгрии до лесистых горных склонов в Китае.
Несмотря на то, что они привязывают инструменты стоимостью 50 000 долларов к деревьям для регистрации потоков газа, многие из этих исследователей не могут устоять перед использованием зажигалки или спички, чтобы получить такое же голубое пламя, которое застало профессора Бушонга врасплох более века назад.
Но исследования теперь основаны не только на новизне. Метан уступает только углекислому газу по важности выбросов парниковых газов, связанных с глобальным потеплением. В трубопроводе природного газа метан является относительно чистым ископаемым топливом.Но это мощное улавливающее тепло дополнение к парниковому эффекту планеты, когда оно накапливается в атмосфере.
Метан, выпущенный огнем дерева. Авторы и права: Дэниел Йип и Кристофер Шадт, Окриджская национальная лаборатория
Газ накапливается до тех пор, пока новые выбросы опережают скорость, с которой естественные химические реакции в воздухе или в некоторых лесных почвах разрушают его (это обычно занимает около десяти лет по сравнению с до веков для двуокиси углерода). С 1750 года концентрация в атмосфере выросла более чем на 250 процентов (с примерно 700 частей на миллиард до более чем 1800 частей на миллиард).Основными человеческими источниками, связанными с ростом, являются глобальное сельское хозяйство, особенно животноводство и рисовые поля, свалки и выбросы от нефтегазовых операций и угольных шахт.
Природные источники всегда производили большое количество газа — в настоящее время наравне с сельскохозяйственными. Основным источником является микробная активность в лишенных кислорода сырых почвах и заболоченных местах. (Похоже, что потепление, вызванное деятельностью человека, расширяет водно-болотные угодья, особенно в высоких широтах, увеличивая выбросы метана. )
)
Полное воздействие метана из деревьев на климат не идет ни в какое сравнение с десятками миллиардов тонн углекислого газа, ежегодно выбрасываемого из дымовых труб и выхлопных труб, или метаном, скажем, от огромных стад крупного рогатого скота или газовых месторождений человечества. Но в оценках, устанавливающих «глобальный баланс метана», существует достаточная неопределенность, поэтому деревья могут оказаться существенным источником.
На данный момент это только что открытая граница, сказал Кристофер Кови, ученый из колледжа Скидмор, занимающийся химией и экологией лесов.
«В глобальном масштабе это может быть огромным»
«Выбросы от отдельного дерева невелики», — сказал Кови. «Но есть несколько триллионов деревьев. В глобальном масштабе это может быть огромным». Прошлой весной Кови организовал международный семинар для определения приоритетов исследований и только что опубликовал статью в журнале New Phytologist , которая, по сути, является призывом о помощи к целому ряду дисциплин, еще не сфокусированных на этом вопросе. Его соавтором является Дж. Патрик Мегонигал, исследователь деревьев из Смитсоновского центра экологических исследований в Мэриленде.
Его соавтором является Дж. Патрик Мегонигал, исследователь деревьев из Смитсоновского центра экологических исследований в Мэриленде.
Новые статьи публикуются месяц за месяцем с поразительной быстротой, при этом каждое полевое измерение, по сути, представляет собой новое открытие, которое можно опубликовать.
«Мы все еще находимся на этапе сбора марок, — сказал Кови.
Находки уже бросают вызов старым нормам. Долгое время считалось, что сухие горные леса удаляют метан из воздуха под действием класса почвенных микробов, называемых метанотрофами. Но работа Мегонигала и других показывает, что выбросы деревьев могут уменьшить или, возможно, превысить способность очистки от метана.
Введенный в заблуждение «плоским миром»
Как этот эффект, измеренный Бушонгом в 1907 году и неофициально отмеченный учеными-лесоводами на протяжении поколений, оставался скрытым так долго?
В течение десятилетий ученые, изучающие потоки метана между наземными экосистемами и воздухом, устанавливали свои инструменты на земле, никогда не думая о том, что деревья могут быть замешаны, сказал Винсент Гаучи, профессор экологии глобальных изменений в Британском открытом университете и автор исследования. ряд недавних работ о роли метана деревьев.
Все упустили из виду, что стебли, стволы и листья деревьев тоже являются поверхностями, и газ может течь и там. «Мы смотрели на плоский мир, — сказал Гаучи.
Не более. Считается, что большая часть метана, который в настоящее время выделяется деревьями в таких влажных условиях, представляет собой микробный метан, который нагнетается и выбрасывается по мере того, как кислород поступает к корням. Но Гаучи и другие ученые обнаруживают множество случаев, когда деревья производят свой собственный метан — иногда из микробов в сердцевине дерева или других тканях, а в других случаях — в результате замечательной прямой фотохимической реакции, которая, как считается, управляется ультрафиолетовыми длинами волн солнечного света.
Выбросы деревьев, измеренные в некоторых регионах, огромны: международная группа под руководством Суниты Пангала из Ланкастерского университета в прошлом году оценила в Nature , что только деревья в сезонно затопляемых лесах Амазонки были источником от 14 до 25 миллионов выбросов. метрических тонн газа в год — количество, аналогичное оценкам выбросов метана из тундры по всей Арктике.
Может показаться не таким уж удивительным думать о деревьях в лесах Амазонки как о каналах для этого газа, учитывая, что влажные почвы, торфяные болота и другие среды с низким содержанием кислорода являются областью обитания микробов, которые производят этот газ.Но другие исследования показали, что деревья выделяют значительное количество метана даже в засушливых горных экосистемах — в некоторых случаях в стволе дерева, а не в почве.
Такие находки стимулировали еще большую работу, и кажется, что куда бы кто ни посмотрел, картина становится более последовательной и запутанной.
В любом масштабе, от целых лесов до групп похожих деревьев в лесу и динамики отдельных деревьев, единственной константой является изменчивость, сказал Мегонигал из Смитсоновского исследовательского центра в Мэриленде.
Кови описал леса, в которых одинаковые деревья на сходных почвах были измерены с пятидесятикратной разницей в выбросах метана.
Было измерено, что некоторые деревья выделяют метан у основания и поглощают его выше по стволу.
Но это еще не все. Более тщательный анализ показал, что отдельное дерево может поглощать метан у основания посредством микробных процессов и выделять его выше по стволу.
Добавляя еще один, возможно, обнадеживающий поворот, оказывается, что некоторые деревья действительно впитывают метан.Работа еще не опубликована, но в прошлом году Гаучи, Пангала и еще один коллега представили ее на собрании Европейского союза наук о Земле.
В ходе исследования изучались потоки метана в деревьях во влажных и сухих почвах из Центральной Америки и Амазонки в Великобританию и Швецию. Деревья во влажных почвах всегда были чистыми источниками метана, но деревья в более сухих условиях в некоторых регионах фактически были чистыми поглотителями газа.
Уроки для климатической политики
Новые данные о метане и лесах, вероятно, вызовут дискуссии о следующих шагах климатической политики, связанной с лесами, которая долгое время была сосредоточена на способности деревьев поглощать и накапливать углекислый газ, при этом уделяя мало внимания к другим свойствам.
«Что мы знаем о лесах, так это то, что они улавливают углерод, — сказал Кови. «Это то, что вы узнаете, что изображено на карикатурном рисунке леса в третьем классе».
С климатом все сложнее. «Глобальное потепление есть, но глобального леса нет», — сказал он.
Парижское соглашение 2015 года об изменении климата поддерживает лесные проекты как способ сокращения выбросов углекислого газа, которые странам до сих пор не удавалось ограничить у источника. Организация Объединенных Наций запустила кампанию «Триллион деревьев».У компаний и потребителей есть множество способов потратить деньги на лесные проекты за счет «компенсации выбросов углерода», чтобы компенсировать выбросы от путешествий и тому подобное.
В интервью Кови и другие исследователи, изучающие вопрос о древесном метане, подчеркивают, что они не утверждают, что такие усилия следует приостановить, отмечая множество преимуществ сохранения лесов, включая хранение углерода, устойчивость к наводнениям и защиту экосистем, богатых видами.
Независимо от климатической дипломатии, страны всего мира работают над ускорением сохранения лесов в рамках отдельного соглашения, Конвенции о биологическом разнообразии, чтобы сохранить их ценность как место обитания огромного количества видов.
Но результаты исследования метана подчеркивают важность оценки всего спектра климатических воздействий — в лучшую или худшую сторону — различных типов леса и деревьев в разных регионах. Как и в случае с более глубоким пониманием экологии леса, это может помочь проектам максимизировать выгоды и ограничить риски.
В последние годы другие исследования, посвященные полному влиянию лесов на климатическую систему, показали, как сосредоточение внимания на CO2 может упустить значительные дополнительные охлаждающие преимущества лесов и — в некоторых регионах и свойствах лесов — значительные эффекты потепления.
«Для некоторых лесов все стрелки указывают в одном направлении», — сказал Кови, описывая различные способы воздействия деревьев на климат. «Есть и другие места, где стрелки не совпадают».
Он и другие исследователи говорят, что более четкое представление может улучшить климатические модели, а также помочь обеспечить максимальную эффективность программ, ориентированных на климатическую ценность лесов.
В более высоких широтах простой переход от отражающей свет открытой земли к темным кронам деревьев с грубой поверхностью может согреть местный климат, поглощая больше солнечного света.Леса в тропиках особенно ценны для местного климата, поскольку они охлаждают воздух вокруг них, поскольку их метаболический механизм приводит к огромному испарению, что также может привести к большему количеству облачного покрова и осадков, блокирующих солнце.
Другая работа показала, как сложный набор летучих органических соединений, выделяемых деревьями, вступает в реакцию, создавая дымку и облака, влияя на температуру и осадки различными способами. В 2014 году разгорелись дебаты по поводу чрезмерных заголовков, подразумевающих, что эта работа, особенно исследования атмосферного химика Надин Унгер, тогда работавшей в Йельском университете, означала, что леса не следует спасать.
Никто из опрошенных для этой статьи, включая Унгера, так не считает. Она сказала, что сейчас в Эксетерском университете необходимы всесторонние оценки лесов и климата с учетом всего набора свойств.
Что особенно примечательно сейчас, так это то, что она и некоторые из ее прошлых критиков подчеркивают, что главное внимание в мире должно быть сосредоточено на сокращении выбросов углекислого газа в источнике, даже несмотря на то, что леса сохранены для всех преимуществ, которые они обеспечивают.
«Наш лучший способ достичь глобальных целей Парижского соглашения по температуре — это сфокусироваться на сокращении выбросов CO2 в результате использования энергии в богатых странах средних широт», — сказал Унгер.
Ее точка зрения перекликается с комментарием ряда ученых в выпуске Science от 1 марта о том, чтобы «естественные климатические решения», включая проекты, ориентированные на леса, не рассматривались как альтернатива проведению глубоких и оперативных сокращений в теплицах. — газовые выбросы. Оба будут необходимы, сказали они.
Уильям Р. Мумоу, почетный профессор международной экологической политики Университета Тафтса, сказал, что всегда будут неточности в измерении всего комплекса климатических влияний лесов.Но это не должно мешать продвижению программ по их расширению или повышению их способности удерживать углерод. По словам Мумо, масса доказательств по-прежнему указывает на то, что леса являются ключом к поддержанию безопасного климата.
«Учитывая, что леса были основными факторами стабильного баланса углерода и температуры в течение последних 10 000 лет, пока люди не начали их вырубать, а также сжигать, можно предположить, что баланс всех факторов был примерно правильным».
Эндрю Ревкин является стратегическим советником по экологической и научной журналистике в Национальном географическом обществе и уже 30 лет пишет о глобальном потеплении.Он является автором трех книг о климате, последняя из которых — «Погода: иллюстрированная история, от атласов облаков до изменения климата ».



 Это означает, что обычно в случае утечки газа в опасности находятся квартиры сверху, но газ может и двигаться в соседние квартиры.
Это означает, что обычно в случае утечки газа в опасности находятся квартиры сверху, но газ может и двигаться в соседние квартиры.
 В следствии этого в организме человека образуется опасное вещество – карбоксигемоглобин.
В следствии этого в организме человека образуется опасное вещество – карбоксигемоглобин. При сильном отравлении человек теряет сознание и наступает смерть.
При сильном отравлении человек теряет сознание и наступает смерть. Например, газовые установки соединили друг с другом в неподходящие дымоходы. Часто устанавливали такие газовые установки в закрытые шкафы. Со временем дымоходы забивались, а сгораемый воздух оставался в квартире.
Например, газовые установки соединили друг с другом в неподходящие дымоходы. Часто устанавливали такие газовые установки в закрытые шкафы. Со временем дымоходы забивались, а сгораемый воздух оставался в квартире.


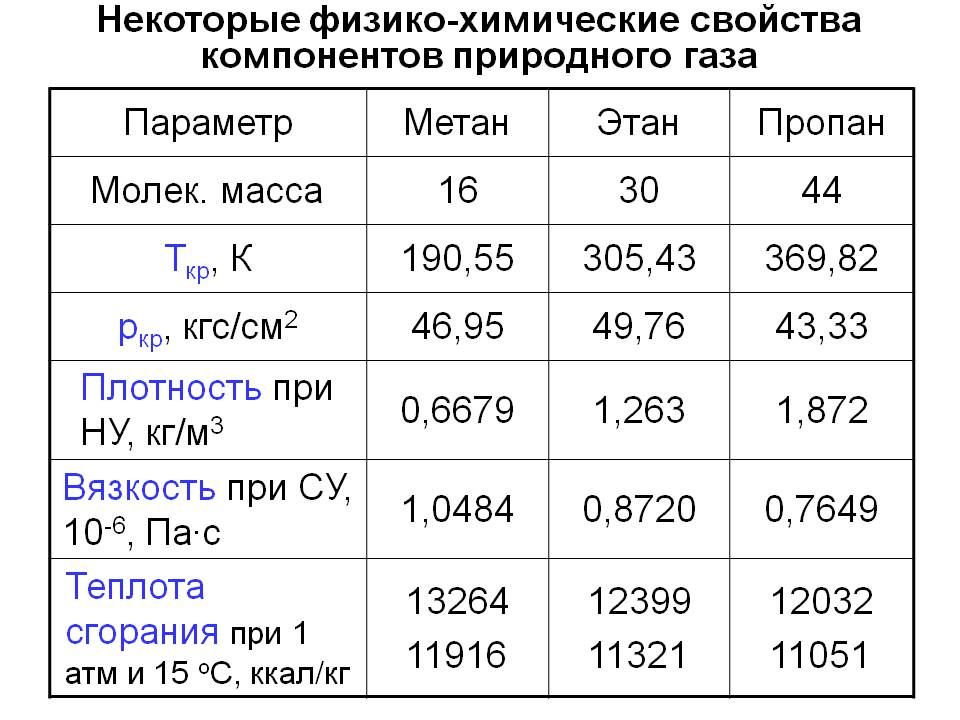 Это значит, что батарейку следует немедленно заменить.
Это значит, что батарейку следует немедленно заменить.