Переход на водород
Водород и сегодня используют для производства удобрений, повышения качества бензина, улучшения свойств стали, а также в пищевой промышленности для производства маргарина и твердых кондитерских жиров методом гидрогенизации растительных масел. Без него не обходятся все процессы гидроочистки, гидрообессеривания, гидрокрекинга, регенерации катализаторов. Его также широко применяют для охлаждения генераторов на электростанциях.
С тех пор как появилась перспектива перехода на водородную энергетику с углеводородной, потребность в водороде увеличилась на порядки. Сегодня эта перспектива стала реальностью, поскольку примерно десять лет назад была решена одна из основных проблем с его хранением для дальнейшего использования в качестве автомобильного топлива. Вместо тяжелых, дорогих и небезопасных стальных баллонов для сжатого под высоким давлением водорода стали применять легкие композитные емкости из углепластика, которые прекрасно помещаются в легковых автомобилях. Кроме того, стало возможным получать водород прямо по месту употребления. Появление таких технологий зажгло для водородной энергетики зеленый свет.
Кроме того, стало возможным получать водород прямо по месту употребления. Появление таких технологий зажгло для водородной энергетики зеленый свет.
Около 20 лет назад во всем мире начали появляться автомобили на водороде, и бывшие выставочные центры пилотных моделей превратились в салоны-магазины серийных образцов. Количество автомобилей на водородном топливе сегодня исчисляется тысячами. Их стоимость составляет около $50–60 тыс. Серийные автомобили на водороде есть у Toyota, Hyundai, Honda. Предсерийные образцы тестируют Audi, Mercedes, BMW, Mazda, Ford и ряд других производителей. Все технические препятствия, столько десятилетий казавшиеся непреодолимыми, пройдены за считаные годы, и теперь вопрос только в экономической целесообразности для массового потребителя. В России такой автомобиль приобрел себе житель Красноярска, но в связи с отсутствием заправок в своем городе перевез машину в Москву и получает топливо в одном из научных институтов.
Как получить водород?
Для развития водородной энергетики нужно будет на государственном уровне решить вопрос, в каком виде доставлять водород к месту его получения.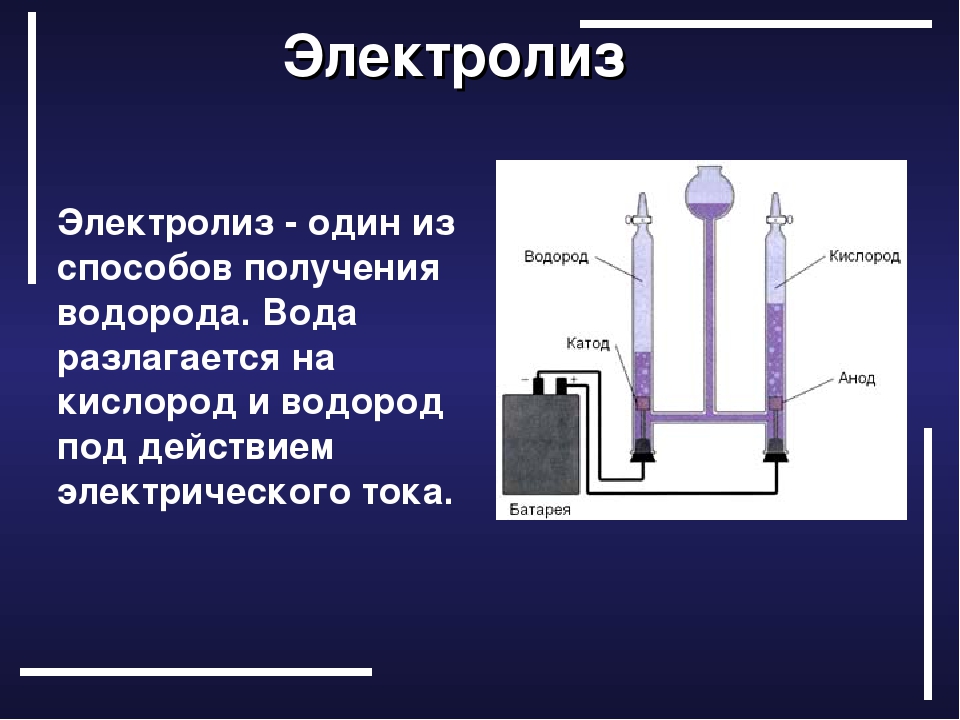 Дело в том, что водород содержится в очень многих видах ископаемых топлив.
Дело в том, что водород содержится в очень многих видах ископаемых топлив.
«Наиболее дешевый водород получается методом паровой конверсии метана,— рассказывает заведующий отделом гетерогенного катализа Института катализа СО РАН Павел Снытников.— Другой способ — из аммиака. Для его транспортировки, как и для природного газа, в нашей стране даже существует трубопровод, так как аммиак сжижается всего при давлении 8,5 атмосферы. Третье решение — перевозка будущего водорода в виде метанола. В Китае метанол используют как автомобильное топливо. Но в России против метанола почему-то предубеждение, по-видимому, в связи с тем, что с давних пор у нас простой народ пил все, что горело, в том числе и метанол, и люди лишались зрения».
А вот получать его лучше всего там же, где будут потреблять, чтобы уйти от проблем транспортировки чистого водорода. Чтобы использовать водород, например, как автомобильное топливо, нужно закачать его в баллоны под давлением 700 атмосфер. Правда, на сжатие нужна дополнительная энергия. Не меньше энергии требуется на сжижение водорода, так что один из подходящих способов его транспортировки — это перевозка в химически связанном состоянии, например в виде метана, из которого водород должен производиться там же, где будет использоваться. То есть до заправки везут метан, а уже на самой заправке устанавливается небольшое производство, например, конвертер метана в водород. Но этот способ не очень хорош для экологии, поскольку на небольших производствах сложно обеспечить качественную очистку выбросов. Зато экономически он себя вполне оправдывает. Опыт Японии, Кореи и ряда других стран показал, что километр пробега на водороде выходит не дороже бензина. 4 кг водорода, закачанного в баллон, хватает примерно на 800 км пути обычного седана.
Правда, на сжатие нужна дополнительная энергия. Не меньше энергии требуется на сжижение водорода, так что один из подходящих способов его транспортировки — это перевозка в химически связанном состоянии, например в виде метана, из которого водород должен производиться там же, где будет использоваться. То есть до заправки везут метан, а уже на самой заправке устанавливается небольшое производство, например, конвертер метана в водород. Но этот способ не очень хорош для экологии, поскольку на небольших производствах сложно обеспечить качественную очистку выбросов. Зато экономически он себя вполне оправдывает. Опыт Японии, Кореи и ряда других стран показал, что километр пробега на водороде выходит не дороже бензина. 4 кг водорода, закачанного в баллон, хватает примерно на 800 км пути обычного седана.
Получать водород можно практически из любого углеводородного топлива: из бензина, дизельного топлива или пропан-бутановых смесей. В Институте катализа им. Г. К. Борескова СО РАН ведется работа по гранту РНФ по тематике получения водорода из дизельного топлива. Также разрабатываются методы получения водорода даже из органических носителей, например из бор-гидридов. Главные задачи на будущее развитие водородной энергетики — это не только получение водорода, но и его хранение. Жидкий водород можно хранить только при низких температурах, поэтому его использовали только в критически важных областях, например, как ракетное топливо.
Также разрабатываются методы получения водорода даже из органических носителей, например из бор-гидридов. Главные задачи на будущее развитие водородной энергетики — это не только получение водорода, но и его хранение. Жидкий водород можно хранить только при низких температурах, поэтому его использовали только в критически важных областях, например, как ракетное топливо.
Если отвлечься от автомобилей и обратить внимание на энергообеспечение более крупных стационарных объектов, например жилых или промышленных комплексов, то вся идеология водородной энергетики строится на ее связке с другими источниками энергии. Например, с возобновляемыми — гидро-, ветряными, солнечными электростанциями или с крупными атомными электростанциями. Производство такой энергии идет в одном режиме, а тратится потребителями она в другом, поэтому, когда есть излишки энергии, ее можно тратить на получение водорода даже из обычной воды методом электролиза.
Голубая мечта о зеленом водороде
Электролиз — это способ получения водорода из воды, который, к сожалению, требует больших энергозатрат, поэтому он оправдан только в тех случаях, когда вырабатываемую энергию необходимо запасти, пусть даже и с невысоким КПД. Лучше всего использовать для этого источники, где постоянно возникают достаточно большие излишки энергии. Емкости аккумуляторов для ее сохранения не хватает, кроме того, аккумуляторы быстро разряжаются, а полученный методом электролиза водород — это гарантированный запас энергии, можно сказать, воплощение мечты о чистой энергии, так называемом зеленом водороде. К сожалению, пока всего 2% общего объема водорода в мире производится методом электролиза. 75% водорода получают из природного газа и 25% — сжиганием угля. Цены топлива, полученного по этим технологиям, также несопоставимы: $1,7 за 1 кг водорода из природного газа и $5–10 за водород, полученный электролизом. Впрочем, стоимость зависит от источника энергии. Например, от энергии АЭС зеленый водород вдвое дешевле ($3–5), чем от возобновляемых источников энергии.
Лучше всего использовать для этого источники, где постоянно возникают достаточно большие излишки энергии. Емкости аккумуляторов для ее сохранения не хватает, кроме того, аккумуляторы быстро разряжаются, а полученный методом электролиза водород — это гарантированный запас энергии, можно сказать, воплощение мечты о чистой энергии, так называемом зеленом водороде. К сожалению, пока всего 2% общего объема водорода в мире производится методом электролиза. 75% водорода получают из природного газа и 25% — сжиганием угля. Цены топлива, полученного по этим технологиям, также несопоставимы: $1,7 за 1 кг водорода из природного газа и $5–10 за водород, полученный электролизом. Впрочем, стоимость зависит от источника энергии. Например, от энергии АЭС зеленый водород вдвое дешевле ($3–5), чем от возобновляемых источников энергии.
Основные организации в России, заинтересованные в получении водорода — это компании «Росатом» и «Газпром». Атомные электростанции нуждаются в сохранении избытка энергии в виде водорода и дальнейшего его использования. А добывающая компания хочет перерабатывать природный газ в водород, имея соответствующие установки непосредственно в местах использования, например на автомобильных заправках. Для решения проблемы транспортировки водорода можно переводить его в спирты — метанол, диметиловый эфир, чтобы получать из них водород, что называется, «по требованию» для дальнейшего использования на энергоустановках. Это химия получения водородсодержащих компонентов, и она достаточно хорошо освоена.
А добывающая компания хочет перерабатывать природный газ в водород, имея соответствующие установки непосредственно в местах использования, например на автомобильных заправках. Для решения проблемы транспортировки водорода можно переводить его в спирты — метанол, диметиловый эфир, чтобы получать из них водород, что называется, «по требованию» для дальнейшего использования на энергоустановках. Это химия получения водородсодержащих компонентов, и она достаточно хорошо освоена.
Как перестать сжигать топливо
Вообще, заявления о том, что водород — это экологически чистое топливо, не совсем справедливы. Из школьного курса химии мы помним, что после сжигания водорода получается вода. Но горит-то он в воздухе, где высокое содержание азота, и в результате реакции кислорода и азота при высоких температурах мы получаем те же токсичные оксиды азота, что и при сжигании бензина, только в меньшем объеме. Собственно, водород здесь ни при чем: любое высокотемпературное горение вызывает в воздухе реакцию взаимодействия кислорода и азота с образованием оксидов. По этой причине получать электричество с помощью сжигания любого топлива — это не самый экологичный способ. А тем более углеводородного, которое сгорает с выделением выбросов углекислого газа в атмосферу. Чтобы решить проблемы с выбросами в атмосферу, нужно прекратить сжигать топливо и снизить градус его потребления до комнатной температуры. В этом могут помочь топливные элементы.
По этой причине получать электричество с помощью сжигания любого топлива — это не самый экологичный способ. А тем более углеводородного, которое сгорает с выделением выбросов углекислого газа в атмосферу. Чтобы решить проблемы с выбросами в атмосферу, нужно прекратить сжигать топливо и снизить градус его потребления до комнатной температуры. В этом могут помочь топливные элементы.
Применение водорода в топливных элементах является самым экологичным. Разные топливные элементы используют водород при разных температурах и могут быть более или менее привередливы к его чистоте. Низкотемпературные топливные элементы работают на чистом водороде, а высокотемпературные вполне удовлетворяются синтез-газом. Топливный элемент — это электрохимическое устройство, которое преобразует химическую энергию водорода в электрическую (процесс, обратный электролизу) с достаточно высоким КПД. Институт катализа СО РАН сотрудничает с российскими производителями топливных элементов — ГК «ИнЭнерджи» и Институтом проблем химической физики РАН, где были разработаны и созданы сверхлегкие топливные элементы для беспилотных летательных аппаратов. В настоящее время там ведутся разработки более крупных топливных элементов для автомобильных передвижных платформ. Рынок топливных элементов еще только формируется, поскольку область их применения постоянно растет. Появляются новые возможности в разработке — осваивается новый экономический сектор. Вопросы могут быть самые разные — например, обеспечение дальних трасс или камер видеонаблюдения источниками связи или возможность установки автономных вышек сотовой связи. Источники водородной энергии всегда работают как тандем «топливный элемент на водороде плюс аккумулятор». Аккумулятор способен сглаживать пиковые нагрузки, а топливный элемент обеспечивает длительную выработку электроэнергии.
В настоящее время там ведутся разработки более крупных топливных элементов для автомобильных передвижных платформ. Рынок топливных элементов еще только формируется, поскольку область их применения постоянно растет. Появляются новые возможности в разработке — осваивается новый экономический сектор. Вопросы могут быть самые разные — например, обеспечение дальних трасс или камер видеонаблюдения источниками связи или возможность установки автономных вышек сотовой связи. Источники водородной энергии всегда работают как тандем «топливный элемент на водороде плюс аккумулятор». Аккумулятор способен сглаживать пиковые нагрузки, а топливный элемент обеспечивает длительную выработку электроэнергии.
Сегодня в мире на топливных элементах работают тысячи небольших энергоустановок. В США, Японии и некоторых странах Европы они уже около 30 лет снабжают водородной энергией небольшие частные поселки, большие и удаленные от города супермаркеты или промышленные объекты. В отличие от дизель-генераторов это намного более бесшумные системы, так что их широко используют как запасные источники энергии в случае сбоев в работе основного источника энергообеспечения.
Сколько стоит чистый воздух
В качестве грантового финансирования на развитие индустрии водородной энергетики некоторые страны ЕС ежегодно выделяют сотни миллионов евро, США — сотни миллионов долларов. Совокупные вложения Европы и США в эту отрасль исчисляются миллиардами. Сейчас многие компании во всем мире делают попытки использовать источники энергии на топливных элементах в самых разных областях. В ближайшие десятилетия может измениться сама концепция человеческого энергопотребления.
В России развитие топливных элементов исторически связано с космическими программами в середине ХХ века. Щелочные топливные элементы использовались во многих космических проектах, где требовались автономные энергоустановки.
В 2020 году правительство России утвердило энергетическую стратегию Российской Федерации на период до 2035 года и ключевые меры развития водородной энергетики. В этом же году был создан консорциум по водородной энергетике, куда вошли ведущие научные институты: Томский политехнический университет, Институт катализа СО РАН, Институт проблем химической физики РАН, Институт нефтехимического синтеза РАН, Самарский государственный политехнический университет и Сахалинский государственный университет. В программе развития водородной энергетики РФ намечено создание водородных кластеров и пилотных проектов по производству и экспорту водорода. Планируется развитие первых коммерческих проектов производства водорода. Сегодня в РФ появляются отдельные пилотные проекты с использованием водородной энергетики, но до массового внедрения пока не дошло: скорее производители демонстрируют свою готовность к реализации подобных проектов в случае выделения финансирования со стороны, например, госкорпораций. Так, в конце 2019 года в Санкт-Петербурге был запущен трамвай на водородном топливе, а ОАО «Газпром» и ОАО «РЖД» в качестве пилотного проекта обсуждают возможность запуска поезда на Сахалине на топливных водородных элементах.
В программе развития водородной энергетики РФ намечено создание водородных кластеров и пилотных проектов по производству и экспорту водорода. Планируется развитие первых коммерческих проектов производства водорода. Сегодня в РФ появляются отдельные пилотные проекты с использованием водородной энергетики, но до массового внедрения пока не дошло: скорее производители демонстрируют свою готовность к реализации подобных проектов в случае выделения финансирования со стороны, например, госкорпораций. Так, в конце 2019 года в Санкт-Петербурге был запущен трамвай на водородном топливе, а ОАО «Газпром» и ОАО «РЖД» в качестве пилотного проекта обсуждают возможность запуска поезда на Сахалине на топливных водородных элементах.
Тестовое оборудование для установок по производству водорода электролизом воды
Водород является уникальным энергоносителем, обладающим высокими эксплуатационными и технологическими показателями. Он имеет очень высокой теплоту сгорания, а продуктом горения в кислороде является вода, которая может вновь использоваться для получения водорода. Низкая вязкость и плотность газа позволяют практически без потерь давления транспортировать его по трубопроводам. Водород может транспортироваться и храниться как в газообразном, так и сжиженном состоянии. А кроме того он безопасен для окружающей среды и не токсичен.
Он имеет очень высокой теплоту сгорания, а продуктом горения в кислороде является вода, которая может вновь использоваться для получения водорода. Низкая вязкость и плотность газа позволяют практически без потерь давления транспортировать его по трубопроводам. Водород может транспортироваться и храниться как в газообразном, так и сжиженном состоянии. А кроме того он безопасен для окружающей среды и не токсичен.
Однако в чистом виде водород в природе не встречается. Существует целый ряд методов его получения. Разнообразие этих методов — одно из преимуществ водородной энергетики. Нет сильной зависимости от какого-либо отдельного вида сырья.
Наиболее распространенным способом получения водорода является паровая конверсия посредством реакции углеводородов (природный газ) с паром при высоких температурах. При этом в качестве побочного продукта выделяются парниковые газы, выброс которых в настоящее время стараются минимизировать. Другой способ производства водорода – электролиз воды. Здесь отсутствуют вредные выбросы. А цена и эффективность процесса электролиза сопоставима с технологией паровой конверсии.
Здесь отсутствуют вредные выбросы. А цена и эффективность процесса электролиза сопоставима с технологией паровой конверсии.
В электролизере под воздействием подаваемого напряжения вода разделяется на водород и кислород. Для получения более чистого водорода оба газа должны быть отделены друг от друга разделительной мембраной. При создании электролизеров стоит задача определения характеристик пропускания таких мембран. Испытательное оборудование должно обеспечивать точную подачу чистых водорода и кислорода, а измерять расход и состав прошедшего через мембрану газа.
Специалистами Bronkhorst было предложено следующее решение. Подача кислорода к испытуемой мембране осуществлялась кориолисовым регулятором массового расхода серии miniCORI-FLOW, а водорода – тепловым регулятором расхода серии EL-FLOW Prestige. Часть подаваемого газа, которая проходит через мембрану, поступает в трехходовой кран. В одном положении крана можно измерять расход прошедшего газа с помощью теплового расходомера EL-FLOW Prestige.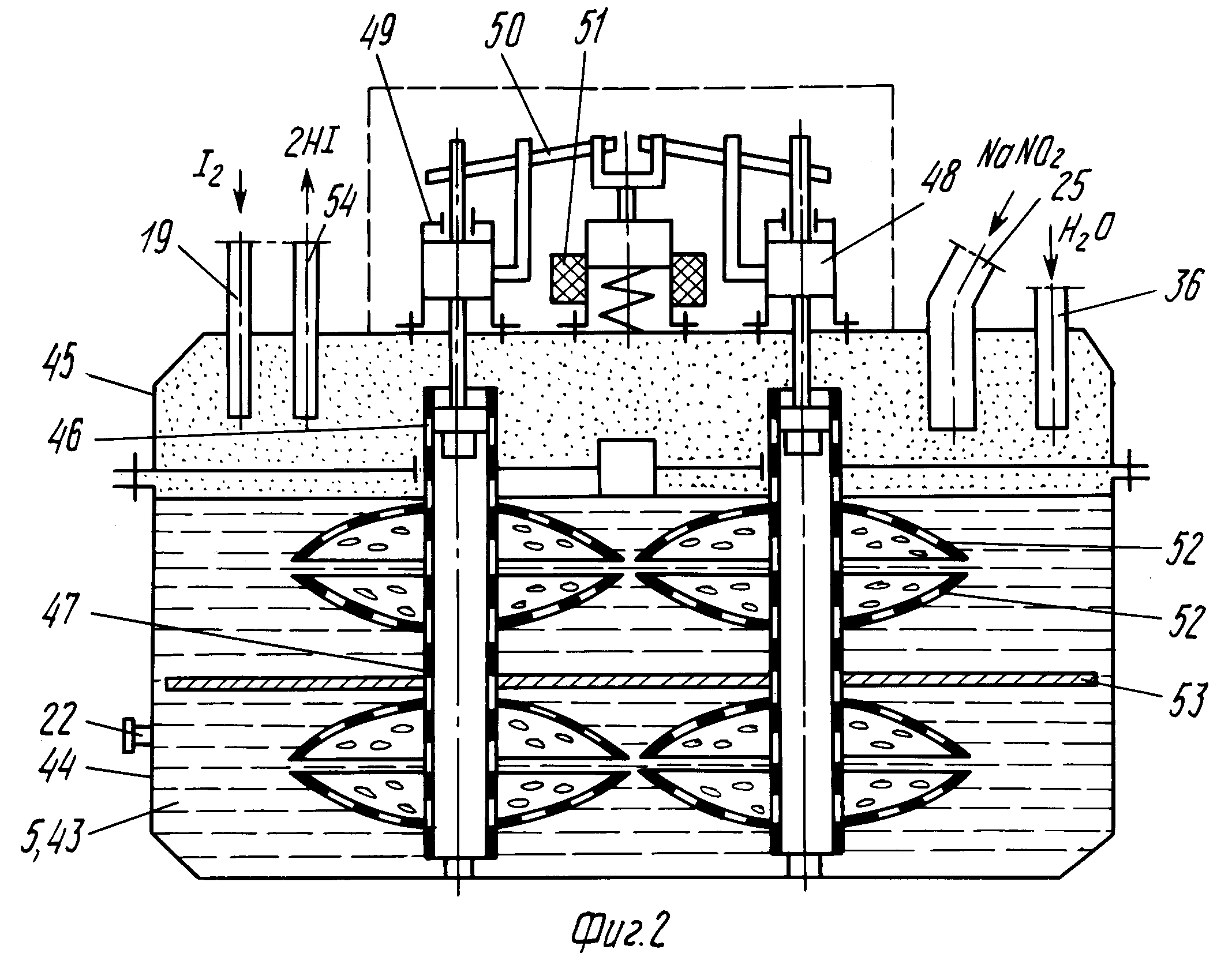 В другом – состав газа с помощью двойного датчика водород/кислород. Особенность использованного датчика состояла в том, что для его работы требовался определенный расход газа.
В другом – состав газа с помощью двойного датчика водород/кислород. Особенность использованного датчика состояла в том, что для его работы требовался определенный расход газа.
Высокая точность и стабильность поддержания расхода использованными расходомерами позволила с успехом решить поставленную задачу. Позже было принято решение об установке четвертого расходомера для измерения части подаваемого газа, не прошедшего через мембрану и имеющего высокую концентрацию кислорода. Выбор был сделан в пользу кориолисового расходомера серии miniCORI-FLOW.
Проблема зеленого водорода, о которой никто не говорит
Гигаватт за гигаваттом зеленой водородной мощности планируется построить в Европе, Азии и Австралии. По мнению сторонников этой технологии, зеленый водород — тот, который вырабатывается электролизом на солнечных батареях, ветре и других возобновляемых источниках энергии, — является лучшим способом обезуглероживания тяжелых загрязнителей окружающей среды. Сейчас много говорят о снижении стоимости солнечной и ветровой энергии и о том, как они очень скоро сделают зеленый водород жизнеспособным. Кажется, никто не хочет говорить о воде. Электролиз — это процесс расщепления воды на составляющие элементы — водород и кислород — с помощью электрического тока. Этот процесс осуществляется в установке, называемой электролизером. Когда сторонники водорода говорят о блестящем будущем технологии, они сосредотачиваются на затратах, связанных с электричеством, необходимым для электролиза. Но для электролиза, кроме электричества, нужна вода.
Сейчас много говорят о снижении стоимости солнечной и ветровой энергии и о том, как они очень скоро сделают зеленый водород жизнеспособным. Кажется, никто не хочет говорить о воде. Электролиз — это процесс расщепления воды на составляющие элементы — водород и кислород — с помощью электрического тока. Этот процесс осуществляется в установке, называемой электролизером. Когда сторонники водорода говорят о блестящем будущем технологии, они сосредотачиваются на затратах, связанных с электричеством, необходимым для электролиза. Но для электролиза, кроме электричества, нужна вода.
Тонны воды — буквально.
Для производства одной тонны водорода путем электролиза требуется в среднем девять тонн воды. Но чтобы получить эти девять тонн воды, недостаточно просто перенаправить течение ближайшей реки. Вода, которую электролизер расщепляет на составные элементы, требует очистки.
В свою очередь, процесс очистки воды довольно расточителен. Системам очистки воды обычно требуется около двух тонн загрязненной воды для производства одной тонны очищенной воды. Другими словами, на одну тонну водорода на самом деле нужно не девять, а 18 тонн воды. С учетом потерь соотношение приближается к 20 тоннам воды на 1 тонну водорода.
Другими словами, на одну тонну водорода на самом деле нужно не девять, а 18 тонн воды. С учетом потерь соотношение приближается к 20 тоннам воды на 1 тонну водорода.
Говоря об очистке воды, химики-органики объясняют, что самый простой способ сделать это — дистиллировать. Этот метод дешев, потому что для него требуется только электричество, но он не быстрый. Что касается стоимости электроэнергии, то для дистилляции литра воды требуется 2,58 мегаджоулей энергии, что в среднем составляет 0,717 кВтч.
На первый взгляд это не так уж и много, но давайте посмотрим, как все выглядит в большем масштабе. Германия — страна с самыми амбициозными планами в отношении зеленого водорода. Стоимость электроэнергии для небытовых потребителей в Германии в прошлом году составляла в среднем 0,19 доллара (0,16 евро) за кВтч. Таким образом, при уровне потребления энергии 0,717 кВтч перегонка литра воды будет стоить 0,14 доллара (0,1147 евро). За тонну воды это будет 135,14 доллара (114,72 евро).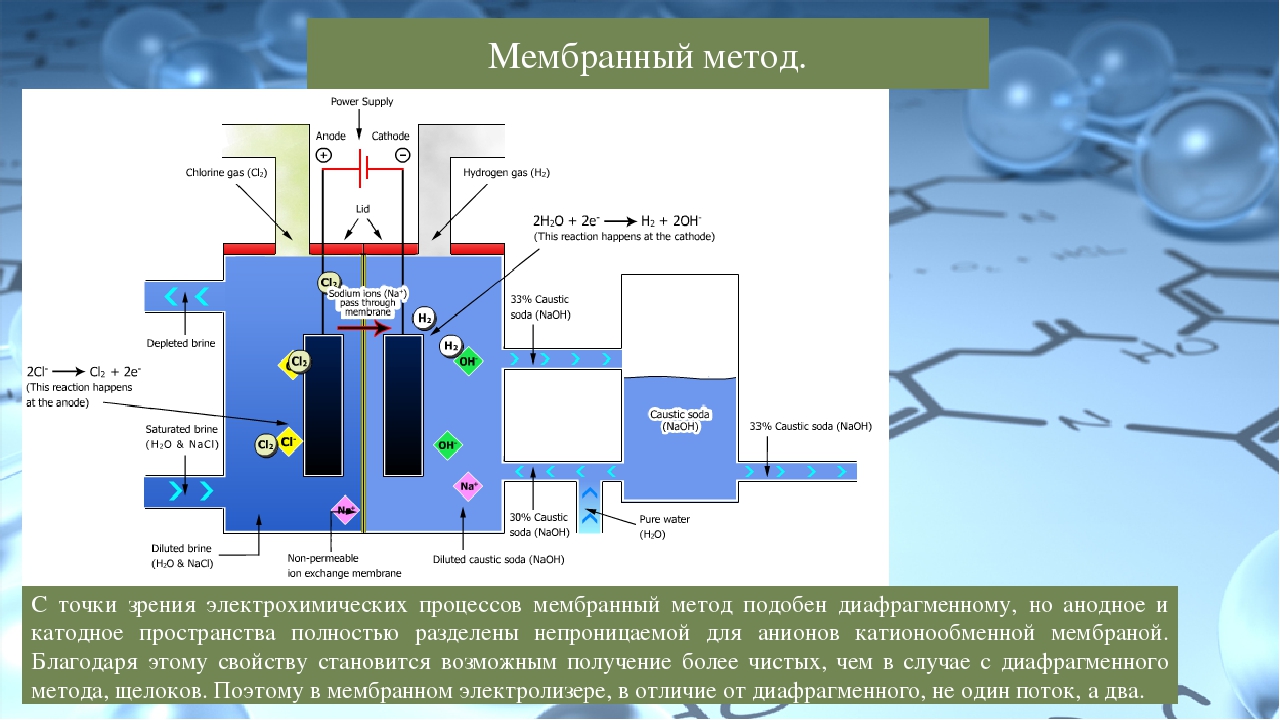
Однако для производства одной тонны водорода для электролиза требуется 18 тонн воды, не считая потерь во время процесса. Это означает, что стоимость очистки воды для производства тонны водорода составит 2432 доллара (2065 евро). Это основано на предположении, что вода будет очищаться самым дешевым из доступных методов. Существуют и другие, гораздо более быстрые, но более дорогие методы с использованием ионообменных смол или молекулярного сита. Другие альтернативы дистилляции, по мнению химиков, на данном этапе ненадежны.
Таким образом, обеспечение правильного типа воды для гидролиза стоит денег, и хотя 2400 долларов за тонну водорода могут показаться не такими уж большими, стоимость очистки воды — не единственные связанные с водой расходы в технологии, которая направлена на получение водорода из возобновляемых источников. Вода, подаваемая в электролизер, не только чистая, но и транспортируется к нему.
Транспортировка тонны за тонной воды к месту установки электролизера означает большие затраты на логистику. Чтобы их сократить, имеет смысл выбрать место, где много воды, например, у реки или моря, или, в качестве альтернативы, рядом с водоочистными сооружениями. Это ограничивает выбор мест, подходящих для крупных электролизеров. Но поскольку электролизер, чтобы быть экологически чистым, должен получать энергию от возобновляемых источников энергии, он также должен располагаться поблизости от солнечной или ветряной электростанции. Их, как мы знаем, невозможно построить где-либо; солнечные фермы наиболее рентабельны в местах с большим количеством солнечного света, а ветряные электростанции лучше всего работают в местах с сильным ветром.
Чтобы их сократить, имеет смысл выбрать место, где много воды, например, у реки или моря, или, в качестве альтернативы, рядом с водоочистными сооружениями. Это ограничивает выбор мест, подходящих для крупных электролизеров. Но поскольку электролизер, чтобы быть экологически чистым, должен получать энергию от возобновляемых источников энергии, он также должен располагаться поблизости от солнечной или ветряной электростанции. Их, как мы знаем, невозможно построить где-либо; солнечные фермы наиболее рентабельны в местах с большим количеством солнечного света, а ветряные электростанции лучше всего работают в местах с сильным ветром.
Излишне говорить, что эти места, как правило, не расположены близко к водным путям, за исключением морского ветра, который кажется идеальным для производства зеленого водорода. К сожалению, морской ветер также является наиболее затратной формой из трех возобновляемых источников — солнечной энергии, берегового ветра и морского ветра — обычно упоминаемых в контексте производства зеленого водорода. По данным Rystad Energy, капитальные затраты на оффшорную ферму в два раза выше, чем у ее наземного аналога, и в четыре раза выше, чем затраты на сопоставимую солнечную установку.
По данным Rystad Energy, капитальные затраты на оффшорную ферму в два раза выше, чем у ее наземного аналога, и в четыре раза выше, чем затраты на сопоставимую солнечную установку.
Не все затраты, связанные с производством водорода из возобновляемых источников энергии, являются затратами на эти возобновляемые источники энергии. Вода — это товар, в котором нуждается этот процесс, и немного странно, что никто, кажется, не хочет обсуждать стоимость воды.
Возможно, стоимость водоснабжения, хранения и очистки незначительна по сравнению с другими затратами, которые необходимо решить в первую очередь. Тем не менее, это фактические затраты, которые следует добавить к общей сумме при оценке того, насколько далеко продвинулась технология производства водорода из возобновляемой электроэнергии и насколько она стала жизнеспособной.
На данный момент эксперты, похоже, единодушны в том, что это нежизнеспособно — не без значительной государственной поддержки.
Росатом в 2024-2025 годы планирует запуск четырех проектов по производству водорода — Экономика и бизнес
МОСКВА, 16 октября. /ТАСС/. Росатом в 2024-2025 годы планирует запуск четырех пилотных проектов по производству водорода. Проекты будут реализованы на территории Калининградской, Мурманской и Сахалинской областей, следует из Атласа российских проектов по производству низкоуглеродного и безуглеродного водорода и аммиака, опубликованного Минпромторгом РФ.
/ТАСС/. Росатом в 2024-2025 годы планирует запуск четырех пилотных проектов по производству водорода. Проекты будут реализованы на территории Калининградской, Мурманской и Сахалинской областей, следует из Атласа российских проектов по производству низкоуглеродного и безуглеродного водорода и аммиака, опубликованного Минпромторгом РФ.
В Калининградской области на 2024 год запланирован запуск производства «зеленого» водорода методом электролиза воды с использованием ветровой энергии. Продукцию планируется продавать на внутреннем рынке и в Европу.
В Мурманской области в 2024 году Росатом запустит проект «Низкоуглеродный водород», ориентированный на европейские рынки. Здесь также предполагается производить низкоуглеродный водород методом электролиза воды. Однако электроэнергию предполагается получать от Кольской АЭС. Прогнозный объем производства в 2024 году — 150 тонн водорода. Достижение промышленных объемов производства запланировано к 2030 году.
Еще два производства госкорпорация предполагает запустить 2025 году на Сахалине. Совместный с французской AirLiquide проект «Голубой водород / аммиак» предполагает производство методом паровой конверсии метана с улавливанием CO2. К 2030 году планируется выйти на уровень ежегодного производства 100 тыс. тонн водорода.
Совместный с французской AirLiquide проект «Голубой водород / аммиак» предполагает производство методом паровой конверсии метана с улавливанием CO2. К 2030 году планируется выйти на уровень ежегодного производства 100 тыс. тонн водорода.
Еще один проект на Сахалине — «Зеленый» водород» — также запланирован на 2025 год. Водород будет производиться методом электролиза воды с использованием ветровой электроэнергии.
Оба сахалинских проекта, как сказано в Атласе Минпромторга, в первую очередь ориентированы на страны Азиатско-Тихоокеанского региона.
Цветовая градация водорода
В настоящее время принята следующая цветовая градация водорода в зависимости от способа его выработки и углеродного следа: «зеленый» произведен с помощью энергии из возобновляемых источников методом электролиза воды, считается самым чистым; «голубой» произведен из природного газа, в этом случае углекислый газ накапливается в специальных хранилищах; «розовый/красный» произведен при помощи атомной энергии; «серый» — при производстве вредные выбросы идут в атмосферу.
Оценка эффективности получения водорода на базе внепиковой электроэнергии АЭС
Аминов Р.З., Байрамов А.Н. Получение водорода на базе внепиковой электроэнергии АЭС
International Scientific Journal for
Alternative Energy and Ecology
© Scientific Technical Centre «TATA», 2015
№ 05-06
(193-194)
2016
Международный научный журнал
«Альтернативная энергетика и экология»
© Научно-технический центр «TATA», 2015
69
14. Малышенко С.П., Назарова О.В., Сарутов
Ю.А. Некоторые термодинамические и технико-эко-
номические аспекты применения водорода как энер-
гоносителя в энергетике // Атомно-водородная энер-
гетика и технология. М.: Энергоатомиздат., 1986.
Вып. 7. С. 105–126.
15. Марченко О.В., Соломин С.В. Анализ эффек-
тивности производства водорода с использованием
ветроэнергетических установок и его использование в
автономной энергосистеме // Международный научный
журнал «Альтернативная энергетика и экология» (IS-
JAEE). 2007. № 3 (47). Р. 112–118.
2007. № 3 (47). Р. 112–118.
16. Якименко Л.М., Модылевская И.Д., Ткачек
З.А. Электролиз воды. М.: Химия, 1970. 263 с.
17. Гусев А.Л. Получение альтернативных энер-
гоносителей с помощью атомно-водородного цикла
и их применение // Международный научный журнал
«Альтернативная энергетика и экология» (ISJAEE).
2007. № 6 (50). Р. 175, 176.
18. Письмен М.К. Производство водорода в неф-
теперерабатывающей промышленности. М.: Химия,
1976. 208 с.
19. Производство и использование водорода.
Технико-инвестиционные показатели установок и
перспективные направления развития на мировом
рынке. Отчет-справочник. ООО «Прима – Химмаш».
Спб, 2005.
20. Вольф Д. Набирающее все большую популяр-
ность локальное производство ультрачистого водо-
рода повышает безопасность, качество и производи-
тельность операций эпитаксиального роста // 41-й
Международный симпозиум по микроэлектронике 2–
6 ноября, Провиденс, Род-Айленд. 2008. С. 404–412.
2008. С. 404–412.
21. Сферы применения водорода. Электронный ре-
сурс: http://airtechnik.ru/listinform/120-sfery-primenenija-
vodoroda/
22. Словецкий Д.И. Плазмохимические процессы
получения чистого водорода // Химия высоких энер-
гий. 2006. С. 42–46.
23. Дытнерский Ю.И., Брыков В.П., Каграманов
Г.Г. Мембранное разделение газов. М.: Химия, 1991.
344с.
24. Хванг С.-Т., Каммермейер К. Мембранные
процессы разделения. М.: Химия, 1981. 464 с.
25. Методы очистки водорода: компания Peak Scien-
tific – поставщик генераторов газа (азот и водород).
Электронный ресурс:
http://peakscientific.hop.ru/peakscientific.ru/page/235-
hydrogen-purification-methods/index.html#.Vs_W332LTcs
26. Гамбург Д.Ю., Семенов В.П., Дубовкин Н.Ф.
и др. Водород. Свойства, получение, хранение,
транспортирование, применение: справочное изд. М.:
Химия, 1989. 672 с.
27. Транспортная экспедиционная компания «Ин-
ком-Карго». Негабаритные железнодорожные пере-
Негабаритные железнодорожные пере-
возки. Электронный ресурс: http://incom-
cargo.com/zhd-perevozki/negabaritnye/
28. Транспортная экспедиционная компания
«ТрансАвтоЦистерна». Электронный ресурс:
http://трансавтоцистерна.рф/prays_list/
References
1. Ènergetičeskaâ strategiâ Rossii na period do 2035.
The Ministry of Energy of the Russian Federation, Mos-
cow, 2014 (in Russ.).
2. Aminov R.Z. et al. AÈS s VVÈR: režimy, harakte-
ristiki, èffektivnost. Moscow: Ènergoatomizdat Publ.,
1990 (in Russ.).
3. Kuznecov N.M., Kanaev A.A., Kopp I.Z. Èner-
getičeskoe oborudovanie blokov AÈS. Leningrad: Maš-
inostroenie Publ., 1987 (in Russ.).
4. Aminov R.Z., Bairamov A.N. Sistemnaâ èf-fektiv-
nost vodorodnyh ciklov na osnove vnepikovoj èlek-
troènergii AÈS. Izvestiâ RAN. Ènergetika, 2011, no. 4,
pp. 52–61 (in Russ.) (in Russ.).
5. Aminov R.Z., Bairamov A.N., Shackova O. V.
V.
Ocenka èffektivnosti vodorodnyh ciklov na baze vnepi-
kovoj èlektroènergii AÈS. Teploènergetika, 2009, no.
11, pp. 41–45 (in Russ.).
6. Bairamov A.N. Razrabotka i obosnovanie shemy
podzemnogo raspoloženiâ metalličeskih ëmkostej hrane-
niâ vodoroda i kisloroda v sostave vodorodnogo èner-
getičeskogo kompleksa. Problemy soveršenstvovaniâ
toplivno-ènergetičeskogo kompleksa, 2012, is. 7, pp. 18–
27 (in Russ.).
7. Bairamov A.N. Tehniko-èkonomičeskie aspekty
podzemnogo raspoloženiâ metalličeskih emkostej hrane-
niâ vodoroda i kisloroda v sostave vodorodnogo èner-
getičeskogo kompleksa. Trudy akademènergo, 2014, no.
2, pp. 79–86 (in Russ.).
8. Aminov R.Z., Bairamov A.N. Sistemnye zadači raz-
vivaûŝejsâ atomnoj ènergetiki i nekotorye puti ih rešeniâ.
Sbornik naučnyh trudov po rezultatam naučno-praktič.
konf.: «Nacionalnyj kongress po ènergetike», 8–12 Sep-
tember 2014, Kazan, Kazan State Power Engineering Uni-
versity, pp. 12–23 (in Russ.).
12–23 (in Russ.).
9. Aminov R.Z, Bairamov A.N. Sistema sžiganiâ vo-
doroda dlâ parovodorodnogo peregreva svežego para v
cikle atomnoj èlektričeskoj stancii. Patent 2427048 RF F
22B 1/26, G 21D5/16, F 01K3/18 // Izobreteniâ. Polez-
nye modeli, 2011, Bul. no. 23 (in Russ.).
10. Bairamov A.N. Obosnovanie èffektivnosti rež-
imnyh uslovij ispolzovaniâ vodorodnogo topliva v pa-
roturbinnom cikle AÈS (na primere turboustanovki K-
1000-60/1500 s reaktorom tipa VVÈR-1000) // Mate-
Вода для производства водорода | Экодар
Водород — газ, который используется в различных сферах промышленности. Одним из способов его получения является
электролиз. Этот процесс подразумевает пропускание через воду электрического тока, в результате чего молекулы воды
разлагаются на водород и кислород.
Для электролиза важна чистота и химический состав воды. Поэтому предприятия химической промышленности должны
предварительно фильтровать воду для производства водорода и нормализовать ее химический состав в соответствии с
установленными требованиями.
Особенности технологии электролиза
Получение водорода методом электролиза — наиболее экономичная и простая технология. Она требует небольших энергозатрат и
позволяет получать большие объемы альтернативного газа. Водород можно добывать из любой воды, но перед этим она должна
проходить очистку от посторонних примесей. Электролиз проводится в деминерализованной воде, чтобы исключить влияние
растворенных и нерастворенных веществ на процесс.
При пропускании через воду электрического тока молекула воды распадается на два атома — водорода и кислорода. Причем
первого получается в 2 раза больше, чем второго (из-за количества атомов). Таким образом, при обработке 0,5 литра воды
можно получить около кубометра обоеих газов. Затраты электричества на разложение молекул составят 4 квт/ч.
Электролиз воды для получения водорода имеет такие преимущества:
- Сырье для производства газа всегда доступно. Воду можно получать из скважин, естественных водоемов или водопровода.
 Но
Но
перед этим она должна пройти фильтрацию на установках обратного осмоса или другом подобном оборудовании. - При производстве водорода не образуется загрязняющих веществ. Под действием электрического тока вода разлагается на
водород и кислород. Дополнительных компонентов в жидкости нет, так как перед этим она пропускается через молекулярную
мембрану. - Процесс электролиза полностью автоматизирован. Не нужно привлекать большое количество персонала для поддержания работы
электрических установок.
Полученный методом электролиза воды водород можно использовать в таких сферах:
- Предприятия химической промышленности для получения других соединений органического происхождения;
- На фабриках по производству продуктов питания для гидрогенизации жиров;
- На производстве электронных компонентов для получения кремния в восстановительных химических реакциях;
- На нефтехимическом производстве для улучшения качества топлива и нефтепродуктов;
- На металлургических заводах для восстановления цветных металлов и получения тугоплавких сплавов;
- В качестве хладагента в охладительных установках электрогенераторов;
- Для получения горючего газа при сваривании металлов;
- Для изготовления ракетного топлива.

Преимущества использования обратного осмоса
Для комплексной очистки воды от различных примесей и дальнейшего ее применения можно использовать установки обратного
осмоса. Эти фильтры отличаются тем, что позволяют удалить из жидкости до 99,9% загрязнений. Таким образом можно
упростить, ускорить и удешевить процесс водоподготовки на производстве.
Технически установка обратного осмоса представляет собой мембрану, через которую под определенным давлением
просачивается вода. Мембрана имеет сетчатую структуру. Но размер ячеек настолько мал, что через них могут просочиться
только молекулы воды. Остальные компоненты остаются и сбрасываются в канализацию.
Для создания обратноосмотического давления используются специальные насосы, которые являются частью промышленной
установки водоочистки.
Обратный осмос может удалить из воды такие загрязнения:
- Любые микроскопические вещества, которые находятся в воде в коллоидном состоянии.
 Более крупные частицы обычно очищаются
Более крупные частицы обычно очищаются
до подачи в обратный осмос с помощью седиментных фильтров. В противном случае ресурс мембраны быстро исчерпается. - Любые растворенные вещества. Обратный осмос может умягчить воду и удалить из нее двухвалентное железо, марганец. Таким
образом никакие вещества не будут мешать протеканию электролиза и выделению водорода с кислородом из воды.
Обратный осмос может иметь высокую производительность. Специалисты компании Экодар выполняют необходимые расчеты и
собирают установки водоочистки, которые позволяют получать большие объемы воды для крупных предприятий.
Установки для очистки воды от компании Экодар
Производственное предприятие Экодар предлагает установки для очистки воды различного назначения и производительности. В
каталоге на сайте можно найти устройства для индивидуального применения, для использования на общественных и
производственных объектах.
Компания предлагает различные виды установок обратного осмоса. Они отличаются друг от друга производительностью,
наличием дополнительных аксессуаров для комфортного использования, сферой применения.
Примеры доступных для заказа устройств:
- Осмос 400 – готовое к использованию решение для водоподготовки. Состоит из фильтра обратного осмоса и дополнительных
модулей, обеспечивающих его работу. Оборудование имеет компактные размеры и легко интегрируются в систему водопровода.
Производительность составляет до 1500 литров в сутки (400 галлонов). Подходит для производства водорода в небольших
количествах. - Осмос 800S — это фильтр обратного осмоса, собранный на компактной раме. Для подключения достаточно врезать систему в
водопровод. Картридж предварительной фильтрации и угольный уже входят в комплект. Эту установку можно использовать для
очистки воды с целью получения водорода. Одна из особенностей модели с индексом S — наличие накопительного бака, в
Одна из особенностей модели с индексом S — наличие накопительного бака, в
котором хранится запас очищенной воды. Производительность модели — 3000 литров или 800 галлонов в сутки. - Промышленная установка обратного осмоса — оборудование с высокой производительностью, длительным сроком службы и
надежностью. С помощью промышленной системы можно максимально очистить воду от примесей в непрерывном режиме.
Для получения консультаций и оформления заказа обратитесь к менеджерам отдела по работе с клиентами.
Россия запланировала зарабатывать на экспорте водорода до $100 млрд в год — РБК
Как нарастить экспорт водорода
В России будут развивать технологии производства как «зеленого», так и «голубого» водорода, заявлял глава Минпромторга Денис Мантуров 13 апреля на конференции Ассоциации европейского бизнеса. По его словам, водород будет использоваться для нужд автотранспорта наряду с другими видами газомоторного топлива (сжиженный и компримированный, или сжатый, природный газ).
Читайте на РБК Pro
Сейчас в России нет промышленных проектов по производству «зеленого» водорода, говорил РБК глава столичного дептранса Максим Ликсутов. «Росатом» производит в год 4,2 тыс. т «желтого» низкоуглеродного водорода, уточняет доцент базовой кафедры возобновляемых источников энергии Российского государственного университета нефти и газа им. Губкина Владислав Карасевич. По его данным, российская нефтяная, атомная и аграрная промышленность производит около 3 млн т «серого» водорода в год для собственных нужд. Ежегодный же экспорт и импорт — это лишь 5 т, добавляет он.
По оценкам Международного энергетического агентства, стоимость производства «зеленого» водорода составляет от $2 до $7 за килограмм, «синего» — $1,6 за 1 кг. Именно высокая себестоимость служит причиной ограничения спроса на экологически чистый водород. Минэнерго ожидает, что благодаря развитию и удешевлению технологий ВИЭ и атомной энергии стоимость производства водорода в России методом электролиза воды, пиролиза или паровой конверсии метана упадет на 30%. Даже сейчас методом электролиза воды его выгоднее производить в России ($4 за килограмм), чем в Азии, где это стоит $7–8 за килограмм, указано в проекте Концепции развития водородной энергетики.
Даже сейчас методом электролиза воды его выгоднее производить в России ($4 за килограмм), чем в Азии, где это стоит $7–8 за килограмм, указано в проекте Концепции развития водородной энергетики.
Концепция предусматривает, что уже к 2024 году экспорт экологически чистого водорода из России вырастет до 200 тыс. — 1 млн т, принося производителям доходы в размере от $0,6 млрд до $3,3 млрд, а к 2035 году поставки достигнут 2–7 млн т с $7,8–21,1 млрд доходов. К 2050 году в зависимости от сценария доходы могут вырасти до $23,6–100,2 млрд в год, прогнозируется в документе.
Россия нацелена занять 20% мирового рынка водорода к 2030 году, говорил замглавы Минэнерго Павел Сорокин на коллегии министерства 12 апреля. «Мы считаем, что это (экспорт из России «зеленого» водорода. — РБК) в 2035 году может быть от 1 млн до 2 млн т в «низком» сценарии, до 7 млн т — при более активном бурном развитии [спроса на водород в мире]», — сказал он.
KPMG оценила ущерб для России от введения углеродного налога в ЕС
По данным Минэнерго, спрос на экологически чистый водород может существенно вырасти из-за планов Евросоюза к 2050 году достичь полной углеродной нейтральности (равенства вредных выбросов, выделяемых в атмосферу и извлекаемых оттуда). Частью «зеленых» инициатив ЕС является введение трансграничного углеродного налога — пошлины на импортируемые товары с большим углеродным следом. Этот налог может обойтись российским экспортерам от €33 млрд до €50,6 млрд до 2030 года, оценивали эксперты KPMG.
Частью «зеленых» инициатив ЕС является введение трансграничного углеродного налога — пошлины на импортируемые товары с большим углеродным следом. Этот налог может обойтись российским экспортерам от €33 млрд до €50,6 млрд до 2030 года, оценивали эксперты KPMG.
Кто планирует производить экологичный водород в России
Для достижения амбициозных целей в области производства и экспорта экологичных типов водорода Минэнерго к 2024 году предлагает создать четыре кластера по географическому принципу — Северо-Западный, Восточный, Арктический и Южный. Ведомство считает необходимым предоставить производителям меры господдержки: от специальных инвестконтрактов и возмещения части затрат на производство высокотехнологичной продукции до возмещения части затрат на купонный доход по «зеленым» облигациям, средства от продажи которых пойдут на финансирование таких проектов.
Для выполнения целей, указанных в проекте Концепции развития водородной энергетики, необходимо уже сейчас значительно активизировать работу по созданию мощностей для производства водорода, ориентированных на экспорт, а также договориться с заинтересованными потребителями и определить возможные варианты его транспортировки, замечает Карасевич.
«Росатом» к лету 2021 года рассчитывает представить результаты технико-экономического обоснования пилотного проекта поставок в Японию водорода, произведенного методом электролиза, сообщил 26 марта вице-президент по маркетингу и развитию бизнеса «Русатом Оверсиз» Антон Москвин, выступая на вебинаре «Водородная стратегия и ключевые тренды энергоперехода». В феврале «Росатом» сообщал, что способен обеспечить до 40% спроса Японии на водород до конца ближайшего десятилетия. В качестве приоритетного сценария экспортного японского проекта рассматривается организация производства сжиженного водорода на территории Сахалинской области и поставок его по морю в Японию. Кроме того, компания планирует в тестовом режиме запустить поезда на водороде на Сахалине.
Замглавы правления «Газпрома» Олег Аксютин в конце марта говорил, что компания планирует экспортировать водород в страны Азии. «Особый интерес представляет возможность производства водорода на территории Дальнего Востока методом парового риформинга метана с обеспечением улавливания и захоронения диоксида углерода («синий» водород. — РБК) и последующим экспортом водорода в страны-потребители (Япония, Южная Корея, Китай)», — отмечал он, не уточняя сроков начала экспорта.
— РБК) и последующим экспортом водорода в страны-потребители (Япония, Южная Корея, Китай)», — отмечал он, не уточняя сроков начала экспорта.
Крупнейший в России производитель сжиженного природного газа НОВАТЭК вместе со своим французским партнером Total прорабатывает проект улавливания CO2 на Ямале и создания производств водорода для собственных нужд и на продажу, указывал начальник управления по связям с инвесторами компании Александр Назаров на конференции Московской школы управления «Сколково». Тогда же президент BP Russia Дэвид Кэмпбелл сказал, что британский мейджор заинтересован в сотрудничестве с российскими компаниями в проектах по производству водорода и развития технологии улавливания и хранения СО2. Сама компания собирается построить завод по производству «голубого» водорода в Великобритании.
РБК направил запросы в пресс-службы «Росатома», «Газпрома» и НОВАТЭКа по поводу их участия в разработке Концепции развития водородной энергетики и планов по производству и экспорту водорода до 2050 года.
Водород для транспорта
В конце 2020 года президент Владимир Путин дал поручение правительству создать городской автобус на водородном топливе. «Нужно обязательно <…> к 2023 году сделать городской автобус на водородном носителе», — заявил он во время совещания с премьером Михаилом Мишустиным. Власти Москвы в ближайшие 30 лет намерены ввести в действие водородные автобусы в рамках стратегии развития сети экологически чистого транспорта, говорится в колонке главы столичного дептранса Максима Ликсутова для РБК. Он мотивировал это необходимостью снижения выбросов парниковых газов в рамках Парижского соглашения по климату и планами Москвы по замене парка дизельных автобусов.
Производство водорода: Электролиз | Министерство энергетики
Как это работает?
Как и топливные элементы, электролизеры состоят из анода и катода, разделенных электролитом. Различные электролизеры работают по-разному, в основном из-за разного типа используемого электролита и ионных частиц, которые он проводит.
Различные электролизеры работают по-разному, в основном из-за разного типа используемого электролита и ионных частиц, которые он проводит.
Мембранные электролизеры с полимерным электролитом
В электролизере с мембраной из полимерного электролита (PEM) электролит представляет собой твердый специальный пластиковый материал.
- Вода реагирует на аноде с образованием кислорода и положительно заряженных ионов водорода (протонов).
- Электроны проходят через внешнюю цепь, а ионы водорода избирательно перемещаются через ФЭУ к катоду.
- На катоде ионы водорода соединяются с электронами из внешней цепи, образуя газообразный водород. Анодная реакция: 2H 2 O → O 2 + 4H + + 4e — Катодная реакция: 4H + + 4e — → 2H 1 2 1 2 1
Щелочные электролизеры
Щелочные электролизеры работают за счет переноса гидроксид-ионов (OH — ) через электролит от катода к аноду с образованием водорода на стороне катода. Электролизеры, в которых в качестве электролита используется жидкий щелочной раствор гидроксида натрия или калия, уже много лет имеются в продаже. Новые подходы с использованием твердых щелочных обменных мембран (AEM) в качестве электролита показывают многообещающие результаты в лабораторных масштабах.
Электролизеры, в которых в качестве электролита используется жидкий щелочной раствор гидроксида натрия или калия, уже много лет имеются в продаже. Новые подходы с использованием твердых щелочных обменных мембран (AEM) в качестве электролита показывают многообещающие результаты в лабораторных масштабах.
Твердооксидные электролизеры
Твердооксидные электролизеры, в которых в качестве электролита используется твердый керамический материал, избирательно проводящий отрицательно заряженные ионы кислорода (O 2-) при повышенных температурах, генерируют водород несколько другим способом.
- Пар на катоде соединяется с электронами из внешней цепи с образованием газообразного водорода и отрицательно заряженных ионов кислорода.
- Ионы кислорода проходят через твердую керамическую мембрану и реагируют на аноде, образуя газообразный кислород и генерируя электроны для внешней цепи.
Твердооксидные электролизеры должны работать при температурах, достаточно высоких для правильного функционирования твердооксидных мембран (около 700–800°C, по сравнению с электролизерами на основе PEM, которые работают при 70–90°C, и коммерческими щелочными электролизерами, которые обычно работать при температуре ниже 100°C). Усовершенствованные лабораторные твердооксидные электролизеры на основе протонпроводящих керамических электролитов демонстрируют перспективность снижения рабочей температуры до 500–600°C. Твердооксидные электролизеры могут эффективно использовать тепло, доступное при этих повышенных температурах (из различных источников, включая ядерную энергию), для уменьшения количества электроэнергии, необходимой для производства водорода из воды.
Усовершенствованные лабораторные твердооксидные электролизеры на основе протонпроводящих керамических электролитов демонстрируют перспективность снижения рабочей температуры до 500–600°C. Твердооксидные электролизеры могут эффективно использовать тепло, доступное при этих повышенных температурах (из различных источников, включая ядерную энергию), для уменьшения количества электроэнергии, необходимой для производства водорода из воды.
Почему рассматривается этот путь?
Электролиз — это ведущий способ производства водорода для достижения цели Hydrogen Energy Earthshot по снижению стоимости чистого водорода на 80% до 1 доллара за 1 килограмм за 1 десятилетие («1 1 1»).Водород, полученный с помощью электролиза, может привести к нулевым выбросам парниковых газов, в зависимости от используемого источника электроэнергии. Источник необходимой электроэнергии, включая его стоимость и эффективность, а также выбросы в результате производства электроэнергии, необходимо учитывать при оценке преимуществ и экономической целесообразности производства водорода с помощью электролиза. Во многих регионах страны сегодняшняя электросеть не идеальна для обеспечения электроэнергией, необходимой для электролиза, из-за выбросов парниковых газов и количества необходимого топлива из-за низкой эффективности процесса выработки электроэнергии.Производство водорода с помощью электролиза используется для возобновляемых источников (ветер, солнце, гидро, геотермальная энергия) и ядерной энергии. Эти пути производства водорода приводят к практически нулевым выбросам парниковых газов и загрязняющих веществ; тем не менее, стоимость производства должна быть значительно снижена, чтобы быть конкурентоспособным с более зрелыми способами, основанными на углероде, такими как риформинг природного газа.
Во многих регионах страны сегодняшняя электросеть не идеальна для обеспечения электроэнергией, необходимой для электролиза, из-за выбросов парниковых газов и количества необходимого топлива из-за низкой эффективности процесса выработки электроэнергии.Производство водорода с помощью электролиза используется для возобновляемых источников (ветер, солнце, гидро, геотермальная энергия) и ядерной энергии. Эти пути производства водорода приводят к практически нулевым выбросам парниковых газов и загрязняющих веществ; тем не менее, стоимость производства должна быть значительно снижена, чтобы быть конкурентоспособным с более зрелыми способами, основанными на углероде, такими как риформинг природного газа.
Потенциал для синергии с производством энергии из возобновляемых источников
Производство водорода с помощью электролиза может предложить возможности для синергии с динамической и прерывистой выработкой энергии, что характерно для некоторых технологий возобновляемых источников энергии. Например, хотя стоимость энергии ветра продолжает снижаться, присущая ветру изменчивость является препятствием для эффективного использования энергии ветра. Водородное топливо и производство электроэнергии могут быть интегрированы в ветряную электростанцию, что позволит гибко переключать производство, чтобы наилучшим образом соответствовать доступности ресурсов с эксплуатационными потребностями системы и рыночными факторами. Кроме того, во времена избыточного производства электроэнергии ветряными электростанциями вместо того, чтобы сокращать электроэнергию, как это обычно делается, можно использовать эту избыточную электроэнергию для производства водорода путем электролиза.
Например, хотя стоимость энергии ветра продолжает снижаться, присущая ветру изменчивость является препятствием для эффективного использования энергии ветра. Водородное топливо и производство электроэнергии могут быть интегрированы в ветряную электростанцию, что позволит гибко переключать производство, чтобы наилучшим образом соответствовать доступности ресурсов с эксплуатационными потребностями системы и рыночными факторами. Кроме того, во времена избыточного производства электроэнергии ветряными электростанциями вместо того, чтобы сокращать электроэнергию, как это обычно делается, можно использовать эту избыточную электроэнергию для производства водорода путем электролиза.
Важно отметить…
- Электроэнергия в настоящее время не является идеальным источником электроэнергии для электролиза, поскольку большая часть электроэнергии вырабатывается с использованием технологий, которые приводят к выбросам парниковых газов и являются энергоемкими. Выработка электроэнергии с использованием технологий возобновляемой или ядерной энергии, либо отдельно от сети, либо в качестве растущей части сети, является возможным вариантом преодоления этих ограничений для производства водорода с помощью электролиза.

- Министерство энергетики США и другие организации продолжают усилия по снижению стоимости производства электроэнергии на основе возобновляемых источников и развитию более эффективного производства электроэнергии на основе ископаемого топлива с улавливанием, утилизацией и хранением углерода. Производство электроэнергии на основе ветра, например, быстро растет в Соединенных Штатах и во всем мире.
Исследования направлены на решение проблем
- Достижение целевого показателя стоимости чистого водорода Hydrogen Shot в размере 1 доллара США за кг H 2 к 2030 году (и промежуточного целевого показателя в размере 2 долларов США за кг H 2 к 2025 году) за счет лучшего понимания компромиссов между производительностью, стоимостью и долговечностью электролизера. системы в прогнозируемых будущих динамических режимах работы с использованием CO 2 — бесплатного электричества.
- Снижение капитальных затрат электролизера и баланса системы.

- Повышение энергоэффективности преобразования электроэнергии в водород в широком диапазоне условий эксплуатации.
- Углубление понимания процессов деградации элементов электролизера и дымовых труб и разработка стратегий смягчения последствий для увеличения срока службы.
Производство водорода путем электролиза — бюллетень h3
Почти 95% водорода производится углеводородным путем из-за его более низких производственных затрат.Этот процесс называется термохимическим, в котором используются тепло и химические реакции для высвобождения водорода из органических материалов, таких как ископаемое топливо и биомасса. Одним из недостатков этого процесса является выброс углерода, особенно при отсутствии улавливания углерода.
Одной из экологически безопасных альтернатив производства водорода является использование воды в качестве исходного сырья. В настоящее время наиболее развитая коммерчески доступная технология получения водорода из воды называется электролизом. Электролиз воды – это разложение воды (H 2 O) на ее основные компоненты, водород (H 2 ) и кислород (O2), при пропускании электрического тока.Благодаря этому процессу электрическая энергия может быть сохранена в виде химической энергии образующегося водорода. Вода является идеальным источником для производства водорода, потому что она выделяет кислород только как побочный продукт во время обработки. Водород, полученный в результате разложения воды при использовании возобновляемого источника энергии, называется зеленым водородом.
Электролиз воды – это разложение воды (H 2 O) на ее основные компоненты, водород (H 2 ) и кислород (O2), при пропускании электрического тока.Благодаря этому процессу электрическая энергия может быть сохранена в виде химической энергии образующегося водорода. Вода является идеальным источником для производства водорода, потому что она выделяет кислород только как побочный продукт во время обработки. Водород, полученный в результате разложения воды при использовании возобновляемого источника энергии, называется зеленым водородом.
Электролиз преобразует электрическую энергию в химическую путем накопления электронов в виде стабильных химических связей. Новообразованная химическая энергия может быть использована в качестве топлива или преобразована обратно в электричество, когда это необходимо.
Электролизер (электролизная ячейка) состоит из двух электродов, называемых катодом и анодом. Катод представляет собой отрицательно заряженный электрод, а анод заряжен положительно. Оба катода разделены мембраной, называемой электролитом, и окружены водой. Существуют разные типы электролизеров, и они функционируют немного по-разному из-за использования электролита другого типа.
Оба катода разделены мембраной, называемой электролитом, и окружены водой. Существуют разные типы электролизеров, и они функционируют немного по-разному из-за использования электролита другого типа.
Есть два типа сепараторов, один используется в электролизере, а другой для топливного элемента.Сепаратор электролиза воды необходим при производстве водорода, который должен выдерживать высокие температуры и влажность. Сепаратор топливных элементов используется в топливных элементах и необходим для утилизации водорода.
Электролит является обязательной частью, так как чистая вода не может нести достаточный заряд из-за отсутствия ионов. На аноде вода окисляется до газообразного кислорода и ионов водорода. На катоде вода восстанавливается до газообразного водорода и ионов гидроксида.
В настоящее время существует три ведущих технологии электролиза.
Щелочной электролиз (AEL)
Щелочной электролиз (AEL) является признанной технологией и используется в промышленных масштабах более 100 лет. Даже первая крупная установка щелочного электролиза была построена в Норвегии в 1927 году. Гидроксид калия (КОН) обычно используется в качестве электролита, сильного основания и щелочи. Электролит проводит электричество для электролиза.
Даже первая крупная установка щелочного электролиза была построена в Норвегии в 1927 году. Гидроксид калия (КОН) обычно используется в качестве электролита, сильного основания и щелочи. Электролит проводит электричество для электролиза.
Анод и катод разделены диафрагмой, разделяющей водород и кислород и предотвращающей их повторное смешивание.На катоде вода расщепляется с образованием h3 и высвобождает анионы гидроксида, которые проходят через диафрагму и рекомбинируют на аноде с образованием O2. Коммерческие щелочные электролизеры работают при температуре 100–150°C
Электролиз с протонообменной мембраной (ПЭМ)
Электролиз с протонообменной мембраной (ПЭМ) является относительно новейшей технологией и используется в коммерческих целях уже несколько лет. Он имеет несколько преимуществ по сравнению с AEL, таких как чистота продуктового газа при частичной нагрузке.В электролизере PEM электролит используется в виде твердого специального пластика. На стороне анода вода разлагается с образованием кислорода и положительно заряженных ионов водорода (протонов). Кроме того, электроны проходят через внешнюю цепь, а ионы водорода проходят через ФЭУ к катоду. На катоде ионы водорода связываются с электронами, вытекающими из внешней цепи, и вместе они образуют газообразный водород. Технология протонного обмена устраняет необходимость в прочных и щелочных основаниях, необходимых для запуска процесса электролиза.Электролизеры ПЭМ работают при температуре 70–90°С.
На стороне анода вода разлагается с образованием кислорода и положительно заряженных ионов водорода (протонов). Кроме того, электроны проходят через внешнюю цепь, а ионы водорода проходят через ФЭУ к катоду. На катоде ионы водорода связываются с электронами, вытекающими из внешней цепи, и вместе они образуют газообразный водород. Технология протонного обмена устраняет необходимость в прочных и щелочных основаниях, необходимых для запуска процесса электролиза.Электролизеры ПЭМ работают при температуре 70–90°С.
Твердооксидный электролизер (SOE)
Щелочные электролизеры и электролизеры PEM известны как низкотемпературные электролизеры (LTE). Однако, с другой стороны, твердооксидный электролизер (SOE) известен как высокотемпературный электролизер (HTE) и использует твердый керамический материал в качестве электролита. Он объединяет воду на катоде с электронами из внешней цепи для получения водорода и отрицательно заряженных ионов кислорода. Затем он переносит ионы кислорода через твердую керамическую мембрану для реакции на аноде с образованием газообразного кислорода и генерацией электронов для внешней цепи.
Эта технология в настоящее время находится в стадии разработки и была использована на нескольких пилотных установках. HTC осуществляет электролиз водяного пара при высоких температурах, что приводит к более высокому КПД (80-90%) по сравнению с предыдущими вариантами. Кроме того, он также может использовать отработанное тепло и компенсировать необходимое электричество. По мере повышения температуры часть энергии, необходимой для расщепления воды, передается в виде тепла, в то время как потребность в электроэнергии или необходимое напряжение снижаются. Электролит представляет собой твердый ионопроводящий материал типа оксида иттрия, стабилизированного всасыванием, из диоксида циркония (YSZ).Поскольку ионная проводимость начинается только при температуре выше 700 °C, для этого типа электролиза рекомендуемая температура для правильной работы составляет от 700 до 800 °C.
Электролиз с анионообменной мембраной (АЕМ) AEM) имеет структуру, аналогичную ячейке PEM, с основным отличием в том, что мембрана переносит анионы (OH–) вместо протонов (H+). Таким образом, технология AEM использует в электродах тот же процесс, что и в традиционных щелочных элементах.Одним из ключевых преимуществ является то, что мембрана дешевле по сравнению с электролизером PEM. В электролизёрах также не используются катализаторы на основе металлов платиновой группы (PGM), такие как элементы PEM. По сравнению с традиционными щелочными электролизерами, AEM также обеспечивает получение водорода высокой чистоты при высоком давлении.
Таким образом, технология AEM использует в электродах тот же процесс, что и в традиционных щелочных элементах.Одним из ключевых преимуществ является то, что мембрана дешевле по сравнению с электролизером PEM. В электролизёрах также не используются катализаторы на основе металлов платиновой группы (PGM), такие как элементы PEM. По сравнению с традиционными щелочными электролизерами, AEM также обеспечивает получение водорода высокой чистоты при высоком давлении.
Вы ищете информацию о водороде? Бюллетень h3 может помочь в ваших исследованиях водорода. Свяжитесь с нами по телефону [email protected] или по телефону: +44 (0) 208 123 7812.
Мы являемся независимыми и очень доступными экспертами, готовыми оказать вам поддержку.
Возобновляемое накопление электроэнергии с помощью электролиза
Abstract
Электролиз преобразует электрическую энергию в химическую путем накопления электронов в виде стабильных химических связей. Химическая энергия может быть использована в качестве топлива или преобразована обратно в электричество, когда это необходимо. Электролиз воды в водород и кислород является хорошо зарекомендовавшей себя технологией, в то время как фундаментальные достижения в электролизе CO 2 все еще необходимы для обеспечения краткосрочного и сезонного хранения энергии в виде жидкого топлива.В этой статье обсуждаются электролитические реакции, которые потенциально могут обеспечить хранение возобновляемой энергии, включая электролиз воды, CO 2 и N 2 . Рассмотрен недавний прогресс и основные препятствия, связанные с управлением электрокатализом и массопереносом на системном уровне. Мы пришли к выводу, что знания и стратегии можно передавать между этими различными электрохимическими технологиями, хотя существуют и уникальные сложности, возникающие из-за специфики вовлеченных реакций.
Химическая энергия может быть использована в качестве топлива или преобразована обратно в электричество, когда это необходимо. Электролиз воды в водород и кислород является хорошо зарекомендовавшей себя технологией, в то время как фундаментальные достижения в электролизе CO 2 все еще необходимы для обеспечения краткосрочного и сезонного хранения энергии в виде жидкого топлива.В этой статье обсуждаются электролитические реакции, которые потенциально могут обеспечить хранение возобновляемой энергии, включая электролиз воды, CO 2 и N 2 . Рассмотрен недавний прогресс и основные препятствия, связанные с управлением электрокатализом и массопереносом на системном уровне. Мы пришли к выводу, что знания и стратегии можно передавать между этими различными электрохимическими технологиями, хотя существуют и уникальные сложности, возникающие из-за специфики вовлеченных реакций.
Создание устойчивых, экологически чистых энергетических систем является одной из самых серьезных проблем, с которыми сталкивается мир в этом столетии.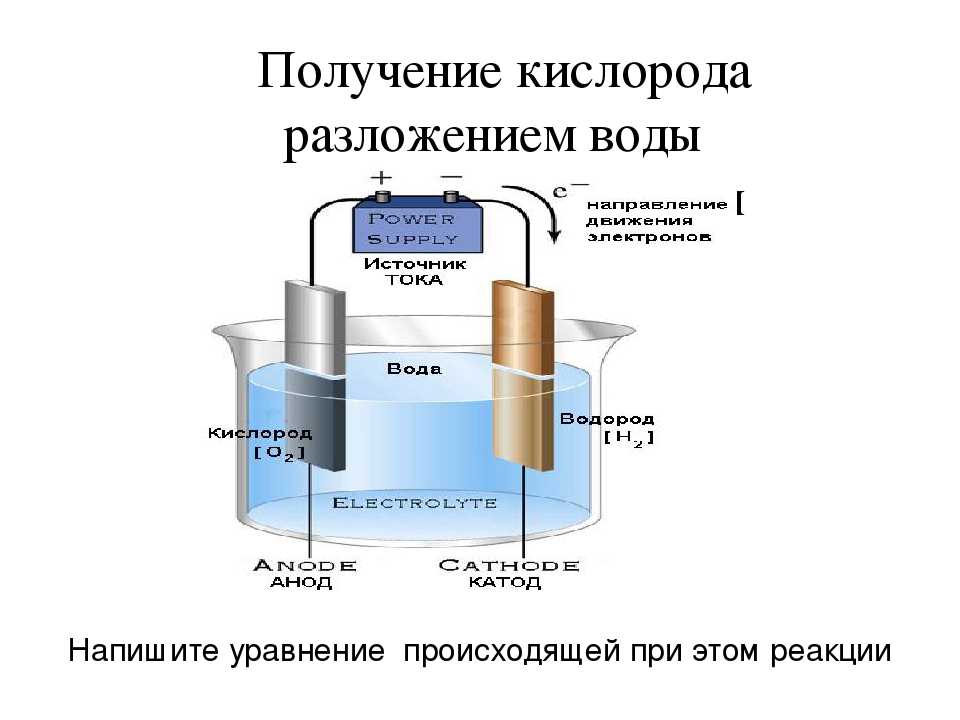 Рост населения и экономическое развитие в ближайшие десятилетия неизбежно приведут к существенному увеличению мирового потребления энергии (1, 2). Традиционные ископаемые источники энергии являются углеродоположительными и вносят существенный вклад в изменение климата. Существуют различные альтернативные источники углеродно-нейтральной энергии, включая ядерное деление, биотопливо и производство электроэнергии из возобновляемых источников, таких как энергия ветра и солнца (1).Прогнозируется, что возобновляемая электроэнергия может обеспечить резкое снижение интенсивности выбросов углекислого газа, определяемой как выбросы углекислого газа на единицу вырабатываемой энергии, несмотря на прогнозируемое увеличение общего потребления энергии (3).
Рост населения и экономическое развитие в ближайшие десятилетия неизбежно приведут к существенному увеличению мирового потребления энергии (1, 2). Традиционные ископаемые источники энергии являются углеродоположительными и вносят существенный вклад в изменение климата. Существуют различные альтернативные источники углеродно-нейтральной энергии, включая ядерное деление, биотопливо и производство электроэнергии из возобновляемых источников, таких как энергия ветра и солнца (1).Прогнозируется, что возобновляемая электроэнергия может обеспечить резкое снижение интенсивности выбросов углекислого газа, определяемой как выбросы углекислого газа на единицу вырабатываемой энергии, несмотря на прогнозируемое увеличение общего потребления энергии (3).
Электричество из возобновляемых источников, таких как ветер и солнечная энергия, стало экономически конкурентоспособным благодаря многолетнему снижению стоимости и развитию технологий. Глобально усредненная нормированная стоимость электроэнергии (LCOE) для солнечной фотоэлектрической (PV) энергии коммунального масштаба упала на 73% с 2010 года, в то время как LCOE от берегового ветра достигла 0 долларов. 03 кВтч в некоторых частях мира (4). По прогнозам, к 2020 году цена на возобновляемую электроэнергию из всех коммерческих источников будет сопоставима или ниже цены на электроэнергию, полученную из ископаемого топлива (4). Одним из основных факторов падения LCE для солнечной и ветровой электроэнергии является резкое снижение затрат на установку. Глобальная средневзвешенная общая стоимость установки новых фотоэлектрических проектов коммунального масштаба снизилась на 68% до примерно 1600 долларов США за кВт с 2010 года.Стоимость строительства новых атомных и угольных электростанций очень неопределенна и зависит от различных факторов; тем не менее, общая стоимость составляет от 5500 до 8100 долларов США/кВт и 3500 долларов США/кВт соответственно, и ожидается, что в будущем они возрастут (5, 6).
03 кВтч в некоторых частях мира (4). По прогнозам, к 2020 году цена на возобновляемую электроэнергию из всех коммерческих источников будет сопоставима или ниже цены на электроэнергию, полученную из ископаемого топлива (4). Одним из основных факторов падения LCE для солнечной и ветровой электроэнергии является резкое снижение затрат на установку. Глобальная средневзвешенная общая стоимость установки новых фотоэлектрических проектов коммунального масштаба снизилась на 68% до примерно 1600 долларов США за кВт с 2010 года.Стоимость строительства новых атомных и угольных электростанций очень неопределенна и зависит от различных факторов; тем не менее, общая стоимость составляет от 5500 до 8100 долларов США/кВт и 3500 долларов США/кВт соответственно, и ожидается, что в будущем они возрастут (5, 6).
Несмотря на быстрый рост возобновляемой электроэнергии, текущая доля электроэнергии, вырабатываемой из возобновляемых источников в структуре электроэнергии, остается низкой, при этом гораздо большая доля электроэнергии производится из газа, нефти и угля. Однако, исходя из прогноза эталонного случая, ожидается, что производство электроэнергии из возобновляемых источников увеличится с 18% до примерно 31% в период с 2018 по 2050 год (3). Одной из проблем с солнечной электроэнергией является прерывистый характер суточного солнечного цикла, который плохо соответствует спросу и, следовательно, требует избыточной генерирующей мощности на уровне сети или резервной мощности на стороне потребителя. Например, на рис. 1 показаны колебания чистой электрической нагрузки в зависимости от времени для весеннего дня в Калифорнии.Начиная примерно с 16:00 для восполнения нехватки электроэнергии солнечной энергии требуется поставка дополнительных 13 000 МВт электроэнергии из несолнечных источников, таких как природный газ и ядерная энергия, в течение 3 часов (7).
Однако, исходя из прогноза эталонного случая, ожидается, что производство электроэнергии из возобновляемых источников увеличится с 18% до примерно 31% в период с 2018 по 2050 год (3). Одной из проблем с солнечной электроэнергией является прерывистый характер суточного солнечного цикла, который плохо соответствует спросу и, следовательно, требует избыточной генерирующей мощности на уровне сети или резервной мощности на стороне потребителя. Например, на рис. 1 показаны колебания чистой электрической нагрузки в зависимости от времени для весеннего дня в Калифорнии.Начиная примерно с 16:00 для восполнения нехватки электроэнергии солнечной энергии требуется поставка дополнительных 13 000 МВт электроэнергии из несолнечных источников, таких как природный газ и ядерная энергия, в течение 3 часов (7).
Рис. 1.
Устойчивое использование энергии. Схемы хранения и использования энергии на основе электролиза. Избыточная электроэнергия из возобновляемых источников может быть сохранена посредством электролиза в качестве химического топлива. Энергия извлекается для выравнивания спроса в краткосрочной перспективе и для удовлетворения потребности в топливе в сезоны, когда возобновляемые источники менее доступны.График прерывистости ( Нижний левый ) данные из ссылки. 7.
Энергия извлекается для выравнивания спроса в краткосрочной перспективе и для удовлетворения потребности в топливе в сезоны, когда возобновляемые источники менее доступны.График прерывистости ( Нижний левый ) данные из ссылки. 7.
Колебания энергии от солнца и ветра, таким образом, требуют массивного хранения энергии, как в краткосрочной, так и в долгосрочной перспективе. Существует несколько способов хранения электроэнергии, включая физические подходы, такие как гидроэлектростанции с насосом и хранение энергии на сжатом воздухе; крупногабаритные батареи, такие как свинцово-кислотные, литиевые, натрий-серные батареи и проточные батареи; и электролиз, при этом гидроэлектростанции с насосами являются в настоящее время ведущей технологией в секторе накопления энергии (8).Недостатком большинства этих методов является то, что они подходят только для краткосрочного хранения или ограничены конкретными географическими требованиями. Электролиз выделяется как способ хранения электрической энергии в виде устойчивых химических связей. Потенциально огромная энергетическая мощность, незначительная скорость саморазряда, существующая инфраструктура и низкие капитальные затраты на содержание возобновляемого углеродного топлива делают их идеальными для сезонного хранения, что очень желательно, учитывая сезонность возобновляемых источников энергии.Потребность в такой технологии будет становиться все более острой в связи с ожидаемым более широким распространением дешевой возобновляемой электроэнергии в энергосистему, как показано на рис. 1. эффективного и экономичного способа хранения электрической энергии в виде жидкого топлива пока не существует. Для того, чтобы такая технология стала экономически конкурентоспособной с обильным ископаемым топливом, нужно начать с очень дешевой электроэнергии.Технико-экономический анализ электролиза CO 2 показывает, что цена на возобновляемую электроэнергию ниже 0,04 долл. США/кВтч потребуется для того, чтобы топливо, полученное электролизом, могло конкурировать с топливом, полученным из ископаемого топлива (9).
Потенциально огромная энергетическая мощность, незначительная скорость саморазряда, существующая инфраструктура и низкие капитальные затраты на содержание возобновляемого углеродного топлива делают их идеальными для сезонного хранения, что очень желательно, учитывая сезонность возобновляемых источников энергии.Потребность в такой технологии будет становиться все более острой в связи с ожидаемым более широким распространением дешевой возобновляемой электроэнергии в энергосистему, как показано на рис. 1. эффективного и экономичного способа хранения электрической энергии в виде жидкого топлива пока не существует. Для того, чтобы такая технология стала экономически конкурентоспособной с обильным ископаемым топливом, нужно начать с очень дешевой электроэнергии.Технико-экономический анализ электролиза CO 2 показывает, что цена на возобновляемую электроэнергию ниже 0,04 долл. США/кВтч потребуется для того, чтобы топливо, полученное электролизом, могло конкурировать с топливом, полученным из ископаемого топлива (9). Согласно базе данных Международного агентства по возобновляемым источникам энергии о затратах на возобновляемые источники энергии, эта цель находится на пути к достижению этой цели (4).
Согласно базе данных Международного агентства по возобновляемым источникам энергии о затратах на возобновляемые источники энергии, эта цель находится на пути к достижению этой цели (4).
На рис. 1 показано, как можно обеспечить устойчивый энергетический цикл путем сочетания электролиза с электричеством, вырабатываемым солнцем и ветром, а также другими возобновляемыми источниками.Электролиз может производить как товарные химические вещества, так и водород, уменьшая прерывистость возобновляемой энергии. В этом сценарии водородно-воздушные топливные элементы могут использоваться для преобразования энергии, хранящейся в виде водорода, обратно в электричество. Жидкое топливо с высокой плотностью энергии является предпочтительной формой для сезонного хранения и может формировать зеленый энергетический цикл, если CO 2 в воздухе можно сконцентрировать для обеспечения эффективного электролиза. Растет исследовательская деятельность по улавливанию углерода из атмосферы (10), и несколько компаний работают над коммерциализацией технологии улавливания углерода. Электролиз CO 2 до CO и водорода (синтез-газ) был достигнут с использованием множества различных электрокатализаторов и обеспечивает сырье для углеводородного топлива с помощью процесса Фишера-Тропша. В качестве альтернативы, продукты сочетания С-С, включая этилен и этанол, могут быть получены непосредственно электролизом на медьсодержащих катализаторах, но эффективность, селективность и производительность этих реакций необходимо улучшить. На рисунке не показано электрохимическое восстановление N 2 до аммиака для производства удобрений.В этом случае электролиз использует неограниченное химическое сырье, поскольку атмосфера Земли обеспечивает азот и воду, необходимые для реакции. В дополнение к производству топлива и удобрений путем электролиза, термохимический катализ обеспечивает установленный метод гидрирования CO 2 , CO и N 2 . Двумя примерами являются процессы Фишера-Тропша и Габера-Боша, которые уже хорошо разработаны в больших масштабах для производства жидких углеводородов и аммиака соответственно.
Электролиз CO 2 до CO и водорода (синтез-газ) был достигнут с использованием множества различных электрокатализаторов и обеспечивает сырье для углеводородного топлива с помощью процесса Фишера-Тропша. В качестве альтернативы, продукты сочетания С-С, включая этилен и этанол, могут быть получены непосредственно электролизом на медьсодержащих катализаторах, но эффективность, селективность и производительность этих реакций необходимо улучшить. На рисунке не показано электрохимическое восстановление N 2 до аммиака для производства удобрений.В этом случае электролиз использует неограниченное химическое сырье, поскольку атмосфера Земли обеспечивает азот и воду, необходимые для реакции. В дополнение к производству топлива и удобрений путем электролиза, термохимический катализ обеспечивает установленный метод гидрирования CO 2 , CO и N 2 . Двумя примерами являются процессы Фишера-Тропша и Габера-Боша, которые уже хорошо разработаны в больших масштабах для производства жидких углеводородов и аммиака соответственно. Следует отметить, что почти 80 % энергии, потребляемой при синтезе аммиака, приходится на получение водорода путем паровой конверсии и реакции конверсии водяного газа (11). Электролиз воды обеспечивает потенциальную углеродно-нейтральную альтернативу для получения водорода для этих реакций.
Следует отметить, что почти 80 % энергии, потребляемой при синтезе аммиака, приходится на получение водорода путем паровой конверсии и реакции конверсии водяного газа (11). Электролиз воды обеспечивает потенциальную углеродно-нейтральную альтернативу для получения водорода для этих реакций.
Электролитический процесс ограничен тремя факторами, которые эффективно действуют как последовательные импедансы: кинетика переноса электронов на электрифицированной границе раздела, массоперенос реагентов и продуктов и последовательное сопротивление, включая перенос ионов.Перенос электронов через наэлектризованный интерфейс определяет кинетику окисления и восстановления, а массоперенос определяет доступность реагента и скорость, с которой продукт может быть удален, как показано на рис. 2 A . Скорость переноса электронов и поток массопереноса связаны, поскольку они оба пропорциональны току. Активные катализаторы необходимы для снижения барьера активации путем связывания и стабилизации определенных переходных состояний, рис. 2 B . Увеличение перенапряжения для одного или обоих электродных процессов ускоряет кинетику реакции за счет эффективного снижения активационного барьера, но дополнительные затраты энергии снижают эффективность преобразования энергии, как показано на рис.2 Д . Когда кинетика переноса электрона достаточно быстрая, самая высокая плотность тока достигается за счет ускорения подачи реагента. В случае электролиза CO 2 это может быть достигнуто за счет подачи реагента и удаления продуктов в газовой фазе, используя более быстрый коэффициент диффузии газов и избегая низкой растворимости CO 2 в жидкой воде, как показано на рис. 2 C .
2 B . Увеличение перенапряжения для одного или обоих электродных процессов ускоряет кинетику реакции за счет эффективного снижения активационного барьера, но дополнительные затраты энергии снижают эффективность преобразования энергии, как показано на рис.2 Д . Когда кинетика переноса электрона достаточно быстрая, самая высокая плотность тока достигается за счет ускорения подачи реагента. В случае электролиза CO 2 это может быть достигнуто за счет подачи реагента и удаления продуктов в газовой фазе, используя более быстрый коэффициент диффузии газов и избегая низкой растворимости CO 2 в жидкой воде, как показано на рис. 2 C .
Рис. 2.
Схема электролиза.( A ) Реагенты транспортируются к поверхности электрода, где происходит катодная реакция. ( B ) Сравнение путей реакции для HER с катализатором и без него. Катализатор стабилизирует промежуточное соединение и снижает энергию активации. ( C ) Электролизеры в газовой конфигурации. Газовый электролиз использует быструю диффузию молекул газа, что обеспечивает высокую плотность тока. Мембранные электролиты обычно требуются для управления ионами и разделения газов.( D ) Кинетика электрохимического ВВ. Энергия переходного состояния уменьшается по мере увеличения перенапряжения.
Газовый электролиз использует быструю диффузию молекул газа, что обеспечивает высокую плотность тока. Мембранные электролиты обычно требуются для управления ионами и разделения газов.( D ) Кинетика электрохимического ВВ. Энергия переходного состояния уменьшается по мере увеличения перенапряжения.
Электролиз воды
Электролиз воды имеет долгую историю, первая опубликованная демонстрация датируется 1789 годом, и в настоящее время это хорошо зарекомендовавшая себя коммерческая технология. Например, большая установка щелочных электролизеров Norsk Hydro (с 1948 по 1990 год) на гидроэлектростанции была способна производить около 70 000 кг H 2 /день (8). Крупнейшая ветро-водородная электростанция была установлена в Норвегии в 2004 г. компаниями Norsk Hydro и Enercon, сочетая ветряную турбину мощностью 600 кВт с электролизером мощностью 48 кВт (12).
За последние два десятилетия интерес к электролизу воды возрос из-за его потенциальной роли в водородной энергетике, включая производство электролита, хранение, транспортировку и использование водорода в качестве топлива (2).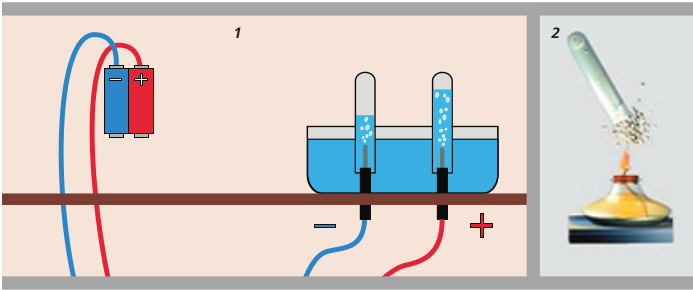 Текущие исследования сосредоточены на электролизёрах воды, которые можно разделить на категории в зависимости от их электролитов: щелочные электролиты, протонообменные мембраны (ПЭМ) и твердотельные протонные или оксидно-ионные проводники. Коммерческие электролизеры PEM достигают наилучшей производительности (энергетическая эффективность ~ 70% при плотности тока 1.7 А/см 2 , Giner Inc.) (13), но большое перенапряжение реакции анодного окисления воды и агрессивная кислотная среда требуют использования катализаторов из драгоценных металлов. Мембранный электролит и изготовление биполярных пластин также значительно увеличивают стоимость. Щелочные электролизеры — самая старая технология с несколько более низкой эффективностью системы (~64% эффективности при плотности тока 1 А/см 2 GHW) и более низкой стоимостью (800 долларов США/кВт) (13). Щелочные электролиты позволяют использовать катализаторы из неблагородных металлов, таких как Ni и Fe.
Текущие исследования сосредоточены на электролизёрах воды, которые можно разделить на категории в зависимости от их электролитов: щелочные электролиты, протонообменные мембраны (ПЭМ) и твердотельные протонные или оксидно-ионные проводники. Коммерческие электролизеры PEM достигают наилучшей производительности (энергетическая эффективность ~ 70% при плотности тока 1.7 А/см 2 , Giner Inc.) (13), но большое перенапряжение реакции анодного окисления воды и агрессивная кислотная среда требуют использования катализаторов из драгоценных металлов. Мембранный электролит и изготовление биполярных пластин также значительно увеличивают стоимость. Щелочные электролизеры — самая старая технология с несколько более низкой эффективностью системы (~64% эффективности при плотности тока 1 А/см 2 GHW) и более низкой стоимостью (800 долларов США/кВт) (13). Щелочные электролиты позволяют использовать катализаторы из неблагородных металлов, таких как Ni и Fe.
В последнее время наблюдается интерес к разработке более совершенных катализаторов для снижения стоимости и повышения эффективности электролиза воды. В кислых электролизерах с ПОМ вулканическая диаграмма коррелирует скорость катодной реакции выделения водорода (HER) с прочностью связи металл-водород на различных металлических катализаторах (рис. 3 A ) (14). Простое объяснение формы вулкана заключается в том, что металлы, которые слишком слабо связывают водород, не могут стабилизировать промежуточное соединение M-H, тогда как те, которые образуют очень сильные связи M-H, заполняют большинство мест связывания, оставляя мало места для нового события адсорбции.В то время как прочность связи M–H является хорошим показателем для большинства катализаторов, некоторые металлы с особыми гранями, такие как Pt (111), демонстрируют в 20–200 раз более высокую плотность тока обмена HER в кислоте, чем в основании, даже несмотря на то, что H-связывание энергия похожа. Механистические исследования указывают на роль адсорбции гидроксида (15) или реорганизации воды под действием межфазного электрического поля во время процесса HER (16). Драгоценные металлы (Pd и Pt) являются лучшими катализаторами, но их стоимость и низкое содержание в природе создают препятствия для использования этой технологии в очень больших масштабах.
В кислых электролизерах с ПОМ вулканическая диаграмма коррелирует скорость катодной реакции выделения водорода (HER) с прочностью связи металл-водород на различных металлических катализаторах (рис. 3 A ) (14). Простое объяснение формы вулкана заключается в том, что металлы, которые слишком слабо связывают водород, не могут стабилизировать промежуточное соединение M-H, тогда как те, которые образуют очень сильные связи M-H, заполняют большинство мест связывания, оставляя мало места для нового события адсорбции.В то время как прочность связи M–H является хорошим показателем для большинства катализаторов, некоторые металлы с особыми гранями, такие как Pt (111), демонстрируют в 20–200 раз более высокую плотность тока обмена HER в кислоте, чем в основании, даже несмотря на то, что H-связывание энергия похожа. Механистические исследования указывают на роль адсорбции гидроксида (15) или реорганизации воды под действием межфазного электрического поля во время процесса HER (16). Драгоценные металлы (Pd и Pt) являются лучшими катализаторами, но их стоимость и низкое содержание в природе создают препятствия для использования этой технологии в очень больших масштабах.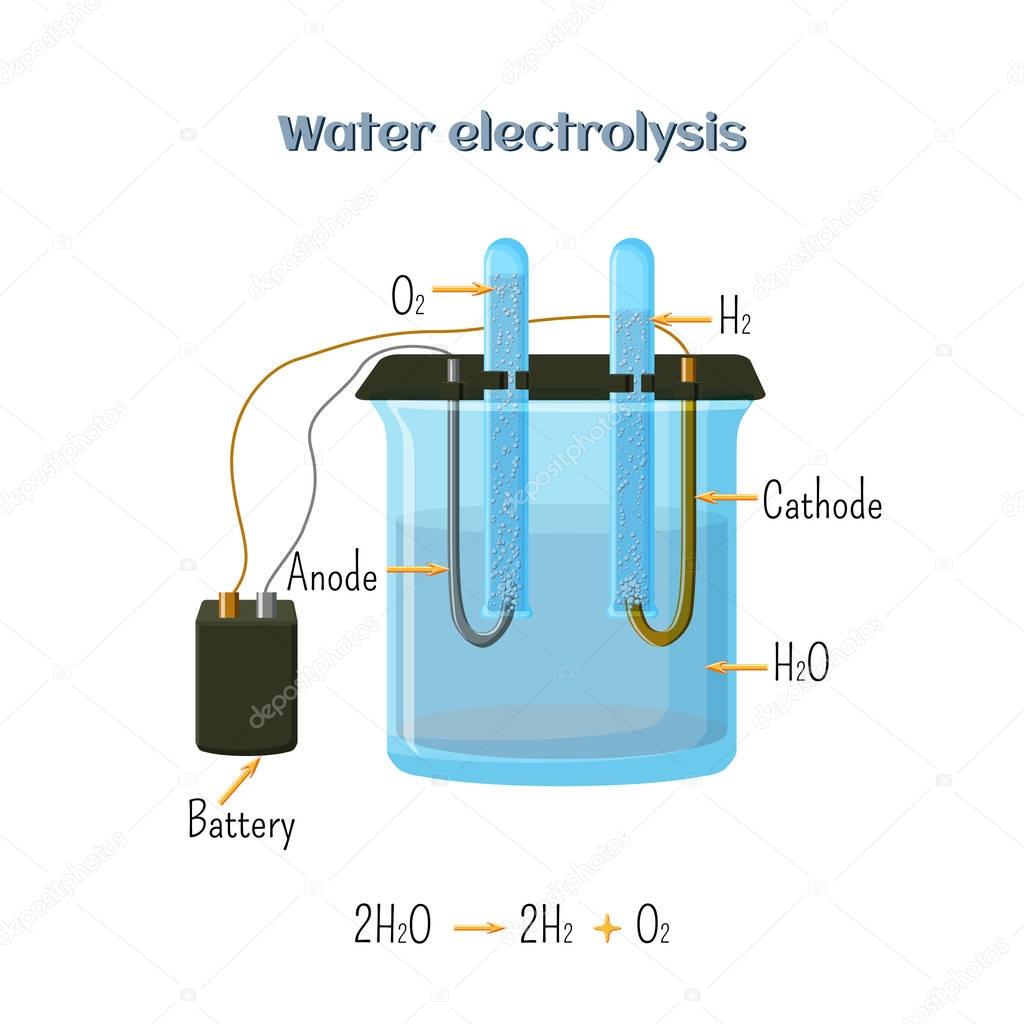 Таким образом, привлекательной стратегией является замена чистой Pt структурами ядро-оболочка, над- и подслоем, легированными и поддерживаемыми структурами. Дальнейшее снижение содержания драгоценных металлов возможно за счет использования одноатомных катализаторов, появившихся в последние несколько лет. Высокая поверхностная энергия отдельных атомов способствует их слиянию и требует поддержки, которая может прочно закрепить их. Носители электрокатализаторов могут также стабилизировать атомы каталитических металлов и модулировать их реакционную способность, отдавая или принимая электроны.Например, есть свидетельства переноса d-электронов между поздним переходным металлом (оксидом) и ранним переходным металлом со слоистыми носителями в сильном взаимодействии металл-носитель (17). Аналогичные соображения могут быть применимы к сплавам, содержащим металлы с различной электронной отрицательностью.
Таким образом, привлекательной стратегией является замена чистой Pt структурами ядро-оболочка, над- и подслоем, легированными и поддерживаемыми структурами. Дальнейшее снижение содержания драгоценных металлов возможно за счет использования одноатомных катализаторов, появившихся в последние несколько лет. Высокая поверхностная энергия отдельных атомов способствует их слиянию и требует поддержки, которая может прочно закрепить их. Носители электрокатализаторов могут также стабилизировать атомы каталитических металлов и модулировать их реакционную способность, отдавая или принимая электроны.Например, есть свидетельства переноса d-электронов между поздним переходным металлом (оксидом) и ранним переходным металлом со слоистыми носителями в сильном взаимодействии металл-носитель (17). Аналогичные соображения могут быть применимы к сплавам, содержащим металлы с различной электронной отрицательностью.
Рис. 3.
Электролиз воды. ( A ) График вулкана HER для каталитических элементов. Данные из исх. 14. ( B ) Диаграмма свободной энергии для OER. Черная кривая относится к идеальному катализатору OER, тогда как красная кривая представляет реальный катализатор (22).( C ) Сравнение низкотемпературного электролизера PEM и высокотемпературного SOEC. Данные из исх. 43. ( D ) Характеристики SOEC в режиме электролизера и топливного элемента с использованием протонного проводника при промежуточных температурах. Повышение температуры на 150 °C резко улучшило плотность тока в ячейке. Данные из исх. 44.
Данные из исх. 14. ( B ) Диаграмма свободной энергии для OER. Черная кривая относится к идеальному катализатору OER, тогда как красная кривая представляет реальный катализатор (22).( C ) Сравнение низкотемпературного электролизера PEM и высокотемпературного SOEC. Данные из исх. 43. ( D ) Характеристики SOEC в режиме электролизера и топливного элемента с использованием протонного проводника при промежуточных температурах. Повышение температуры на 150 °C резко улучшило плотность тока в ячейке. Данные из исх. 44.
Одним из важных факторов электрокатализа является каталитически активная площадь поверхности. Плотность тока, нормализованная к площади активной поверхности, часто показывает скорость обновления сайта и энергию активации, подобные плоскому аналогу, даже если ток может отличаться на порядки величины (18).Однако при измерении площади поверхности могут возникать погрешности из-за экспериментальных условий, включая проводимость электролита, покрытие поверхности и шкалу времени (19). Кроме того, поскольку кинетика переноса электронов в кислых водных электролитах является быстрой, активность HER обычно ограничена переносом массы и требует методов принудительной конвекции или ультрамикроэлектродов для измерения его внутренней активности.
Кроме того, поскольку кинетика переноса электронов в кислых водных электролитах является быстрой, активность HER обычно ограничена переносом массы и требует методов принудительной конвекции или ультрамикроэлектродов для измерения его внутренней активности.
Недавно был обнаружен ряд катализаторов HER на основе неблагородных металлов. Вдохновленные кофактором MoFe нитрогеназы, который имеет энергию связи водорода, близкую к энергии Pt, было показано, что краевые участки MoS 2 , а также несколько катализаторов на основе фосфидов металлов активны по отношению к HER (20).Недавние исследования показали, что S-вакансии и инженерия деформации также являются эффективными способами улучшения характеристик HER (21).
Реакция выделения кислорода с 4 электронами и 4 протонами (OER) более механистически сложна и неизменно включает значительные (от 250 до 300 мВ) начальные перенапряжения в кислой среде. Считается, что реакция протекает через адсорбированные частицы M – OH с последующей стадией депротонирования. Газообразный кислород образуется либо из поверхностного гидроперокси-промежуточного соединения M-OOH, либо в результате бимолекулярной рекомбинации M-O.Для катализаторов OER на основе оксидов со структурой каменной соли, рутила, шпинели и перовскита диаграммы вулканизма были построены на основе теоретических соображений (22). Идеальный OER с оптимальными энергиями связи имеет разность свободных энергий между M-OOH и M-OH (ΔGOH-ΔGOOH) 2,46 эВ, что требует начального потенциала 1,23 В (рис. 3 B ). Однако начальные потенциалы реальных катализаторов значительно выше, потому что (ΔGOH-ΔGOOH) отклоняется от идеального случая и, как предполагается, регулируется свободной энергией связи М-О.Универсальное среднее значение (ΔGOH-ΔGOOH), равное 3,2 эВ, согласуется с несколькими группами катализаторов, поскольку сила связывания OH линейно зависит от силы связывания OOH (22). Хотя скейлинговое соотношение является полезной концепцией для понимания каталитической активности, экспериментальная количественная оценка усложняется тем фактом, что свойства поверхности катализатора могут изменяться во время электрохимической операции, особенно в анодных условиях.
Газообразный кислород образуется либо из поверхностного гидроперокси-промежуточного соединения M-OOH, либо в результате бимолекулярной рекомбинации M-O.Для катализаторов OER на основе оксидов со структурой каменной соли, рутила, шпинели и перовскита диаграммы вулканизма были построены на основе теоретических соображений (22). Идеальный OER с оптимальными энергиями связи имеет разность свободных энергий между M-OOH и M-OH (ΔGOH-ΔGOOH) 2,46 эВ, что требует начального потенциала 1,23 В (рис. 3 B ). Однако начальные потенциалы реальных катализаторов значительно выше, потому что (ΔGOH-ΔGOOH) отклоняется от идеального случая и, как предполагается, регулируется свободной энергией связи М-О.Универсальное среднее значение (ΔGOH-ΔGOOH), равное 3,2 эВ, согласуется с несколькими группами катализаторов, поскольку сила связывания OH линейно зависит от силы связывания OOH (22). Хотя скейлинговое соотношение является полезной концепцией для понимания каталитической активности, экспериментальная количественная оценка усложняется тем фактом, что свойства поверхности катализатора могут изменяться во время электрохимической операции, особенно в анодных условиях. Степень окисления металлов, например, зависит от приложенного потенциала, и этот эффект может привести к резким изменениям каталитической активности, проводимости и стабильности.Переход от Ni 2+ к Ni 3+ обычно является предпосылкой для высокой активности OER в щелочных катализаторах на основе никеля, поскольку первый является изолирующим. Предварительная обработка поверхности катализатора перед испытанием важна для значимой оценки и сравнения. Оксиды металлов с высокой растворимостью при более высоких степенях окисления часто нестабильны в кислых средах, и наблюдается компромисс между стабильностью и активностью Pt, Pd, Au и Ru (23). В настоящее время оксид иридия является единственным известным устойчивым катализатором выделения кислорода в кислых средах и используется только в чистом виде в слое катализатора.
Степень окисления металлов, например, зависит от приложенного потенциала, и этот эффект может привести к резким изменениям каталитической активности, проводимости и стабильности.Переход от Ni 2+ к Ni 3+ обычно является предпосылкой для высокой активности OER в щелочных катализаторах на основе никеля, поскольку первый является изолирующим. Предварительная обработка поверхности катализатора перед испытанием важна для значимой оценки и сравнения. Оксиды металлов с высокой растворимостью при более высоких степенях окисления часто нестабильны в кислых средах, и наблюдается компромисс между стабильностью и активностью Pt, Pd, Au и Ru (23). В настоящее время оксид иридия является единственным известным устойчивым катализатором выделения кислорода в кислых средах и используется только в чистом виде в слое катализатора.
Токопроводящие подложки могут использоваться для снижения содержания драгоценных металлов, что приводит к снижению затрат и более эффективному использованию катализаторов. Однако, хотя углерод можно использовать в качестве проводящей подложки для обеих полуреакций в топливном элементе, его можно использовать только на стороне водорода в электролизере PEM; со стороны кислорода он быстро корродирует. Оксидные носители, такие как мезопористый оксид олова, легированный индием, показали высокую проводимость (0,3 См/см) и многообещающую электрохимическую стабильность при анодных потенциалах (24).Двумя ключевыми темами исследований в области кислотного электролиза, таким образом, являются поиск более распространенного и недорогого альтернативного катализатора оксида иридия для выделения кислорода и/или обнаружение проводящей подложки, которая также обладает долговременной стабильностью в условиях выделения кислорода в кислой среде.
Однако, хотя углерод можно использовать в качестве проводящей подложки для обеих полуреакций в топливном элементе, его можно использовать только на стороне водорода в электролизере PEM; со стороны кислорода он быстро корродирует. Оксидные носители, такие как мезопористый оксид олова, легированный индием, показали высокую проводимость (0,3 См/см) и многообещающую электрохимическую стабильность при анодных потенциалах (24).Двумя ключевыми темами исследований в области кислотного электролиза, таким образом, являются поиск более распространенного и недорогого альтернативного катализатора оксида иридия для выделения кислорода и/или обнаружение проводящей подложки, которая также обладает долговременной стабильностью в условиях выделения кислорода в кислой среде.
CO
2 Электролиз
Электрохимическое восстановление CO 2 до жидкого топлива и химикатов с добавленной стоимостью представляет собой возможное решение для сезонного хранения возобновляемой электроэнергии с нулевым выбросом углерода.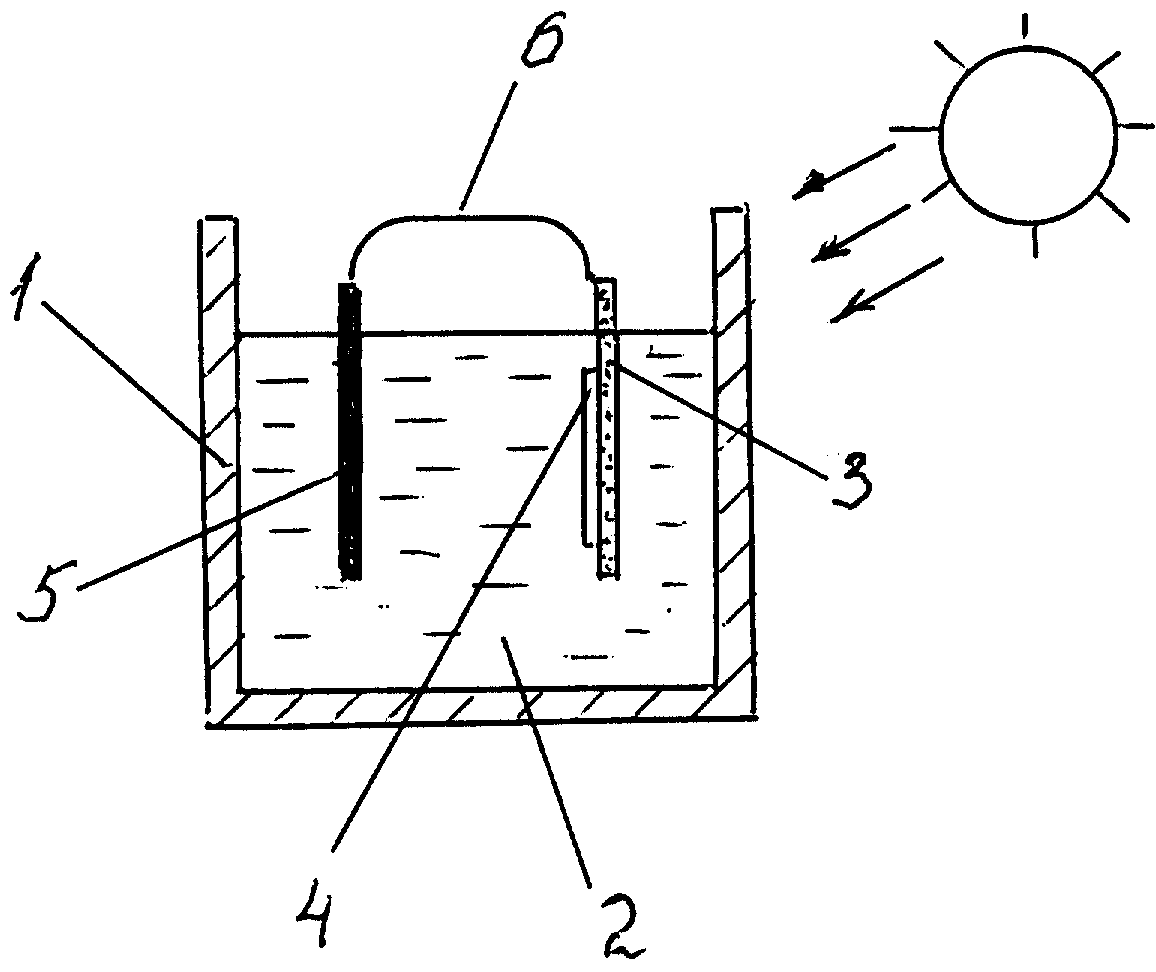 CO 2 может быть восстановлен до различных продуктов C1, включая монооксид углерода (CO), формиат, метан, метанол и продукты C2+, включая этилен и этанол (25). Восстановление CO 2 с высокой селективностью по отношению к CO и формиату уже реализовано, поскольку эти реакции представляют собой процесс переноса двух электронов (26). Более сложно получить продукт C2+ с высокой селективностью, поскольку процесс требует переноса более 2 электронов и нескольких протонов, что требует множества промежуточных продуктов реакции, некоторые из которых являются общими с различными возможными продуктами.Высокое перенапряжение, необходимое для большинства катализаторов восстановления CO 2 , также подразумевает низкую эффективность преобразования энергии, <50% (по сравнению с 60-70% для водных электролизеров) (9).
CO 2 может быть восстановлен до различных продуктов C1, включая монооксид углерода (CO), формиат, метан, метанол и продукты C2+, включая этилен и этанол (25). Восстановление CO 2 с высокой селективностью по отношению к CO и формиату уже реализовано, поскольку эти реакции представляют собой процесс переноса двух электронов (26). Более сложно получить продукт C2+ с высокой селективностью, поскольку процесс требует переноса более 2 электронов и нескольких протонов, что требует множества промежуточных продуктов реакции, некоторые из которых являются общими с различными возможными продуктами.Высокое перенапряжение, необходимое для большинства катализаторов восстановления CO 2 , также подразумевает низкую эффективность преобразования энергии, <50% (по сравнению с 60-70% для водных электролизеров) (9).
Как обсуждалось для OER, эффективность восстановления CO 2 на металлических катализаторах ограничивается линейными масштабными соотношениями.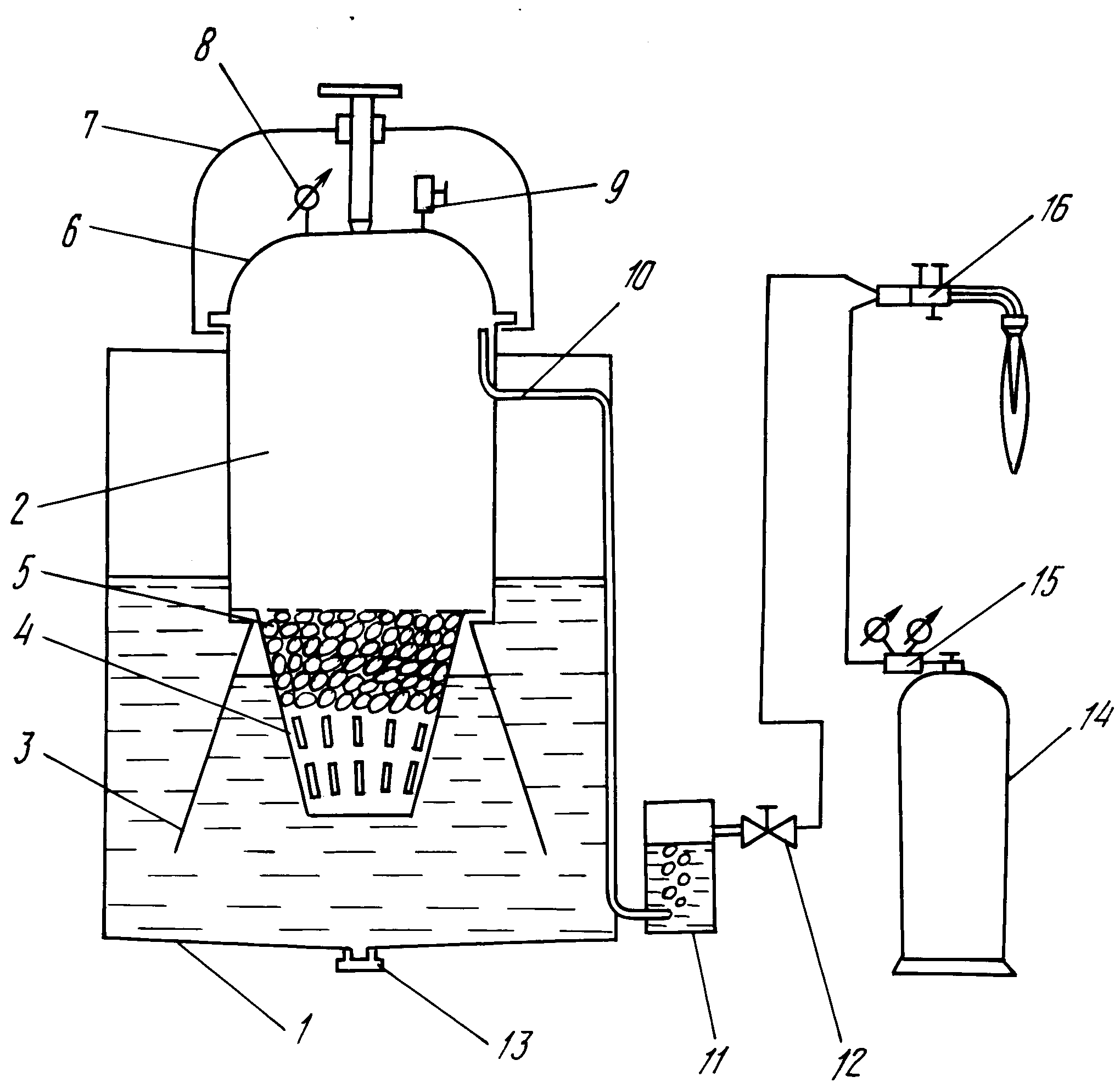 Например, на рис. 4 A показана корреляция свободной энергии (рассчитанная с помощью теории функционала плотности, DFT) двух промежуточных соединений при восстановлении CO 2 до CO, E(COOH) и E(CO).Желательна более низкая свободная энергия и более стабильная связь M-COOH, тогда как более слабое связывание с CO необходимо для оптимизации десорбции продукта (27). Это сложно для катализатора с одним металлом, если промежуточные продукты связываются с одним и тем же сайтом, потому что прочность связи M-C линейно увеличивается. Мультиметаллические катализаторы вдохновлены активным центром фермента CO-дегидрогеназы CODH, в котором совместное связывание с двумя атомами металла стабилизирует переходное состояние CO 2 — (28, 29).Cu является уникальным катализатором восстановления CO 2 , потому что он благоприятствует продуктам C2+, в том числе таким, как этанол, которые идеально подходят для сезонного хранения. Cu образует умеренно прочную связь с CO, но не настолько сильную, чтобы отравить поверхность, что обеспечивает достаточное покрытие для связывания C-C или стадий протонирования (30, 31).
Например, на рис. 4 A показана корреляция свободной энергии (рассчитанная с помощью теории функционала плотности, DFT) двух промежуточных соединений при восстановлении CO 2 до CO, E(COOH) и E(CO).Желательна более низкая свободная энергия и более стабильная связь M-COOH, тогда как более слабое связывание с CO необходимо для оптимизации десорбции продукта (27). Это сложно для катализатора с одним металлом, если промежуточные продукты связываются с одним и тем же сайтом, потому что прочность связи M-C линейно увеличивается. Мультиметаллические катализаторы вдохновлены активным центром фермента CO-дегидрогеназы CODH, в котором совместное связывание с двумя атомами металла стабилизирует переходное состояние CO 2 — (28, 29).Cu является уникальным катализатором восстановления CO 2 , потому что он благоприятствует продуктам C2+, в том числе таким, как этанол, которые идеально подходят для сезонного хранения. Cu образует умеренно прочную связь с CO, но не настолько сильную, чтобы отравить поверхность, что обеспечивает достаточное покрытие для связывания C-C или стадий протонирования (30, 31). Каталитические пути, ведущие к углеводородам или оксигенатам на Cu, сложны и сильно взаимосвязаны, о чем свидетельствует относительно низкая фарадеевская эффективность (FE) для производства этилена и этанола (рис.4 В ). Легирование Cu другими металлами (29, 32⇓–34) и создание наноструктур, которые модулируют химическое окружение сайта связывания CO (35⇓–37), являются интересными стратегиями управления распределением продуктов C2+. Учитывая сложность этой проблемы, необходимы более совершенные спектроскопические зонды и микроскопы, которые могут охарактеризовать структуру электрокаталитических центров. Систематический высокопроизводительный скрининг, управляемый вычислениями и машинным обучением, также становится эффективным средством решения электрокаталитических проблем такого рода (38).
Каталитические пути, ведущие к углеводородам или оксигенатам на Cu, сложны и сильно взаимосвязаны, о чем свидетельствует относительно низкая фарадеевская эффективность (FE) для производства этилена и этанола (рис.4 В ). Легирование Cu другими металлами (29, 32⇓–34) и создание наноструктур, которые модулируют химическое окружение сайта связывания CO (35⇓–37), являются интересными стратегиями управления распределением продуктов C2+. Учитывая сложность этой проблемы, необходимы более совершенные спектроскопические зонды и микроскопы, которые могут охарактеризовать структуру электрокаталитических центров. Систематический высокопроизводительный скрининг, управляемый вычислениями и машинным обучением, также становится эффективным средством решения электрокаталитических проблем такого рода (38).
Рис. 4.
СО 2 электролиз. ( A ) Масштабное соотношение между силой адсорбции СООН и СО на различных металлических поверхностях и в ферментах. Перепечатано с разрешения исх. 27. Copyright 2013 Американское химическое общество. ( B ) Сравнение плотности тока и FE восстановления CO 2 до этилена (синий) и этанола (красный). Сплошные символы относятся к опубликованным тестам стабильности. Более высокая плотность тока достигается в конфигурации с трехфазной границей (TPB) по сравнению с водной фазой восстановления CO 2 (Aq.). Данные от исх. 29, 32⇓–34 и 35⇓–37. ( C ) Усиленный массоперенос CO 2 вблизи поверхности иглы Au. Сильное электрическое поле на кончике иглы Au притягивает гидратированный K + , который концентрирует CO 2 в своей сольватной оболочке. Адаптировано с разрешения исх. 39, Springer Nature: Nature , авторское право 2016 г. ( D ) Строительство TPB в газовом электролизе CO 2 . Катализатор Cu напыляется на пористую подложку из ПТФЭ, которая обеспечивает путь диффузии газа.Из исх. 40. Перепечатано с разрешения AAAS.
27. Copyright 2013 Американское химическое общество. ( B ) Сравнение плотности тока и FE восстановления CO 2 до этилена (синий) и этанола (красный). Сплошные символы относятся к опубликованным тестам стабильности. Более высокая плотность тока достигается в конфигурации с трехфазной границей (TPB) по сравнению с водной фазой восстановления CO 2 (Aq.). Данные от исх. 29, 32⇓–34 и 35⇓–37. ( C ) Усиленный массоперенос CO 2 вблизи поверхности иглы Au. Сильное электрическое поле на кончике иглы Au притягивает гидратированный K + , который концентрирует CO 2 в своей сольватной оболочке. Адаптировано с разрешения исх. 39, Springer Nature: Nature , авторское право 2016 г. ( D ) Строительство TPB в газовом электролизе CO 2 . Катализатор Cu напыляется на пористую подложку из ПТФЭ, которая обеспечивает путь диффузии газа.Из исх. 40. Перепечатано с разрешения AAAS.
Существуют также острые системные проблемы с электролизом CO 2 .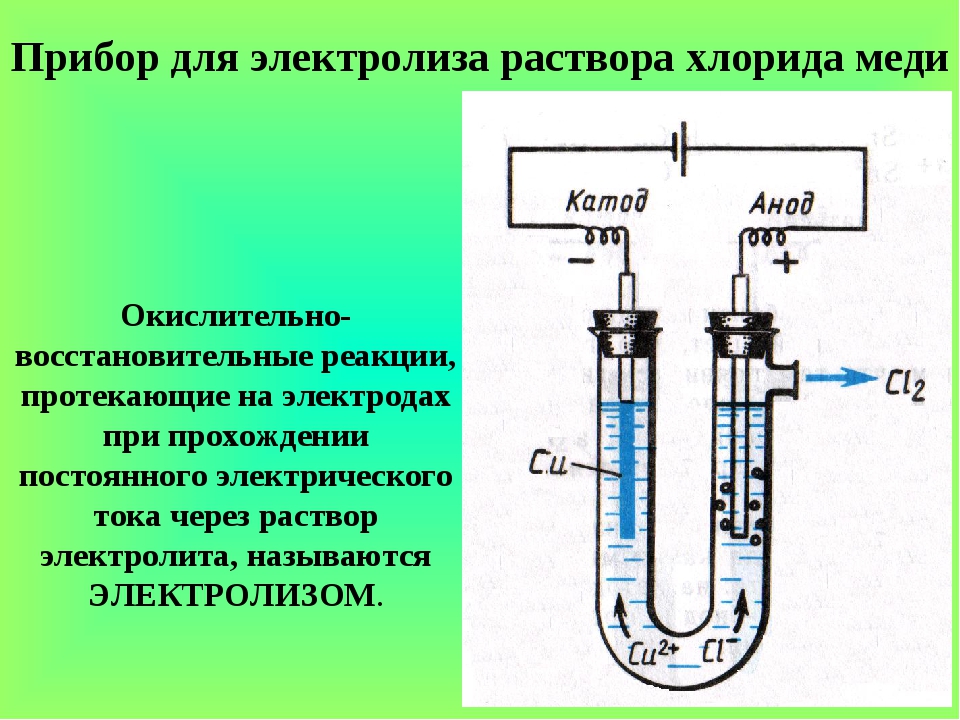 Низкая растворимость СО 2 в воде в кислых условиях создает ограничение массопереноса, а при высоких перенапряжениях реакция ГВР становится доминирующей. Стратегии концентрации CO 2 на поверхности электрода могут в определенной степени смягчить эту проблему (рис. 4 C ) (39), и массоперенос значительно улучшается, когда CO 2 подается в газовой фазе.В этом случае важно построить трехфазную границу (TPB) с большой площадью поверхности, где встречаются катализатор, электролит и газообразный реагент. На рис. 4 D показан TPB, изготовленный путем напыления слоя катализатора Cu на подложку из политетрафторэтилена (ПТФЭ), которая предотвращает затопление системы, поверх которой нанесен углеродный проводящий слой. Газообразный CO 2 диффундирует через пористый слой ПТФЭ, а HER подавляется с помощью щелочного электролита (40). Уроки биологических систем, таких как растения C4 (растения с альтернативным путем фотосинтеза, включающие CO 2 в промежуточное соединение C4, оксалоацетат), могут вдохновить на другие стратегии концентрации CO 2 в конфигурации TPB.
Низкая растворимость СО 2 в воде в кислых условиях создает ограничение массопереноса, а при высоких перенапряжениях реакция ГВР становится доминирующей. Стратегии концентрации CO 2 на поверхности электрода могут в определенной степени смягчить эту проблему (рис. 4 C ) (39), и массоперенос значительно улучшается, когда CO 2 подается в газовой фазе.В этом случае важно построить трехфазную границу (TPB) с большой площадью поверхности, где встречаются катализатор, электролит и газообразный реагент. На рис. 4 D показан TPB, изготовленный путем напыления слоя катализатора Cu на подложку из политетрафторэтилена (ПТФЭ), которая предотвращает затопление системы, поверх которой нанесен углеродный проводящий слой. Газообразный CO 2 диффундирует через пористый слой ПТФЭ, а HER подавляется с помощью щелочного электролита (40). Уроки биологических систем, таких как растения C4 (растения с альтернативным путем фотосинтеза, включающие CO 2 в промежуточное соединение C4, оксалоацетат), могут вдохновить на другие стратегии концентрации CO 2 в конфигурации TPB. Фотосинтезирующие организмы развили способность направлять CO 2 в рибулозо-1,5-бисфосфат в качестве источника углерода для цикла Кальвина. Растения C4 приобретают дополнительную концентрацию, улавливая CO 2 в 4-углеродном соединении и пропуская его в клетки оболочки для декарбоксилирования, что приводит к локальному снабжению CO 2 для фиксации (41). Аналогичное хранение и доставка CO 2 решит основную проблему электролизеров CO 2 , работающих на газе, поскольку скорость однопроходной конверсии в современных электролизерах низка.Можно представить себе оснащение диффузионного слоя в электролизере локализованными в градиенте «ячейками оболочки пучка», которые спасают непрореагировавший газ CO 2 из TPB и пропускают его вниз к реакционноспособным участкам, достигая более высоких скоростей конверсии.
Фотосинтезирующие организмы развили способность направлять CO 2 в рибулозо-1,5-бисфосфат в качестве источника углерода для цикла Кальвина. Растения C4 приобретают дополнительную концентрацию, улавливая CO 2 в 4-углеродном соединении и пропуская его в клетки оболочки для декарбоксилирования, что приводит к локальному снабжению CO 2 для фиксации (41). Аналогичное хранение и доставка CO 2 решит основную проблему электролизеров CO 2 , работающих на газе, поскольку скорость однопроходной конверсии в современных электролизерах низка.Можно представить себе оснащение диффузионного слоя в электролизере локализованными в градиенте «ячейками оболочки пучка», которые спасают непрореагировавший газ CO 2 из TPB и пропускают его вниз к реакционноспособным участкам, достигая более высоких скоростей конверсии.
Ряд уроков, извлеченных из электролизеров воды, можно применить к проблеме электролиза CO 2 , хотя некоторые проблемы специфичны для CO 2 . Градиенты pH, возникающие в мембранном электролите, требуют энергии в электролизёрах воды, которые работают в нейтральном или почти нейтральном растворе, и по этой причине все электролизеры воды работают в сильнокислых или сильнощелочных условиях.Использование буферных растворов в электролизе CO 2 создает градиенты pH и проблемы с управлением протонами при высокой плотности тока. Для электролизеров воды биполярная мембрана (BPM) решает эту проблему, работая катодом и анодом в кислоте и щелочи соответственно. Такое расположение сводит к минимуму поляризационные потери мембраны, поскольку автодиссоциация воды в BPM поставляет ионы H + и OH — на катод и анод соответственно. Эта стратегия может быть применена к электролизу CO 2 , но с некоторыми изменениями, поскольку восстановление CO 2 требует другого оптимального pH от HER.Использование BPM также смягчает проблему перекрестного взаимодействия как анионных, так и нейтральных продуктов (42).
Градиенты pH, возникающие в мембранном электролите, требуют энергии в электролизёрах воды, которые работают в нейтральном или почти нейтральном растворе, и по этой причине все электролизеры воды работают в сильнокислых или сильнощелочных условиях.Использование буферных растворов в электролизе CO 2 создает градиенты pH и проблемы с управлением протонами при высокой плотности тока. Для электролизеров воды биполярная мембрана (BPM) решает эту проблему, работая катодом и анодом в кислоте и щелочи соответственно. Такое расположение сводит к минимуму поляризационные потери мембраны, поскольку автодиссоциация воды в BPM поставляет ионы H + и OH — на катод и анод соответственно. Эта стратегия может быть применена к электролизу CO 2 , но с некоторыми изменениями, поскольку восстановление CO 2 требует другого оптимального pH от HER.Использование BPM также смягчает проблему перекрестного взаимодействия как анионных, так и нейтральных продуктов (42).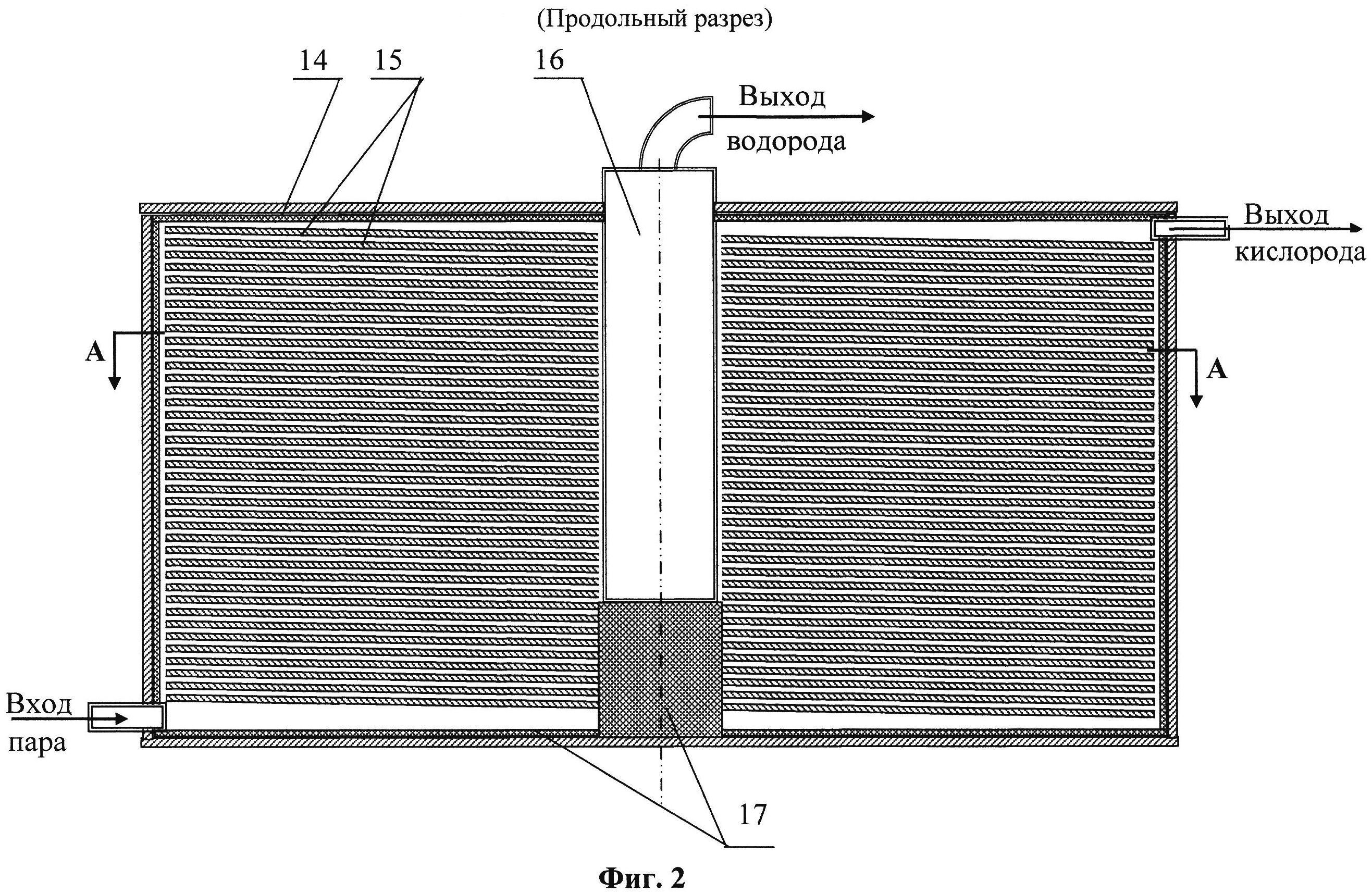
Твердотельные электролиты
Поскольку скорость химических реакций экспоненциально возрастает с температурой, электролизеры средней и высокой температуры эффективно снижают перенапряжения электродов как для анодных, так и для катодных реакций. На рис. 3 C сравниваются поляризационные кривые ячейки PEM при 60 °C с ячейкой твердооксидного электролиза (SOEC) при 800 °C (43), а на рис.3 D показывает данные для ячейки, содержащей твердотельный электролит с протонной проводимостью (44). Электродные реакции в среднетемпературных (от 250 до 500 °С) и высокотемпературных (от 600 до 800 °С) электролизерах несколько отличаются от таковых в полимерных электролизерах в зависимости от типа используемого электролита. Например, в SOEC водяной пар или CO 2 реагируют на катоде с образованием H 2 или CO соответственно и O 2− в двухэлектронном процессе. На аноде ионы O 2− объединяются, образуя газ O 2 .
(La 1-x Sr x ) 1-y MnO 3 является одним из наиболее изученных катализаторов для анода SOEC, но имеет проблемы с отслоением от электролита, вызывая увеличение поляризации (45 ). На катоде часто используются никель и другие поздние переходные металлы в качестве катализаторов SOEC, но обычно они не очень стабильны при требуемых температурах (46). Были проведены испытания с использованием перовскитов, включая La 0,6 Sr 0,4 VO 3-d и (La 0.75 Sr 0,25 ) 0,95 Mn 0,5 Cr 0,5 O 3 в качестве катализаторов на катоде, а также с многообещающими результатами (47, 48). La 1-x Sr x Ga 1-y Mg y O 3 имеет оксидно-ионную проводимость в 5 раз выше, чем типичные электролиты на основе диоксида циркония, но его стабильность в ТЭП подробно не исследована ( 49). Одно исследование с использованием La 1-x Sr x Ga 1-y Mg y O 3 в твердооксидном топливном элементе показало, что выходное напряжение спадает при скорости 1 мВ/ч (50), т.е. не подходит для коммерческой системы.
На катоде часто используются никель и другие поздние переходные металлы в качестве катализаторов SOEC, но обычно они не очень стабильны при требуемых температурах (46). Были проведены испытания с использованием перовскитов, включая La 0,6 Sr 0,4 VO 3-d и (La 0.75 Sr 0,25 ) 0,95 Mn 0,5 Cr 0,5 O 3 в качестве катализаторов на катоде, а также с многообещающими результатами (47, 48). La 1-x Sr x Ga 1-y Mg y O 3 имеет оксидно-ионную проводимость в 5 раз выше, чем типичные электролиты на основе диоксида циркония, но его стабильность в ТЭП подробно не исследована ( 49). Одно исследование с использованием La 1-x Sr x Ga 1-y Mg y O 3 в твердооксидном топливном элементе показало, что выходное напряжение спадает при скорости 1 мВ/ч (50), т.е. не подходит для коммерческой системы. Электролиты с протонной проводимостью также очень перспективны, поскольку они могут достигать более высокой проводимости, чем материалы с оксидной проводимостью, при относительно низких температурах (51). Наиболее изученным типом протонпроводящих электролитов являются перовскиты BaZrO 3 и BaCeO 3 , где первый более стабилен, а второй более проводящий (52). Хорошим компромиссом между ними стало их объединение в BaCe 0,5 Zr 0,3 Y 0,2 O 3-d , что привело к впечатляющей плотности тока 830 мА/см 2 при 1.5 В (53). Недостатком керамических протонных или оксидно-ионных проводников является то, что ионная проводимость не так высока, как у полимерных электролитов, а высокие рабочие температуры вызывают со временем деградацию даже материалов электродов и электролитов. Один из способов, которым исследователи попытались свести к минимуму деградацию, — это снизить рабочую температуру. Недавно было показано, что твердые кислоты являются хорошими проводниками протонов при промежуточных температурах.
Электролиты с протонной проводимостью также очень перспективны, поскольку они могут достигать более высокой проводимости, чем материалы с оксидной проводимостью, при относительно низких температурах (51). Наиболее изученным типом протонпроводящих электролитов являются перовскиты BaZrO 3 и BaCeO 3 , где первый более стабилен, а второй более проводящий (52). Хорошим компромиссом между ними стало их объединение в BaCe 0,5 Zr 0,3 Y 0,2 O 3-d , что привело к впечатляющей плотности тока 830 мА/см 2 при 1.5 В (53). Недостатком керамических протонных или оксидно-ионных проводников является то, что ионная проводимость не так высока, как у полимерных электролитов, а высокие рабочие температуры вызывают со временем деградацию даже материалов электродов и электролитов. Один из способов, которым исследователи попытались свести к минимуму деградацию, — это снизить рабочую температуру. Недавно было показано, что твердые кислоты являются хорошими проводниками протонов при промежуточных температурах.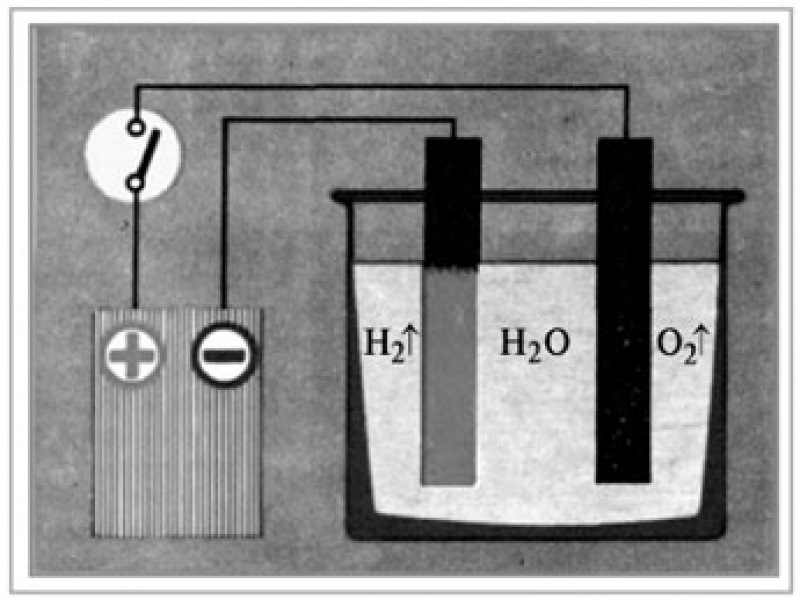 Например, CsHSO 4 , CsH 2 PO 4 и Cs 2 (HSO 4 ) (H 2 PO 4 ) показали высокую протонную проводимость, а также некоторые другие, включая 4 , показали высокую протонную проводимость. RB 3 H (SEO 2 ) 2 , (NH 4 ) 3 H (SO 4 ) 2 , а также K 3 H (SO 4 ) 2 .Эти материалы достигают проводимости при температурах от 120 до 300 °C, но ограничены их хрупкими механическими свойствами (54). Будущие исследования должны быть сосредоточены на улучшении интерфейса электролита и катализатора, чтобы свести к минимуму расслоение. Другой интересной разработкой стало использование электролитов, которые могут проводить как протоны, так и ионы оксидов. Одна группа сделала гибридный SOEC, используя BaZr 0,1 Ce 0,7 Y 0,1 Yb 0,1 O 3-d в качестве электролита, который мог производить 3.
Например, CsHSO 4 , CsH 2 PO 4 и Cs 2 (HSO 4 ) (H 2 PO 4 ) показали высокую протонную проводимость, а также некоторые другие, включая 4 , показали высокую протонную проводимость. RB 3 H (SEO 2 ) 2 , (NH 4 ) 3 H (SO 4 ) 2 , а также K 3 H (SO 4 ) 2 .Эти материалы достигают проводимости при температурах от 120 до 300 °C, но ограничены их хрупкими механическими свойствами (54). Будущие исследования должны быть сосредоточены на улучшении интерфейса электролита и катализатора, чтобы свести к минимуму расслоение. Другой интересной разработкой стало использование электролитов, которые могут проводить как протоны, так и ионы оксидов. Одна группа сделала гибридный SOEC, используя BaZr 0,1 Ce 0,7 Y 0,1 Yb 0,1 O 3-d в качестве электролита, который мог производить 3. 16 А/см 2 при 1,3 В и 750 °C. Эти характеристики намного лучше, чем для электролитов с одиночной ионной проводимостью (55). Исследования твердотельных систем как для расщепления воды, так и для электролиза CO 2 показывают устойчивый прогресс и являются перспективными для производства топлива и химического сырья (H 2 и CO) из электрической энергии. Haldor Topsøe уже производит SOEC для крупномасштабного производства CO по запросу из CO 2 с чистотой до 99.999% (56).
16 А/см 2 при 1,3 В и 750 °C. Эти характеристики намного лучше, чем для электролитов с одиночной ионной проводимостью (55). Исследования твердотельных систем как для расщепления воды, так и для электролиза CO 2 показывают устойчивый прогресс и являются перспективными для производства топлива и химического сырья (H 2 и CO) из электрической энергии. Haldor Topsøe уже производит SOEC для крупномасштабного производства CO по запросу из CO 2 с чистотой до 99.999% (56).
Электрохимическое восстановление азота
Электросинтез аммиака (ЭСА) изучается для лучшего понимания электрокаталитической активации диазота и ее ограничений. Это было сделано в диапазоне температур путем взаимодействия газа N 2 на катоде и воды на аноде, которые разделены протонпроводящим электролитом, или путем взаимодействия N 2 и воды на катоде с использованием анионпроводящего электролита. электролит. Из-за 6-электронной природы реакции восстановления N 2 фарадеевская и энергетическая эффективность сочетания окисления воды и восстановления азота имеют тенденцию быть очень низкими. Более широко изучаемый подход заключается в использовании более высоких температур и подаче H 2 на анод. Это может увеличить FE за счет окисления H 2 , но высокие температуры могут привести к разложению образовавшегося NH 3 (57). В низкотемпературном ESA наиболее часто изучаемой мембраной является нафион из-за его высокой проводимости и стабильности, хотя один из самых высоких FE, о которых сообщалось до сих пор (41%), был получен из анионообменной полимерной мембраны с железным катодом (58). Другие протестированные катализаторы включают Pt, Ru и проводящие оксиды металлов с аналогичными результатами (59).Несколько попыток использовать расплавы солей при 400 °C с N 3− в качестве подвижного иона в электролите и Ni в качестве катализатора показали, что FE достигает 80%, а скорость синтеза выше, чем у любого твердооксидного проводника (60). В этом случае электрокатализаторы обычно представляют собой поздние переходные металлы, такие как серебро, никель или палладий, а электролиты часто те же, что и в SOEC с расщеплением воды (59).
Более широко изучаемый подход заключается в использовании более высоких температур и подаче H 2 на анод. Это может увеличить FE за счет окисления H 2 , но высокие температуры могут привести к разложению образовавшегося NH 3 (57). В низкотемпературном ESA наиболее часто изучаемой мембраной является нафион из-за его высокой проводимости и стабильности, хотя один из самых высоких FE, о которых сообщалось до сих пор (41%), был получен из анионообменной полимерной мембраны с железным катодом (58). Другие протестированные катализаторы включают Pt, Ru и проводящие оксиды металлов с аналогичными результатами (59).Несколько попыток использовать расплавы солей при 400 °C с N 3− в качестве подвижного иона в электролите и Ni в качестве катализатора показали, что FE достигает 80%, а скорость синтеза выше, чем у любого твердооксидного проводника (60). В этом случае электрокатализаторы обычно представляют собой поздние переходные металлы, такие как серебро, никель или палладий, а электролиты часто те же, что и в SOEC с расщеплением воды (59). Одна исследовательская группа также использовала CH 4 в качестве источника водорода вместо H 2 с аналогичными результатами (61).Низкий КЭ и низкая плотность тока являются постоянными проблемами для исследований ЕКА. При более высоких температурах КЭ колеблется от <1 до 80%, но плотность тока слишком мала для практических целей и находится в диапазоне от <1 до 23 мА/см 2 . Для температур ниже 100 °C КЭ обычно составляет всего 1–2 %, хотя есть несколько отчетов, которые значительно выше и могут быть многообещающими, если удастся улучшить плотность тока (58). Расчеты DFT помогли прояснить проблемы электрокатализа азота.В частности, одна группа обнаружила, что различия в энергиях адсорбции для промежуточных продуктов NH x * далеки от оптимальных значений для желаемой реакции, что представляет собой трудную проблему для ESA (62).
Одна исследовательская группа также использовала CH 4 в качестве источника водорода вместо H 2 с аналогичными результатами (61).Низкий КЭ и низкая плотность тока являются постоянными проблемами для исследований ЕКА. При более высоких температурах КЭ колеблется от <1 до 80%, но плотность тока слишком мала для практических целей и находится в диапазоне от <1 до 23 мА/см 2 . Для температур ниже 100 °C КЭ обычно составляет всего 1–2 %, хотя есть несколько отчетов, которые значительно выше и могут быть многообещающими, если удастся улучшить плотность тока (58). Расчеты DFT помогли прояснить проблемы электрокатализа азота.В частности, одна группа обнаружила, что различия в энергиях адсорбции для промежуточных продуктов NH x * далеки от оптимальных значений для желаемой реакции, что представляет собой трудную проблему для ESA (62).
Перспективы
Рост мощности возобновляемых источников энергии из солнечной, ветровой и других углеродно-нейтральных источников ограничивается отсутствием адекватных решений для краткосрочного и долгосрочного хранения энергии. Жидкое топливо на основе углерода идеально подходит для долговременного хранения энергии из-за его высокой плотности энергии и хорошо развитой инфраструктуры для его транспортировки, хранения и использования.Электролиз обеспечивает ключевую связь между электрической энергией и жидким топливом либо путем прямого электросинтеза из CO 2 и воды, либо путем производства сырья для синтеза топлива, такого как водород и синтетический газ. Последние электролитические процессы, которые включают 2-электронные, 2-протонные катодные реакции, уже хорошо разработаны с научной и технологической точки зрения. Электролиз воды с использованием щелочных электролизеров был коммерциализирован в тех частях мира, где гидроэлектроэнергия дешева и изобилует.Демонстрация технологий производства CO и синтез-газа прошла успешно как с низкотемпературными системами на основе полимерных электролитов, так и с высокотемпературными твердотельными электролизерами.
Жидкое топливо на основе углерода идеально подходит для долговременного хранения энергии из-за его высокой плотности энергии и хорошо развитой инфраструктуры для его транспортировки, хранения и использования.Электролиз обеспечивает ключевую связь между электрической энергией и жидким топливом либо путем прямого электросинтеза из CO 2 и воды, либо путем производства сырья для синтеза топлива, такого как водород и синтетический газ. Последние электролитические процессы, которые включают 2-электронные, 2-протонные катодные реакции, уже хорошо разработаны с научной и технологической точки зрения. Электролиз воды с использованием щелочных электролизеров был коммерциализирован в тех частях мира, где гидроэлектроэнергия дешева и изобилует.Демонстрация технологий производства CO и синтез-газа прошла успешно как с низкотемпературными системами на основе полимерных электролитов, так и с высокотемпературными твердотельными электролизерами.
Прямое электролитическое производство жидких топлив, таких как этанол или аммиак, требует от нас освоения каскадов электрокаталитических реакций помимо простых одноэлектронных промежуточных продуктов. Хотя восстановление CO 2 до продуктов сочетания С-С на медьсодержащих катализаторах известно с 1980-х годов, подробный механизм был понят только недавно путем объединения теории электронной структуры с экспериментальными электрохимическими и спектроскопическими экспериментами.Обнадеживающий прогресс был достигнут в поиске катализаторов и электролитов, которые позволяют селективно производить продукты C 2 , такие как этилен и этанол, но высокие катодные и анодные перенапряжения ограничивают эффективность этих процессов. В дополнение к изучению катализа стратегии улучшения транспорта реагентов, продуктов и ионов также важны для разработки эффективных электролизеров для CO 2 и N 2 .
Хотя восстановление CO 2 до продуктов сочетания С-С на медьсодержащих катализаторах известно с 1980-х годов, подробный механизм был понят только недавно путем объединения теории электронной структуры с экспериментальными электрохимическими и спектроскопическими экспериментами.Обнадеживающий прогресс был достигнут в поиске катализаторов и электролитов, которые позволяют селективно производить продукты C 2 , такие как этилен и этанол, но высокие катодные и анодные перенапряжения ограничивают эффективность этих процессов. В дополнение к изучению катализа стратегии улучшения транспорта реагентов, продуктов и ионов также важны для разработки эффективных электролизеров для CO 2 и N 2 .
Наше понимание хорошо разработанных технологий, таких как электролиз воды, является полезным руководством для решения других проблем электрохимического преобразования энергии.Принципы катализа в многоэлектронных реакциях, например линейные скейлинговые соотношения, можно перенести из одной реакции в другую. Уроки на системном уровне также являются общими для разных электролитических систем. Например, управление протонами с помощью BPM решает проблемы системного уровня как для воды, так и для электролиза CO 2 . Снижение перенапряжений электродов при повышенных температурах эффективно для электролиза воды и CO 2 с получением H 2 и CO и в будущем может быть применено к реакциям, которые непосредственно производят жидкое топливо.Природные ферментативные системы также вдохновляют на разработку новых стратегий предварительного концентрирования и доставки реагентов, а также контроля среды каталитически активных центров для повышения как селективности, так и эффективности электрокатализаторов для производства жидкого топлива.
Уроки на системном уровне также являются общими для разных электролитических систем. Например, управление протонами с помощью BPM решает проблемы системного уровня как для воды, так и для электролиза CO 2 . Снижение перенапряжений электродов при повышенных температурах эффективно для электролиза воды и CO 2 с получением H 2 и CO и в будущем может быть применено к реакциям, которые непосредственно производят жидкое топливо.Природные ферментативные системы также вдохновляют на разработку новых стратегий предварительного концентрирования и доставки реагентов, а также контроля среды каталитически активных центров для повышения как селективности, так и эффективности электрокатализаторов для производства жидкого топлива.
Заявление о доступности данных
Нет данных, связанных с этой статьей.
Благодарности
Авторы выражают признательность Управлению фундаментальных энергетических наук, Отделу химических наук, наук о земле и энергетических биологических науках Министерства энергетики за поддержку их исследований в области солнечной фотоэлектрохимии по контракту DE-FG02-07ER15911 и Канадскому институту перспективных исследований.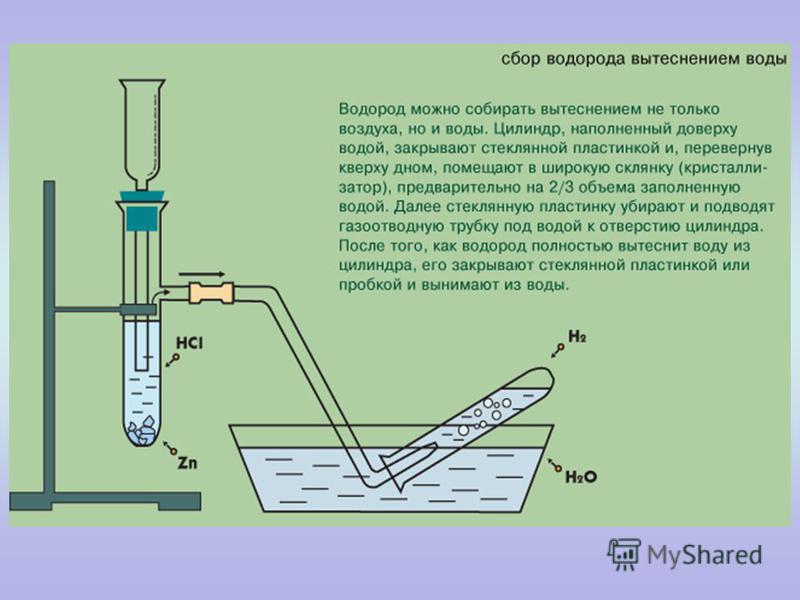 Исследовательская программа Bio-Inspired Solar Energy для поддержки их работы по электрокатализу CO 2 .
Исследовательская программа Bio-Inspired Solar Energy для поддержки их работы по электрокатализу CO 2 .
Сноски
Вклад авторов: J.A.T. и Т.Э.М. проектное исследование; З.Ю. и Дж.Л.Х. проведенное исследование; и Z.Y., J.L.H., J.A.T. и T.E.M. написал бумагу.
Авторы заявляют об отсутствии конкурирующих интересов.
Этот документ является результатом коллоквиума Артура М. Саклера Национальной академии наук «Состояние и проблемы декарбонизации нашего энергетического ландшафта», состоявшегося 10–12 октября 2018 г. в Центре Арнольда и Мейбл Бекман Национальной академии наук. Академии наук и инженерии в Ирвине, Калифорния.Коллоквиумы NAS начались в 1991 г. и публикуются в PNAS с 1995 г. С февраля 2001 г. по май 2019 г. коллоквиумы поддерживались щедрым подарком от Дамы Джиллиан и Фонда искусств, наук и гуманитарных наук доктора Артура М. Саклера в память мужа дамы Саклер, Артура М. Саклера. Полная программа и видеозаписи большинства презентаций доступны на веб-сайте НАН по адресу: http://www.
 nasonline.org/decarbonizing.
nasonline.org/decarbonizing.Эта статья является прямой отправкой PNAS.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка браузера на прием файлов cookie
Существует множество причин, по которым файл cookie не может быть установлен правильно. Ниже приведены наиболее распространенные причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки браузера, чтобы принять файлы cookie, или спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файл cookie. - Ваш браузер не поддерживает файлы cookie.
 Попробуйте другой браузер, если вы подозреваете это.
Попробуйте другой браузер, если вы подозреваете это. - Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы это исправить, установите правильное время и дату на своем компьютере. - Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Предоставить доступ без файлов cookie
потребует от сайта создания нового сеанса для каждой посещаемой вами страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в файле cookie; никакая другая информация не фиксируется.
Как правило, в файле cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт
не может определить ваше имя электронной почты, если вы не решите ввести его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступ к
остальной части вашего компьютера, и только сайт, создавший файл cookie, может его прочитать.
Обзор электролиза щелочной воды, электролиза воды PEM и электролиза воды при высокой температуре
Производство водорода электролизом воды: обзор электролиза щелочной воды, электролиза воды PEM и
Электролиз воды при высокой температуре
91
Опубликовано:
Blue Eyes Intelligence Engineering
& Sciences Publication Pvt. ООО
[15] Берджесс Г., Фернандес-Веласко Дж.Г. Материалы, рабочая энергия
входы и коэффициент полезной энергии для фотобиологического производства водорода.
Международная ассоциация водородной энергетики 2007 г.; 32: 1225 — 234.
[16] Мингён Ван, Чжи Ван, Сюйчжун Гонг, Чжаньчэн Го. Технологии
интенсификации электролиза воды для производства водорода
– Обзор. Обзор возобновляемых и устойчивых источников энергии
2014 г.; 29: 573–588.
[17] Лерой Р.Л. Промышленный электролиз воды – настоящее и будущее.
Международный журнал водородной энергетики, 1983 г.; 8: 401-17.
[18] Смолинка Т. Электролиз воды.Институт солнечной энергии Фраунгофера
Systems ISE, Фрайбург, Германия 2009: 394-413.
[19] Балат М. Потенциальная важность водорода как
решения экологических и транспортных проблем в будущем. Международный журнал
Hydrogen Energy 2008; 33: 4013–29.
[20] Ni M, Leung MKH, Leung DYC. Электрохимическая модель твердооксидного парового электролизера
для производства водорода. Chem Eng
Technol 2006; 29: 636 — 42.
[21] Розен М. А. Энергетический и эксергетический анализ производства электролитического водорода
А. Энергетический и эксергетический анализ производства электролитического водорода
. Международная ассоциация водородной энергетики, 1995 г.; 20: 547 — 53.
[22] Лутц А.Е., Брэдшоу Р.В., Келлер Дж.О., Витмер Д.Э. Термодинамический
анализ водорода методом паровой конверсии. Int J Hydrogen Energy
2003; 28: 159 — 67.
[23] Ni M, Leung MKH, Leung DYC. Энергетический и эксергетический анализ производства водорода
на установке твердооксидного парового электролизера.Int J
Hydrogen Energy 2007; 32: 4648 — 60.
[24] Хоучэн Чжан, Госин Линь, Цзиньцань Чен. Оценка и
расчет эффективности системы электролиза воды для
производства водорода. Международный журнал водородной энергетики 2010 г.;
35:10851 – 858.
[25] Б. Лаун. Термодинамический аспект получения водорода высокого давления
электролизом воды. Revue des Energies Renouvelables
2007; 10 №3: 435 – 444.
[26] Marangio F.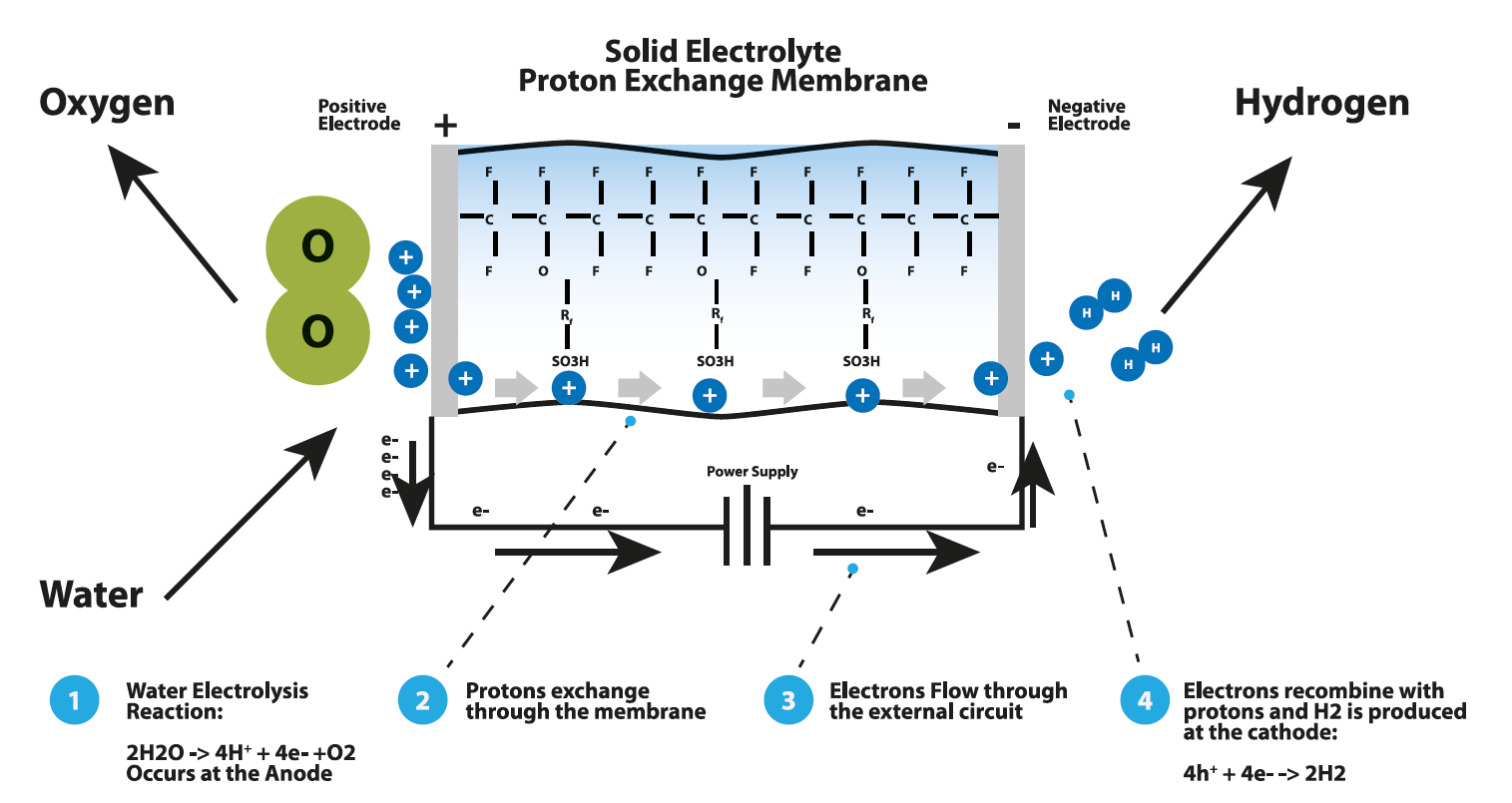 Теоретическая модель и экспериментальный анализ электролизера воды PEM высокого давления
Теоретическая модель и экспериментальный анализ электролизера воды PEM высокого давления
для производства водорода. Int J
Hydrogen Energy 2009; 34: 1143 — 85.
[27] Ni M, Leung MKH, Leung DYC. Энергетический и эксергетический анализ
производства водорода с помощью протонообменной мембраны (PEM)
электролизерной установки. Energy Convers Manag 2008; 49: 2748 — 56.
[28] Мартинес-Фриас Дж., Фам А.К., Асевес С.М.Паровой электролизер, работающий на природном газе
, для высокоэффективного производства водорода. Int J
Hydrogen Energy 2003; 28: 483 — 90.
[29] Балта М.Т., Динсер И., Хепбасли А. Термодинамическая оценка использования геотермальной энергии
в производстве водорода. Int J Hydrogen
Energy 2009; 34: 2925 — 39.
[30] Shin Y, Park W, Chang J, and Park J. Оценка электролиза пара при высокой температуре
для получения водорода.Int J
Hydrogen Energy 2007; 32: 1486 — 91.
[31] Йылдыз Б., Казими М.С. Эффективность системы производства водорода
с использованием альтернативных ядерных технологий. Int J Hydrogen Energy
2006; 31: 77 — 92.
[32] Fujiwara S, Kasai S, Yamauchi H, Yamada K, Makino S, Matsunaga
K, et al. Производство водорода методом высокотемпературного электролиза на ядерном реакторе
. Прогресс Нукл Энерджи 2008; 50: 422 — 26.
[33] Розен М.А. Эксергетический анализ образования водорода при термохимическом разложении воды
по циклу Испра Марк-10.
Международная ассоциация водородной энергетики 2008 г.; 33: 6921 — 33.
[34] Williams JH, DeBenedictis A, Ghanadan R, Mahone A, Moore J,
Morrow III WR, et al. Технологический путь к глубокому сокращению выбросов парниковых газов
к 2050 году: ключевая роль электричества. Наука 2012;
335: 53 — 59.
[35] Santos DMF, Sequeira CAC, Maccio` D, Saccone A, Figueiredo JL.
Платино-редкоземельные электроды для выделения водорода в щелочном
электролизе воды.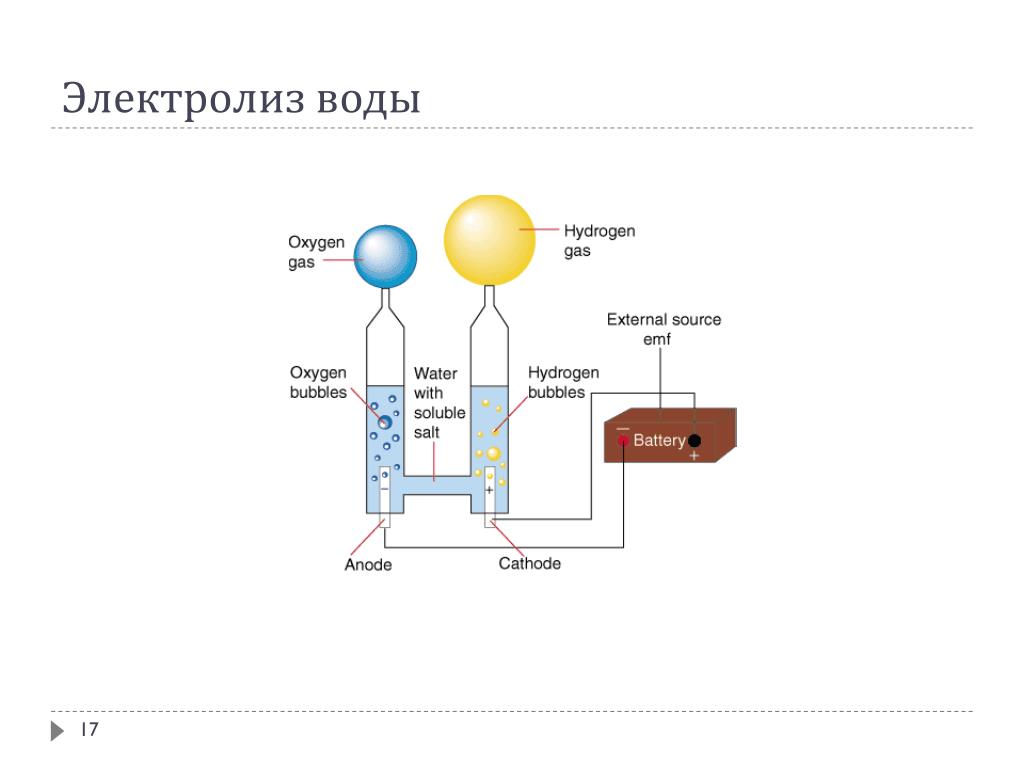 Международная ассоциация водородной энергетики, 2013 г.; 2: 3137 — 45.
Международная ассоциация водородной энергетики, 2013 г.; 2: 3137 — 45.
[36] Исида Т., Харута М. Золотые катализаторы: на пути к устойчивой химии.
Angew Chem Int Ed Engl 2007; 46: 7154 — 56.
[37] А. Манабэ, М. Кашивасэ, Т. Хасимото, Т. Хаясида, А. Като, К.
Хирао, И. Симомура, И. Нагасима. Базовое исследование щелочной воды
Электролиз
.Электрохимика Акта 2013; 100: 249– 256.
[38] Марсело Кармо, Дэвид Л. Фриц, Юрген Мергель, Детлеф Столтен. Всесторонний обзор
по электролизу воды PEM. Международный журнал
по водородной энергии 2031; 38: 4901 — 934.
[39] Pool DH, Stewart MP, O’Hagan M, Shaw WJ, Roberts JAS и
Bullock RM, etal. Кислые ионные жидкости / водный раствор как среда
и источник протона для электрокаталитического H
2
эволюция [Ni (P
2
N
2
) 2]
2
þ
комплексы.Труды Национальной академии наук 2012 г .;
109:15634–39.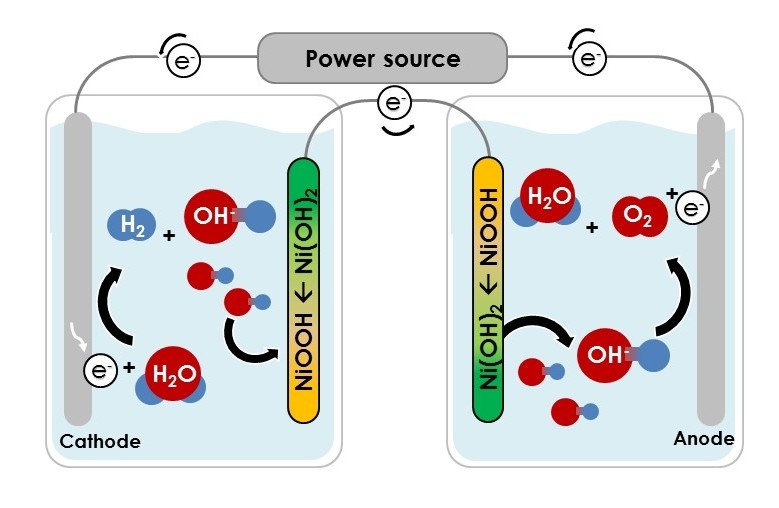
[40] Souza RF, Padilha JC, Goncalves RS, Souza MO, Rault-Berthelot J.
Электрохимическое производство водорода из электролиза воды с использованием ионной жидкости
в качестве электролита: на пути к лучшему устройству. Журнал Power
Sources 2007; 164: 792–98.
[41] Souza RF, Loget G, Padilha JC, Martini EMA, Souza MO.
Электроды молибденовые для получения водорода водой
электролиз с использованием ионных жидких электролитов.Электрохимия
Связь 2008; 10: 1673–75.
[42] Канинский М.П.М., Сапонич Д.П., Николич В.М., Зугич Д.Л., Ташич Г.С.
Энергоемкость и стабильность Ni-Moэлектродов для производства щелочного водорода
в промышленных условиях. International
Journal of Hydrogen Energy 2011; 36: 8864–68.
[43] Максич А.Д., Миулович С.М., Николич В.М., Перович М., Канинский М.П.М.
Потребление энергии при производстве электролитического водорода с использованием активаторов на основе
Ni–W – Часть I. Прикладной катализ A: General 2011;
Прикладной катализ A: General 2011;
405: 25–28.
[44] Николич В.М., Ташич Г.С., Максич А.Д., Сапонич Д.П., Миулович С.М.,
Канинский М.П.М. Повышение эффективности производства водорода из
электролиза щелочной воды – энергосбережение. Международный журнал
Hydrogen Energy 2010; 35: 12369–73.
[45] Стойич Д., Марсета М.П., Совиль С.П., Милянич С.С. Получение водорода
из электролиза воды — возможности энергосбережения.Журнал
Источники питания 2003; 118 (1-2): 315–19.
[46] Тасич Г.С., Масловара С.П., Зугич Д.Л., Максич А.Д. Характеристика
Ni-Mo катализатора, образовавшегося in situ во время получения водорода в результате электролиза
щелочной воды. Международный журнал водородной энергетики
2011; 36: 11588–95.
[47] Wei ZD, Ji MB, Chen SG, Liu Y, Sun CX, Yin GZ и др. Вода
Электролиз на угольных электродах с добавлением поверхностно-активного вещества.
Электрохимика Acta 2007; 52: 3323–29.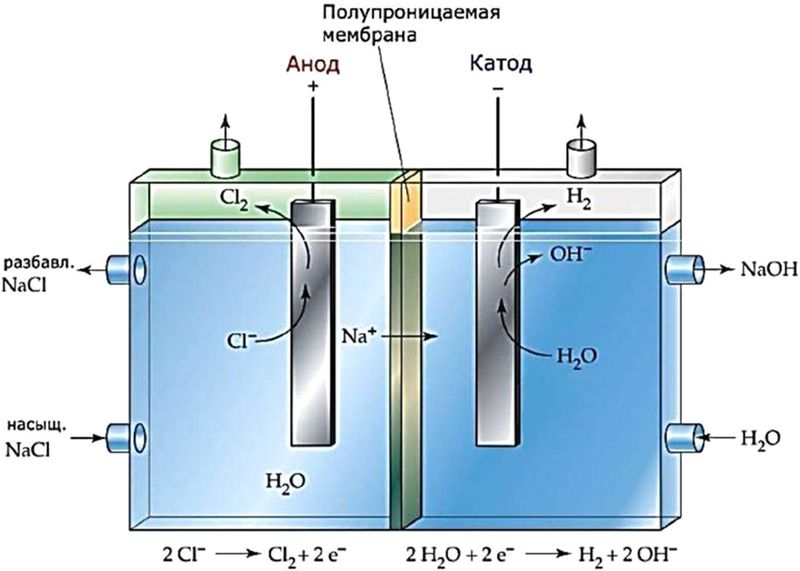
[48] Росси А., Будтс JFC. Оксидные электроды на основе Ir: реакция выделения кислорода
из смешанного растворителя. Журнал прикладной электрохимии
2002; 32: 735–41.
[49] Michaud PA, Panizza M, Ouattara L, Diaco T, Foti G, Comninellis C.
Электрохимическое окисление воды на синтетических легированных бором
анодах из тонкого сплава алмаза. Журнал прикладной электрохимии 2003;
33: 151–54.
[50] Ромдан Бен Слама. Производство водорода электролизом
воды: влияние типа электролита на характеристики электролиза
. Вычислительная вода, энергетика и окружающая среда
Инженерия, 2013; 2: 54-58.
[51] Fujishima A, Honda K. Электрохимический фотолиз воды на полупроводниковом электроде
. Природа 1972; 238: 37.
[52] Лихт С., Ван Б., Мукерджи С., Сога Т., Умено М., Трибуч Х.Более
18% конверсия солнечной энергии в производство водородного топлива; теория
и эксперимент по эффективному расщеплению солнечной воды. Int J Hydrogen
Int J Hydrogen
Energy 2001; 26: 653–59.
[53] Гибсон Т.Л., Келли Н.А. Оптимизация производства водорода
на солнечной энергии с использованием фотоэлектрических электролизных устройств. Int J Hydrogen
Energy 2008; 33: 5931–40.
[54] Рассел Дж. Х., Наттолл Л. Дж., Фикетт А. П. Получение водорода путем электролиза воды с твердым
полимерным электролитом.Американское химическое общество
Препринты отдела химии топлива 1973; 18(3): 24-40.
[55] Грабб ВТ. Миграция ионов в ионообменных мембранах. Журнал
Физическая химия 1959; 63 (1): 55 — 67.
[56] Грабб В.Т. Аккумуляторы с твердыми ионообменными электролитами I. вторичные
элементы с металлическими электродами. Журнал Электрохимического общества
, 1959 г .; 106 (4): 275 — 78.
[57] H. Takenaka, Тенденции развития производства водорода
Технология электролиза воды, Journal of the Fuel Society of
Japan 1991; 70: 487.
[58] H. Micishita, H. Matsumoto, T. Ishihara, Влияние давления на
Micishita, H. Matsumoto, T. Ishihara, Влияние давления на
Характеристики электролиза воды в ячейке с использованием Nafion
Membrane Electrode, Electrochemistry 2008; 76: 288.
[59] С.А. Григорьев, В.И. Порембский, В.Н. Фатеев, Чистый водород
производство электролизом PEM для производства водорода,
International Journal of Hydrogen Energy 2006; 31(2): 171-175.
[60] Ф.Барбир, электролиз PEM для производства водорода из
возобновляемых источников энергии, солнечная энергия; 2005 г.; 78(5): 661 — 669.
[61] В.Н. Фатеев, О.В. Арчаков, Е.К. Лютикова, Л.Н. Куликова, В.И.
Порембский, Электролиз воды в системах с твердым полимерным электролитом
, Электрохимический журнал 1993; 29(4): 551-
557.
[62] К.А. Linkous, HR Anderson, RW Kopitzke, GL Nelson,
Разработка новых электролитов с протонообменной мембраной для электролиза воды при более высоких температурах, International Journal of
Hydrogen Energy 1998; 23(7): 525-529.
[63] Р. Гарса-Вальверде, К. Мигель, Р. Мартнез-Бьяр, А. Урбина.
Оптимизированное соединение фотогальванического генератора и электролизера воды
через управляемый преобразователь постоянного тока Int. Дж. Гидрог. Энергия 2008;
33: 5352 — 62
[64] Хуанэн Су, Бернард Ян Бладергроен, Сивакумар Пасупати,
Владимир Линьков, Шан Цзи*. Исследование характеристик мембран
Электродные сборки для производства водорода твердым полимером
Прорыв в электролизе может решить загадку водорода
Предоставлено: Университет Монаша.
Газообразный водород — идеальное экологически чистое топливо: его можно извлекать из воды, и он не загрязняет окружающую среду.Но хотя водород является самым распространенным элементом во Вселенной, в природе он не встречается в больших количествах в виде газа на Земле.
Газообразный водород — идеальное экологически чистое топливо: его можно извлекать из воды, и он не загрязняет окружающую среду.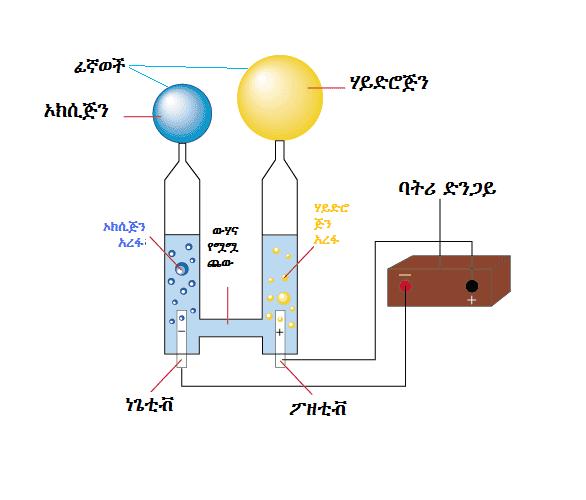 Но хотя водород является самым распространенным элементом во Вселенной, в природе он не встречается в больших количествах в виде газа на Земле.
Но хотя водород является самым распространенным элементом во Вселенной, в природе он не встречается в больших количествах в виде газа на Земле.
Началась гонка по поиску дешевых, эффективных и экологически чистых способов производства и хранения водорода.Давно известно, что электрический ток заставляет элементы воды — водород и кислород — расщепляться с образованием газообразных водорода и кислорода в процессе, известном как электролиз. Этот процесс также можно обратить вспять для выработки электроэнергии, когда газообразные водород и кислород взаимодействуют в топливном элементе (НАСА использует топливные элементы для питания спутников и космических капсул с 1960-х годов).
До недавнего времени стоимость электроэнергии была препятствием для производства промышленных объемов газообразного водорода путем электролиза.Но недорогие технологии возобновляемой электроэнергии устранили этот барьер.
Еще одним препятствием является то, что для эффективного расщепления воды на водород и кислород требуются катализаторы из редких и дорогих металлов, таких как платина и иридий. Иридий — один из самых редких и дорогих элементов на Земле — его часто приносят сюда метеориты. И даже самые стабильные катализаторы на основе иридия выдерживают электролиз лишь короткое время.
Иридий — один из самых редких и дорогих элементов на Земле — его часто приносят сюда метеориты. И даже самые стабильные катализаторы на основе иридия выдерживают электролиз лишь короткое время.
«Если вы повысите температуру во время электролиза проточной воды, катализатор на основе иридия растворится, и вы потеряете его», — объясняет доктор.Александр Симонов из Школы химии Монаша. «Это худшее, что может случиться, растворить что-то, что стоит сотни долларов за грамм. Это также может попасть в другие компоненты вашего электролитического устройства, загрязняя их и препятствуя их правильной работе».
Первые электролизеры воды использовали щелочную воду, и это остается традиционным подходом, говорит д-р Симонов. Но более продвинутая и эффективная технология использует кислую среду, используя твердотельные электролиты — к сожалению, катализаторы не могут выдерживать эту среду долго.
Д-р Симонов и члены его исследовательской группы, в том числе д-р Манджунат Чатти и Джеймс Гардинер, сделали открытие с огромным потенциалом для решения проблемы нестабильности, сделав получение водорода путем электролиза воды более экономически выгодным.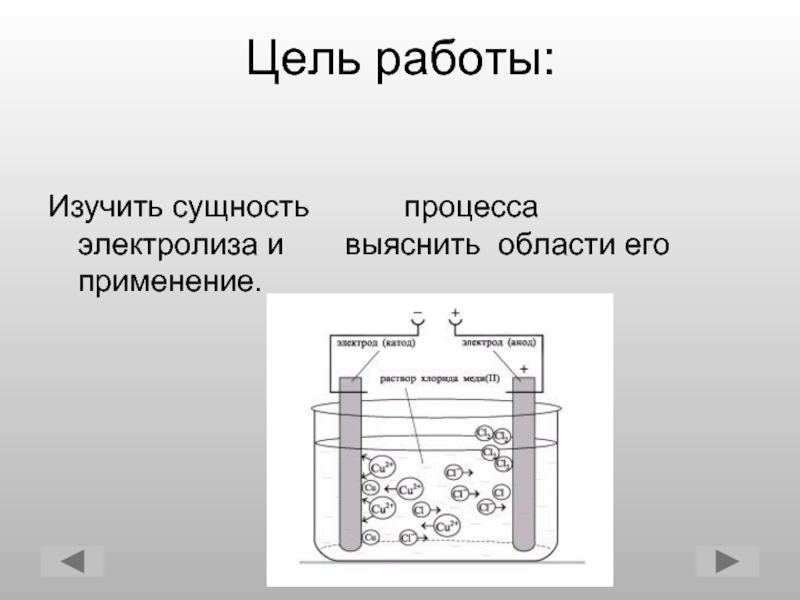
«Мы заменяем иридий элементами, которые доступны в изобилии, дешевы и работают более стабильно», — сказал доктор.говорит Симонов. «Мы продемонстрировали их стабильность в очень сильнокислых условиях и при температуре до 80°C, что является приемлемой для промышленности температурой. Мы не добились абсолютно никакого разложения».
Автобусы на водороде уже на дорогах Бразилии. Предоставлено: Университет Монаша.
Доктор Симонов описывает систему, которую он разрабатывает со своей командой, как «самовосстанавливающуюся». Поскольку все металлы, даже иридий, растворяются во время электролиза, исследователи задались вопросом, может ли растворенный материал повторно осаждаться на электроде во время работы.
«Оказалось, что может», — говорит он. «Мы создали высокоактивную поверхность электрода на основе распространенных металлов, которая поддерживает промышленно приемлемые скорости расщепления воды». Высокая температура и сильнокислая среда «делят нашу последнюю работу отличной от почти всех работ в научном мире и приближают нас к промышленному применению», — говорит он.
«Мы создали высокоактивную поверхность электрода на основе распространенных металлов, которая поддерживает промышленно приемлемые скорости расщепления воды». Высокая температура и сильнокислая среда «делят нашу последнюю работу отличной от почти всех работ в научном мире и приближают нас к промышленному применению», — говорит он.
Австралийское агентство по возобновляемым источникам энергии (ARENA) финансирует дальнейшие исследования с целью повышения эффективности и разработки масштабируемого процесса изготовления электродов, подходящего для промышленности.Доктор Симонов и его команда работают над достижением этой цели вместе с профессором химии Монаша Дугласом МакФарлейном и сотрудниками из Австралийского национального университета, профессорами Антонио Триколи и профессором Юнь Лю.
Австралия, с ее обильным солнцем и ветром, может стать сверхдержавой, использующей возобновляемые источники энергии. С помощью электролиза газообразный водород может быть получен из избыточной электроэнергии, вырабатываемой крупными проектами по производству возобновляемой электроэнергии.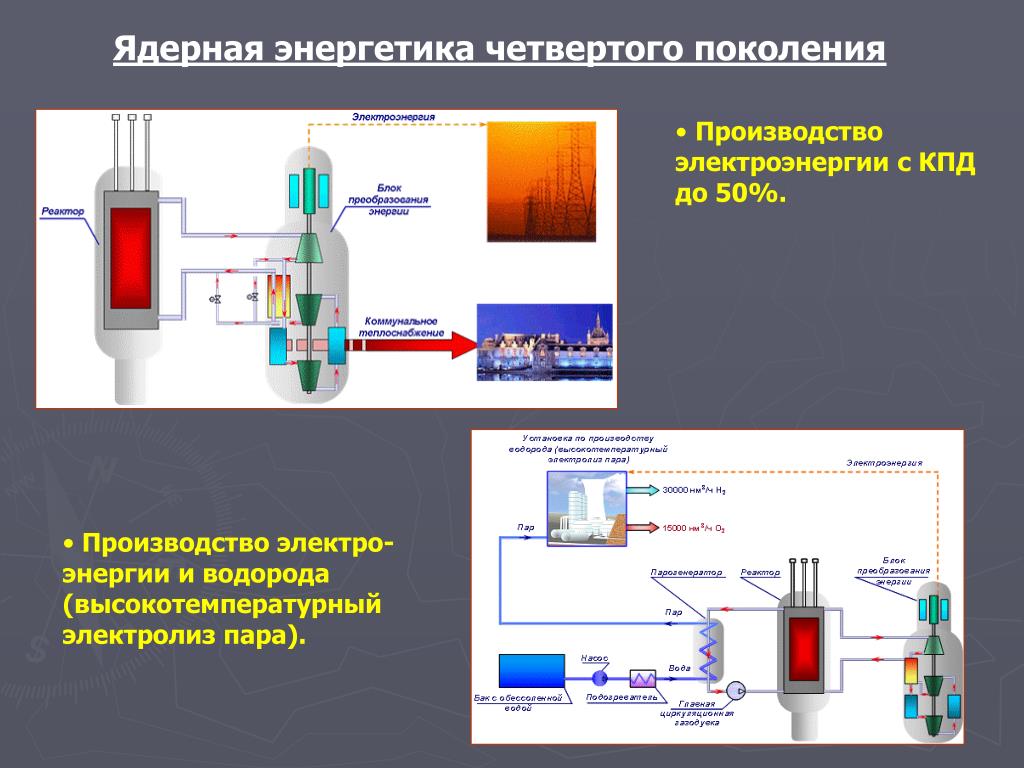 Этот водород можно было бы использовать в качестве топлива в Австралии и экспортировать в страны, нуждающиеся в альтернативах ископаемому топливу.
Этот водород можно было бы использовать в качестве топлива в Австралии и экспортировать в страны, нуждающиеся в альтернативах ископаемому топливу.
Автобусы, работающие на водороде, уже ездят по дорогам Бразилии, а Южная Корея и Япония уже продемонстрировали твердое намерение использовать водородные автомобили и водород в качестве основного энергоносителя.
Министр федеральных ресурсов Мэтт Канаван на этой неделе подписал с Южной Кореей письмо о намерениях разработать план по водороду к концу года, сигнализируя о намерении правительства Австралии расширить экспортный потенциал. Этот толчок совпал с публикацией отчета Geoscience Australia, в котором страна названа будущим «мировым лидером» в этой области.
Но газообразный водород легко воспламеняется, и его транспортировка сопряжена с некоторыми трудностями. Одной из будущих возможностей является преобразование газа в аммиак. Эта цель также исследуется доктором Симоновым и его коллегами в рамках проекта Monash Ammonia Project под руководством профессора МакФарлейна.
Д-р Симонов говорит, что в то же время поставщик энергии AGL изучает, как можно масштабировать прорыв в области электролиза, чтобы добавить экологически чистое производство водорода к линиям природного газа в Австралии в качестве способа сокращения выбросов углерода.По словам доктора Симонова, водород уже используется таким образом в северном полушарии. Другой ведущей австралийской компанией, проявляющей большой интерес к водородным технологиям, является Woodside, которая вложила значительные средства в исследования Монаша.
Доктор Симонов и профессор МакФарлейн также сотрудничают с новой австралийской компанией ANT Energy Solutions, которая разрабатывает портативный водородный электролизер при финансовой поддержке Программы совместных исследовательских центров. Портативный блок можно загрузить на грузовик и доставить туда, где доступна дешевая возобновляемая энергия.говорит Симонов.
Исследовательская группа возглавляет прорыв в области зеленой химии для возобновляемых источников энергии.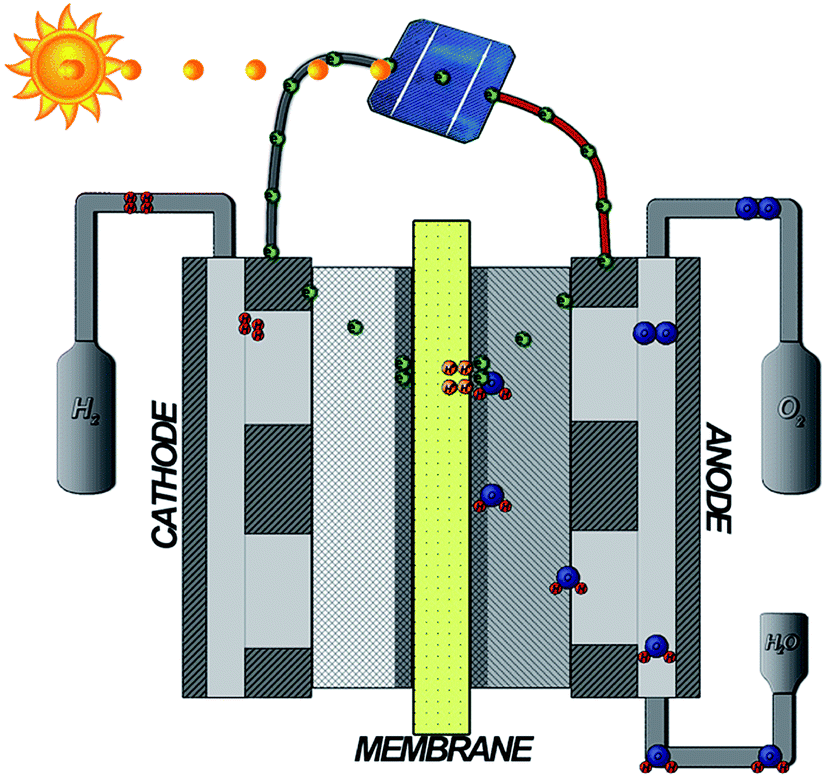
Предоставлено
Университет Монаша
Цитата :
Прорыв в электролизе может решить водородную загадку (2019, 25 сентября)
получено 10 февраля 2022 г.
с https://физ.org/news/2019-09-electrolysis-breakthrough-hydrogen-conundrum.html
Этот документ защищен авторским правом. Помимо любой добросовестной сделки с целью частного изучения или исследования, никакие
часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в ознакомительных целях.
Контент предоставляется только в ознакомительных целях.
Производство водорода — У.S. Управление энергетической информации (EIA)
Как производится водород?
Чтобы получить водород, его необходимо отделить от других элементов в молекулах, в которых он встречается. Существует множество различных источников водорода и способов его производства для использования в качестве топлива. Двумя наиболее распространенными методами производства водорода являются паровая конверсия метана и электролиз (расщепление воды электричеством. Исследователи изучают другие методы производства водорода или пути .
Процессы производства водорода
Источник: Министерство энергетики США, Управление по энергоэффективности и возобновляемым источникам энергии, Пути производства водорода (общественное достояние)
Нажмите, чтобы увеличить
Паро-метановый риформинг — широко используемый метод производства товарного водорода
На паровой конверсию метана в настоящее время приходится почти весь промышленно производимый водород в Соединенных Штатах. Коммерческие производители водорода и нефтеперерабатывающие заводы используют паровую конверсию метана для отделения атомов водорода от атомов углерода в метане (CH 4 ). При паровой конверсии метана высокотемпературный пар (от 1300°F до 1800°F) под давлением 3–25 бар (1 бар = 14,5 фунтов на квадратный дюйм) реагирует с метаном в присутствии катализатора с образованием водорода, монооксида углерода. , и относительно небольшое количество углекислого газа (CO 2 ).
Коммерческие производители водорода и нефтеперерабатывающие заводы используют паровую конверсию метана для отделения атомов водорода от атомов углерода в метане (CH 4 ). При паровой конверсии метана высокотемпературный пар (от 1300°F до 1800°F) под давлением 3–25 бар (1 бар = 14,5 фунтов на квадратный дюйм) реагирует с метаном в присутствии катализатора с образованием водорода, монооксида углерода. , и относительно небольшое количество углекислого газа (CO 2 ).
Природный газ является основным источником метана для производства водорода промышленными предприятиями и нефтеперерабатывающими заводами.Свалочный газ/биогаз, который можно назвать биометаном или возобновляемым природным газом , является источником водорода для нескольких электростанций на топливных элементах в Соединенных Штатах. Биотопливо и нефтяное топливо также являются потенциальными источниками водорода.
Электролиз использует электричество для производства водорода
Электролиз — это процесс выделения водорода из воды с помощью электрического тока.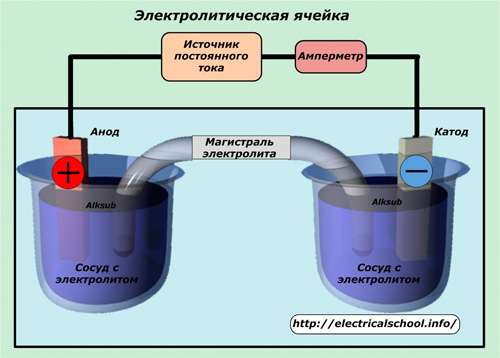 Электролиз обычно используется для демонстрации химических реакций и производства водорода на уроках естествознания в средней школе.В крупном коммерческом масштабе этот процесс можно назвать энергия-газ , где мощность это электричество, а водород газ . Электролиз сам по себе не производит никаких побочных продуктов или выбросов, кроме водорода и кислорода. Электричество для электролиза может поступать из возобновляемых источников, ядерной энергии или ископаемого топлива. Если электроэнергия для электролиза производится из ископаемого топлива (угля, природного газа и нефти) или сжигания биомассы, то соответствующие воздействия на окружающую среду и выбросы CO 2 косвенно связаны с этим водородом.
Электролиз обычно используется для демонстрации химических реакций и производства водорода на уроках естествознания в средней школе.В крупном коммерческом масштабе этот процесс можно назвать энергия-газ , где мощность это электричество, а водород газ . Электролиз сам по себе не производит никаких побочных продуктов или выбросов, кроме водорода и кислорода. Электричество для электролиза может поступать из возобновляемых источников, ядерной энергии или ископаемого топлива. Если электроэнергия для электролиза производится из ископаемого топлива (угля, природного газа и нефти) или сжигания биомассы, то соответствующие воздействия на окружающую среду и выбросы CO 2 косвенно связаны с этим водородом.
Прочие способы получения водорода
- Использование микробов, использующих свет для получения водорода
- Преобразование биомассы в газ или жидкость и выделение водорода
- Использование технологий солнечной энергии для отделения водорода от молекул воды
Категории водорода
Производители водорода, продавцы, государственные учреждения и другие организации могут классифицировать или определять водород в соответствии с источниками энергии для его производства, и они используют цветовой код для классификации водорода. Например, водород, произведенный с использованием возобновляемых источников энергии, может обозначаться как возобновляемый водород или зеленый водород . Водород, полученный из угля, можно назвать коричневым водородом , а водород, полученный из природного газа или нефти, можно назвать серым водородом . Производство коричневого или серого водорода в сочетании с улавливанием и хранением/депонированием углерода может обозначаться как синий водород . Водород, полученный с помощью ядерной энергии, может называться розовым водородом или чистым водородом
Например, водород, произведенный с использованием возобновляемых источников энергии, может обозначаться как возобновляемый водород или зеленый водород . Водород, полученный из угля, можно назвать коричневым водородом , а водород, полученный из природного газа или нефти, можно назвать серым водородом . Производство коричневого или серого водорода в сочетании с улавливанием и хранением/депонированием углерода может обозначаться как синий водород . Водород, полученный с помощью ядерной энергии, может называться розовым водородом или чистым водородом
.
Последнее обновление: 21 января 2022 г.
.


 Более крупные частицы обычно очищаются
Более крупные частицы обычно очищаются
 Одна из особенностей модели с индексом S — наличие накопительного бака, в
Одна из особенностей модели с индексом S — наличие накопительного бака, в

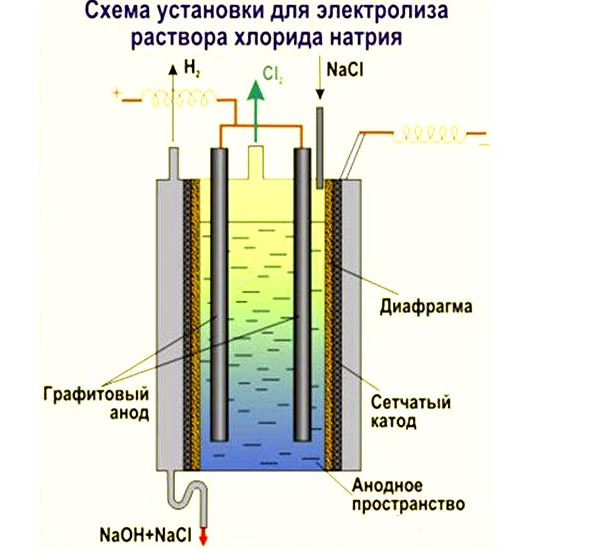
 nasonline.org/decarbonizing.
nasonline.org/decarbonizing. Попробуйте другой браузер, если вы подозреваете это.
Попробуйте другой браузер, если вы подозреваете это.