Из каких элементов состоит аккумуляторная батарея
- Категория: Поддержка по аккумуляторным батареям
- Опубликовано 01.03.2016 05:05
- Автор:
Abramova Olesya
Электрохимическая батарея состоит из катода, анода и электролита. При зарядке аккумуляторной батареи происходит накопление электронов на аноде, которое создает потенциал напряжения между анодом и катодом. При обычной работе в качестве источника питания ток протекает от катода к аноду через нагрузку. При зарядке аккумулятора ток течет в противоположном направлении.
Электроды батареи связаны между собой двумя различными путями, первый это электрический контур, через который электроны текут питать нагрузку, а второй — через электролит, где ионы движутся между электродами через диэлектрический разделитель (сепаратор). Рассмотрим подробнее эти три компонента батареи.
Анод и катод
Электрод, который высвобождает электроны в ходе окислительно-восстановительной реакции, называется анод. Электрический потенциал анода гальванического элемента отрицателен по отношению к катоду. Химическая реакция в аккумуляторной батарее является обратимым процессом, и, следовательно, полярность электродов меняется в зависимости от режима работы (заряд/разряд), но обозначение клемм всегда постоянно. В таблицах 1a, b, c и d описывается состав и процессы в литиевых, свинцовых, никелевых и щелочных батареях.
Электрический потенциал анода гальванического элемента отрицателен по отношению к катоду. Химическая реакция в аккумуляторной батарее является обратимым процессом, и, следовательно, полярность электродов меняется в зависимости от режима работы (заряд/разряд), но обозначение клемм всегда постоянно. В таблицах 1a, b, c и d описывается состав и процессы в литиевых, свинцовых, никелевых и щелочных батареях.
| Литий-ионная батарея | Катод | Анод | Электролит |
| Материальный состав элементов | Оксиды кобальта, никеля, марганца, железа и алюминия | На углеродной основе | Соли лития в органическом растворителе |
| Состав и процессы при заряженном состоянии | Оксид металла с интеркаляционной структурой | Миграция ионов лития к аноду | |
| Состав и процессы при разряженном состоянии | Ионы лития возвращаются к положительному электроду | В основном, углеродная основа |
Таблица 1a: Состав и процессы в литий-ионном аккумуляторе.
| Свинцово-кислотная батарея | Катод | Анод | Электролит |
| Материальный состав элементов | Диоксид свинца | Серый губчатый свинец | Соляная кислота |
| Состав и процессы при заряженном состоянии | Диоксид свинца PbO2, электроны присоединяются | Свинец Pb, электроны отсоединяются | Сильная серная кислота |
| Состав и процессы при разряженном состоянии | Свинец преобразуется в сульфид свинца, на аноде – с выделением электронов, а на катоде — с присоединением | Слабая серная кислота (разбавленная водой) | |
Таблица 1b: Состав и процессы в свинцово-кислотном аккумуляторе.
| NiMH, NiCd | Катод | Анод | Электролит |
| Материальный состав элементов | Никель | NiMH: водородопоглощающий сплав NiCd: кадмий | Гидроксид калия |
Таблица 1c: Состав никель-металл-гидридного и никель-кадмиевого аккумуляторах.
| Щелочная (алкалиновая) батарейка | Катод | Анод | Электролит |
| Материальный состав элементов | Диоксид марганца | Цинк | Водный раствор щелочи |
Таблица 1d: Состав щелочной (алкалиновой) батарейки.
Электролит и сепаратор
При затопленной негерметичной системе конструкции аккумулятора, жидкий электролит свободно течет между двумя электродами. В герметичных же конструкциях электролит обычно выступает в роли пропитки для сепаратора, чтобы обеспечивать движение ионов от катода к аноду и в обратном направлении при зарядке. Ионы – это атомы, которые присоединили или потеряли электроны. Потеряв благодаря этому электронейтральность, они приобретают способность двигаться между электродами через сепаратор. Сам же сепаратор является диэлектрическим, то есть не способным к электропроводности. Смотрите также: Какую функцию выполняет в электрической батарее сепаратор? и Для чего в электрической батарее нужен электролит?
Смотрите также: Какую функцию выполняет в электрической батарее сепаратор? и Для чего в электрической батарее нужен электролит?
Батареи для Tesla и накопителей электроэнергии: кто лидеры инноваций? | Экономика в Германии и мире: новости и аналитика | DW
Если ключевой элемент традиционного автомобиля — двигатель внутреннего сгорания, то во все более популярных электромобилях это — аккумуляторная батарея: от нее зависят дальность пробега, скорость зарядки, вес и, главное, цена машины.
Если в традиционной электроэнергетике принципиальную роль играет турбина, то для развития все более популярных возобновляемых источников энергии (ВИЭ) крайне важны накопители энергии: без них не решить главную проблему ветряных и солнечных электростанций — зависимость от переменчивости погоды.
Илон Маск: новое поколение аккумуляторов и Tesla за 25 000 долларов
Так что батареи и аккумуляторы — это сейчас одно из магистральных направлений технологического развития на планете.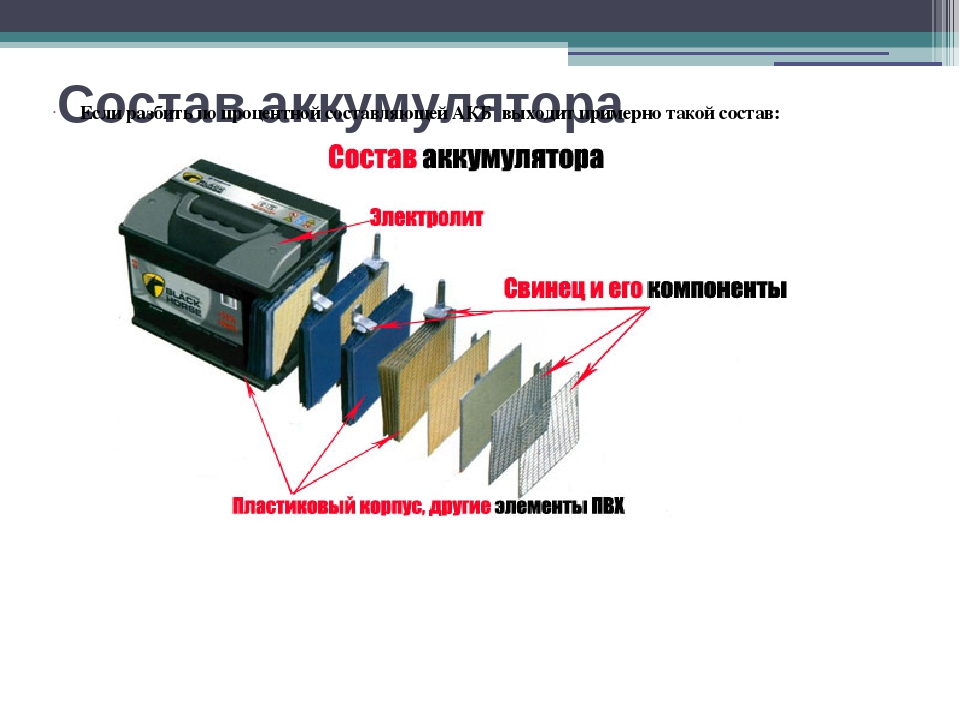 Весьма симптоматично, что американский предприниматель Илон Маск решил устроить 22 сентября специальную онлайн-презентацию под названием Tesla Battery Day, а Европейское патентное ведомство (EPO) и Международное энергетическое агентство (IEA) провели совместное исследование «Инновации в области батарей и накопителей электроэнергии». Его результаты опубликовали в тот же день.
Весьма симптоматично, что американский предприниматель Илон Маск решил устроить 22 сентября специальную онлайн-презентацию под названием Tesla Battery Day, а Европейское патентное ведомство (EPO) и Международное энергетическое агентство (IEA) провели совместное исследование «Инновации в области батарей и накопителей электроэнергии». Его результаты опубликовали в тот же день.
Электромобили Tesla на территории завода комапнии в Фримонте ждут отправки покупателям
Для главы компании Tesla аккумуляторные батареи — это ключ к массовому рынку. «У нас нет доступного автомобиля, но он у нас будет. Однако для этого мы должны снизить стоимость батарей», — заявил Илон Маск в ходе презентации, за которой в интернете следили 270 000 зрителей. Он обещал примерно через три года наладить серийное производство нового поколения аккумуляторов, которые будут существенно мощнее и долговечнее нынешних, но обойдутся в два раза дешевле.
И тогда, заверил Илон Маск, «мы сможем выпускать очень убедительный электромобиль по цене 25 тысяч долларов» (это примерно 21 000 евро). Глава Tesla объявил, что на первом этапе выпускать аккумуляторы нового поколения будут вблизи головного завода компании в калифорнийском Фримонте, для чего потребуется специальная монтажная линия. Одновременно предприниматель сообщил, что на гигафабрике Tesla в Неваде будет налажена утилизация отслуживших аккумуляторных батарей.
Глава Tesla объявил, что на первом этапе выпускать аккумуляторы нового поколения будут вблизи головного завода компании в калифорнийском Фримонте, для чего потребуется специальная монтажная линия. Одновременно предприниматель сообщил, что на гигафабрике Tesla в Неваде будет налажена утилизация отслуживших аккумуляторных батарей.
Кобальт от «Норникеля» может и не понадобиться
Для России особенно важно то, что батареи нового поколения планируется выпускать практически без использования редкого, а потому весьма дорогого металла кобальта. Его единственным российским производителем и экспортером является компания «Норникель» в Норильске.
Кобальтовые слитки на заводе «Норникель». Главные производители этого металла — ДР Конго и Китай
После Battery Day курс акций Tesla, стремительно взлетевший в этом году, что превратило американского производителя электромобилей в самого дорогостоящего автостроителя мира, упал. Биржевых инвесторов и спекулянтов разочаровало то, что Илон Маск говорил о среднесрочной перспективе в три года, а они, похоже, рассчитывали на анонс немедленных прорывов.
Одновременно несколько снизились котировки акций поставщиков батарей для Tesla — японской корпорации Panasonic и южнокорейской LG Chem, входящей в группу LG. Но это тоже не более чем сиюминутное недовольство биржевых игроков: средне- и долгосрочные перспективы этих компаний представляются весьма многообещающими. Об этом свидетельствует совместное исследование Европейского патентного ведомства и Международного энергетического агентства.
Аккумуляторы для электромобилей подешевели почти на 90%
Эксперты двух организаций проанализировали зарегистрированные с 2000 по 2018 годы патенты на изобретения и разработки в сфере аккумуляторных батарей и накопителей энергии, и на основании этого весьма объективного критерия сделали целый ряд выводов.
До 2011 года разработчики сосредотачивались на совершенствовании аккумуляторов для смартфонов
Первый и главный из них: «В последние десять лет патентирование в сфере хранения электроэнергии росло существенно быстрее патентирования в других сферах». Иными словами, именно на этом направлении сосредоточены сейчас особенно крупные материальные и интеллектуальные ресурсы, именно здесь накапливаются многочисленные инновации.
Иными словами, именно на этом направлении сосредоточены сейчас особенно крупные материальные и интеллектуальные ресурсы, именно здесь накапливаются многочисленные инновации.
Авторы исследования обнаружили, что число патентов, связанных с аккумуляторными батареями для электромобилей, еще в 2011 году превысило число патентов из области батарей для мобильной бытовой электроники (прежде всего смартфонов), и с тех пор неуклонно растет. Они также подсчитали, что особое внимание изобретателей к литий-ионным технологиям привело к тому, что с 2010 года аккумуляторы для электромобилей подешевели почти на 90%, а аккумуляторы для стационарных установок в электроэнергетике — примерно на две трети.
Япония и Южная Корея — лидеры в области батарейных технологий
Второй ключевой вывод исследования: «Япония и Республика Корея являются лидерами в глобальном соревновании в области батарейных технологий, что заставляет другие страны пытаться добиться конкурентных преимуществ в определенных нишах вдоль цепочки создания дополнительной стоимости при производстве батарей». Если говорить более просто: догнать ушедшие в этой сфере далеко вперед две азиатские страны уже настолько трудно, что остальным приходится довольствоваться узкой специализацией в отдельных сегментах.
Если говорить более просто: догнать ушедшие в этой сфере далеко вперед две азиатские страны уже настолько трудно, что остальным приходится довольствоваться узкой специализацией в отдельных сегментах.
Аккумуляторные батареи для электромобилей — это сложная высокотехнологичная продукция
Так, девять из десяти крупнейших обладателей патентов — компании из Азии: семь японских во главе с Panasonic и Toyota, а также южнокорейские Samsung и LG Electronics. Единственный представитель других континентов в Топ-10 — немецкий концерн Bosch, занявший пятое место.
В Топ-25 ближе к концу вошли также немецкие Daimler, BASF и Volkswagen. Всего же в этом списке шесть представителей Европы: это еще ирландская многопрофильная компания Johnson Controls и французский научно-исследовательский институт атомной и альтернативной энергетики CEA. Америка представлена автостроителями General Motors и Ford.
Разные типы аккумуляторов: NMC, NCA и LFP
Вклад Китая в глобальное развитие батарейных технологий, отмечается в исследовании, к 2018 году практически сравнялся с американским и приблизился к европейскому. Явная специфика Европы и США — значительно число патентов регистрируют малые и средние предприятия, а также вузы и государственные научно-исследовательские институты. В Азии подавляющее большинство изобретений приходится на крупные концерны.
Явная специфика Европы и США — значительно число патентов регистрируют малые и средние предприятия, а также вузы и государственные научно-исследовательские институты. В Азии подавляющее большинство изобретений приходится на крупные концерны.
Третий вывод исследования касается перспективных направлений инновационной деятельности. В минувшем десятилетии стремительно нарастало число патентов, связанных с литий-никель-марганец-кобальт-оксидными аккумуляторами (NMC). Теперь многообещающей альтернативой, полагают авторы исследования, становятся литий-никель-кобальт-алюминий-оксидные аккумуляторы (NCA), которые, к примеру, производит Panasonic и использует Tesla.
BYD — крупнейший китайский производитель электрических легковых машин и автобусов
Однако стремление снизить долю кобальта или вовсе от него отказаться приведет к тому, что будет расти роль литий-железо-фосфатных аккумуляторов (LFP), на которые тоже делает ставку Tesla, а также, к примеру, китайский автостроитель BYD, указывается в исследовании. Если в 2010 году практически вообще не было патентов, связанных с данной технологией, то в последние годы их число стало заметно нарастать.
Если в 2010 году практически вообще не было патентов, связанных с данной технологией, то в последние годы их число стало заметно нарастать.
Поэтому можно предположить, что ее разработчикам просто еще нужно пару лет. Может быть, как раз те три года, о которых Илон Маск говорил на Tesla Battery Day.
Смотрите также:
Технологии хранения энергии из возобновляемых источников
Электростанция из аккумуляторов
Как хранить в промышленных масштабах излишки электроэнергии, выработанной ветрогенераторами и солнечными панелями? Соединить как можно больше аккумуляторов! В Германии эту технологию с 2014 года отрабатывают в институте общества Фраунгофера в Магдебурге (фото). По соседству, в Шверине, тогда же заработала крупнейшая в Европе коммерческая аккумуляторная электростанция фирмы WEMAG мощностью 10 МВт.
Технологии хранения энергии из возобновляемых источников
Большие батареи на маленьком острове
Крупнейшие аккумуляторные электростанции действуют в США и странах Азии.
 А на карибском острове Синт-Эстатиус (Нидерландские Антилы) с помощью этой технологии резко снизили завоз топлива для дизельных электрогенераторов. Днем местных жителей, их около 4 тысяч, электричеством с 2016 года снабжает солнечная электростанция, а вечером и ночью — ее аккумуляторы, установленные фирмой из ФРГ.
А на карибском острове Синт-Эстатиус (Нидерландские Антилы) с помощью этой технологии резко снизили завоз топлива для дизельных электрогенераторов. Днем местных жителей, их около 4 тысяч, электричеством с 2016 года снабжает солнечная электростанция, а вечером и ночью — ее аккумуляторы, установленные фирмой из ФРГ.Технологии хранения энергии из возобновляемых источников
Главное — хорошие насосы
Гидроаккумулирующие электростанции (ГАЭС) — старейшая и хорошо отработанная технология хранения электроэнергии. Когда она в избытке, электронасосы перекачивают воду из нижнего водоема в верхний. Когда она нужна, вода сбрасывается вниз и приводит в действие гидрогенератор. Однако далеко не везде можно найти подходящий водоем и нужный перепад высот. В Хердеке в Рурской области условия подходящие.
Технологии хранения энергии из возобновляемых источников
Место хранения — норвежские фьорды
Оптимальные природные условия для ГАЭС — в норвежских фьордах.
 Поэтому по такому кабелю с 2020 года подводная высоковольтная линия электропередачи NordLink длиной в 623 километра и мощностью в 1400 МВт будет перебрасывать излишки электроэнергии из ветропарков Северной Германии, где совершенно плоский рельеф, на скалистое побережье Норвегии. И там они будут храниться до востребования.
Поэтому по такому кабелю с 2020 года подводная высоковольтная линия электропередачи NordLink длиной в 623 километра и мощностью в 1400 МВт будет перебрасывать излишки электроэнергии из ветропарков Северной Германии, где совершенно плоский рельеф, на скалистое побережье Норвегии. И там они будут храниться до востребования.Технологии хранения энергии из возобновляемых источников
Электроэнергия превращается в газ
Избытки электроэнергии можно хранить в виде газа. Методом электролиза из обычной воды выделяется водород, который с помощью СО2 превращается в метан. Его закачивают в газохранилища или на месте используют для заправки автомобилей. Идея технологии Power-to-Gas родилась в 2008 году в ФРГ, сейчас здесь около 30 опытно-промышленных установок. На снимке — пилотный проект в Рапперсвиле (Швейцария).
Технологии хранения энергии из возобновляемых источников
Водород в сжиженном виде
Идея Power-to-Gas дала толчок разработкам в разных направлениях.
 Зачем, к примеру, превращать в метан полученный благодаря электролизу водород? Он и сам по себе отличное топливо! Но как транспортировать этот быстро воспламеняющийся газ? Ученые университета Эрлангена-Нюрнберга и фирма Hydrogenious Technologies разработали технологию его безопасной перевозки в цистернах с органической жидкостью.
Зачем, к примеру, превращать в метан полученный благодаря электролизу водород? Он и сам по себе отличное топливо! Но как транспортировать этот быстро воспламеняющийся газ? Ученые университета Эрлангена-Нюрнберга и фирма Hydrogenious Technologies разработали технологию его безопасной перевозки в цистернах с органической жидкостью.Технологии хранения энергии из возобновляемых источников
В чем тут соль?
Соль тут в тех круглых резервуарах, которые установлены посреди солнечной электростанции на краю Сахары близ города Уарзазат в Марокко. Хранящаяся в них расплавленная соль выступает в роли аккумуляторной системы. Днем ее нагревают, а ночью используют накопленное тепло для производства водяного пара, подаваемого в турбину для производства электричества.
Технологии хранения энергии из возобновляемых источников
Каверна в роли подземной батарейки
На северо-западе Германии много каверн — пещер в соляных пластах.
 Одну из них энергетическая компания EWE и ученые университета Йены превратили в полигон для испытания технологии хранения электроэнергии в соляном растворе, обогащенном особыми полимерами, которые значительно повышают эффективность химических процессов. По сути дела, речь идет о попытке создать гигантскую подземную батарейку.
Одну из них энергетическая компания EWE и ученые университета Йены превратили в полигон для испытания технологии хранения электроэнергии в соляном растворе, обогащенном особыми полимерами, которые значительно повышают эффективность химических процессов. По сути дела, речь идет о попытке создать гигантскую подземную батарейку.Технологии хранения энергии из возобновляемых источников
Крупнейший «кипятильник» Европы
Человечество давно уже использует тепло для производства электроэнергии. Возобновляемая энергетика поставила задачу, наоборот, превращать электричество, в том числе и избыточное, в тепло (Power-to-Heat). Строительство в Берлине крупнейшего «кипятильника» Европы мощностью 120 МВт для отопления 30 тысяч домашних хозяйств компания Vattenfall намерена завершить к концу 2019 года.
Технологии хранения энергии из возобновляемых источников
Накопители энергии на четырех колесах
Когда по дорогам мира будут бегать миллионы электромобилей с мощными аккумуляторными батареями, они превратятся в еще один крупный накопитель энергии из возобновляемых источников.
 Этому поспособствуют умные сети энергоснабжения (Smart grid): они будут стимулировать подзарядку по низким ценам в моменты избытка электричества. (На фото — заправка для электромобилей в Китае).
Этому поспособствуют умные сети энергоснабжения (Smart grid): они будут стимулировать подзарядку по низким ценам в моменты избытка электричества. (На фото — заправка для электромобилей в Китае).Автор: Андрей Гурков
ENERGON
Вакансия
Менеджер отдела продаж (специализированная дистрибуция), Хабаровск
Менеджер по продажам, Москва
Секретарь, Москва
Экономист
Pre-sale менеджер направления тяговые литиевые аккумуляторы, Москва
Бухгалтер по валютному контролю
Аналитик товарного запаса
Специалист отдела управленческого учета
Бухгалтер (участок реализация)
Менеджер по закупкам, Москва
Руководитель производственного склада, Балашиха
Грузчик / Сотрудник склада, Дзержинский
Грузчик / Комплектовщик / Сотрудник склада
Технико-коммерческий инженер направления ВИЭ
Сервисный инженер, Балашиха
Старший технический контролер, Дзержинский
Технический тренер, Москва
Поле заполнено неверно
Литий-ионные аккумуляторные батареи – Особенности интерфейса и менеджмента ЛИАБ – ПАО Сатурн
Обеспечение надежности и безопасности ЛИАБ
Защита от перезаряда и переразряда внешне обеспечивается электронным устройством, абсолютно надежным в управлении.
Внутреннее КЗ предотвращается конструктивно: обертыванием (пакетированием) электродов сепараторами и тем, что при этом между электродами находится трехслойный сепаратор, который при достижении критической температуры теряет пористость (заплавляется) и останавливает электрохимический процесс.
Исключение из цепи отказавших или аномально деградировавших аккумуляторов выполняется применением байпасных переключателей.
Основные требования, которые предъявляются к байпасному переключателю для литий-ионной аккумуляторной батареи для космического аппарата, это надежность, минимальные энергетические потери, минимальная масса, сохранение неразрывности цепи ЛИАБ при переключении и механическая и радиационная стойкость.
Схема подключения байпасного переключателя и временная диаграмма работы переключателя обеспечивает сохранение неразрывности при переключении цепи соединения аккумуляторов в аккумуляторной батарее.
Таким образом, отказ любого элемента не приводит к отказу ЛИАБ. Надежность ЛИАБ обеспечивается также всеобъемлющей квалификацией (в том числе ресурсными испытаниями) и тщательным контролем при изготовлении.
Тяговые литий-ионные батареи Tesla, что внутри?
Тяговые литий-ионные батареи Tesla, что внутри?
Тесла Моторс является создателем поистине революционных экомобилей — электромобилей, которые не только выпускаются серийно, но и обладают уникальными показателями, позволяющими их использование буквально ежедневно. Сегодня мы заглянем внутрь тяговой аккумуляторной батареи электромобиля Tesla Model S, узнаем, как она устроена и раскроем магию успеха этой аккумуляторной батареи.
Сегодня мы заглянем внутрь тяговой аккумуляторной батареи электромобиля Tesla Model S, узнаем, как она устроена и раскроем магию успеха этой аккумуляторной батареи.
Поставка батарей клиентам осуществляется в таких вот ящиках из ОСБ.
Самая крупная и дорогая запчасть для Tesla Model S – блок тяговой аккумуляторной батареи.
Блок тяговой аккумуляторной батареи находится в днище автомобиля (по сути это пол электромобиля — машины), за счёт чего Tesla Model S имеет очень низкий центр тяжести и великолепную управляемость. Батарея крепится к силовой части кузова при помощи мощных кронштейнов (см. фото ниже) или выполняет роль силовой – несущей части кузова авто.
По данным североамериканского Агентства по защите окружающей US Environmental Protection Agency (EPA) одного заряда тяговой литий-ионной аккумуляторной батареи Tesla с номинальным напряжением 400В DC, ёмкостью 85 кВт·ч хватает на 265 миль (426 км) пробега, что позволяет преодолевать наибольшую дистанцию среди подобных электромобилей. При этом от 0 до 100 км/ч подобная машина разгоняется всего за 4,4 секунды.
При этом от 0 до 100 км/ч подобная машина разгоняется всего за 4,4 секунды.
Секрет успеха Tesla Model S – это высокоэффективные цилиндрические литий-ионные батареи высокой энергоёмкости, поставщик базовых элементов известная японская фирма Panasonic. Вокруг этих батарей ходит немало слухов.
Один из них – это не влезай, убьёт!
Один из владельцев и энтузиастов Tesla Model S из США решил полностью разобрать использованную батарею для Tesla Model S энергоёмкостью 85 кВт·ч, чтобы детально изучить её конструкцию. Кстати, её стоимость, как запчасти, в США составляет 12 000 USD.
Сверху блок батареи размещено тепло и звука изоляционное покрытие, которое закрывается толстой полиэтиленовой плёнкой. Снимаем это покрытие, в виде ковра и готовимся к разборке. Для работы с батареей необходимо иметь изолированный инструмент и пользоваться резиновой обувью, и резиновыми защитными перчатками.
Батарея Tesla. Разбираем!
Тяговая аккумуляторная батарея Tesla (блок тяговой аккумуляторной батареи) состоит 16 батарейных модулей, каждый номинальным напряжением 25В (исполнение батарейного блока — IP56). Шестнадцать батарейных модулей соединены последовательно в батарею с номинальным напряжением 400В. Каждый батарейный модуль состоит из 444 элементов (аккумуляторов) 18650 Panasonic (вес одного аккумулятора 46 г), которые соединены по схеме 6s74p (6 элементов последовательно и 74 таких групп параллельно). Всего в тяговой аккумуляторной батарее Tesla – 7104 таких элементов (аккумуляторов). Батарея защищена от окружающей среды посредством использования металлического корпуса с алюминиевой крышкой. На внутренней стороне общей алюминиевой крышки имеются пластиковые накладки, в виде плёнки.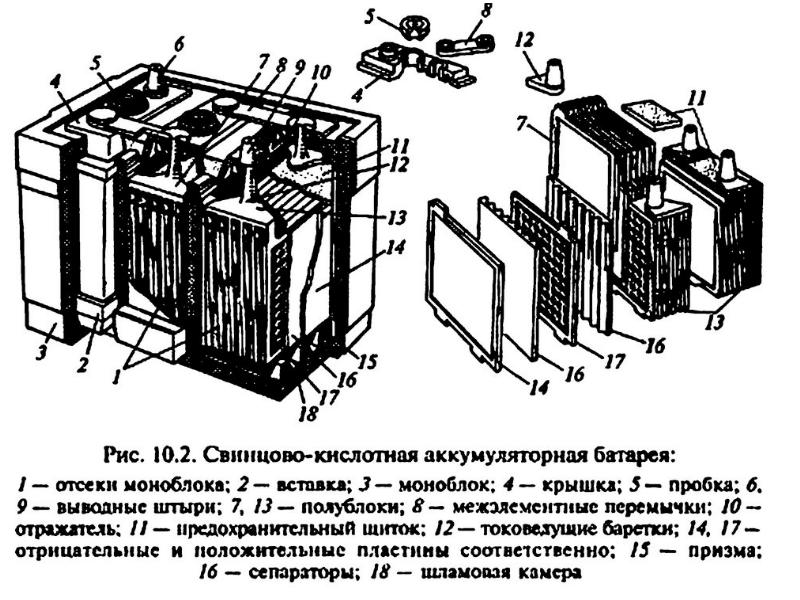 Общая алюминиевая крышка крепится винтами с металлическими, и резиновыми прокладками, которые герметизируются, дополнительно силиконовым герметиком. Блок тяговой аккумуляторной батареи разделен на 14 отсеков, в каждом отсеке размещен батарейный модуль. В каждом отсеке сверху и снизу батарейных модулей размещены листы прессованной слюды. Листы слюды обеспечивают хорошую изоляцию батареи электрическую, и тепловую от корпуса электромобиля. Отдельно спереди батареи под своей крышкой размещены два таких же батарейных модуля. В каждом из 16 батарейных модулей имеется встроенный блок BMU, который соединён с общей системой BMS, которая управляет работой, следит за параметрами, а так же обеспечивает защиту всей аккумуляторной батареи. Общие выводные клеммы (терминал) находится в задней части блока тяговой батареи.
Общая алюминиевая крышка крепится винтами с металлическими, и резиновыми прокладками, которые герметизируются, дополнительно силиконовым герметиком. Блок тяговой аккумуляторной батареи разделен на 14 отсеков, в каждом отсеке размещен батарейный модуль. В каждом отсеке сверху и снизу батарейных модулей размещены листы прессованной слюды. Листы слюды обеспечивают хорошую изоляцию батареи электрическую, и тепловую от корпуса электромобиля. Отдельно спереди батареи под своей крышкой размещены два таких же батарейных модуля. В каждом из 16 батарейных модулей имеется встроенный блок BMU, который соединён с общей системой BMS, которая управляет работой, следит за параметрами, а так же обеспечивает защиту всей аккумуляторной батареи. Общие выводные клеммы (терминал) находится в задней части блока тяговой батареи.
До того, как полностью её разобрать, было замерено электрическое напряжение (оно составили около 313,8В), что говорит о том, что батарея разряжена, но находится в рабочем состоянии.
Батарейные модули отличается высокой плотностью элементов (аккумуляторов) 18650 Panasonic, которые там размещены и точностью подгонки деталей. Весь процесс сборки на заводе Tesla проходит в полностью стерильном помещении, с использованием роботов, выдерживается даже определенная температура и влажность.
Каждый батарейный модуль состоит из 444 элементов (аккумуляторов), которые по виду крайне схожих с простыми пальчиковыми батарейками — это литий-ионные цилиндрические аккумуляторы 18650, производства компании Panasonic. Энергоемкость каждого батарейного модуля из таких элементов составляет 5,3 кВт·ч.
В аккумуляторах 18650 Panasonic положительный электрод — графит, а отрицательный электрод — никель, кобальт и оксид алюминия.
Тяговая аккумуляторная батарея Tesla весит 540 кг, а её размеры равны 210 см в длину, 150 см в ширину, и 15 см в толщину. Количество энергии (5,3 кВт·ч), вырабатываемой всего одним блоком (из 16 батарейных модулей), равно количеству, производимому сотней аккумуляторов от 100 портативных компьютеров.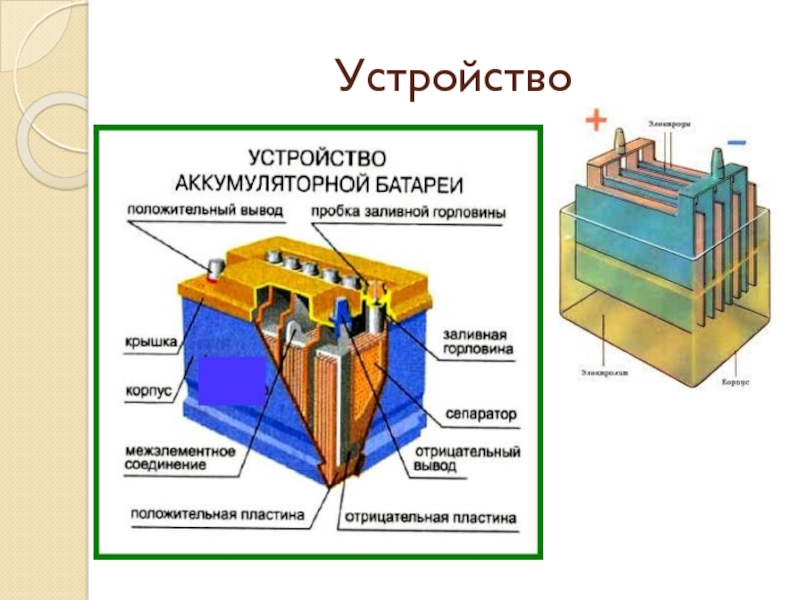 К минусу каждого элемента (аккумулятора) в качестве соединителя припаяна проволочка (внешний токовый ограничитель), который при превышении тока (или при коротком замыкании) сгорает и защищает цепь, при этом не работает только группа (из 6 аккумуляторов), в которой был этот элемент, все остальные аккумуляторы продолжают работать.
К минусу каждого элемента (аккумулятора) в качестве соединителя припаяна проволочка (внешний токовый ограничитель), который при превышении тока (или при коротком замыкании) сгорает и защищает цепь, при этом не работает только группа (из 6 аккумуляторов), в которой был этот элемент, все остальные аккумуляторы продолжают работать.
Тяговая аккумуляторная батарея Tesla охлаждается и подогревается с помощью жидкостной системы на основе антифриза.
При сборке своих батарей Тесла применяет элементы (аккумуляторы), произведенные компанией Panasonic в различных странах, таких, как Индия, КНР и Мексика. Финальная доработка и размещение в корпус батарейного отсека, производятся в Соединенных Штатах. Компания Tesla предоставляет гарантийной обслуживание своей продукции (в том числе и аккумуляторной батареи) на срок до 8 лет.
На фото (сверху) элементы — аккумуляторы 18650 Panasonic (завальцовка у элементов со стороны плюса «+»).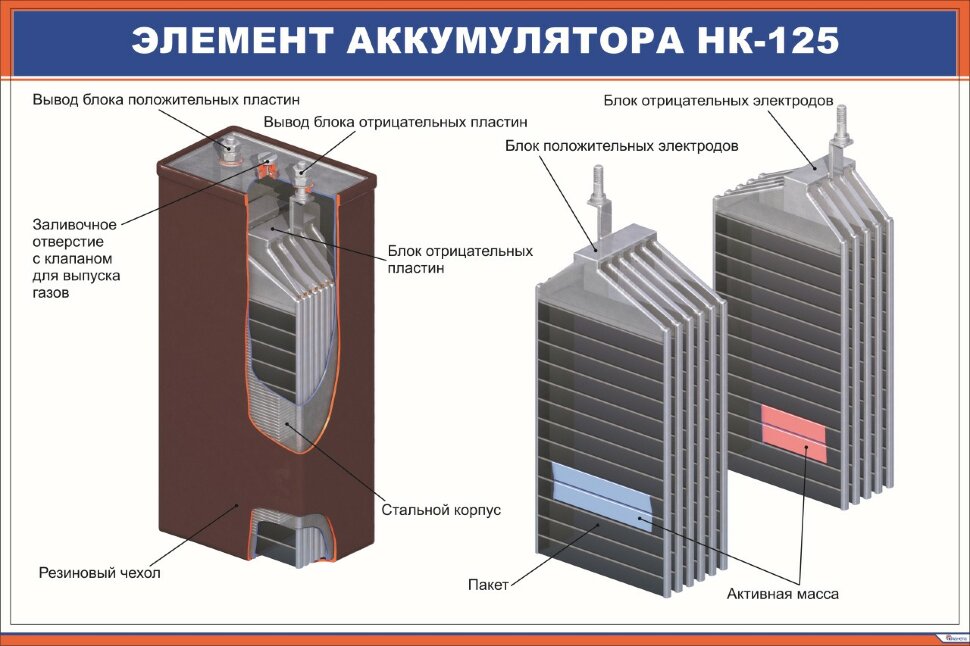
Таким образом, мы узнали, из чего состоит тяговая аккумуляторная батарея Tesla Model S.
Благодарим за внимание!
Типы аккумуляторных батарей для систем автономного электроснабжения
В этой заметке содержатся общие советы по выбору аккумуляторов для систем с возобновляемыми источниками энергии. В заметке затронуты 3 основные технологии: литий-ионные, никель-металл-гидридные и свинцово-кислотные (AGM, или Gel).
Мы постараемся избегать формул и научных обоснований, просто приведем причины, по которым нужно выбирать тот или иной тип аккумуляторов в зависимости от конкретного применения системы электроснабжения.
Основные типы аккумуляторов
Существует 3 лидирующих технологии аккумуляторных батарей: свинцово-кислотные, щелочные и литий-ионные. Каждая из этих технологий имеет свои уникальные достоинства и недостатки, которые определяют их применение в различных случаях. Смотрите по ссылкам для более подробной информации о каждом из типов аккумуляторов:
Свинцово-кислотные аккумуляторы
Наиболее распространенным типом АБ являются свинцово-кислотные, как с жидким электролитом, так и герметизированные (в последнее время становятся все более популярными вследствие снижения цены).
Специальные батареи с намазными пластинами для использования в системах автономного электроснабжения часто собираются из отдельных аккумуляторов с напряжением 2 вольта, соединенных вместе. АБ меньшей емкости с напряжением 6 и 12 вольт также используются, но реже. Такие батареи выпускаются в основном в Европе и в США. Они сравнительно дорогие. В последнее время на российском рынке появились такие аккумуляторы китайского производства. При практически таких же характеристиках, китайские аккумуляторы значительно (в полтора-два раза) дешевле.
Тяговые аккумуляторы, как с жидким электролитом, так и герметизированные, предназначены для цикличных режимов работы. Аналогичными параметрами обладают и модификации deep cycle (глубокого разряда). Они более подходят для автономных систем энергоснабжения. Они дороже обычных герметизированных АБ, но и срок службы у них больше.
Герметичные свинцово-кислотные аккумуляторы имеют аналогичный принцип действия, как и обычные автомобильные стартерные аккумуляторы. Это наиболее зрелая технология, и по некоторым уникальным параметрам ей до сих пор не найдена замена. Эти аккумуляторы нельзя выбрасывать просто на свалку, так как они содержат высокотоксичные свинец и серную кислоту. Однако они очень легко утилизируются и свинец может быть использован повторно. Эти аккумуляторы заряжаются гораздо медленнее, чем другие аккумуляторы (примерна в 5 раз медленнее), но зато в состоянии обеспечивать гораздо больше мощности для питания мощных потребителей.
Это наиболее зрелая технология, и по некоторым уникальным параметрам ей до сих пор не найдена замена. Эти аккумуляторы нельзя выбрасывать просто на свалку, так как они содержат высокотоксичные свинец и серную кислоту. Однако они очень легко утилизируются и свинец может быть использован повторно. Эти аккумуляторы заряжаются гораздо медленнее, чем другие аккумуляторы (примерна в 5 раз медленнее), но зато в состоянии обеспечивать гораздо больше мощности для питания мощных потребителей.
Самым большим недостатком свинцово-кислотных аккумуляторов является их вес. Из-за этого они имеют наихудшие показатели по удельной плотности энергии. Однако, широкое распространение элементов, используемых в этих аккумуляторах и простота их производства обуславливают не только их широкое применение, но и намного меньшую цену.
Подробно различные типы свинцово-кислотных АБ рассмотрены в статье «Типы свинцово-кислотных аккумуляторов«.
Щелочные аккумуляторы
Кислотный аккумулятор не переносит глубокой разрядки, но не прочь подзаряжаться порциями при каждом удобном случае.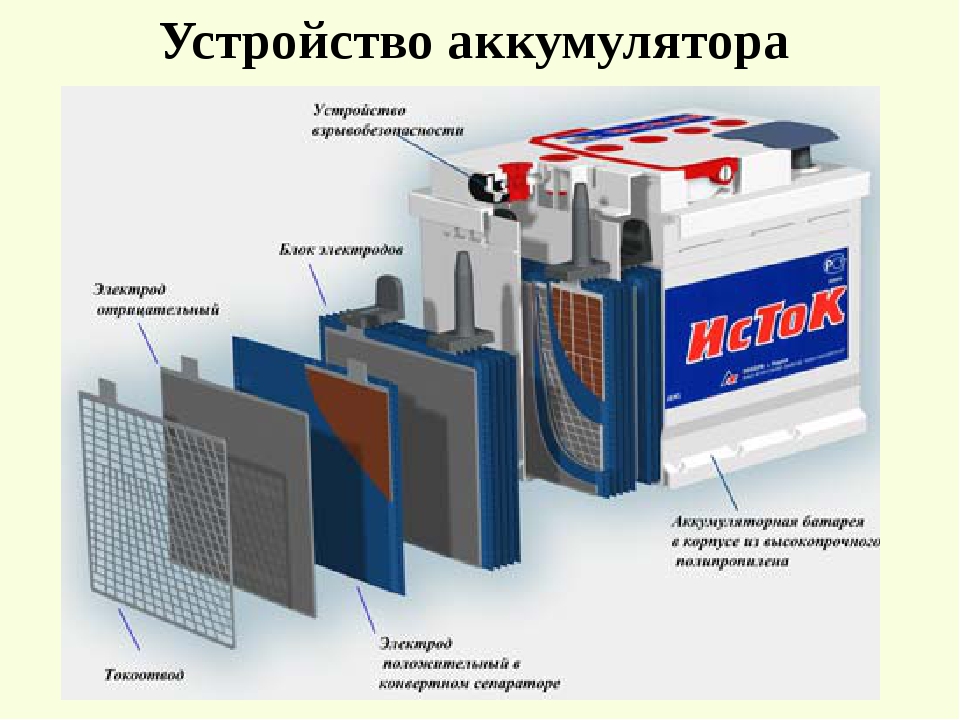 Щелочной наоборот, не любит отдавать больших токов, зато токи в количестве примерно 1/10 емкости готов отдавать долго и до изнеможения. То есть полный разряд он не только допускает, но и всячески приветствует (поскольку, если зарядить не разряженный полностью щелочной аккумулятор, он не наберет полной емкости — действует так называемый «эффект памяти», наиболее выраженный у никель-кадмиевых аккумуляторов). Короче, заряжать/разряжать щелочной аккумулятор порциями нельзя — только "от и до". Зато при правильной эксплуатации (помимо зарядки/разрядки она подразумевает промывку банок и замену электролита раз в сезон ) щелочники служат до 20 лет (точнее, 1000-1500 полных циклов). Также, щелочные аккумуляторы плохо заряжаются малыми токами. То есть, ток через них течет, а заряда нет.
Щелочной наоборот, не любит отдавать больших токов, зато токи в количестве примерно 1/10 емкости готов отдавать долго и до изнеможения. То есть полный разряд он не только допускает, но и всячески приветствует (поскольку, если зарядить не разряженный полностью щелочной аккумулятор, он не наберет полной емкости — действует так называемый «эффект памяти», наиболее выраженный у никель-кадмиевых аккумуляторов). Короче, заряжать/разряжать щелочной аккумулятор порциями нельзя — только "от и до". Зато при правильной эксплуатации (помимо зарядки/разрядки она подразумевает промывку банок и замену электролита раз в сезон ) щелочники служат до 20 лет (точнее, 1000-1500 полных циклов). Также, щелочные аккумуляторы плохо заряжаются малыми токами. То есть, ток через них течет, а заряда нет.
Этим объясняется тот факт, что щелочные аккумуляторы не нашли широкого применения в системах автономного электроснабжения с возобновляемыми источниками энергии. Никель-кадмиевые и никель-металгидридные герметичные батареи могут использоваться в некоторых случаях. Хотя они намного дороже кислотных, зато имеют очень большой срок службы и имеют более стабильное напряжение в процессе разряда. Применяются обычно в переносных или мобильных источниках питания, т.к. позволяют запасать большее количество энергии на кг веса.
Хотя они намного дороже кислотных, зато имеют очень большой срок службы и имеют более стабильное напряжение в процессе разряда. Применяются обычно в переносных или мобильных источниках питания, т.к. позволяют запасать большее количество энергии на кг веса.
NiMh аккумуляторы появились на массовом рынке в 1980-х годах как более экологически чистая альтернатива никель-кадмиевым аккумуляторам. NiCd батареи используют высокотоксичный элемент кадмий в своем составе, и так как массовый бытовой потребитель не особо задумывается об утилизации отработанных аккумуляторов, это представляло большую проблему для окружающей среды. К недостаткам NiMh батарей относится сравнительно высокий саморазряд, который приводит к потере примерно 30% энергии в течение 1 месяца. Они также заряжаются в 2 раза дольше, чем литиевые или никель-кадмиевые аккумуляторы.
Хотя электрические параметры NiMh батарей не такие хорошие, как у NiCd, никель-металлгидридные батареи более стабильны и не так страдают от «эффекта памяти» никель-кадмиевых батарей. Их не нужно полностью разряжать перед зарядом, так как это требуют NiCd аккумуляторы, для предотвращения роста внутренних кристаллов, которые приводят к трещинам корпуса NiCd батареи. NiMh аккумуляторы формата «АА» соответствуют обычным алкалиновым батарейкам, и поэтому наиболее популярны при использовании в цифровых фотоаппаратах и камерах, портативных плеерах, радиоприемниках и фонариках.
Их не нужно полностью разряжать перед зарядом, так как это требуют NiCd аккумуляторы, для предотвращения роста внутренних кристаллов, которые приводят к трещинам корпуса NiCd батареи. NiMh аккумуляторы формата «АА» соответствуют обычным алкалиновым батарейкам, и поэтому наиболее популярны при использовании в цифровых фотоаппаратах и камерах, портативных плеерах, радиоприемниках и фонариках.
Никель-кадмиевые и никель-железные аккумуляторы с жидким электролитом дешевле герметичных, но содержат жидкий электролит, выделяют газы при заряде и требуют периодического обслуживания и специального вентилируемого помещения. По стоимости запасенной энергии в цикле заряд-разряд сопоставимы или даже дешевле герметичных свинцово-кислотных батарей.
Мы рекомендуем использовать никель-железные аккумуляторы (обычно их используют в качестве тяговых на электротранспорте, а также на железной дороге) только в одном случае — в составе автономной дизель-аккумуляторной системы, в которой топливный генератор является единственным источником энергии. Из нашего опыта знаем, что свинцово-кислотные АБ не долго держатся в таких системах — глубокие циклы и хронический недозаряд делают свое черное дело. В этих условиях работы можно смириться с такими недостатками щелочных АБ, как невозможность заряда малыми токами (можно от генератора выставить любой, и даже лучше если ток будет большой — быстрее зарядится), эффект памяти (циклы будут как раз глубокие) и низкий КПД заряда. Для генераторной системы эффект памяти не важен — АБ разряжаются как можно сильнее, чтобы запускать генератор как можно реже.
Из нашего опыта знаем, что свинцово-кислотные АБ не долго держатся в таких системах — глубокие циклы и хронический недозаряд делают свое черное дело. В этих условиях работы можно смириться с такими недостатками щелочных АБ, как невозможность заряда малыми токами (можно от генератора выставить любой, и даже лучше если ток будет большой — быстрее зарядится), эффект памяти (циклы будут как раз глубокие) и низкий КПД заряда. Для генераторной системы эффект памяти не важен — АБ разряжаются как можно сильнее, чтобы запускать генератор как можно реже.
По поводу КПД — если щелочные АБ можно заряжать большим током, то его низкий КПД с лихвой окупится более эффективным режимом работы генератора. Ведь для дозаряда свинцовых АБ требуется долго заряжать их малыми токами, т.е. практически на холостом ходу генератора. А у щелочных ограничения при заряде — это температура аккумуляторов, а также газовыделение.
практически на холостом ходу генератора. А у щелочных ограничения при заряде — это температура аккумуляторов, а также газовыделение.
Еще раз подчеркнем, что не для всякой резервной или автономной системы подходят щелочные аккумуляторы. Если есть солнечные батареи или ветроустановки, т.е. источники, которые выдают разные токи, в т.ч. и малые, щелочные аккумуляторы ставить смысла нет — энергия малых токов будет просто теряться без пользы.
Литий-ионные и литий-полимерные аккумуляторы
Это одна из наиболее новых технологий, которая развивается быстрее других. Существуют несколько вариаций химических процессов литий-ионных технологий, но их обсуждение здесь не затрагивается. Литий-ионные аккумуляторы широко применяются в малых электронных устройствах, таких как мобильные телефоны, гаджеты и аудиоплееры, электронные часы, карманные компьютеры и ноутбуки. Эти аккумуляторы очень хорошо снабжают малой мощностью в течение длительного времени. Они имеют очень высокую удельную плотность заряда, что значит они могут хранить значительное количество электрической энергии в малом объеме. Однако, такая концентрация энергии приводит в определенной уязвимости литий-ионных батарей.
Однако, такая концентрация энергии приводит в определенной уязвимости литий-ионных батарей.
Химия процесса литий-ионных аккумуляторов требует строгого соблюдения технологии изготовления, и загрязнения при производстве этих аккумуляторов часто приводят к ухудшению качества аккумуляторов. Многие возможно помнят отзыв тысяч ноутбуков Dell и Apple летом 2006 года, когда оказалось, что их аккумуляторы, произведенные Sony, содержат загрязнители, приводящие к их перегреву. Литиевые батареи не переносят перегрев, поэтому часто имеют встроенные электронные схемы, которые обеспечивают их безопасность за счет предотвращения перезаряда — заряд прекращается, если напряжение достигло предельного значения.
Литий-полимерные батареи, которые разработаны в последнее время, являются ‘сухой’ версией литий-ионных батарей. Они лучше себя ведут при высоких температурах (более 25C), а также позволяют изготавливать исключительно плоские батареи, вплоть до толщины кредитной карты. Вследствие особенностей технологии производства, эти батареи очень дороги, и редко их использование оправдано по сравнению с более обычными литий-ионными батареями.
Для систем электроснабжения лучше всего подходят литий-железо-фосфатные аккумуляторы. См. по ссылке подробную информацию по этому типу аккумуляторов. Купить такие аккумуляторы можно в нашем магазине.
В последнее время на российском рынке появились относительно недорогие литий-железо-фосфатные аккумуляторы производства завода Лиотех. Выпускаемые емкости — от 250 А*ч, поэтому их применение ограничено относительно мощными системами автономного или резервного электроснабжения. Также, есть неоднозначные отзывы об этих батареях.
Одни из новейших разработок — литий-титанатные аккумуляторы. Они имеют срок службы до 25000 тысяч циклов.
Как выбрать правильную батарею?
Итак, главный вопрос — какая батарея наиболее подходит для моего случая? Ответ довольно прост, а предопределяется природой каждой из вышеперечисленных технологий аккумуляторов.
Для маленьких, маломощных электронных устройств
Литиевые аккумуляторы применяются в карманных компьютерах, мобильных телефонах, и т. п. Они обеспечивают быстрый заряд, малый вес и компактные размеры, и не требуют обслуживания. Обычно вы скорее замените свое электронное устройство, чем литиевая батарея выработает своей ресурс.
п. Они обеспечивают быстрый заряд, малый вес и компактные размеры, и не требуют обслуживания. Обычно вы скорее замените свое электронное устройство, чем литиевая батарея выработает своей ресурс.
Автомобильные адаптеры существуют для большинства этих электронных устройств, и эти же адаптеры можно использовать с 12V солнечной батареей (обычно мощностью до 10 Вт).
Для цифровых фотоаппаратов и камер, радиоприемников и фонариков
Здесь применяются NiMh аккумуляторы как замена стандартных алкалиновых элементов типа ‘AA’ или ‘AAA’. Они питают достаточно хорошо вспышки фотоаппаратов, доступны повсеместно и есть очень много зарядных устройств хорошего качества в любом специализированном магазине.
основным недостатком NiMh аккумуляторов является их неспособность сохранять заряд в течение длительного времени. В 2008 году появились новые технологии NiMh батарей, которые преодолевают эти недостатки (например PowerEx Imedion).
Когда дело доходит до заряда АА батарей, появляются много возможностей. Но лучше купить хорошее зарядное устройство. Многие зарядные устройства, которые позволяют быстро заряжать аккумуляторы, приводят к их перегреву. Помните, что оптимальный ток заряда составляет 200-300 мА. Появившиеся в последнее время мощные зарядные устройства с током до 1 А не позволяют полностью заряжать ваши батареи и сокращают их срок службы.
Но лучше купить хорошее зарядное устройство. Многие зарядные устройства, которые позволяют быстро заряжать аккумуляторы, приводят к их перегреву. Помните, что оптимальный ток заряда составляет 200-300 мА. Появившиеся в последнее время мощные зарядные устройства с током до 1 А не позволяют полностью заряжать ваши батареи и сокращают их срок службы.
Для солнечных электростанций
Когда нужно сохранить энергию, выработанную солнечными батареями, королями по прежнему являются свинцово-кислотные аккумуляторы. Домашние фотоэлектрические системы используют специальные аккумуляторы глубокого разряда (похожие на аккумуляторы для гольф-каров). Они имеют низкую цену, широко доступны и способны сохранять энергию месяцами при очень малом саморазряде. когда вы инвестируете в солнечные батареи, очень важно не терять так дорого достающуюся электроэнергию. Работа свинцово-кислотных батарей показала в течение многих лет эксплуатации их стабильность и предсказуемость.
Маленькие переносные устройства с солнечными батареями используют маломощные литиевые аккумуляторы для того, чтобы обеспечить их малый вес и не повлиять отрицательно на их дизайн.
Почему не применяются щелочные и метал-гидридные аккумуляторы в солнечных электросистемах, предлагаемых компанией «Ваш Солнечный Дом»?
Химические процессы в литиевых и метал-гидридных аккумуляторах становятся нестабильными при больших размерах батарей. Сложность регулирования и схемы управления сильно возрастает при увеличении емкости литиевых аккумуляторов. Было бы конечно заманчиво иметь батарею намного более легкую, чем свинцово-кислотная, но, к сожалению, сейчас литиевые и металгидридные аккумуляторы наиболее подходят только для маломощных потребителей постоянного тока. Исключение составляют современные литий-железо-фосфатные аккумуляторы. При правильном подборе системы управления зарядом они могут быть заменой свинцово-кислотным аккумуляторам в системах автономного и резервного электроснабжения.
NiMh батареи трудно сделать большими, и максимальная емкость одного аккумулятора из тех, которые есть на рынке, составляет 4 А*ч. При неправильном заряде, NiMh аккумуляторы могут выделять водород . Это не проблема для пальчиковых батарей, но если аккумуляторная батарея довольно большая, то это нужно учитывать при эксплуатации. Также, если NiMh батарея выходит из строя, это происходит практически сразу. т.е. один день она работает хорошо, но на следующий день она может выдать не более 50% емкости — это не очень хорошо, если вы находитесь далеко от электрической розетки.
Это не проблема для пальчиковых батарей, но если аккумуляторная батарея довольно большая, то это нужно учитывать при эксплуатации. Также, если NiMh батарея выходит из строя, это происходит практически сразу. т.е. один день она работает хорошо, но на следующий день она может выдать не более 50% емкости — это не очень хорошо, если вы находитесь далеко от электрической розетки.
Литиевые батареи содержать специальные электронные схемы для обеспечения безопасной работы, и которые не позволяют их заряжать слишком быстро или перезаряжать, а также ограничивают разрядные токи. Большинство литиевых батарей не смогут выдать больше, чем их двойная номинальная емкость. Это означает, что самые большие батареи для ноутбука не могут обеспечить более 100Вт мощности. Попробуйте подключить инвертор к 12В литиевой батареи, и он даже не сможет распознать, что к нему подключена батарея. Почти все аккумуляторные батареи на литиевых аккумуляторах не поддерживают даже самые маленькие инверторы, если к ним подключена нагрузка. Также, как и NiMh аккумуляторы, литиевые выходят из строя неожиданно, когда приближается окончание их срока службы. Многие замечали, что их сотовые телефоны неожиданно начинают работать намного меньше, чем совсем недавно. Это также не добавляет уверенности в работе аккумуляторов, если вы уезжаете далеко от электрической розетки, от которой можно в любое время подзарядить аккумулятор.
Также, как и NiMh аккумуляторы, литиевые выходят из строя неожиданно, когда приближается окончание их срока службы. Многие замечали, что их сотовые телефоны неожиданно начинают работать намного меньше, чем совсем недавно. Это также не добавляет уверенности в работе аккумуляторов, если вы уезжаете далеко от электрической розетки, от которой можно в любое время подзарядить аккумулятор.
Поэтому, для использования в автономных системах электроснабжения остаются только «медленные» свинцово-кислотные аккумуляторы. Они имеют большой срок службы, просты в эксплуатации и предсказуемы в работе. Эти батареи работают как резервуары, которые хранят вашу солнечную энергию до тех пор, пока она не понадобится. Они также работают как буфер для тех моментов, когда ваша солнечная батарея не может полностью обеспечить нагрузку. Они могут быть подключены к оборудованию и заряжаться одновременно — в отличие от литиевых аккумуляторов. Даже 7 А*ч аккумулятор, такой как используется в комплекте для ноутбука, может питать ноутбуки, зарядные устройства для батарей, может заряжаться от солнечных батарей и весит не так уж много.
Почитайте разделы по солнечным батареям и по контроллерам заряда, чтобы иметь более ясное представление о том, как работает солнечная энергосистема, какие режимы заряда и разряда необходимы для обеспечения надежного обеспечения энергией вдали от сетей централизованного электроснабжения.
Выбор батарей: итоговые замечания
Литиевые батареи
- могут обеспечивать до 5000 зарядных циклов
- Наиболее длительный срок службы при разряде на 80%
- Могут заряжаться за 1-2 часа
- Могут работать при минусовых температурах, но заряжать нужно при плюсовых температурах
- Не могут заряжаться малыми токами
- Требуют обслуживания, выравнивания и специальной системы управления зарядом и разрядом
- Саморазряд на уровне примерно 10% в месяц
- Можно хранить в холодном месте при заряженности не менее 40% от полной
- Низкая токсичность, но желательно утилизировать после окончания срока службы
Никель-металгидридные батареи
- Могут обеспечить до 3000 зарядных циклов
- Заряд происходит за 2-4 часа
- Могут работать при минусовых температурах
- Не могут заряжаться малыми токами, низкая устойчивость к перезаряду
- Могут обеспечивать большие токи при мощности до 200Вт (для самых больших NiMh батарей)
- Требуют периодического обслуживания и выравнивания (каждые 3 месяца)
- Саморазряд на уровне примерно 30% в месяц
- Можно хранить в холодном месте при заряженности не менее 40% от полной
- Низкая токсичность, но желательно утилизировать после окончания срока службы
Герметичные свинцово-кислотные аккумуляторы
- Могут обеспечить до 3000 зарядных циклов
- Заряжаются за 8-16 часов
- Могут работать при минусовых температурах
- Могут заряжаться малыми токами
- Не требуют обслуживания, но желательно следить за уровнем заряженности и периодически проводить тренировочные циклы
- Могут обеспечить высокие разрядные токи при больших мощностях
- Желательно не разряжать более, чем на 50%
- Саморазряд — около 3% в месяц
- Хранить при комнатной температуре и полностью заряженными
- Содержат токсичные материалы и должны быть утилизированы после окончания срока службы
Подробно о видах и применении свинцово-кислотных аккумуляторов в статье Типы свинцово-кислотных аккумуляторов
Эта статья прочитана 29823 раз(а)!
Продолжить чтение
69
Эксплуатационный ресурс герметичных свинцовых аккумуляторных батарей в составе электронного оборудования Мерунко Александр Анатольевич Технический директор ООО «Диск», г.
 Томск В настоящее время на потребительском рынке вторичных источников тока лидирующее положения (вследствие относительно низкой стоимости) занимают герметичные свинцовые аккумуляторные батареи. Их применяют…
Томск В настоящее время на потребительском рынке вторичных источников тока лидирующее положения (вследствие относительно низкой стоимости) занимают герметичные свинцовые аккумуляторные батареи. Их применяют…68
Какая емкость аккумуляторной батареи нужна в системе электроснабжения? При расчете системы автономного или резервного электроснабжения очень важно правильно выбрать емкость аккумуляторной батареи. Специалисты компании «Ваш Солнечный Дом» помогут Вам правильно рассчитать необходимую емкость АБ для вашей энергосистемы. Для предварительного расчета…
68
Классификация аккумуляторов для мобильных устройств Источник Идеального аккумулятора энергии до сих пор не существует — в разных областях для каждого типа мобильных устройств и конкретных решений сложилась определенная специфика применения источников питания, а также технологические предпочтения. Однако если вы хорошо…
65
Аккумуляторы для систем электроснабжения. Руководство покупателя В интернете есть много разрозненной информации по разным типам аккумуляторов, их возможностям, характеристикам, областям применения, достоинствам и недостаткам.
 При этом во многих случаях информация эта однобокая — связано это бывает или с недостаточными знаниями…
При этом во многих случаях информация эта однобокая — связано это бывает или с недостаточными знаниями…61
Применение и эксплуатация кислотно-свинцовых герметичных аккумуляторов Автор: Журавлев О. В. В статье рассмотрены вопросы применения и эксплуатации кислотно-свинцовых герметичных аккумуляторных батарей, наиболее широко используемых для резервирования аппаратуры охранно-пожарной сигнализации (ОПС) Появившиеся на российском рынке в начале 90-х годов кислотно-свинцовые герметичные…
60
Как продлить срок службы свинцово-кислотных аккумуляторов? Зачастую представляет определенные трудности использовать напрямую энергию, генерируемую солнечными, ветровыми или микрогидроэлектрическими установками. Поэтому электричество обычно сохраняется в специальных аккумуляторных батареях для последующего использования. Эти батареи очень часто работают по тому же принципу, что…
Информация об аккумуляторных батареях ASUS
Жизненный цикл батареи
- Из-за химических свойств ионов лития емкость батареи постепенно уменьшается с течением времени.
 Это нормальное явление.
Это нормальное явление. - Срок службы литий-ионной батареи составляет примерно 300-500 циклов. При нормальных условиях использования и температуре окружающей среды (25 ℃) литий-ионный аккумулятор должен нормально разряжаться и заряжаться в течение 300 циклов (или около одного года). После этого емкость аккумулятора падает до 80% от первоначальной.
- Снижение срока службы батареи зависит от конструкции системы, модели, энергопотребления системы, потребления программ и операционного программного обеспечения, а также настроек управления питанием. Высокие / низкие рабочие температуры и ненормальная работа могут привести к быстрому сокращению срока службы батареи на 60% или более за короткое время.
- Скорость разряда аккумулятора зависит от программного обеспечения ноутбука или планшета и настроек управления питанием. Например, выполнение требовательных к вычислениям программ, таких как графическое программное обеспечение, игровое программное обеспечение и воспроизведение видео, потребляет больше энергии, чем выполнение обычного программного обеспечения для обработки текстов.
 Когда ноутбук с заряженным аккумулятором подключается к дополнительным устройствам USB или Thunderbolt извне, аккумулятор также разряжается быстрее.
Когда ноутбук с заряженным аккумулятором подключается к дополнительным устройствам USB или Thunderbolt извне, аккумулятор также разряжается быстрее.
Механизмы защиты аккумулятора
- Частая зарядка аккумулятора под высоким напряжением ускоряет ее старение. Чтобы продлить срок службы батареи, батарея поддерживает уровень заряда 90% -100% после полной зарядки, в этом диапазоне система может не заряжаться из-за механизмов защиты батареи.
*Емкость инициирования заряда батареи (%) обычно устанавливается между 90% -99%. Фактическое значение будет отличаться в зависимости от модели.
- Аккумуляторы, заряженные или хранящиеся при высоких температурах окружающей среды, могут повредиться и ускорить сокращение срока службы батареи. Когда температура батареи слишком высокая и аккумулятор перегревается, зарядная емкость батареи будет ограничена или прекращена совсем. Это часть механизмов защиты батареи системы.

- Несмотря на то, что устройство было выключено, а адаптер переменного тока удален, системе по-прежнему требуется небольшое энергопотребление, поэтому это нормальный сценарий, когда уровень заряда батареи все еще падает.
Износ аккумулятора
- Батареи по сути это расходные материалы. Литий-ионные аккумуляторы с непрерывными химическими реакциями естественным образом разряжаются и теряют емкость.
- После использования аккумулятора в течение некоторого времени, при определенных условиях аккумулятор может незначительно вздуться. Это не создаст проблем безопасности.
- Вздутые батареи должны быть заменены и выброшены должным образом, даже если они не влияют на безопасность. При замене вздувшихся батарей не выбрасывайте старую батарею в бытовые отходы. Обратитесь в местную службу поддержки ASUS для утилизации батарей.
Стандартный уход за аккумулятором
- Если ноутбук, мобильный телефон или планшет не будут использоваться в течение длительного времени, зарядите аккумулятор до 50%, выключите устройство и отсоедините источник питания переменного тока (адаптер).
 Подзаряжайте аккумулятор каждые три месяца до 50%, чтобы предотвратить повреждение аккумулятора из-за чрезмерной разрядки из-за длительного хранения без использования.
Подзаряжайте аккумулятор каждые три месяца до 50%, чтобы предотвратить повреждение аккумулятора из-за чрезмерной разрядки из-за длительного хранения без использования. - Когда источник питания переменного тока постоянно используется для ноутбука, мобильных телефонов или планшетов, пользователь должен разряжать аккумулятор до 50% не реже одного раза в две недели, чтобы освободить аккумулятор от постоянного высокого напряжения, что может сократить срок его службы. Пользователи ноутбуков могут продлить срок службы батареи с помощью программного обеспечения ASUS Battery Health Charging.
- Наилучшими условиями хранения аккумуляторов являются температура окружающей среды от 10 до 35 ° C, поддержание заряда на уровне 50% и увеличение срока службы батареи с помощью программного обеспечения ASUS Battery Health Charging.
- Избегайте хранения батарей во влажной среде, которая может привести к увеличению скорости разряда батареи. Среда с более низкой температурой будет вредить внутренним химическим веществам батареи, в то время как батареи, хранящиеся при более высокой температуре, подвергаются риску взрыва.

- Не размещайте компьютер, мобильный телефон или аккумулятор рядом с радиаторами, каминами, печами, электронагревателями или другими источниками тепла выше 60 ℃ (140 ° F). Перегрев аккумулятора может привести к его взрыву или протечке, что может привести к возгоранию.
- Поскольку в ноутбуках используется встроенный аккумулятор, аккумулятор не будут получать питания, если компьютер не использовался или не заряжался, а затем время и настройки BIOS вернутся к значениям по умолчанию. Если вы не собираетесь использовать компьютер в течение длительного времени, заряжайте аккумулятор раз в месяц.
Оптимальные настройки Батареи
Держа адаптеры переменного тока подключенными к ноутбукам, сотовым телефонам или планшетам во время использования, аккумуляторы остаются слишком заряженными, что может сократить срок их службы. Чтобы защитить аккумулятор при таком использовании, пользователи ноутбука могут продлить срок его службы с помощью программного обеспечения ASUS Battery Health Charging.
Введение ASUS Battery Health Charging
https://www.asus.com/ru/support/FAQ/1032726/
Поставки моделей с 4 квартала 2017 содержат это приложение.
Условия гарантии на аккумуляторы ASUS
- ASUS заменит новую аккумуляторную батарею в следующих случаях (применяются условия гарантии https://www.asus.com/ru/support/Article/606/):
- (a) батарея не заряжается;
- (b) батарея вызывает самопроизвольное включение/выключение/перезагрузку ноутбука;
- (c) батарея быстро разряжается;
- (d) батарея не определяется системой;
- (e) система неоднократно предупреждает пользователя о необходимости замены батареи;
- (f) индикатор зарядки батареи работает некорректно;
Обзор аккумуляторов ASUS
Литий-ионные батареи
Преимущества литий-ионных аккумуляторов включают высокую плотность энергии, большую емкость, малый вес, длительный срок службы, отсутствие эффекта памяти и быструю зарядку. Они широко используются в потребительских товарах, таких как мобильные телефоны, ноутбуки и планшеты.
Они широко используются в потребительских товарах, таких как мобильные телефоны, ноутбуки и планшеты.
Что внутри батареи
Главная » Что внутри батареи?
Что внутри батареи?
Обычная батарея требует 3 частей для создания электричества:
- Анод — отрицательная сторона батареи
- Катод — положительная сторона аккумулятора
- Электролит — химическая паста, которая разделяет анод и катод и преобразует химическую энергию в электрическую
Внутри каждой батареи есть восстанавливаемые ресурсы, независимо от ее типа
Возьмем, к примеру, одноразовую щелочную батарейку.Это неперезаряжаемые батареи типа AAA, AA, C, D, 9 вольт и различных размеров таблеточных элементов.
В среднем 25% батареи состоит из стали (корпус). Знаете ли вы, что сталь можно перерабатывать бесконечно? Наш механический процесс позволяет восстановить 100% стали в каждой батарее для повторного использования.
Батарея на 60% состоит из комбинации таких материалов, как цинк (анод), марганец (катод) и калий. Все эти материалы являются земными элементами. Эта комбинация материалов на 100% регенерируется и повторно используется в качестве микроэлемента при производстве удобрений для выращивания кукурузы.
Остальные 15% по весу составляют бумага и пластик (этикетка и защитная крышка). Эти материалы отправляются на производство энергии из отходов для производства электроэнергии.
Когда вы перерабатываете свои щелочные батареи в Raw Materials Company, вы можете быть уверены, что 100% каждой батареи используется повторно, и никакие материалы не будут выброшены на свалку.
Вы живете в Онтарио, Канада?
Если это так, вы можете поискать ближайший к вам магазин по переработке аккумуляторов. Просто введите свой почтовый индекс или название города в наш инструмент поиска. Если вы живете за пределами Онтарио, обратитесь в местный муниципалитет, чтобы найти ближайший к вам пункт утилизации.
Просто введите свой почтовый индекс или название города в наш инструмент поиска. Если вы живете за пределами Онтарио, обратитесь в местный муниципалитет, чтобы найти ближайший к вам пункт утилизации.
Спасибо
Мы получили ваше сообщение и ответим вам в ближайшее время.
Быстрые ссылки
Для вашего удобства, вот список важных ссылок, связанных с этой страницей.
Знаете ли вы?
Цинк является одним из наиболее часто используемых металлов в мире.Приблизительно 30% цинка сегодня поступает из переработанных источников. Компания Raw Materials может извлекать цинк из батарей, которые вы перерабатываете. Цинк, который мы извлекаем, затем повторно используется в качестве питательных микроэлементов в удобрениях для выращивания кукурузы для производства биотоплива.
Благодаря переработанным материалам RMC фермеры могут увеличить свою урожайность более чем на 20 бушелей с акра. Это важно, учитывая наше растущее население и необходимость эффективного использования наших существующих сельскохозяйственных угодий.
Это важно, учитывая наше растущее население и необходимость эффективного использования наших существующих сельскохозяйственных угодий.
Узнайте больше о нашей технологии и о том, как вместе мы превращаем отходы в ценный ресурс.
Что такое батарея? — Learn.sparkfun.com
Избранное
Любимый
22
Введение
Батареи представляют собой набор из одной или нескольких ячеек, химические реакции которых создают поток электронов в цепи. Все батареи состоят из трех основных компонентов: анода (сторона «-»), катода (сторона «+») и электролита (вещество, которое химически реагирует с анодом и катодом).
Когда анод и катод батареи подключены к цепи, между анодом и электролитом происходит химическая реакция. Эта реакция заставляет электроны течь по цепи и возвращаться к катоду, где происходит другая химическая реакция. Когда материал в катоде или аноде расходуется или больше не может использоваться в реакции, батарея не может производить электричество. В этот момент ваша батарея «умерла».
Когда материал в катоде или аноде расходуется или больше не может использоваться в реакции, батарея не может производить электричество. В этот момент ваша батарея «умерла».
Батарейки, которые необходимо выбрасывать после использования, называются первичными батареями .Батареи, которые можно перезаряжать, называются вторичными батареями .
Литий-полимерные батареи, например, можно перезаряжать
Без батарей ваш квадрокоптер был бы привязан к стене, вам пришлось бы вручную заводить машину, а ваш контроллер Xbox должен был бы быть все время подключен к сети (как в старые добрые времена). Батареи предлагают способ хранения электрической потенциальной энергии в портативном контейнере.
Батарейки бывают разных форм, размеров и химического состава.
Изобретение современной батареи часто приписывают Алессандро Вольта. На самом деле все началось с удивительного происшествия, связанного с вскрытием лягушки.
Чему вы научитесь
В этом руководстве будут подробно рассмотрены следующие темы:
- Как были изобретены батареи
- Из каких частей состоит батарея
- Как работает аккумулятор
- Общие термины, используемые для описания батарей
- Различные способы использования батарей в цепях
Предлагаемая литература
Есть несколько понятий, с которыми вы, возможно, захотите ознакомиться перед тем, как начать читать это руководство:
Хотите изучить различные батареи?
Мы вас прикроем!
Щелочная батарея 9В
В наличии
ПРТ-10218
Это ваши стандартные 9-вольтовые щелочные батареи от Rayovac.Даже не думайте пытаться перезарядить их. Используйте их с…
1
История
Срок Батарея
Исторически слово «батарея» использовалось для описания «серии подобных объектов, сгруппированных вместе для выполнения определенной функции», как в артиллерийской батарее. В 1749 году Бенджамин Франклин впервые использовал этот термин для описания серии конденсаторов, которые он соединил вместе для своих экспериментов с электричеством.Позже этот термин будет использоваться для любых электрохимических элементов, соединенных вместе с целью обеспечения электроэнергии.
В 1749 году Бенджамин Франклин впервые использовал этот термин для описания серии конденсаторов, которые он соединил вместе для своих экспериментов с электричеством.Позже этот термин будет использоваться для любых электрохимических элементов, соединенных вместе с целью обеспечения электроэнергии.
Батарея лейденской банки «конденсаторы», соединенные вместе
(Изображение предоставлено Alvinrune из Викисклада)
Изобретение батареи
В один роковой день в 1780 году итальянский физик, врач, биолог и философ Луиджи Гальвани препарировал лягушку, прикрепленную к медному крючку. Когда он коснулся лягушачьей лапки железным скальпелем, та дернулась.Гальвани предположил, что энергия исходит от самой ноги, но его коллега-ученый Алессандро Вольта считал иначе.
Вольта предположил, что импульсы лапок лягушки на самом деле были вызваны различными металлами, пропитанными жидкостью. Он повторил эксперимент, используя ткань, смоченную в рассоле, вместо трупа лягушки, что привело к аналогичному напряжению. Вольта опубликовал свои открытия в 1791 году, а позже в 1800 году создал первую батарею, вольтов столб.
Вольта опубликовал свои открытия в 1791 году, а позже в 1800 году создал первую батарею, вольтов столб.
Вольтов столб, состоящий из стопки цинковых и медных пластин, разделенных тканью, пропитанной соляным раствором
Стопка
Volta страдала от двух основных проблем: из-за веса стека электролит вытекал из ткани, а особые химические свойства компонентов приводили к очень короткому сроку службы (около часа).Следующие двести лет уйдут на совершенствование конструкции Вольты и решение этих проблем.
Исправления в Вольтовом столбе
Уильям Круикшенк из Шотландии решил проблему утечки, положив гальваническую батарею на бок, чтобы сформировать «корытообразную батарею».
Батарея желоба решила проблему утечки вольтовой батареи
Вторая проблема, короткий срок службы, была вызвана разложением цинка из-за примесей и образованием пузырьков водорода на меди.В 1835 году Уильям Стерджен обнаружил, что обработка цинка ртутью предотвращает деградацию.
Британский химик Джон Фредерик Дэниелл использовал второй электролит, который реагировал с водородом, предотвращая отложения на медном катоде. Двухэлектролитная батарея Даниэля, известная как «ячейка Даниэля», станет очень популярным решением для обеспечения энергией зарождающихся телеграфных сетей.
Коллекция клеток Даниэля 1836 года
Первая аккумуляторная батарея
В 1859 году французский физик Гастон Планте создал батарею из двух скрученных листов свинца, погруженных в серную кислоту.При реверсировании электрического тока через батарею химический состав вернется в исходное состояние, создав таким образом первую перезаряжаемую батарею.
Позже, в 1881 году, Камилла Альфонс Фор улучшила конструкцию Планте, превратив свинцовые листы в пластины. Эта новая конструкция упростила производство аккумуляторов, и свинцово-кислотные аккумуляторы получили широкое распространение в автомобилях.
-> Дизайн обычного «автомобильного аккумулятора» существует уже более 100 лет.
(Изображение предоставлено Эмилианом Робертом Виколом из Wikimedia Commons)
Сухая камера
Вплоть до конца 1800-х годов электролит в батареях находился в жидком состоянии.Это делало транспортировку батарей очень осторожным делом, и большинство батарей никогда не предназначалось для перемещения после подключения к цепи.
В 1866 году Жорж Лекланше создал батарею, используя цинковый анод, катод из диоксида марганца и раствор хлорида аммония в качестве электролита. В то время как электролит в элементе Лекланше все еще был жидким, химический состав батареи оказался важным шагом на пути к изобретению сухого элемента.
Карл Гасснер придумал, как создать электролитную пасту из хлорида аммония и гипса.Он запатентовал новую «сухую» батарею в 1886 году в Германии.
Эти новые сухие элементы, обычно называемые «цинково-угольными батареями», производились массово и пользовались огромной популярностью до конца 1950-х годов. Хотя углерод не используется в химической реакции, он выполняет важную роль электрического проводника в угольно-цинковой батарее.
-> 3-вольтовая угольно-цинковая батарея 1960-х годов
(Изображение предоставлено PhFabre из Викисклада) <-
В 1950-х годах Льюис Урри, Пол Марсал и Карл Кордеш из компании Union Carbide (позже известной как «Eveready», а затем «Energizer») заменили электролит хлорида аммония щелочным веществом на основе химического состава батареи, сформулированного Вальдемаром. Юнгнера в 1899 г.Щелочные сухие батареи могли удерживать больше энергии, чем угольно-цинковые батареи того же размера, и имели более длительный срок хранения.
Щелочные батареи
приобрели популярность в 1960-х годах, обогнали цинко-угольные батареи и с тех пор стали стандартными первичными элементами для потребительского использования.
-> Щелочные батареи бывают разных форм и размеров
(Изображение предоставлено Aney~commonswiki из Викисклада) <-
Аккумуляторы 20-го века
В 1970-х годах COMSAT разработал никель-водородную батарею для использования в спутниках связи. Эти батареи хранят водород в газообразной форме под давлением. Многие искусственные спутники, такие как Международная космическая станция, по-прежнему используют никель-водородные батареи.
Эти батареи хранят водород в газообразной форме под давлением. Многие искусственные спутники, такие как Международная космическая станция, по-прежнему используют никель-водородные батареи.
Исследования нескольких компаний с конца 1960-х годов привели к созданию никель-металлогидридной (NiMH) батареи. NiMH аккумуляторы были выпущены на потребительский рынок в 1989 году и стали более дешевой альтернативой перезаряжаемым никель-водородным элементам.
Asahi Chemical из Японии создала первую литий-ионную батарею в 1985 году, а Sony создала первую коммерческую литий-ионную батарею в 1991 году.В конце 1990-х годов для литий-ионных аккумуляторов был создан мягкий гибкий корпус, что привело к появлению «литий-полимерных» или «LiPo» аккумуляторов.
Химические реакции в литий-полимерном аккумуляторе практически такие же, как и в литий-ионном аккумуляторе
Очевидно, что было изобретено, произведено и устарело намного больше химических элементов аккумуляторов. Если вы хотите узнать больше о современных и популярных технологиях аккумуляторов, ознакомьтесь с нашим руководством по технологиям аккумуляторов.
Если вы хотите узнать больше о современных и популярных технологиях аккумуляторов, ознакомьтесь с нашим руководством по технологиям аккумуляторов.
Компоненты
Аккумуляторы
состоят из трех основных компонентов: анода , катода и электролита . Сепаратор часто используется для предотвращения соприкосновения анода и катода, если электролита недостаточно. Для хранения этих компонентов аккумуляторы обычно имеют какой-нибудь кожух .
Хорошо, большинство батарей на самом деле не разделены на три равные секции, но вы поняли идею.Лучшее поперечное сечение щелочной ячейки можно найти в Википедии.
И анод, и катод относятся к типам электродов . Электроды — это проводники, по которым электричество входит или выходит из компонента в цепи.
Анод
Электроны вытекают из анода в устройстве, подключенном к цепи. Это означает, что обычный «ток» течет в анод.
Это означает, что обычный «ток» течет в анод.
На батареях анод помечен как отрицательная (-) клемма
В батарее химическая реакция между анодом и электролитом вызывает накопление электронов в аноде.Эти электроны хотят двигаться к катоду, но не могут пройти через электролит или сепаратор.
Катод
Электроны текут в катод в устройстве, подключенном к цепи. Это означает, что обычный «ток» течет из катода.
На батареях катод обозначен как положительная (+) клемма
В батареях химическая реакция внутри или вокруг катода использует электроны, произведенные в аноде.Единственный способ для электронов добраться до катода — через цепь, внешнюю по отношению к батарее.
Электролит
Электролит – это вещество, часто жидкое или гелеобразное, способное переносить ионы между химическими реакциями, протекающими на аноде и катоде. Электролит также препятствует потоку электронов между анодом и катодом, так что электроны легче проходят через внешнюю цепь, а не через электролит.
-> Щелочные батареи могут вытекать из своего электролита, гидроксида калия, при воздействии сильного нагрева или обратного напряжения
(Изображение предоставлено Вильямом Дэвисом из Викисклада) <-
Электролит имеет решающее значение в работе аккумулятора.Поскольку электроны не могут пройти через него, они вынуждены путешествовать по электрическим проводникам в виде цепи, соединяющей анод с катодом.
Сепаратор
Сепараторы представляют собой пористые материалы, препятствующие соприкосновению анода и катода, что может вызвать короткое замыкание в аккумуляторе. Сепараторы могут быть изготовлены из различных материалов, включая хлопок, нейлон, полиэстер, картон и синтетические полимерные пленки. Сепараторы химически не реагируют ни с анодом, ни с катодом, ни с электролитом.
В гальваническом столбе использовалась ткань или картон (разделитель), пропитанные солевым раствором (электролитом), чтобы держать электроды друг от друга
Ионы в электролите могут быть положительно заряжены, отрицательно заряжены и могут иметь различные размеры. Могут быть изготовлены специальные сепараторы, которые пропускают одни ионы, но не пропускают другие.
Могут быть изготовлены специальные сепараторы, которые пропускают одни ионы, но не пропускают другие.
Корпус
Большинству батарей нужен способ содержать химические компоненты. Корпуса, также известные как «корпуса» или «оболочки», представляют собой просто механические конструкции, предназначенные для удержания внутренних частей батареи.
Эта свинцово-кислотная батарея имеет пластиковый корпус
Корпуса аккумуляторов могут быть изготовлены практически из чего угодно: пластика, стали, пакетов из мягкого полимерного ламината и так далее. В некоторых батареях используется проводящий стальной корпус, электрически соединенный с одним из электродов. В случае обычного щелочного элемента АА стальной корпус соединен с катодом.
Операция
Для работы батарей обычно требуется несколько химических реакций.По крайней мере, одна реакция происходит на аноде или вокруг него, и одна или несколько реакций происходят на катоде или вокруг него. Во всех случаях реакция на аноде производит дополнительные электроны в процессе, называемом окислением , а реакция на катоде использует дополнительные электроны во время процесса, известного как восстановление .
Во всех случаях реакция на аноде производит дополнительные электроны в процессе, называемом окислением , а реакция на катоде использует дополнительные электроны во время процесса, известного как восстановление .
Когда переключатель замкнут, цепь замыкается, и электроны могут течь от анода к катоду. Эти электроны обеспечивают химические реакции на аноде и катоде.
По сути, мы разделяем определенный вид химической реакции, реакцию восстановления-окисления или окислительно-восстановительную реакцию, на две отдельные части. Окислительно-восстановительные реакции происходят, когда электроны переносятся между химическими веществами. Мы можем использовать движение электронов в этой реакции, чтобы течь за пределы батареи, чтобы питать нашу цепь.
Окисление анода
Эта первая часть окислительно-восстановительной реакции, окисление, происходит между анодом и электролитом и производит электроны (обозначены как e — ).
В некоторых реакциях окисления образуются ионы, например, в литий-ионном аккумуляторе. В других химических реакциях расходуются ионы, как в обычной щелочной батарее. В любом случае ионы могут свободно проходить через электролит, а электроны — нет.
Катодное восстановление
Другая половина окислительно-восстановительной реакции, восстановление, происходит на катоде или вблизи него. Электроны, образующиеся в результате реакции окисления, расходуются при восстановлении.
В некоторых случаях, например, в литий-ионных батареях, положительно заряженные ионы лития, образующиеся в ходе реакции окисления, расходуются при восстановлении.В других случаях, например, в щелочных батареях, при восстановлении образуются отрицательно заряженные ионы.
Электронный поток
В большинстве батарей некоторые или все химические реакции могут происходить, даже если батарея не подключена к электрической цепи. Эти реакции могут повлиять на срок годности батареи.
По большей части реакции будут происходить в полную силу только тогда, когда электрическая проводящая цепь замкнута между анодом и катодом. Чем меньше сопротивление между анодом и катодом, тем больше электронов может протекать и тем быстрее происходят химические реакции.
Создание короткого замыкания в аккумуляторе (в данном случае даже случайного) может быть опасным. Известно, что литий-ионные батареи перегреваются и даже дымят или загораются при наличии короткого замыкания.
Мы можем пропустить эти движущиеся электроны через различные электрические компоненты, известные как «нагрузка», чтобы выполнить что-то полезное. На моушн-графике в начале этого раздела мы зажигаем виртуальную лампочку нашими движущимися электронами.
Разряженная батарея
Химические вещества в батарее в конечном итоге достигнут состояния равновесия. В этом состоянии химические вещества больше не будут реагировать, и в результате батарея больше не будет генерировать электрический ток. В этот момент аккумулятор считается «разряженным».
В этот момент аккумулятор считается «разряженным».
Первичные элементы должны быть утилизированы, когда батарея разряжена. Вторичные элементы можно перезаряжать, и это достигается путем подачи обратного электрического тока через батарею.Перезарядка происходит, когда химические вещества выполняют еще одну серию реакций, чтобы вернуть их в исходное состояние.
Терминология
Люди часто используют общий набор терминов, когда говорят о напряжении батареи, емкости, возможностях источника тока и так далее.
Сотовый
Элемент относится к одному аноду и катоду, разделенным электролитом, используемым для получения напряжения и тока. Аккумулятор может состоять из одной или нескольких ячеек.Например, одна батарея типа АА представляет собой одну ячейку. Автомобильные аккумуляторы содержат шесть ячеек по 2,1 В каждая.
Обычная 9-вольтовая батарея содержит шесть щелочных элементов 1,5 В, установленных друг над другом
Первичный
Первичные клетки содержат химию, которую нельзя обратить.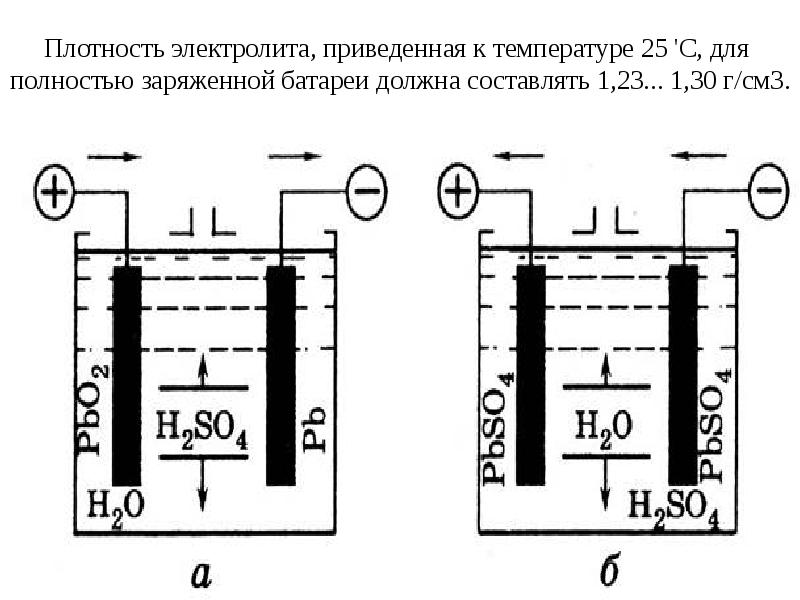 В результате батарея должна быть выброшена после того, как она мертва.
В результате батарея должна быть выброшена после того, как она мертва.
Среднее
Вторичные элементы можно перезарядить и вернуть их химический состав в исходное состояние.Эти элементы, также известные как «перезаряжаемые батареи», можно использовать много раз.
Номинальное напряжение
Номинальное напряжение батареи – это напряжение, указанное производителем.
Например, щелочные батареи AA указаны как имеющие напряжение 1,5 В. В этой статье от Mad Scientist Hut показано, что их протестированные щелочные батареи начинаются с напряжения около 1,55 В, а затем постепенно теряют напряжение по мере разрядки. В этом примере номинальное напряжение «1,5 В» относится к максимальному или начальному напряжению батареи.
Этот аккумуляторный блок Storm для квадрокоптеров показывает кривую разрядки их LiPo элементов, начиная с 4,2 В и падая примерно до 2,8 В по мере разрядки. Номинальное напряжение, указанное для большинства литий-ионных и LiPo элементов, составляет 3,7 В.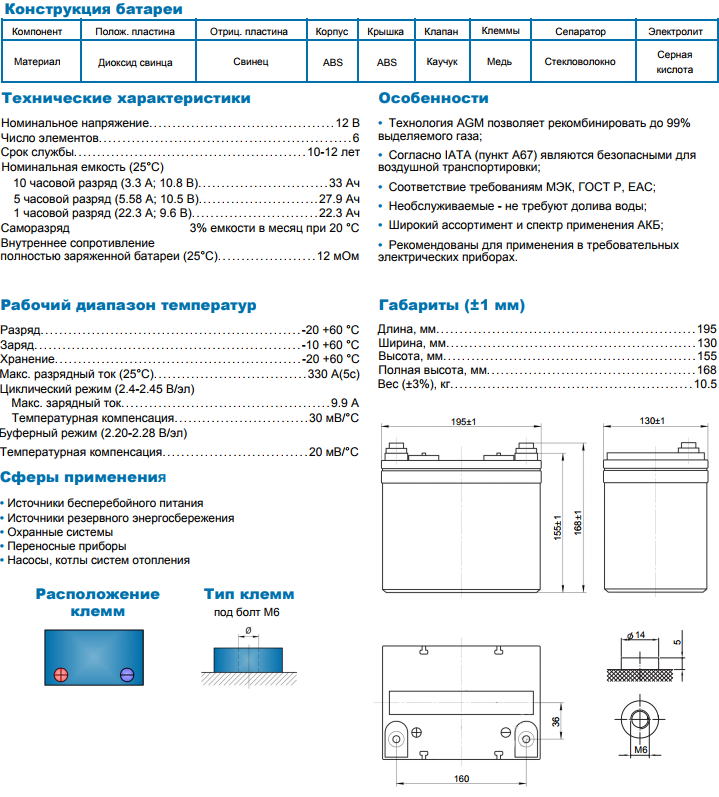 В этом случае номинальное напряжение «3,7 В» относится к среднему напряжению батареи в течение цикла ее разрядки.
В этом случае номинальное напряжение «3,7 В» относится к среднему напряжению батареи в течение цикла ее разрядки.
Емкость
Емкость аккумулятора — это мера количества электрического заряда, который он может отдать при определенном напряжении. Большинство аккумуляторов рассчитаны на ампер-часы (Ач) или миллиампер-часы (мАч).
Этот аккумулятор LiPo рассчитан на 1000 мАч, что означает, что он может обеспечить 1 ампер в течение 1 часа, прежде чем он будет считаться разряженным.
Большинство графиков разряда батареи показывают напряжение батареи как функцию емкости, например, эти тесты батареи AA от PowerStream. Чтобы выяснить, достаточно ли емкости аккумулятора для питания вашей схемы, найдите минимальное допустимое напряжение и найдите соответствующее значение в мАч или Ач.
C-рейтинг
Многие аккумуляторы, особенно мощные литий-ионные аккумуляторы, обозначают ток разряда как «C-Rate», чтобы более четко определить атрибуты аккумулятора. C-Rate — это скорость разряда относительно максимальной емкости аккумулятора.
C-Rate — это скорость разряда относительно максимальной емкости аккумулятора.
1С — это величина тока, необходимая для разрядки аккумулятора за 1 час. Например, батарея емкостью 400 мАч, обеспечивающая ток 1С, будет обеспечивать 400 мА. 5С для той же батареи будет 2 А.
Большинство аккумуляторов теряют емкость при повышенном потреблении тока. Например, этот информационный график продукта от Chargery показывает, что их аккумулятор LiPo имеет меньшую емкость мАч при более высоких показателях C-Rate.
ПРИМЕЧАНИЕ: Общий совет гласит, что вы должны заряжать аккумуляторы LiPo при температуре 1С или меньше.
В Массачусетском технологическом институте есть фантастическое руководство по спецификациям аккумуляторов и терминологии, которое идет гораздо дальше этого обзора.
Использование
Одноэлементный
Некоторые схемы могут питаться от одного элемента, но убедитесь, что батарея может обеспечивать достаточное напряжение и ток.
Этот Photon Battery Shield питается от одного элемента LiPo
Если напряжение слишком высокое или слишком низкое для вашей схемы, вам, вероятно, понадобится преобразователь постоянного тока в постоянный.
Серия
Чтобы увеличить напряжение между клеммами батареи, вы можете соединить элементы последовательно. Серия означает укладку элементов встык, соединяя анод одного с катодом следующего.
Соединяя аккумуляторы последовательно, вы увеличиваете общее напряжение. Добавьте напряжение всех ячеек, чтобы определить рабочее напряжение. Емкость остается прежней.
В этом примере последовательно соединены четыре элемента по 1,5 В.Напряжение на нагрузке составляет 6 В, а общий комплект аккумуляторов имеет емкость 2000 мАч.
В большинстве устройств бытовой электроники, в которых используются щелочные батареи, батареи устанавливаются последовательно. Например, этот держатель для двух батарей типа АА может повысить номинальное напряжение до 3 В для проекта.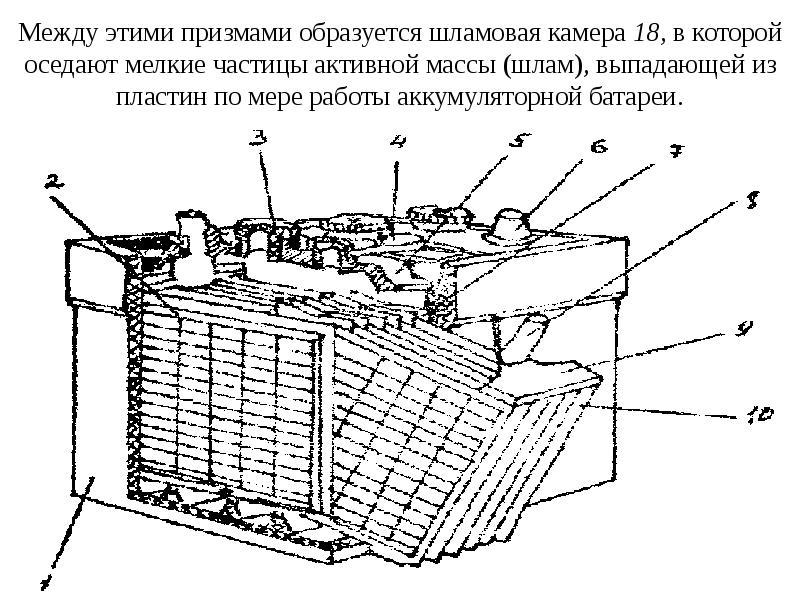
ПРИМЕЧАНИЕ: Если вы заряжаете литий-ионные или LiPo аккумуляторы последовательно, вам необходимо обязательно использовать специальную схему, известную как «балансир», чтобы обеспечить постоянное напряжение между элементами.Некоторые зарядные устройства, такие как это, имеют балансиры для безопасной зарядки.
Параллельный
Если напряжения одного элемента достаточно для нагрузки, вы можете добавить батареи параллельно, чтобы увеличить емкость. Обратите внимание, что это также означает увеличение доступного тока (C-Rate).
Будьте осторожны при параллельном соединении батарей! Все элементы должны иметь одинаковое номинальное напряжение и одинаковый уровень заряда. Если есть какие-либо перепады напряжения, может произойти короткое замыкание, что приведет к перегреву и возгоранию.
В этом примере четыре элемента по 1,5 В соединены параллельно. Напряжение на нагрузке остается на уровне 1,5 В, но общая емкость увеличивается до 8000 мАч.
Серия
и параллельная
Если вы хотите увеличить напряжение и емкость, вы можете комбинировать последовательные и параллельные батареи. Еще раз убедитесь, что уровень напряжения для батарей, включенных параллельно, одинаков, так как может произойти короткое замыкание.
В этом примере общее напряжение на нагрузке составляет 3 В, а общая емкость аккумуляторов составляет 4000 мАч.
В больших аккумуляторных батареях, особенно литий-ионных, вы часто видите конфигурацию, указанную с использованием букв «S» и «P» для последовательного и параллельного подключения. Конфигурация схемы выше — 2S2P. В качестве практического примера современные электромобили используют массивные батареи, соединенные последовательно и параллельно.
Ресурсы и дальнейшее продвижение
К этому моменту вы уже должны понимать, как были изобретены батареи и как они работают. Батареи — это один из способов обеспечения электроэнергией вашего проекта, и они могут быть невероятно полезны, если вам нужен портативный источник питания.
Если вы хотите узнать больше об аккумуляторах, вот еще несколько руководств:
Хотите увидеть батареи в действии? Взгляните на эти проекты, в которых используются разные батареи в разных конфигурациях:
Беспроводная связь Саймона Сплозиона
В этом учебном пособии демонстрируется одна из многих техник «взлома» Саймона. Мы расскажем, как взять ваш Simon Says Wireless.
Литий-ионный аккумулятор — Институт чистой энергии
Основные результаты исследований
Один из способов, с помощью которого CEI работал над достижением этой цели, заключается в прямой визуализации, в частности, с использованием рентгеновской спектроскопии.Недавно в лаборатории профессора Джерри Зайдлера был разработан метод проведения рентгеновской спектроскопии ближней краевой структуры (XANES) на рабочем столе. Этот метод может позволить относительно подробные измерения определенных характеристик внутреннего состояния батареи без необходимости вскрывать ее и, таким образом, нарушать работу системы.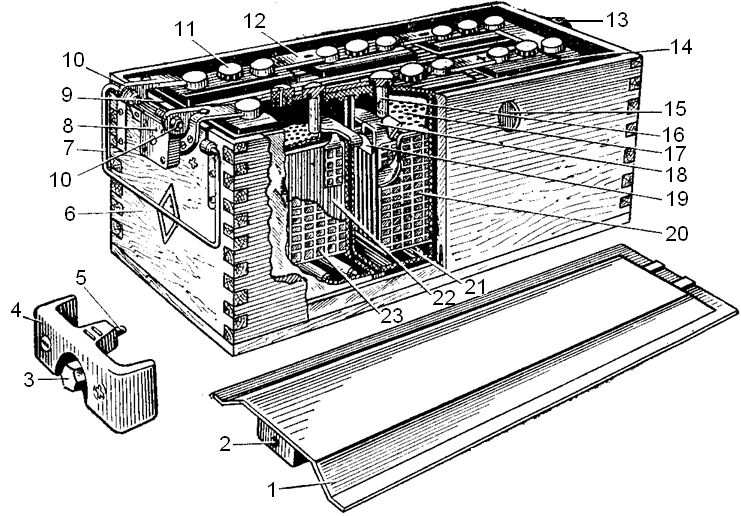 Раньше XANES можно было реализовать только с чрезвычайно высоким потоком излучения от таких инструментов, как синхротрон. Это чрезвычайно большие и дорогие установки стоимостью до 1 миллиарда долларов, которые пользуются таким большим спросом среди ученых, что многомесячные списки ожидания становятся нормой.Используя преимущества новых передовых оптических технологий, лаборатория Зайдлера смогла изготовить небольшой прибор стоимостью 25 000 долларов, который может имитировать измерения, проводимые на синхротроне. С помощью этого нового инструмента ученые могут получать результаты в течение нескольких часов без значительного времени ожидания, что значительно увеличивает скорость разработки нестандартных технологий.
Раньше XANES можно было реализовать только с чрезвычайно высоким потоком излучения от таких инструментов, как синхротрон. Это чрезвычайно большие и дорогие установки стоимостью до 1 миллиарда долларов, которые пользуются таким большим спросом среди ученых, что многомесячные списки ожидания становятся нормой.Используя преимущества новых передовых оптических технологий, лаборатория Зайдлера смогла изготовить небольшой прибор стоимостью 25 000 долларов, который может имитировать измерения, проводимые на синхротроне. С помощью этого нового инструмента ученые могут получать результаты в течение нескольких часов без значительного времени ожидания, что значительно увеличивает скорость разработки нестандартных технологий.
Еще один аспект исследования аккумуляторов CEI включает создание физических, математических и вычислительных моделей внутреннего состояния аккумулятора.Это может помочь оптимизировать производительность батареи и циклы зарядки/разрядки, а также прогнозировать и предотвращать опасные отказы батареи. Профессор Венкат Субраманян, руководитель Лаборатории моделирования, анализа и управления технологическими процессами для электрохимических систем (MAPLE), разрабатывает и переформулирует физические модели батарей, а также работает над методами моделирования и решения этих моделей с большей эффективностью и точностью. Предоставив более эффективную, универсальную и точную модель технологии литий-ионных аккумуляторов, M.А.П.Л.Е. Исследования лаборатории могут помочь в разработке аккумуляторов более точно для более безопасной и эффективной работы.
Профессор Венкат Субраманян, руководитель Лаборатории моделирования, анализа и управления технологическими процессами для электрохимических систем (MAPLE), разрабатывает и переформулирует физические модели батарей, а также работает над методами моделирования и решения этих моделей с большей эффективностью и точностью. Предоставив более эффективную, универсальную и точную модель технологии литий-ионных аккумуляторов, M.А.П.Л.Е. Исследования лаборатории могут помочь в разработке аккумуляторов более точно для более безопасной и эффективной работы.
Другие фокусы
Большая часть текущих исследований CEI направлена на разработку способов лучшего понимания и управления важными внутренними состояниями литий-ионных аккумуляторов. Понимание внутренней работы батареи имеет важное значение для улучшения конструкции и оценки режимов ее отказа.
Другим крупным направлением исследований CEI является разработка новых материалов для улучшения характеристик аккумуляторов. В центре внимания CEI находятся как наука о материалах высокого уровня, такая как разработка и замена альтернативных материалов в литий-ионных батареях, так и характеристика и проектирование наноструктурированных материалов или материалов, свойства которых определяются даже с точностью до нанометра. . Исследователи CEI также изучают материалы, которые могут предложить альтернативу технологиям литий-ионных аккумуляторов.
В центре внимания CEI находятся как наука о материалах высокого уровня, такая как разработка и замена альтернативных материалов в литий-ионных батареях, так и характеристика и проектирование наноструктурированных материалов или материалов, свойства которых определяются даже с точностью до нанометра. . Исследователи CEI также изучают материалы, которые могут предложить альтернативу технологиям литий-ионных аккумуляторов.
Кремний исследуется в качестве анодного материала, поскольку он может образовывать трехмерную клетку, обладающую большей способностью поглощать литий.
Твердотельная батарея — обзор
Твердые электролиты
Одним из ключевых компонентов перезаряжаемой технологии ASSB является твердый электролит. Твердые электролиты, подробно описанные в разделе 4, должны удовлетворять таким технологическим требованиям, как высокая ионная проводимость в сочетании с незначительной электронной проводимостью, широкий диапазон напряжений, химическая совместимость с материалами катода и анода, а также относительно простое производство в больших масштабах с низкой стоимостью. (Мантирам и др., 2017). Как правило, твердые литий- или натрий-ионные проводники делятся на три класса, которые могут дополнять друг друга для удовлетворения этим требованиям: (1) неорганические стекловидные или керамические соединения; (2) органические полимеры и (3) композитные или гибридные электролиты, состоящие из комбинации материалов первых двух классов (Manthiram et al., 2017; Hou et al., 2018a; Zheng et al., 2018).
(Мантирам и др., 2017). Как правило, твердые литий- или натрий-ионные проводники делятся на три класса, которые могут дополнять друг друга для удовлетворения этим требованиям: (1) неорганические стекловидные или керамические соединения; (2) органические полимеры и (3) композитные или гибридные электролиты, состоящие из комбинации материалов первых двух классов (Manthiram et al., 2017; Hou et al., 2018a; Zheng et al., 2018).
Ионный транспорт в твердых неорганических электролитах определяется концентрацией подвижных ионов и вакансий, относительными размерами связанных путей проводимости в кристаллических структурах с точечными дефектами Шоттки и Френкеля, а также свойствами диффузии ионов на границах зерен (Hou et al., 2018а,б; Чжэн и др., 2018). Перспективные твердые неорганические литий-ионные электролиты включают аморфный фосфороксинитрид лития (LiPON) и с проводимостью при комнатной температуре до нескольких мСм см − 1 стеклокерамика на основе сульфида лития, фосфат типа NASICON [Li 1 + x AL x x Ti 2 — x (PO 4 ) 3 (Li 3 (Li 7 La 3 ZR 2 o 12 (LLZO)] керамические электролиты.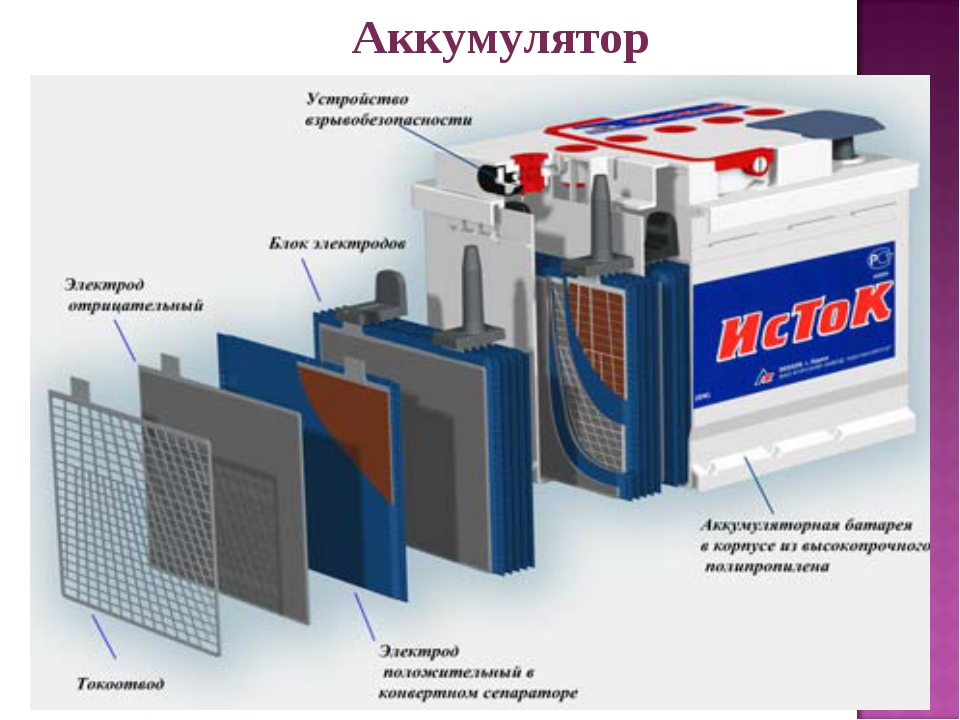 Типичные твердые неорганические электролиты для Na(-ion) ASSB, также обладающие относительно высокой ионной проводимостью при комнатной температуре свыше 1 мСм см — 1 , включают Na-β″-оксид алюминия, суперионные проводники Na [NASICON, т.е. Na 3.1 ZR 1.95 MG 0.05 SI 2 Po 2 PO 12 (песня et al., 2016)], Сульфиды (IE, Na 3 PS 4, Na 10.8 SH 1,9 PS 11.8 ) и сложные гидриды (например, боргидрид натрия) (Yu et al., 2018б; Хоу и др., 2018a,b).
Типичные твердые неорганические электролиты для Na(-ion) ASSB, также обладающие относительно высокой ионной проводимостью при комнатной температуре свыше 1 мСм см — 1 , включают Na-β″-оксид алюминия, суперионные проводники Na [NASICON, т.е. Na 3.1 ZR 1.95 MG 0.05 SI 2 Po 2 PO 12 (песня et al., 2016)], Сульфиды (IE, Na 3 PS 4, Na 10.8 SH 1,9 PS 11.8 ) и сложные гидриды (например, боргидрид натрия) (Yu et al., 2018б; Хоу и др., 2018a,b).
Твердые полимерные электролиты, как правило, имеют значительно более низкую ионную проводимость, чем керамические электролиты, но демонстрируют механическую гибкость, малый вес, удобство процесса изготовления и приспособление к изменениям объема электродов во время заряда/разряда. В твердых полимерных электролитах соли лития или натрия сольватируются полимерными цепями, например, в полимерах на основе полиэтиленоксида (ПЭО) или полисилоксана, и ионы лития или натрия перемещаются по связанным полимерным цепям. Ионная проводимость твердого полимерного электролита связана с количеством подвижных ионов и сегментарными движениями полимерных цепей. Ионный транспорт в соединенных полимерных цепях может блокироваться сегментами кристаллических цепей, которые образуются ниже температуры стеклования ( T g ). T г можно уменьшить, например, за счет добавления наноразмерных наполнителей. Однако относительно низкая ионная проводимость при комнатной температуре по-прежнему представляет собой главный недостаток полимерных электролитов (Zheng et al., 2018; Хоу и др., 2018a,b).
Ионная проводимость твердого полимерного электролита связана с количеством подвижных ионов и сегментарными движениями полимерных цепей. Ионный транспорт в соединенных полимерных цепях может блокироваться сегментами кристаллических цепей, которые образуются ниже температуры стеклования ( T g ). T г можно уменьшить, например, за счет добавления наноразмерных наполнителей. Однако относительно низкая ионная проводимость при комнатной температуре по-прежнему представляет собой главный недостаток полимерных электролитов (Zheng et al., 2018; Хоу и др., 2018a,b).
Композитные или гибридные электролиты, сочетающие в себе преимущества (стекло)керамических и полимерных ионных проводников, обеспечивают улучшенную ионную проводимость с высокой гибкостью для снижения межфазного сопротивления между твердыми электролитами и электродами (Zheng et al., 2018; Hou et al. , 2018а,б).
Свинцово-кислотный аккумулятор – обзор
3.11.4.2 Свинцово-кислотный аккумулятор
Свинцово-кислотный аккумулятор представляет собой наиболее важное применение свинца во всем мире.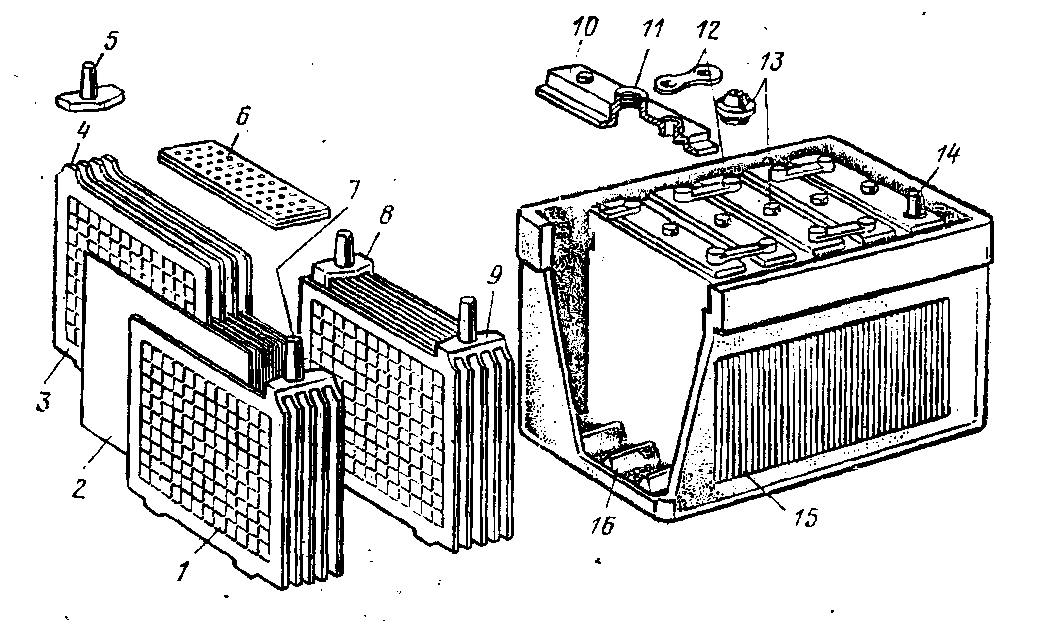 Технология свинцово-кислотных аккумуляторов все еще постоянно совершенствуется и технически все еще очень актуальна; 77 В этом разделе кратко обсуждаются самые общие аспекты технологии. Свинцово-кислотные батареи обычно состоят из подложек из свинцового сплава, которые несут электрохимически активную массу, состав которой различается между положительными и отрицательными пластинами и состоянием заряда батареи. Отказ обычно происходит в положительной сетке батареи. Основной причиной выхода из строя является потеря контакта между сеткой и активной массой из-за «роста сетки», вызванного изменением объема активного материала во время цикла зарядки/разрядки, а также коррозией поверхности металла. которое может быть ускорено стрессом.Аккумуляторы для автомобилей, электромобилей, резервных служб и т. д. имеют разные характеристики и требования, которым отвечает конструкция аккумуляторной решетки и выбор сплава. 78,79
Технология свинцово-кислотных аккумуляторов все еще постоянно совершенствуется и технически все еще очень актуальна; 77 В этом разделе кратко обсуждаются самые общие аспекты технологии. Свинцово-кислотные батареи обычно состоят из подложек из свинцового сплава, которые несут электрохимически активную массу, состав которой различается между положительными и отрицательными пластинами и состоянием заряда батареи. Отказ обычно происходит в положительной сетке батареи. Основной причиной выхода из строя является потеря контакта между сеткой и активной массой из-за «роста сетки», вызванного изменением объема активного материала во время цикла зарядки/разрядки, а также коррозией поверхности металла. которое может быть ускорено стрессом.Аккумуляторы для автомобилей, электромобилей, резервных служб и т. д. имеют разные характеристики и требования, которым отвечает конструкция аккумуляторной решетки и выбор сплава. 78,79
Традиционно аккумуляторные сетки изготавливают из свинца с содержанием сурьмы 6–14%, с небольшим содержанием мышьяка.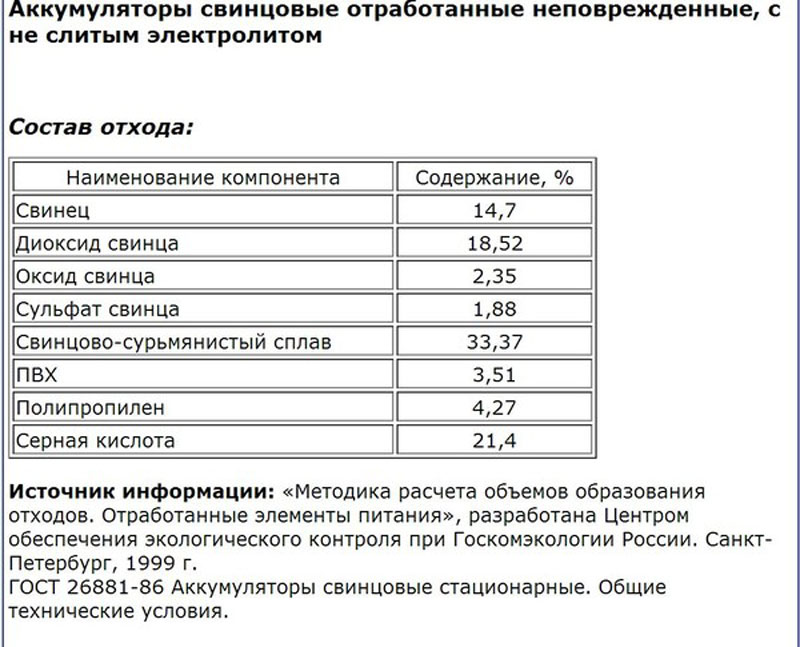 Сплавы с высоким содержанием сурьмы имеют существенный электрохимический недостаток, т. е. снижают перенапряжение для выделения водорода на свинце, что приводит к электролизу электролита (до водорода и кислорода).Таким образом, батареи из традиционных материалов требуют регулярного обслуживания (дозаправки) путем добавления дистиллированной воды. В то время как сплавы с содержанием сурьмы в районе 5–6% все еще используются в некоторых промышленных, глубоких разрядных и тяговых устройствах, высокое содержание сурьмы было в значительной степени заменено в автомобильных батареях комплексом с низким содержанием сурьмы или без сурьмы свинец-кальций-(олово). сплавы. В современных автомобильных аккумуляторных батареях теперь используются сплавы на основе свинца и кальция, не требующие доливки (при условии, что они эксплуатируются в пределах расчетных электрических параметров).Это снижение содержания сурьмы стало возможным благодаря введению добавок зародышей кристаллизации, таких как селен и сера, которые способствуют мелкозернистой структуре.
Сплавы с высоким содержанием сурьмы имеют существенный электрохимический недостаток, т. е. снижают перенапряжение для выделения водорода на свинце, что приводит к электролизу электролита (до водорода и кислорода).Таким образом, батареи из традиционных материалов требуют регулярного обслуживания (дозаправки) путем добавления дистиллированной воды. В то время как сплавы с содержанием сурьмы в районе 5–6% все еще используются в некоторых промышленных, глубоких разрядных и тяговых устройствах, высокое содержание сурьмы было в значительной степени заменено в автомобильных батареях комплексом с низким содержанием сурьмы или без сурьмы свинец-кальций-(олово). сплавы. В современных автомобильных аккумуляторных батареях теперь используются сплавы на основе свинца и кальция, не требующие доливки (при условии, что они эксплуатируются в пределах расчетных электрических параметров).Это снижение содержания сурьмы стало возможным благодаря введению добавок зародышей кристаллизации, таких как селен и сера, которые способствуют мелкозернистой структуре. Также все чаще можно найти различные сплавы, используемые в положительных и отрицательных решетках и оптимизированные для этих приложений.
Также все чаще можно найти различные сплавы, используемые в положительных и отрицательных решетках и оптимизированные для этих приложений.
Сплавы с высоким содержанием сурьмы обладают высокой прочностью, хорошей литейностью и хорошими характеристиками при глубоком циклировании. Последнее требует, чтобы активная масса имела хорошую адгезию к металлу, была структурно устойчива при циклировании, не пассивировалась.Сурьма снижает выпадение активного вещества из клеток, образует более пористую поверхностную пленку, которая становится более пористой при циклировании, способствуя стабильности активной массы. Также было показано, что PbSO 4 менее склонен к зародышеобразованию на сурьмяном свинце. 80 Хотя скорость коррозии может казаться довольно высокой, коррозия обычно носит общий характер, что обеспечивает удовлетворительный срок службы. Это связано с тем, что эвтектика преимущественно подвергается коррозии, что снижает межкристаллитную коррозию.Сурьма снижает перенапряжение кислорода на положительной сетке, а ионы Sb 5+ мигрируют с положительной сетки на отрицательную и восстанавливаются до металлической сурьмы.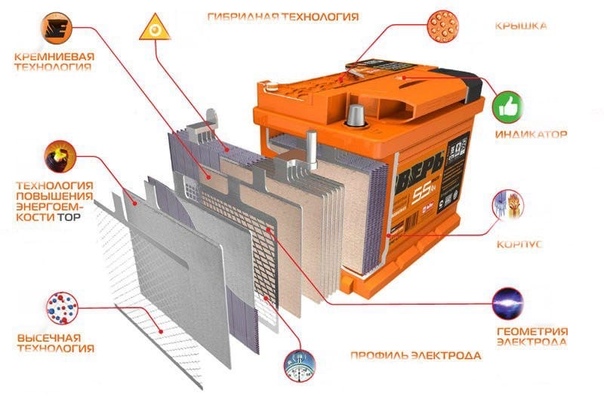 81 Это снижает перенапряжение водорода, что приводит к чрезмерному газовыделению, потреблению воды из электролита, снижению эффективности заряда и высвобождению стибина (SbH 3 ). При перезаряде сурьма увеличивает скорость образования внутреннего коррозионного слоя на положительной сетке.
81 Это снижает перенапряжение водорода, что приводит к чрезмерному газовыделению, потреблению воды из электролита, снижению эффективности заряда и высвобождению стибина (SbH 3 ). При перезаряде сурьма увеличивает скорость образования внутреннего коррозионного слоя на положительной сетке.
Аккумуляторы с низким уровнем обслуживания, которые требуют редкого добавления воды во второй половине срока их службы, используют сплавы с низким содержанием сурьмы, которые обычно содержат менее 3% сурьмы, а некоторые сплавы содержат всего 0.6%. Наиболее часто используемые сплавы содержат 1,3–1,8 % Sb. Они всегда содержат As для облегчения отверждения и зародышеобразующий агент, такой как Se или S с Cu. Это необходимо, потому что грубая дендритная структура склонна к пористости и горячему растрескиванию во время литья. Добавление зародышеобразователей дает мелкозернистую структуру с хорошей коррозионной стойкостью. Олово часто добавляют для повышения текучести литейных сплавов.
Свинцово-кальциево-(оловянные) сплавы используются в необслуживаемых автомобильных пусковых, осветительных, запальных (SLI) батареях, в стационарных батареях и некоторых тяговых батареях.Очень важно использовать правильное содержание кальция и подходящее соотношение кальция и олова. В бинарных сплавах свинец-кальций мелкозернистая структура с зазубренными границами зерен образуется в результате прерывистой реакции осаждения. 82 Добавление олова изменяет характер реакций осаждения, обеспечивая две области стабильности. Один с высоким содержанием кальция и низким содержанием олова, а другой находится в области ниже 1,8% олова и менее 0,07% кальция. Аккумуляторы, изготовленные из этих сплавов, имеют гораздо более низкую скорость саморазряда по сравнению со сплавами сурьмы, что обеспечивает более длительный срок хранения и поддерживает высокое напряжение разряда в течение всего срока службы.
17.5 Батареи и топливные элементы – химия
Цели обучения
К концу этого раздела вы сможете:
- Классифицировать батареи как первичные или вторичные
- Перечислите некоторые характеристики и ограничения батарей
- Дайте общее описание топливного элемента
Батарея представляет собой гальванический элемент или ряд элементов, которые производят электрический ток. В принципе, любой гальванический элемент можно использовать в качестве батареи.Идеальная батарея никогда не разряжается, обеспечивает неизменное напряжение и способна выдерживать экстремальные температуры и влажность окружающей среды. Реальные батареи обеспечивают баланс между идеальными характеристиками и практическими ограничениями. Например, масса автомобильного аккумулятора составляет около 18 кг или около 1% от массы среднего легкового автомобиля или малотоннажного грузовика. Батарея такого типа будет давать почти неограниченную энергию при использовании в смартфоне, но будет отклонена для этого приложения из-за ее массы. Таким образом, ни одна батарея не является «лучшей», и батареи выбираются для конкретного применения с учетом таких факторов, как масса батареи, ее стоимость, надежность и емкость по току.Существует два основных типа аккумуляторов: первичные и вторичные. Ниже описаны несколько батарей каждого типа.
В принципе, любой гальванический элемент можно использовать в качестве батареи.Идеальная батарея никогда не разряжается, обеспечивает неизменное напряжение и способна выдерживать экстремальные температуры и влажность окружающей среды. Реальные батареи обеспечивают баланс между идеальными характеристиками и практическими ограничениями. Например, масса автомобильного аккумулятора составляет около 18 кг или около 1% от массы среднего легкового автомобиля или малотоннажного грузовика. Батарея такого типа будет давать почти неограниченную энергию при использовании в смартфоне, но будет отклонена для этого приложения из-за ее массы. Таким образом, ни одна батарея не является «лучшей», и батареи выбираются для конкретного применения с учетом таких факторов, как масса батареи, ее стоимость, надежность и емкость по току.Существует два основных типа аккумуляторов: первичные и вторичные. Ниже описаны несколько батарей каждого типа.
Посетите этот сайт, чтобы узнать больше о батареях.
Первичные батареи являются одноразовыми батареями, поскольку их нельзя перезаряжать. Обычной основной батареей является сухой элемент (рис. 1). Сухой элемент представляет собой угольно-цинковую батарею. Цинковая банка служит как контейнером, так и отрицательным электродом. Положительный электрод представляет собой углеродный стержень, окруженный пастой из оксида марганца (IV), хлорида цинка, хлорида аммония, угольного порошка и небольшого количества воды.{-}[/latex] с общим потенциалом элемента, который изначально составляет около 1,5 В, но снижается по мере использования батареи. Важно помнить, что напряжение, выдаваемое батареей, одинаково независимо от размера батареи. По этой причине батареи D, C, A, AA и AAA имеют одинаковое номинальное напряжение. Однако большие батареи могут доставлять больше молей электронов. Поскольку цинковый контейнер окисляется, его содержимое в конечном итоге вытекает, поэтому аккумуляторы этого типа не следует оставлять в электрических устройствах на длительное время.
Рисунок 1. На схеме показано поперечное сечение батарейки для фонарика, угольно-цинкового сухого элемента.
Посетите этот сайт, чтобы узнать больше о угольно-цинковых батареях.
Щелочные батареи (рис. 2) были разработаны в 1950-х годах частично для решения некоторых проблем с производительностью угольно-цинковых сухих элементов. Они производятся для точной замены угольно-цинковых сухих элементов. Как следует из названия, в этих типах батарей используются щелочные электролиты, часто гидроксид калия.{\circ} = +1,43\;\text{V} \end{массив}[/latex]
Щелочная батарея может вырабатывать примерно в три-пять раз больше энергии, чем углеродно-цинковая сухая батарея аналогичного размера. Щелочные батареи склонны к утечке гидроксида калия, поэтому их также следует удалять из устройств для длительного хранения. Хотя некоторые щелочные батареи перезаряжаемы, большинство из них перезаряжаемы. Попытки перезарядить щелочную батарею, которая не подлежит перезарядке, часто приводят к разрыву батареи и утечке электролита гидроксида калия.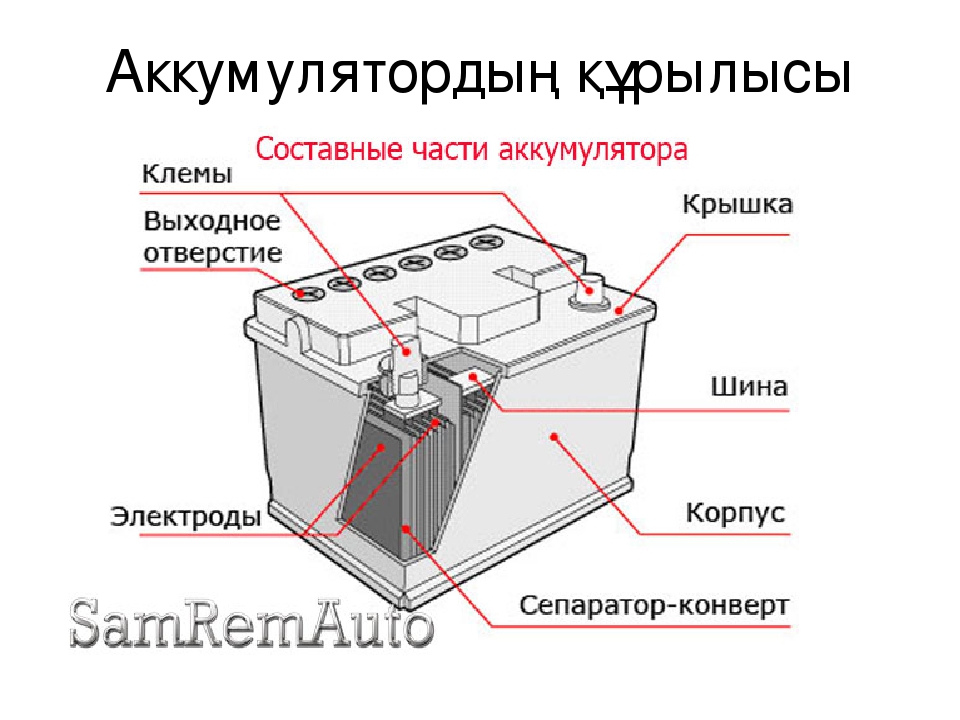
Рисунок 2. Щелочные батареи были разработаны как прямая замена угольно-цинковым батареям (сухие элементы).
Посетите этот сайт, чтобы узнать больше о щелочных батареях.
Вторичные батареи перезаряжаемые. Это типы батарей, которые можно найти в таких устройствах, как смартфоны, электронные планшеты и автомобили.
Никель-кадмиевые или NiCd батареи (рис. 3) состоят из никелированного катода, кадмиевого анода и электрода из гидроксида калия.{-}(водн.) \\[0.5em] \hline \\[-0.25em] \text{общий:} & \text{Cd}(s)\;+\;\text{NiO}_2(s) \;+\;2\text{H}_2\text{O}(l) & \text{Cd(OH)}_2(s)\;+\;\text{Ni(OH)}_2(s) \end{массив}[/латекс]
Напряжение составляет от 1,2 В до 1,25 В при разрядке аккумулятора. При правильном обращении никель-кадмиевую батарею можно перезарядить около 1000 раз. Кадмий является токсичным тяжелым металлом, поэтому никель-кадмиевые аккумуляторы нельзя открывать или выбрасывать в обычный мусор.
Рисунок 3. Никель-кадмиевые батареи имеют конструкцию «свернутого желе», что значительно увеличивает величину тока, которую батарея может отдавать, по сравнению с щелочными батареями аналогичного размера.{-}\;+\;x\;\text{C}_6 & x\;\text{LiC}_6 \\[0.5em] \hline \\[-0.25em] \text{общий:} & \ text{LiCoO}_2\;+\;x\;\text{C}_6 & \text{Li}_{x\;-\;1}\text{CoO}_2\;+\;x\;\ текст{LiC}_6 \end{массив}[/latex]
С коэффициентами, представляющими моли, x составляет не более 0,5 молей. Напряжение батареи составляет около 3,7 В. Литиевые батареи популярны, потому что они могут обеспечивать большой ток, они легче, чем сопоставимые батареи других типов, создают почти постоянное напряжение при разрядке и лишь медленно теряют заряд при хранении.
Рисунок 4. В ионно-литиевой батарее заряд протекает между электродами по мере того, как ионы лития перемещаются между анодом и катодом.
Посетите этот сайт для получения дополнительной информации о ионно-литиевых батареях.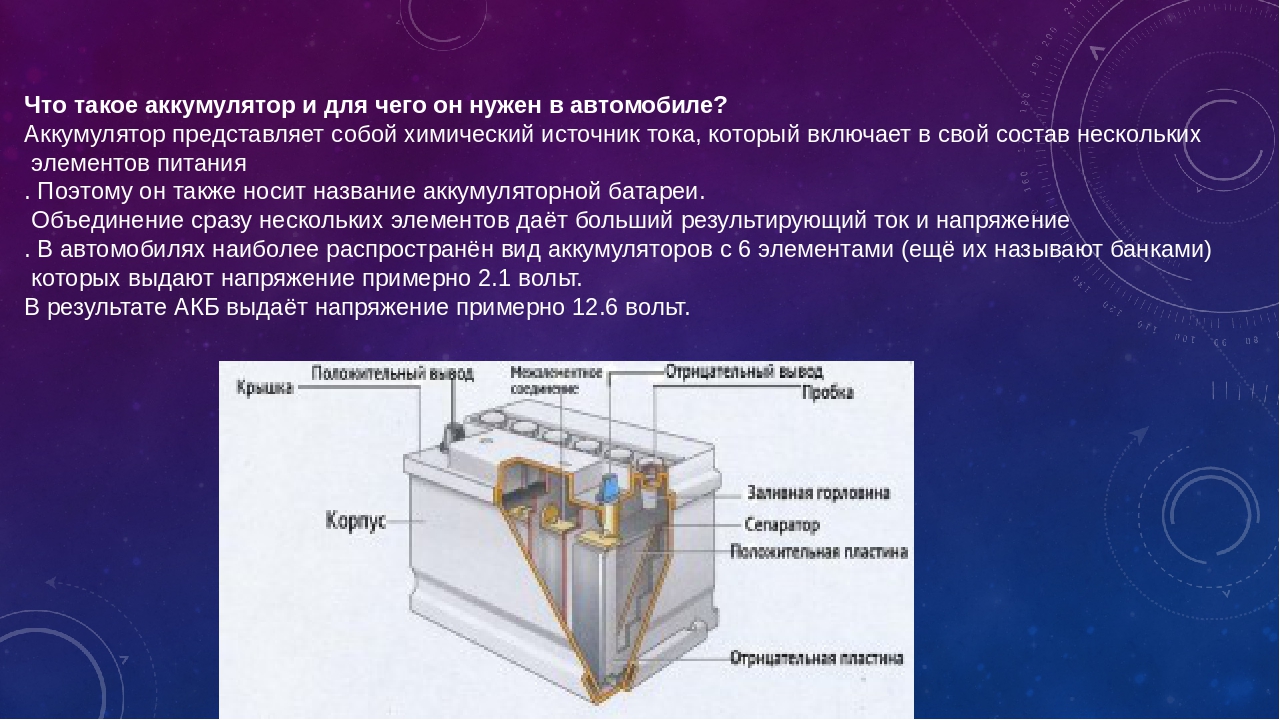 {- } \\[0.{-} & \text{PbSO}_4(s)\;+\;2\text{H}_2\text{O}(l) \\[0,5em] \hline \\[-0,25em] \text {всего:} & \text{Pb}(s)\;+\;\text{PbO}_2(s)\;+\;2\text{H}_2\text{SO}_4(aq) & 2 \text{PbSO}_4(s)\;+\;2\text{H}_2\text{O}(l) \end{массив}[/latex]
{- } \\[0.{-} & \text{PbSO}_4(s)\;+\;2\text{H}_2\text{O}(l) \\[0,5em] \hline \\[-0,25em] \text {всего:} & \text{Pb}(s)\;+\;\text{PbO}_2(s)\;+\;2\text{H}_2\text{SO}_4(aq) & 2 \text{PbSO}_4(s)\;+\;2\text{H}_2\text{O}(l) \end{массив}[/latex]
Каждая ячейка производит 2 В, поэтому шесть ячеек соединены последовательно, чтобы получить автомобильный аккумулятор на 12 В. Свинцово-кислотные батареи тяжелые и содержат едкий жидкий электролит, но часто по-прежнему являются предпочтительными батареями из-за их высокой плотности тока. Поскольку эти батареи содержат значительное количество свинца, их всегда необходимо утилизировать надлежащим образом.
Рисунок 5. Свинцово-кислотный аккумулятор в вашем автомобиле состоит из шести элементов, соединенных последовательно и обеспечивающих напряжение 12 В. Низкая стоимость и высокий выходной ток делают эти аккумуляторы отличными кандидатами для питания автомобильных стартеров.
Посетите этот сайт для получения дополнительной информации о свинцово-кислотных батареях. {-} \\[0.{2-} \\[0.5em] \hline \\[-0.25em] \text{всего:} & 2\text{H}_2\;+\;\text{O}_2 & 2\text{H }_2\text{O} \end{массив}[/latex]
{-} \\[0.{2-} \\[0.5em] \hline \\[-0.25em] \text{всего:} & 2\text{H}_2\;+\;\text{O}_2 & 2\text{H }_2\text{O} \end{массив}[/latex]
Напряжение составляет около 0,9 В. КПД топливных элементов обычно составляет от 40% до 60%, что выше, чем у типичного двигателя внутреннего сгорания (от 25% до 35%), и, в случае водородного топливного элемента, дает только вода в качестве выхлопа. В настоящее время топливные элементы довольно дороги и имеют особенности, которые приводят к их выходу из строя через относительно короткое время.
Перейдите по этой ссылке, чтобы узнать больше о топливных элементах.
Батареи — это гальванические элементы или набор элементов, которые производят электрический ток. Когда элементы объединены в батареи, потенциал батареи является целым числом, кратным потенциалу отдельной ячейки. Существует два основных типа аккумуляторов: первичные и вторичные. Первичные батареи являются «одноразовыми» и не подлежат перезарядке. Сухие элементы и (большинство) щелочных батарей являются примерами первичных батарей.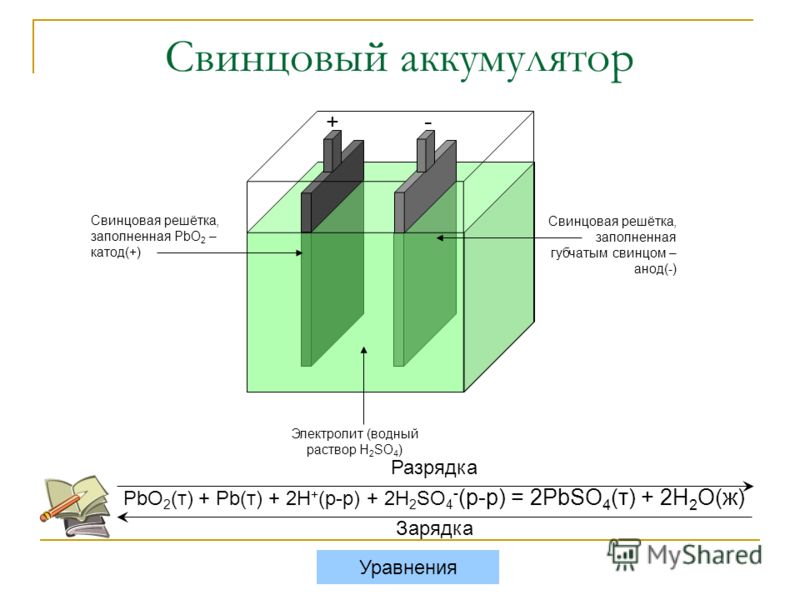 Второй тип является перезаряжаемым и называется вторичной батареей. Примеры вторичных батарей включают никель-кадмиевые (NiCd), свинцово-кислотные и ионно-литиевые батареи.Топливные элементы аналогичны батареям в том, что они генерируют электрический ток, но требуют постоянного добавления топлива и окислителя. Водородный топливный элемент использует водород и кислород из воздуха для производства воды и, как правило, более эффективен, чем двигатели внутреннего сгорания.
Второй тип является перезаряжаемым и называется вторичной батареей. Примеры вторичных батарей включают никель-кадмиевые (NiCd), свинцово-кислотные и ионно-литиевые батареи.Топливные элементы аналогичны батареям в том, что они генерируют электрический ток, но требуют постоянного добавления топлива и окислителя. Водородный топливный элемент использует водород и кислород из воздуха для производства воды и, как правило, более эффективен, чем двигатели внутреннего сгорания.
Химия Упражнения в конце главы
- Каковы желательные качества электрической батареи?
- Перечислите некоторые аспекты, которые обычно учитываются при выборе батареи для нового приложения.
- Рассмотрим батарею, состоящую из одного полуэлемента, состоящего из медного электрода в растворе 1 M CuSO 4 , и другого полуэлемента, состоящего из свинцового электрода в растворе 1 M Pb(NO 3 ) . 2 решение.
а) Каковы реакции на аноде, катоде и общая реакция?
(б) Каков стандартный потенциал ячейки для батареи?
(c) Большинство устройств, предназначенных для использования сухих батарей, могут работать в диапазоне от 1.
 {\circ} = -0.{\circ} = +0,53\;\text{V} \end{массив}[/latex]
{\circ} = -0.{\circ} = +0,53\;\text{V} \end{массив}[/latex]Подойдет ли этот аккумулятор для смартфонов? Почему или почему нет?
- Почему аккумуляторы разряжаются, а топливные элементы нет?
- Объясните, что происходит с напряжением батареи при ее использовании, используя уравнение Нернста.
- Используя информацию из этой главы, объясните, почему электроника с батарейным питанием плохо работает при низких температурах.
Глоссарий
- щелочная батарея
- , в которой используется щелочной (часто гидроксид калия) электролит; разработан, чтобы быть точной заменой сухого элемента, но с большим накоплением энергии и меньшей утечкой электролита, чем типичный сухой элемент
первичная батарея
- аккумулятор
- гальванический элемент или ряд элементов, вырабатывающих ток; по идее любой гальванический элемент
- сухая камера
- , также называемая угольно-цинковой батареей; может использоваться в любой ориентации, поскольку в качестве электролита используется паста; имеет тенденцию вытекать электролит при хранении
первичная батарея
- топливный элемент
- устройства, производящие электрический ток при непрерывном добавлении горючего и окислителя; эффективнее двигателей внутреннего сгорания
- свинцово-кислотная батарея
- , состоящая из нескольких элементов; свинцово-кислотная батарея, используемая в автомобилях, имеет шесть элементов и напряжение 12 В
аккумуляторная батарея
.
- литий-ионный аккумулятор
- очень популярная вторичная батарея; использует ионы лития для проведения тока, легкий, перезаряжаемый и создает почти постоянный потенциал при разрядке
- никель-кадмиевая батарея
- (никель-кадмиевая батарея) вторичная батарея, в которой используется кадмий, являющийся токсичным тяжелым металлом; тяжелее литий-ионных аккумуляторов, но с аналогичными ТТХ
- основная батарея
- одноразовая неперезаряжаемая батарея
- аккумуляторная батарея
- , который можно перезаряжать
Аккумулятор
Решения
Ответы на упражнения по химии в конце главы
2.Соображения включают в себя: стоимость материалов, используемых в батарее, токсичность различных компонентов (что представляет собой правильная утилизация), должна ли это быть первичная или вторичная батарея, требования к энергии («размер» батареи / как долго она должна работать) , будет ли течь конкретный аккумулятор при использовании нового устройства в соответствии с указаниями, и его масса (общая масса нового устройства). {\circ} = 0.{\circ} = 0,7996\;\text{V} \end{массив}[/latex]; (б) 3,5 × 10 15 ; (в) 5.6 × 10 −9 М
{\circ} = 0.{\circ} = 0,7996\;\text{V} \end{массив}[/latex]; (б) 3,5 × 10 15 ; (в) 5.6 × 10 −9 М
6. Батареи являются автономными и имеют ограниченный запас реагентов, которые необходимо израсходовать, прежде чем они разрядятся. В качестве альтернативы побочные продукты реакции батареи накапливаются и мешают реакции. Поскольку топливный элемент постоянно пополняется реагентами, а продукты выбрасываются, он может продолжать функционировать до тех пор, пока подаются реагенты.
8. E ячейка , как описано в уравнении Нернста, имеет член, который прямо пропорционален температуре.При низких температурах этот срок уменьшается, что приводит к более низкому напряжению ячейки, подаваемому батареей к устройству, — тот же эффект, что и при разряженной батарее.
Будущий спрос на материалы для автомобильных аккумуляторов на основе лития
Обзор модели
Мы разрабатываем модель динамического анализа материальных потоков (MFA), которая часто используется для анализа запасов и потоков материалов 47 . Наша модель MFA, основанная на запасах, оценивает будущий спрос на материалы для аккумуляторов электромобилей, а также материалы EoL, доступные для переработки.Он состоит из слоя электромобиля, слоя батареи и слоя материала и рассматривает ключевые технические и социально-экономические параметры на трех уровнях (дополнительный рисунок 1). Слой электромобилей моделирует будущее развитие парка (парка) электромобилей до 2050 года, а также необходимую емкость аккумуляторов. Затем запас электромобилей определяет запас аккумуляторов, который, в свою очередь, определяет приток аккумуляторов и, с учетом их распределения по сроку службы (см. Дополнительный метод 1), отток аккумуляторов EoL (см. Дополнительный метод 2).Уровень аккумуляторов учитывает будущие разработки в области химии аккумуляторов и доли рынка. Слой материала моделирует химический состав батареи с использованием модели BatPaC 48 . Судьба батарей EoL моделируется с учетом трех сценариев переработки и сценария повторного использования, и они определяют доступность материалов для переработки в замкнутом цикле.
Наша модель MFA, основанная на запасах, оценивает будущий спрос на материалы для аккумуляторов электромобилей, а также материалы EoL, доступные для переработки.Он состоит из слоя электромобиля, слоя батареи и слоя материала и рассматривает ключевые технические и социально-экономические параметры на трех уровнях (дополнительный рисунок 1). Слой электромобилей моделирует будущее развитие парка (парка) электромобилей до 2050 года, а также необходимую емкость аккумуляторов. Затем запас электромобилей определяет запас аккумуляторов, который, в свою очередь, определяет приток аккумуляторов и, с учетом их распределения по сроку службы (см. Дополнительный метод 1), отток аккумуляторов EoL (см. Дополнительный метод 2).Уровень аккумуляторов учитывает будущие разработки в области химии аккумуляторов и доли рынка. Слой материала моделирует химический состав батареи с использованием модели BatPaC 48 . Судьба батарей EoL моделируется с учетом трех сценариев переработки и сценария повторного использования, и они определяют доступность материалов для переработки в замкнутом цикле.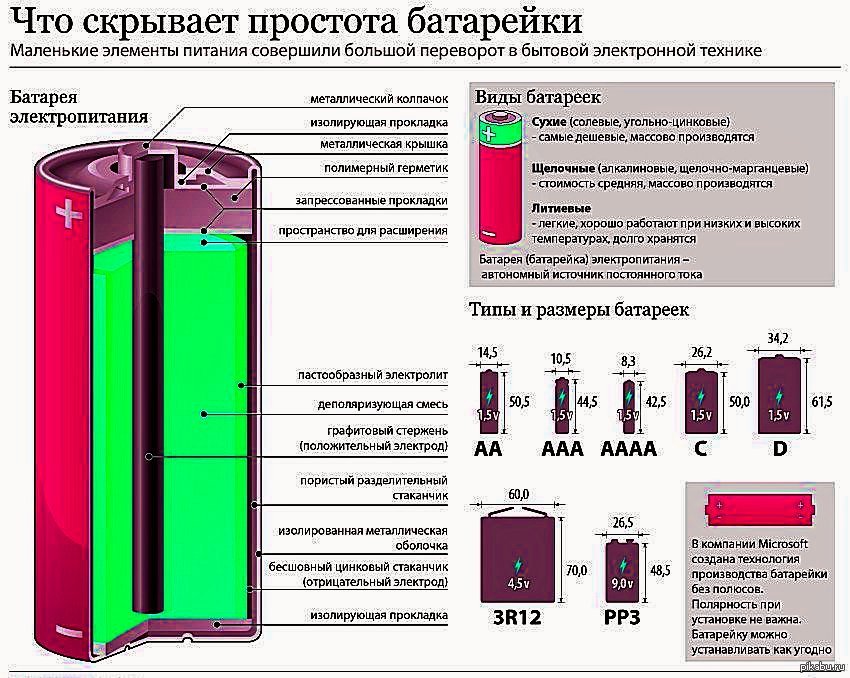 Слои и параметры модели описаны ниже.
Слои и параметры модели описаны ниже.
Сценарии развития парка электромобилей и требуемая емкость аккумуляторной батареи
Прогнозы развития парка электромобилей различаются, но большинство исследований прогнозируют существенное проникновение электромобилей на рынок легковых автомобилей (LDV) в будущем (дополнительный рис.2). Мы используем два сценария развития парка электромобилей МЭА до 2030 года: сценарий заявленной политики (STEP) и сценарий устойчивого развития (SD) 3 (и оцениваем годовой запас электромобилей на основе эквивалентных сценариев МЭА 2019 49 , см. Дополнительный рис. 21). Затем мы экстраполируем проникновение электромобилей до 2050 года с использованием логистической модели (см. дополнительные рисунки 22) 50 на основе целевого проникновения электромобилей на рынок легковых автомобилей в 2050 году, составляющего 25% в сценарии STEP и 50% в сценарии SD. (что соответствует другим прогнозам EV, как показано на дополнительном рис.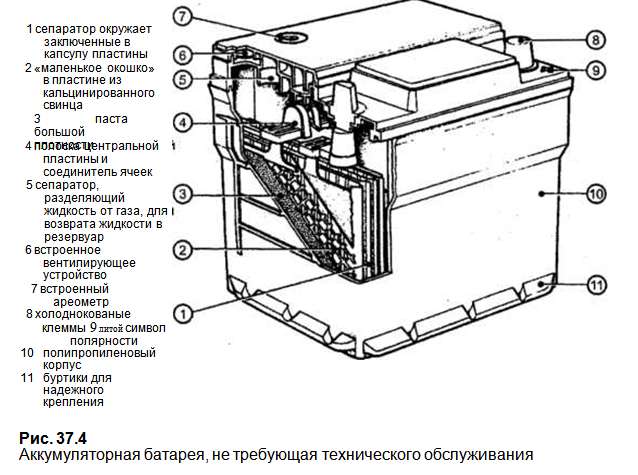 2). Чтобы оценить будущий парк электромобилей до 2050 года, мы также предполагаем линейный рост мирового парка легковых автомобилей с 503 миллионов автомобилей в 2019 году до 3,9 миллиарда автомобилей в 2050 году, что соответствует прогнозу Fuel Freedom Foundation 51 . Глобальные прогнозы будущего развития акций BEV и PHEV недоступны. Чтобы оценить будущие доли BEV и PHEV в запасе электромобилей, мы предположили, что глобальная доля BEV увеличится так же, как доля BEV в США, прогнозируемая Управлением энергетической информации США 52 , но начиная с уровней 2030 г. Сценарии STEP и SD (т.т. е., с 66% в 2030 г. до 71% в 2050 г. в сценарии STEP и с 70% в 2030 г. до 75% в 2050 г. в сценарии SD, см. Дополнительный рисунок 23).
2). Чтобы оценить будущий парк электромобилей до 2050 года, мы также предполагаем линейный рост мирового парка легковых автомобилей с 503 миллионов автомобилей в 2019 году до 3,9 миллиарда автомобилей в 2050 году, что соответствует прогнозу Fuel Freedom Foundation 51 . Глобальные прогнозы будущего развития акций BEV и PHEV недоступны. Чтобы оценить будущие доли BEV и PHEV в запасе электромобилей, мы предположили, что глобальная доля BEV увеличится так же, как доля BEV в США, прогнозируемая Управлением энергетической информации США 52 , но начиная с уровней 2030 г. Сценарии STEP и SD (т.т. е., с 66% в 2030 г. до 71% в 2050 г. в сценарии STEP и с 70% в 2030 г. до 75% в 2050 г. в сценарии SD, см. Дополнительный рисунок 23).
Мы классифицируем модели электромобилей по трем рыночным сегментам (маленькие, средние и большие автомобили как для BEV, так и для PHEV) на основе классов размеров транспортных средств, используемых в Руководстве по экономии топлива Агентства по охране окружающей среды (см. Дополнительную таблицу 13) 53 и собирать глобальные продажи каждой модели электромобиля из базы данных Marklines 54 . Мы используем распределение совокупных продаж до 2019 года, чтобы представить доли рынка продаж электромобилей среди малых, средних и крупных сегментов (дополнительные рисунки 24 и 25).В результате мы получили 19, 48 и 34% для малых, средних и больших автомобилей для BEV и 23, 45 и 32% для PHEV. Мы предполагаем, что доля рынка продаж электромобилей останется неизменной; тем не менее, анализ чувствительности проводится для получения верхней и нижней границ требований к материалам, если все транспортные средства были большими BEV или малыми PHEV (см. анализ чувствительности).
Дополнительную таблицу 13) 53 и собирать глобальные продажи каждой модели электромобиля из базы данных Marklines 54 . Мы используем распределение совокупных продаж до 2019 года, чтобы представить доли рынка продаж электромобилей среди малых, средних и крупных сегментов (дополнительные рисунки 24 и 25).В результате мы получили 19, 48 и 34% для малых, средних и больших автомобилей для BEV и 23, 45 и 32% для PHEV. Мы предполагаем, что доля рынка продаж электромобилей останется неизменной; тем не менее, анализ чувствительности проводится для получения верхней и нижней границ требований к материалам, если все транспортные средства были большими BEV или малыми PHEV (см. анализ чувствительности).
Мы собираем запас хода, экономию топлива и мощность двигателя каждой модели электромобиля из центра данных Advanced Fuels Министерства энергетики США 55 и рассчитываем средневзвешенный запас хода, экономию топлива и мощность двигателя для трех сегментов рынка как для электромобилей, так и для электромобилей. PHEV (дополнительные таблицы 1 и 2).Предполагая 85% доступной емкости аккумулятора для вождения электромобилей на основе модели BatPaC 48 , мы получаем 33, 66 и 100 кВтч для малых, средних и больших электромобилей (см. Дополнительную таблицу 2 для PHEV).
PHEV (дополнительные таблицы 1 и 2).Предполагая 85% доступной емкости аккумулятора для вождения электромобилей на основе модели BatPaC 48 , мы получаем 33, 66 и 100 кВтч для малых, средних и больших электромобилей (см. Дополнительную таблицу 2 для PHEV).
Срок службы легковых автомобилей варьируется от 9 до 23 лет в странах со средним сроком службы около 15 лет 56 . Срок службы электромобиля зависит от поведения потребителей, технического срока службы (см. следующий раздел) и других факторов. Здесь мы используем распределение Вейбулла 57 для моделирования продолжительности жизни электромобилей, предполагая, что минимальная, максимальная и наиболее вероятная продолжительность жизни электромобилей составляет 1, 20 и 15 лет соответственно (см.6). Мы не рассматриваем возможность восстановления и повторного использования аккумуляторов с одного электромобиля на другой из-за снижения производительности, технической совместимости и приемлемости для потребителей.
Сценарии химического состава аккумуляторов и доля рынка
Несмотря на то, что для снижения стоимости и повышения производительности были разработаны различные химические составы аккумуляторов для электромобилей, текущие основные планы развития аккумуляторов в США 58 , ЕС 25 , Германии 59 и Китае 60 сосредоточиться на разработке катодных материалов с учетом высокоэнергетического NCM (переход к низкому содержанию кобальта и высокому содержанию никеля) и химии на основе NCA, которые, вероятно, станут следующим поколением ЛИА для электромобилей в следующем десятилетии, а также на разработке анодных материалов с учетом добавления Si в графитовый анод.Это также отражено в коммерческой деятельности производителей аккумуляторов (например, LG Chem или CATL) 61 и прогнозах доли рынка до 2030 года компании Avicenne Energy 17 , которые мы используем в этом исследовании. Мы предполагаем, что батареи NCM продолжают снижать содержание кобальта и увеличивать содержание никеля после 2030 года, и компилируем сценарий NCX (где X представляет либо Al, либо Mn) до 2050 года (включая восемь химических процессов, см. Дополнительную таблицу 14). В сценарии NCX мы предполагаем, что NCM955 (90 % никеля, 5 % кобальта, 5 % марганца) будет представлен в 2030 году 18 и постепенно заменит другие предыдущие химические вещества пропорционально, чтобы достичь доли рынка в одну треть к 2050 году (т.т. е. предполагается, что рыночные доли аккумуляторов NCM111, NCM523, NCM622, NCM622-Graphite (Si), NCM811-Graphite (Si), NCA и LFP сократятся пропорционально после 2030 г., см. рис. 2b).
Дополнительную таблицу 14). В сценарии NCX мы предполагаем, что NCM955 (90 % никеля, 5 % кобальта, 5 % марганца) будет представлен в 2030 году 18 и постепенно заменит другие предыдущие химические вещества пропорционально, чтобы достичь доли рынка в одну треть к 2050 году (т.т. е. предполагается, что рыночные доли аккумуляторов NCM111, NCM523, NCM622, NCM622-Graphite (Si), NCM811-Graphite (Si), NCA и LFP сократятся пропорционально после 2030 г., см. рис. 2b).
Будущие разработки в области химического состава аккумуляторов после 2030 г. неясны, но возможный химический состав аккумуляторов, помимо аккумуляторов NCM и NCA, включает уже существующие аккумуляторы LFP 21,62 , а также литий-металлические твердотельные аккумуляторы большой емкости, такие как Li -S и Li-Air 23,25 . Поэтому мы включили два дополнительных сценария «что, если» рядом со сценарием NCX: сценарий LFP и сценарий Li-S/Air.В сценарии LFP предполагается, что рыночная доля химии LFP будет линейно увеличиваться примерно с 30 % в 2019 г.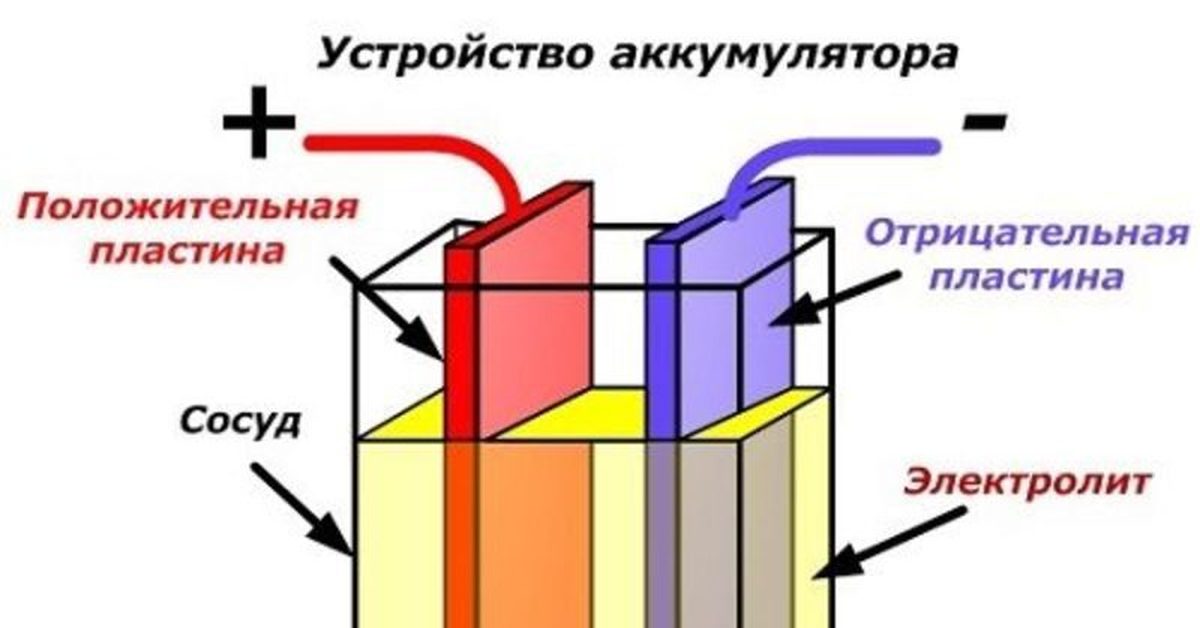 до 60 % к 2030 г. и останется на этом уровне до 2050 г. Рис. 2б). В сценарии Li-S/Li-Air мы предполагаем, что Li-S и Li-Air аккумуляторы появятся в продаже в 2030 году, исходя из коммерческих планов Li-S от OXIS Energy 63 и Li-Air от Samsung Electronics 64 , а затем получают линейно увеличивающуюся долю рынка до 30 % каждая (всего 60 %) к 2040 г. и сохраняют эту долю до 2050 г.2б).
до 60 % к 2030 г. и останется на этом уровне до 2050 г. Рис. 2б). В сценарии Li-S/Li-Air мы предполагаем, что Li-S и Li-Air аккумуляторы появятся в продаже в 2030 году, исходя из коммерческих планов Li-S от OXIS Energy 63 и Li-Air от Samsung Electronics 64 , а затем получают линейно увеличивающуюся долю рынка до 30 % каждая (всего 60 %) к 2040 г. и сохраняют эту долю до 2050 г.2б).
Реальный срок службы батарей зависит от дополнительных факторов, которые здесь не моделируются, таких как температура окружающей среды, глубина и скорость заряда и разряда, циклы движения 65 . Мы используем технический срок службы батарей. Мы предполагаем, что до 2020 года срок службы батарей, вероятно, составит 8 лет (исходя из гарантии производителей электромобилей) 66 , что меньше срока службы электромобиля (дополнительная таблица 15). Мы предполагаем, что до 2020 года уровень замены батарей для электромобилей составит 50% (т.т. е. на один электромобиль в среднем требуется 1,5 блока аккумуляторов). Программы исследований аккумуляторов в США 58 , ЕС 25 и Китае 60 включают цели по увеличению срока службы аккумуляторов, поэтому мы предполагаем, что после 2020 г. требуются батареи (дополнительная таблица 16). Обратите внимание, что мы предполагаем более длительный срок службы батарей LFP (в среднем 20 лет) (дополнительный рис. 6), что приводит к более высокому потенциалу повторного использования, чем для других типов батарей.
Программы исследований аккумуляторов в США 58 , ЕС 25 и Китае 60 включают цели по увеличению срока службы аккумуляторов, поэтому мы предполагаем, что после 2020 г. требуются батареи (дополнительная таблица 16). Обратите внимание, что мы предполагаем более длительный срок службы батарей LFP (в среднем 20 лет) (дополнительный рис. 6), что приводит к более высокому потенциалу повторного использования, чем для других типов батарей.
Составы материалов аккумуляторов
Составы материалов аккумуляторов рассчитаны с использованием модели BatPaC версии 3.1 48 в зависимости от 2 типов электромобилей (BEV или PHEV), 3 сегментов рынка электромобилей (малый, средний и большие автомобили) и 8 химических элементов аккумуляторов (LFP, NCA, NCM11, NCM523, NCM622, NCM622-графит (Si), NCM811-графит (Si), NCM955-графит (Si)), что дает 48 уникальных химических элементов аккумуляторов. Входные параметры включают запас хода электромобиля, экономию топлива и мощность двигателя, которые определяют требуемую емкость каждого типа электромобиля и сегмента рынка (дополнительные таблицы 1 и 2), а также химический состав батареи и другие параметры (например, конструкция аккумуляторных модулей и ячеек). компоненты), для которых мы используем значения по умолчанию в модели BatPaC.Для расчета составов химических элементов аккумуляторов, которых нет в BatPaC (например, NCM523, NCM622-графит (Si), NCM811-графит (Si), NCM955-графит (Si)), мы используем наиболее близкий химический состав аккумуляторов в BatPaC. в качестве основы, а затем адаптировать технические параметры, такие как содержание Ni, Co, Mn в положительном активном материале и содержание Si и графита в отрицательном активном материале, по стехиометрии, а также емкости активного материала (дополнительные таблицы 17–19) и напряжение холостого хода (см. дополнительную таблицу 20 и примечание 1).
компоненты), для которых мы используем значения по умолчанию в модели BatPaC.Для расчета составов химических элементов аккумуляторов, которых нет в BatPaC (например, NCM523, NCM622-графит (Si), NCM811-графит (Si), NCM955-графит (Si)), мы используем наиболее близкий химический состав аккумуляторов в BatPaC. в качестве основы, а затем адаптировать технические параметры, такие как содержание Ni, Co, Mn в положительном активном материале и содержание Si и графита в отрицательном активном материале, по стехиометрии, а также емкости активного материала (дополнительные таблицы 17–19) и напряжение холостого хода (см. дополнительную таблицу 20 и примечание 1).
Для химии Li-S и Li-Air мы провели обзор литературы по удельной энергии и составу материалов элементов Li-S и Li-Air (дополнительные таблицы 21 и 22), а затем линейно масштабируем их для соответствия требуемой батарее. мощности для каждого типа электромобиля и сегмента рынка (дополнительное примечание 2). Предполагается, что компоненты упаковки Li-S и Li-Air основаны на конфигурациях упаковки химии NCA (т. е. такое же весовое соотношение между компонентами ячейки и компонентами упаковки). В дополнительной таблице 23 показаны составы материалов, использованные в этой статье.
е. такое же весовое соотношение между компонентами ячейки и компонентами упаковки). В дополнительной таблице 23 показаны составы материалов, использованные в этой статье.
Сценарии переработки
Переработка батарей EoL обеспечивает вторичную поставку материалов. Здесь мы предполагаем уровень сбора 100% и исследуем влияние эффективности переработки трех сценариев переработки (см. Дополнительную таблицу 24) на спрос на первичные материалы, включая восстановленные количества и некоторое обсуждение качества переработанных материалов. Потребность в первичных материалах при отсутствии сбора и переработки батарей EoL отражает сценарий «без переработки» (рис.4). В настоящее время коммерциализированные технологии переработки включают пирометаллургическую (пиро) и гидрометаллургическую (гидро) переработку. Прямая рециркуляция находится в стадии разработки для катодной рециркуляции. Для батарей NCX и LFP предполагается пиро-, гидро- и прямая переработка в трех сценариях переработки, соответственно, в то время как механическая переработка предполагается для Li-S и Li-Air батарей во всех трех сценариях.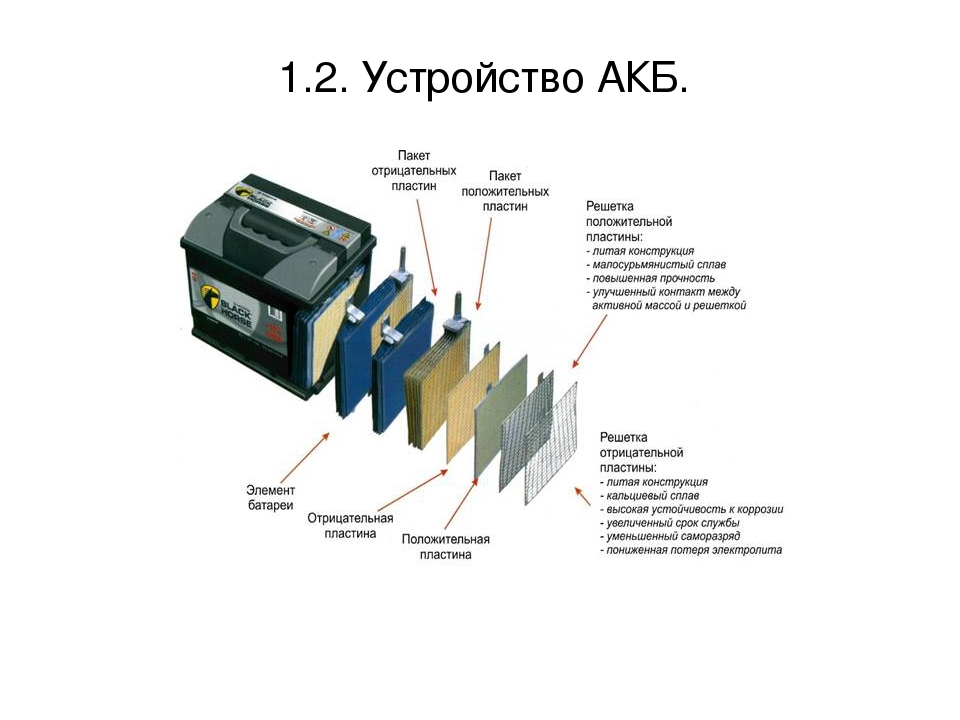 Технологии рециклинга различаются перерабатываемыми материалами, химическими формами, эффективностью рекуперации и экономическими перспективами 46,67,68 (рис.5).
Технологии рециклинга различаются перерабатываемыми материалами, химическими формами, эффективностью рекуперации и экономическими перспективами 46,67,68 (рис.5).
Рассматриваемый нами сценарий пирометаллургического рециклинга на самом деле является гибридным пиро- и гидропроцессом. После подачи разобранных аккумуляторных модулей и/или элементов в плавильный цех графит выжигается, алюминий и литий попадают в шлак, а никель, кобальт и медь попадают в штейн. После выщелачивания штейна ионы меди извлекаются в виде металлической меди путем электролиза, а ионы никеля и кобальта извлекаются в виде соединений никеля и кобальта для аккумуляторных батарей путем экстракции растворителем или осаждения.Литий в шлаке можно перерабатывать для производства соединений лития для аккумуляторных батарей, но это экономически выгодно только при высокой цене на литий и масштабной переработке. Технически алюминий в шлаке также может быть восстановлен, но это неэкономично и не рассматривается компаниями по пиропереработке (шлак может использоваться, например, в качестве заполнителя в строительных материалах).
Сценарий гидрометаллургической переработки начинается с измельчения разобранных модулей и/или элементов. Затем измельченный материал проходит ряд этапов физического разделения для сортировки материалов на катодный порошок, анодный порошок и смешанные алюминиевые и медные отходы.В зависимости от цен на металлолом смешанный алюминиевый и медный лом может быть дополнительно рассортирован на алюминиевый лом и медный лом. Медный лом можно снова включить в цепочку поставок аккумуляторов с минимальной обработкой (т. е. переплавкой). Переработка алюминия в замкнутом цикле является более сложной задачей, поскольку восстановленный алюминиевый лом представляет собой смесь различных алюминиевых сплавов (например, из токоприемника и корпуса), и поэтому алюминий, как правило, перерабатывается. Замкнутый цикл переработки алюминия потребует разделения алюминиевого сплава до или во время процесса переработки, что может быть или не быть экономичным 69 .Катодный порошок впоследствии выщелачивается кислотой, при этом никель, кобальт и марганец выщелачиваются в виде ионов и извлекаются в виде соединений, пригодных для аккумуляторных батарей, после экстракции растворителем и осаждения. Литий попадает в твердые отходы, которые также можно использовать в качестве строительных материалов. Подобно пиропереработке, литий из твердых отходов можно восстановить в виде соединения, пригодного для использования в аккумуляторных батареях, но экономическая эффективность зависит от цены на литий. Анодный порошок, извлеченный с помощью гидроэлектростанции, который может представлять собой смесь графита и кремния, не подходит для аккумуляторных батарей.Хотя они могут быть усовершенствованы до аккумуляторного качества, в настоящее время их экономическая целесообразность неясна.
Литий попадает в твердые отходы, которые также можно использовать в качестве строительных материалов. Подобно пиропереработке, литий из твердых отходов можно восстановить в виде соединения, пригодного для использования в аккумуляторных батареях, но экономическая эффективность зависит от цены на литий. Анодный порошок, извлеченный с помощью гидроэлектростанции, который может представлять собой смесь графита и кремния, не подходит для аккумуляторных батарей.Хотя они могут быть усовершенствованы до аккумуляторного качества, в настоящее время их экономическая целесообразность неясна.
Сценарий прямой переработки аналогичен гидроэлектростанции, за исключением рециркуляции катодного порошка. В прямом процессе катодный порошок восстанавливается, а затем регенерируется путем взаимодействия с источником лития (повторное литирование и облагораживание). Таким образом, литий, никель, кобальт и марганец извлекаются как одно соединение, пригодное для аккумуляторных батарей. Поскольку здесь нет необходимости в рафинировании лития, как в случае пиро и гидро, извлечение лития в прямом процессе экономически выгодно, по крайней мере, с точки зрения лабораторного масштаба.
Эффективность извлечения материала для пиро-, гидро- и прямого нагрева взята из модели EverBatt 67 , разработанной в Аргоннской национальной лаборатории (дополнительная таблица 24). Что касается механической переработки Li-S и Li-Air аккумуляторов, мы предполагаем, что в процессе извлекается только металлический литий. Предполагается, что эффективность извлечения металлического лития составляет 90%, а извлечение считается экономичным из-за относительно простого процесса и высокой стоимости восстановленного металлического лития.
Сценарии вторичного использования/использования
Аккумуляторы EoL EV могут повторно использоваться для менее требовательных приложений (неавтомобильных), таких как стационарные накопители энергии, поскольку их остаточная емкость часто составляет около 70–80 % от их первоначальной емкости. вместимость 70,71 . Существуют технические барьеры (например, производительность перепрофилированных батарей) и экономическая неопределенность (стоимость перепрофилирования, включая разборку, тестирование и переупаковку), которые зависят от химического состава батареи, состояния ее работоспособности и предполагаемого применения вторичного использования 72 ,73 . Здесь мы различаем показатели повторного использования LFP и других химических веществ из-за длительного срока службы 20 и снижения вероятности каскадного отказа LFP 74 . Предполагается, что батареи LFP имеют коэффициент вторичного использования 100%. Для остальных химических элементов аккумуляторов мы предполагаем коэффициент повторного использования 50 % до 2020 года, который возрастет до 75 % в период с 2020 по 2050 год из-за увеличения технического срока службы аккумуляторов для электромобилей (см. Дополнительную таблицу 6). Применения вторичного использования варьируются от домашнего использования до интеграции системы электроснабжения, в результате чего срок службы вторичного использования варьируется от 6 до 30 лет 75 .Мы предполагаем типичный 10-летний срок службы вторичного использования 71 , чтобы изучить влияние повторного использования на доступность материалов для переработки. Обратите внимание, что повторное использование предполагает 100% повторное использование аккумуляторных модулей, в то время как компоненты упаковки поступают на переработку напрямую.
Здесь мы различаем показатели повторного использования LFP и других химических веществ из-за длительного срока службы 20 и снижения вероятности каскадного отказа LFP 74 . Предполагается, что батареи LFP имеют коэффициент вторичного использования 100%. Для остальных химических элементов аккумуляторов мы предполагаем коэффициент повторного использования 50 % до 2020 года, который возрастет до 75 % в период с 2020 по 2050 год из-за увеличения технического срока службы аккумуляторов для электромобилей (см. Дополнительную таблицу 6). Применения вторичного использования варьируются от домашнего использования до интеграции системы электроснабжения, в результате чего срок службы вторичного использования варьируется от 6 до 30 лет 75 .Мы предполагаем типичный 10-летний срок службы вторичного использования 71 , чтобы изучить влияние повторного использования на доступность материалов для переработки. Обратите внимание, что повторное использование предполагает 100% повторное использование аккумуляторных модулей, в то время как компоненты упаковки поступают на переработку напрямую.
Анализ чувствительности
Влияние важных факторов, таких как размер парка электромобилей и химический состав аккумуляторов, исследуется в рамках специальных сценариев. Кроме того, мы проводим анализ чувствительности для (а) срока службы батареи, (б) требуемой емкости батареи на транспортное средство, (в) проникновения на рынок аккумуляторов, не содержащих кобальт и никель, и (г) будущей удельной энергии литий-ионных аккумуляторов. Химия S и Li-Air (для которых были приняты консервативные цифры).
- (а)
Срок службы батареи оказывает важное влияние на количество батарей, необходимых для электромобилей. Мы проводим анализ чувствительности влияния более низкого срока службы батареи на потребность в материалах для батарей, предполагая, что и после 2020 года для одного электромобиля в среднем потребуется 1,5 батареи (результаты на дополнительном рис. 20).
- (б)
Будущие доли рынка электромобилей и гибридов и емкость аккумуляторов электромобилей также являются ключевыми факторами для определения количества необходимых материалов.
 В то время как емкость аккумулятора определяется многими факторами, такими как запас хода электромобиля, экономия топлива и конфигурации трансмиссии, мы проводим анализ чувствительности для двух крайних ситуаций: 100% BEV с мощностью 110 кВтч (большие внедорожники, такие как Tesla Model S Long Range Plus 37 ). , см. Дополнительную таблицу 25 для состава материалов) и 100% PHEV мощностью 10 кВтч (см. Дополнительную таблицу 26 для состава материалов), чтобы изучить границы будущего спроса на материалы (см. соответствующие совокупные потребности в материалах на рис.4 и дополнительный рисунок 11, см. годовые результаты на дополнительном рисунке 10).
В то время как емкость аккумулятора определяется многими факторами, такими как запас хода электромобиля, экономия топлива и конфигурации трансмиссии, мы проводим анализ чувствительности для двух крайних ситуаций: 100% BEV с мощностью 110 кВтч (большие внедорожники, такие как Tesla Model S Long Range Plus 37 ). , см. Дополнительную таблицу 25 для состава материалов) и 100% PHEV мощностью 10 кВтч (см. Дополнительную таблицу 26 для состава материалов), чтобы изучить границы будущего спроса на материалы (см. соответствующие совокупные потребности в материалах на рис.4 и дополнительный рисунок 11, см. годовые результаты на дополнительном рисунке 10). - (с)
Аналогичным образом мы также изучаем влияние 100% доли рынка LFP в сценарии LFP и 100% доли рынка Li-S и Li-Air в сценарии Li-S/Air (см. Дополнительный рис. 17 и связанные требования к материалам). на дополнительных рисунках 18 и 19 соответственно).
- (г)
Улучшение характеристик материалов в химическом составе аккумуляторов, особенно удельной энергии (запас энергии на единицу веса), может резко снизить потребность в материалах.


 А на карибском острове Синт-Эстатиус (Нидерландские Антилы) с помощью этой технологии резко снизили завоз топлива для дизельных электрогенераторов. Днем местных жителей, их около 4 тысяч, электричеством с 2016 года снабжает солнечная электростанция, а вечером и ночью — ее аккумуляторы, установленные фирмой из ФРГ.
А на карибском острове Синт-Эстатиус (Нидерландские Антилы) с помощью этой технологии резко снизили завоз топлива для дизельных электрогенераторов. Днем местных жителей, их около 4 тысяч, электричеством с 2016 года снабжает солнечная электростанция, а вечером и ночью — ее аккумуляторы, установленные фирмой из ФРГ. Поэтому по такому кабелю с 2020 года подводная высоковольтная линия электропередачи NordLink длиной в 623 километра и мощностью в 1400 МВт будет перебрасывать излишки электроэнергии из ветропарков Северной Германии, где совершенно плоский рельеф, на скалистое побережье Норвегии. И там они будут храниться до востребования.
Поэтому по такому кабелю с 2020 года подводная высоковольтная линия электропередачи NordLink длиной в 623 километра и мощностью в 1400 МВт будет перебрасывать излишки электроэнергии из ветропарков Северной Германии, где совершенно плоский рельеф, на скалистое побережье Норвегии. И там они будут храниться до востребования. Зачем, к примеру, превращать в метан полученный благодаря электролизу водород? Он и сам по себе отличное топливо! Но как транспортировать этот быстро воспламеняющийся газ? Ученые университета Эрлангена-Нюрнберга и фирма Hydrogenious Technologies разработали технологию его безопасной перевозки в цистернах с органической жидкостью.
Зачем, к примеру, превращать в метан полученный благодаря электролизу водород? Он и сам по себе отличное топливо! Но как транспортировать этот быстро воспламеняющийся газ? Ученые университета Эрлангена-Нюрнберга и фирма Hydrogenious Technologies разработали технологию его безопасной перевозки в цистернах с органической жидкостью.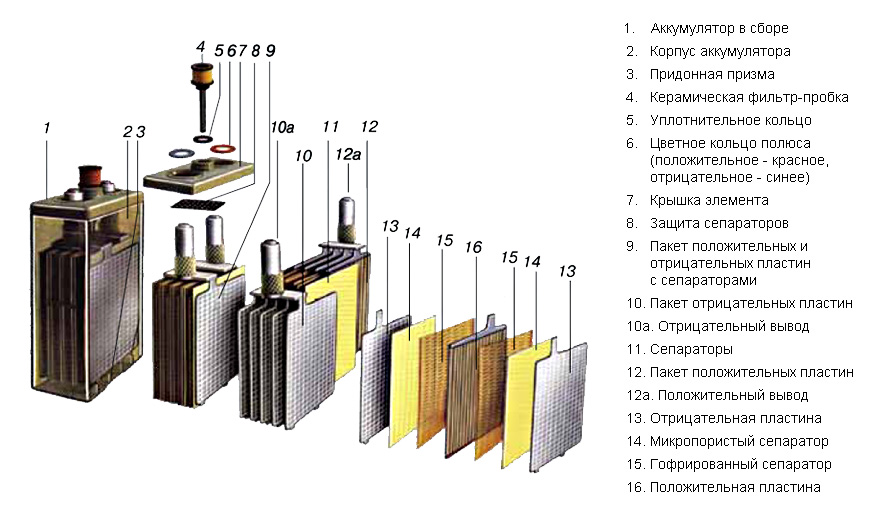 Одну из них энергетическая компания EWE и ученые университета Йены превратили в полигон для испытания технологии хранения электроэнергии в соляном растворе, обогащенном особыми полимерами, которые значительно повышают эффективность химических процессов. По сути дела, речь идет о попытке создать гигантскую подземную батарейку.
Одну из них энергетическая компания EWE и ученые университета Йены превратили в полигон для испытания технологии хранения электроэнергии в соляном растворе, обогащенном особыми полимерами, которые значительно повышают эффективность химических процессов. По сути дела, речь идет о попытке создать гигантскую подземную батарейку. Этому поспособствуют умные сети энергоснабжения (Smart grid): они будут стимулировать подзарядку по низким ценам в моменты избытка электричества. (На фото — заправка для электромобилей в Китае).
Этому поспособствуют умные сети энергоснабжения (Smart grid): они будут стимулировать подзарядку по низким ценам в моменты избытка электричества. (На фото — заправка для электромобилей в Китае).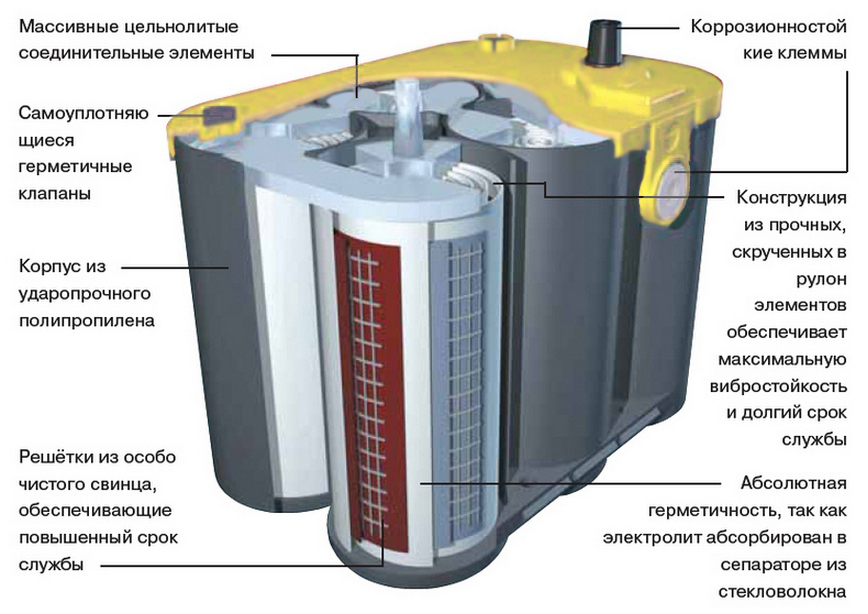 Томск В настоящее время на потребительском рынке вторичных источников тока лидирующее положения (вследствие относительно низкой стоимости) занимают герметичные свинцовые аккумуляторные батареи. Их применяют…
Томск В настоящее время на потребительском рынке вторичных источников тока лидирующее положения (вследствие относительно низкой стоимости) занимают герметичные свинцовые аккумуляторные батареи. Их применяют…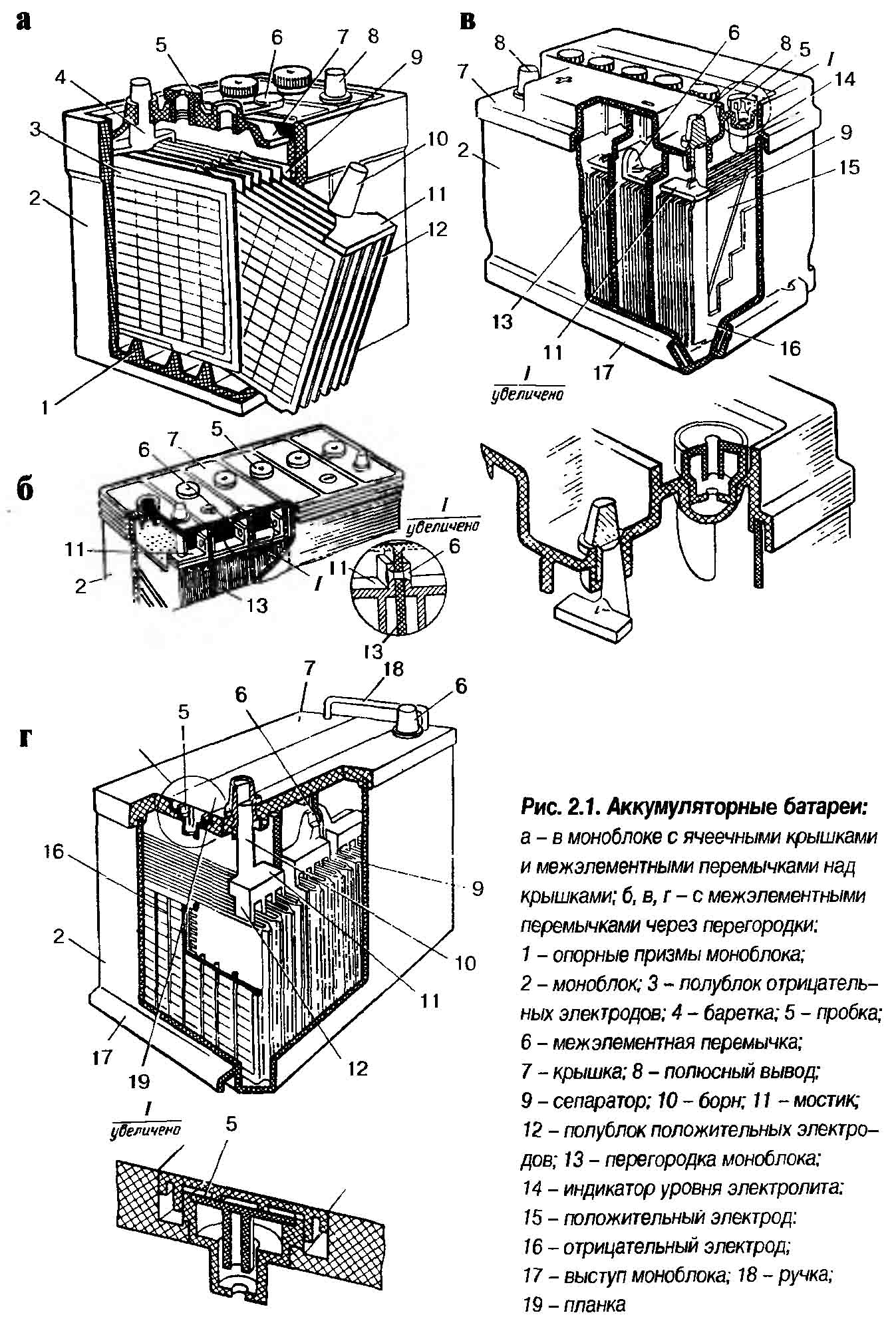 При этом во многих случаях информация эта однобокая — связано это бывает или с недостаточными знаниями…
При этом во многих случаях информация эта однобокая — связано это бывает или с недостаточными знаниями… Это нормальное явление.
Это нормальное явление. Когда ноутбук с заряженным аккумулятором подключается к дополнительным устройствам USB или Thunderbolt извне, аккумулятор также разряжается быстрее.
Когда ноутбук с заряженным аккумулятором подключается к дополнительным устройствам USB или Thunderbolt извне, аккумулятор также разряжается быстрее.
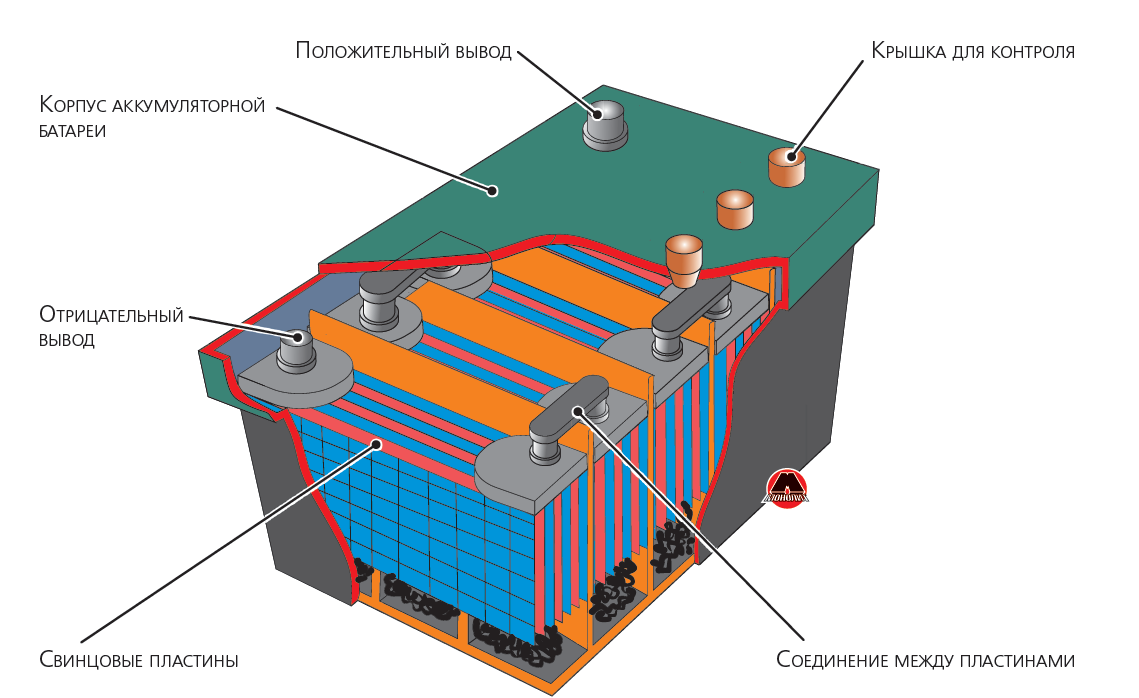 Подзаряжайте аккумулятор каждые три месяца до 50%, чтобы предотвратить повреждение аккумулятора из-за чрезмерной разрядки из-за длительного хранения без использования.
Подзаряжайте аккумулятор каждые три месяца до 50%, чтобы предотвратить повреждение аккумулятора из-за чрезмерной разрядки из-за длительного хранения без использования.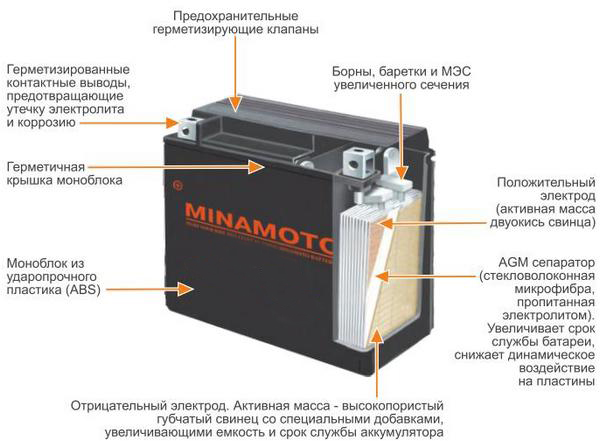
 {\circ} = -0.{\circ} = +0,53\;\text{V} \end{массив}[/latex]
{\circ} = -0.{\circ} = +0,53\;\text{V} \end{массив}[/latex] В то время как емкость аккумулятора определяется многими факторами, такими как запас хода электромобиля, экономия топлива и конфигурации трансмиссии, мы проводим анализ чувствительности для двух крайних ситуаций: 100% BEV с мощностью 110 кВтч (большие внедорожники, такие как Tesla Model S Long Range Plus 37 ). , см. Дополнительную таблицу 25 для состава материалов) и 100% PHEV мощностью 10 кВтч (см. Дополнительную таблицу 26 для состава материалов), чтобы изучить границы будущего спроса на материалы (см. соответствующие совокупные потребности в материалах на рис.4 и дополнительный рисунок 11, см. годовые результаты на дополнительном рисунке 10).
В то время как емкость аккумулятора определяется многими факторами, такими как запас хода электромобиля, экономия топлива и конфигурации трансмиссии, мы проводим анализ чувствительности для двух крайних ситуаций: 100% BEV с мощностью 110 кВтч (большие внедорожники, такие как Tesla Model S Long Range Plus 37 ). , см. Дополнительную таблицу 25 для состава материалов) и 100% PHEV мощностью 10 кВтч (см. Дополнительную таблицу 26 для состава материалов), чтобы изучить границы будущего спроса на материалы (см. соответствующие совокупные потребности в материалах на рис.4 и дополнительный рисунок 11, см. годовые результаты на дополнительном рисунке 10).