Получение водорода — Основы химии на Ида Тен
Содержание статьи
История открытия водорода История водорода начинается с XVI века, когда было замечено, что при действии кислот на железо и другие металлы выделяется некий неизвестный газ. Первоначально его назвали «горючим воздухом». Такое название газ получил из-за способности гореть. Во второй половине XVIII века английский ученый Генри Кавендиш получил водород при действии соляной кислоты HCl на цинк:
Zn + 2HCl = ZnCl2 + h3
Что же такое кислота с точки зрения химии? Кислота – это сложное вещество, в состав которого всегда входят атомы водорода. В формулах кислот атомы водорода принято писать на первом месте. Атомы, следующие в формуле за водородом, называют кислотным остатком. Так, в соляной кислоте HCl кислотный остаток – Cl.
Например, в серной кислоте h3SO4, кислотный остаток – SO4. Кислота – сложное вещество, в состав которого входят атомы водорода и кислотный остаток Генри Кавендиш изучил свойства «горючего воздуха». Он установил, что этот газ намного легче воздуха, а при сгорании на воздухе образует прозрачные капли жидкости. Этой жидкостью оказалась вода.
Генри Кавендиша считают первооткрывателем водорода. Вывод о том, что «горючий воздух» представляет собой простое вещество, был сделан в 1784 году французским химиком Антуаном Лораном Лавуазье. Антуан Лоран Лавуазье дал этому веществу латинское название (Hydrogenium), которое происходило от греческих слов «хюдор» – вода и «геннао» – рождаю. В те годы под элементами подразумевали простые вещества, которые нельзя далее разложить на составные части. Поэтому у химического элемента водорода такое же название, как и у просто вещества h3. Русское слово водород – это точный перевод латинского названия Hydrogenium.
Получение водорода в лаборатории
Современный лабораторный способ получения водорода не отличается от того, которым его получал Генри Кавендиш. Это реакции металлов с кислотами. В лаборатории водород получают в аппарате Киппа (рисунок 152).
Аппарат Киппа изготовляется из стекла и состоит из нескольких частей:
- реакционная колба с резервуаром;
- воронка с длинной трубкой;
- газоотводная трубка.
Реакционная колба имеет верхнюю шарообразную часть с отверстием, в которое вставляется газоотводная трубка, снабженная краном или зажимом, и нижний резервуар в виде полусферы. Нижний резервуар и реакционная колба разделены резиновой или пластиковой прокладкой с отверстием, через которое проходит в нижний резервуар длинная трубка воронки, доходящая почти до дна. На прокладку через боковое отверстие шпателем насыпают твёрдые вещества (мрамор, цинк). Отверстие закрывается пробкой с газоотводной трубкой. Затем при открытом кране или зажиме в верхнюю воронку заливается раствор кислоты. Когда уровень жидкости достигает вещества на прокладке, начинается химическая реакция с выделением газа. При закрытии крана давление выделяющегося газа выдавливает жидкость из реактора в верхнюю часть воронки. Реакция прекращается. Открытие крана приводит к возобновлению реакции. Поместим в реакционную колбу кусочки цинка. В качестве кислоты воспользуемся серной кислотой. При контакте цинка и серной кислоты протекает реакция:
Zn + h3SO4 = ZnSO4 + h3
Водородом можно заполнить мыльный пузырь.
Для этого необходимо опустить газоотводную трубку в мыльный раствор. На конце трубки начнется формирование мыльного пузыря, заполненного водородом; со временем пузырь отрывается и улетает вверх, что доказывает легкость водорода. Соберем выделяющийся водород. С учетом того, что водород намного легче воздуха, для сбора водорода сосуд, в котором собирается газ, необходимо располагать вверх дном, или производить собирание методом вытеснения воды. Как обнаружить водород? Заполним пробирку водородом, держа ее вверх дном, по отношению к газоотводной трубке. Поднесем пробирку отверстием к пламени спиртовки – слышится характерный хлопок.
Хлопок – это признак того, что в пробирке содержится водород. При поднесении пробирки к пламени водород вступает в реакцию с кислородом, содержащимся в воздухе. При малых количествах реакция кислорода и водорода сопровождается хлопком. Более подробно об этой реакции будет рассказано в следующем параграфе.
Получение водорода в промышленности
Одним из промышленных способов получения водорода является реакция разложения воды под действием электрического тока:
2h3O эл.ток → 2h3 + O2.
Данный метод позволяет получить чистый водород и кислород. Процесс превращения химических веществ в другие вещества под действием электричества называется электролизом.
Электролиз – химическая реакция, протекающая под действием электрического тока Проведем электролиз воды. В стакан наполненный водой, опустим металлические электроды. Поверх электродов опустим в стакан пробирки, заполненные водой. Подсоединим электроды к источнику тока – батарейке. В пробирках наблюдается выделение газов – водорода и кислорода, которые вытесняют воду. Наблюдая за процессом электролиза, можно заметить, что в одной из пробирок газа собирается в два раза больше, чем в другой. Проанализировав уравнение реакции электролиза воды, можно сделать вывод, в какой пробирке выделяется водород, а в какой – кислород. Попробуйте это сделать самостоятельно.
Существуют и другие способы получения водорода. Железо-паровой метод долгое время широко применялся в промышленности. Через электрическую трубчатую печь проходит трубка из нержавеющей стали, заполненная железными стружками. Через трубку с железными стружками пропускают водяной пар. При температуре около 800°С пары воды взаимодействуют с железом, образуя оксид Fe3O4 (железную окалину) и газообразный водород:
3Fe + 4Н2О = 4Н2 + Fe3O4.
Можно получить Н2, пропуская Н2О через слой раскаленного угля. При этом образуется смесь двух газов – СО и Н2 (водяной газ):
Н2О + С = CO + Н2
В настоящее время водород получают взаимодействием углеводородов (в основном метана, СН4) с водяным паром или неполным окислением метана кислородом:
СН4 + Н2О = СО + 3Н2
2СН4 + О2 = 2СО + 4Н2
Итог статьи:
- В лаборатории водород получают в аппарате Киппа
- Исходными веществами для получения водорода в лаборатории являются некоторые металлы и кислоты
- Собирать водород нужно методом вытеснения воды, или методом вытеснения воздуха, расположив пробирку вверх дном по отношению к газоотводной трубке
- Кислота – сложное вещество, в состав которого входят атомы водорода и кислотный остаток
- Обнаружить водород можно по характерному хлопку при поднесении пробирки с водородом к пламени
- Одним из промышленных способов получения водорода является электролиз воды
- Электролиз – химическая реакция, протекающая под действием электрического тока
Получение водорода — Знаешь как
 Рис. 56. Шарик натрия на поверхности воды
Рис. 56. Шарик натрия на поверхности воды
Атом водорода состоит из ядра и одного электрона. С атомами металлоидов атомы водорода образуют ковалентные связи, более или менее поляризованные. В некоторых из этих соединений (Н2O, НСl и др.) состояние атома водорода приближается к ионизированному Н+.
Главным источником получения водорода служит вода. Для получения из нее водорода можно воспользоваться способностью многих металлов вытеснять из воды водород с одновременным образованием гидроокисей или окисей взятых металлов. Особенно легко уже при обыкновенной температуре взаимодействуют с водой щелочные металлы натрий и калий, а также кальций, барий и др.
Если кусочек натрия бросить в чашку с водой, то происходит энергичная реакция; натрий с шипением начинает двигаться по поверхности воды, вытесняя из нее водород. При этом образуется так много тепла, что натрий плавится и превращается в шарик, который быстро уменьшается в размерах и вскоре исчезает (рис. 56). Иногда разогревание столь сильно, что выделяющийся водород загорается.
Взаимодействие натрия с водой выражается уравнением
2Na + 2Н2O = 2NaOH + Н2
Сущность этой реакции заключается в отдаче электрона атомом натрия одному иону водорода из молекулы воды. Атомы натрия превращаются при этом в положительно заряженные ионы, в виде которых и входят в состав NaOH, а ионы водорода превращаются в атомы, связывающиеся затем попарно с образованием молекул Н2. Аналогично протекает реакция с калием и кальцием.
Кроме указанных металлов, с водой могут взаимодействовать и другие металлы, но уже при более высоких температурах. Так, магний вытесняет водород из воды при температуре ее кипения, цинк и железо только при накаливании их в струе водяного пара. Во всех этих случаях водород, находящийся в состоянии, близком к ионизированному, получает электроны от атомов металла и превращается в нейтральные атомы.
В промышленности для получения водорода из воды пользуются следующими методами.
Конверсионный метод является наиболее распространенным методом получения водорода, особенно идущего на синтез аммиака. При работе по этому методу сквозь слой раскаленного угля пропускают водяной пар. Образующаяся при этом смесь окиси углерода с водородом носит название водяного
г а з а и может применяться как газообразное топливо . Если процесс ведется с целью получения водорода, то для удаления из полученной смеси окиси углерода водяной газ пропускают вместе с водяным паром над раскаленной окисью железа, служащей катализатором. Окись углерода взаимодействует с водяным паром, образуя водород и углекислый газ. Эта реакция, называемая конверсией окиси углерода, выражается уравнением
(Н2) + СО + Н2О ⇄ СО2 + Н2 + (Н2) + 10 ккал
При низких температурах равновесие сдвинуто вправо, а с повышением температуры смещается в сторону образования исходных веществ.
Так как реакция протекает с достаточной скоростью только при температурах не ниже 450°, то для повышения степени конверсии окиси углерода водяной пар добавляют к водяному газу в количестве, значительно большем, чем это следует из уравнения реакции, благодаря чему равновесие, несмотря на высокую температуру, остается сильно сдвинутым вправо.
Образовавшийся в результате конверсии углекислый газ отделяют от водорода, промывая газовую смесь водой, под давлением 20 ат. Для окончательной очистки водород пропускают еще через ряд растворов, поглощающих все примеси.
При работе по конверсионному методу вместо водяного газа часто пользуются другими газами, содержащими окись углерода, в частности генераторным газом.
Железо-паровой метод является наиболее старым из методов получения водорода, утратившим в настоящее время свое былое значение. Метод основан на взаимодействии железа с водяным паром при пропускании последнего над накаленными железными стружками:
3Fe + 4Н2О ⇄Fe3О4 + 4Н2 + 35,3 ккал
Реакция обратима и в направлении слева направо идет с выделением тепла. Следовательно, в соответствии с принципом Ле-Шателье, чем ниже температура, тем сильнее равновесие должно быть сдвинуто в сторону образования водорода. Однако при низких температурах из-за малой скорости реакции равновесие устанавливается слишком медленно. Поэтому на практике реакцию ведут при температурах не ниже 700°. При 700° равновесная смесь содержит приблизительно равные объемы водорода и водяного пара, т. е. половина пропускаемого пара остается неиспользованной. Так как образующийся водород вместе с избытком водяного пара сейчас же удаляется из сферы реакции, то процесс идет непрерывно до тех пор, пока все железо не превратится в окалину. Образовавшуюся окалину восстанавливают затем водяным газом и снова пускают в реакцию.
Электрохимический метод получения водорода
При наличии дешевой электрической — энергии экономически целесообразно получать водород из воды, разлагая ее электрическим током. Преимуществом этого метода является высокая степень чистоты получаемого водорода, что исключает необходимость в весьма сложных устройствах для его очистки от примесей. Кроме того, с электролизом воды в настоящее время связано и получение тяжелой воды, необходимой для ядерных реакторов.
Электрохимическим методом получают около 18% мировой продукции водорода.
Некоторое количество водорода получается также методом глубокого охлаждения коксового газа. При нагревании каменного угля без доступа воздуха до 900—1200° образуется так называемый коксовый газ — смесь, содержащая около 50—60% водорода; твердый остаток представляет собой кокс. Для выделения водорода из коксового газа последний подвергают глубокому охлаждению. При этом все газы, кроме водорода, переходят в жидкое состояние и таким путем отделяются от водорода.
За последние двадцать лет в качестве источника получения водорода стал широко применяться метан, содержащийся в природных газах и газах переработки нефти. В 1940 году в США из нового вида сырья было получено 5% водорода, идущего на синтез аммиака, в 1945 году — уже 45%, а в 1953 году—-66%.
Получение водорода из метана можно осуществить разными способами:
1) термическим разложением метана:
СН4 = С + 2Н2 + 18 ккал
2) взаимодействием метана с водяным паром:
СН4 + Н2О = СО + 3Н2 — 49 ккал
3) взаимодействием метана с двуокисью углерода или со смесью двуокиси углерода я водяного пара:
СН4 + СО2 = 2СО + 2Н2 —60,1 ккал
3СН4 + СО2 + 2Н2О = 4СО + 8Н2 — 158,6 ккал
4) неполным окислением метана:
2СН4 + О2 = 2СО + 4Н2 + 16,1 ккал
При всех этих способах, кроме первого, получаются газовые смеси с сравнительно высоким содержанием окиси углерода. Для увеличения выхода водорода эти смеси вместе с водяным паром подвергают конверсии.
Если водород не используют непосредственно на месте получения, то его транспортируют в сжатом состоянии в стальных баллонах, где он находится под большим давлением.
В лабораториях водород обычно получают действием разбавленной серной или соляной кислоты на цинк:
Zn + H2SО4 = ZnО4 + Н2
Вместо цинка можно взять железо, но в этом случае реакция идет гораздо медленнее.
Водород, получающийся при действии кислот на цинк и другие металлы, всегда содержит пары воды, а также некоторые газообразные примеси. Если нужен сухой водород, то получающийся газ освобождают от водяных паров, пропуская через концентрированную серную кислоту, жадно поглощающую влагу. Для удаления других примесей пользуются растворами различных солей.
65 66 67
Вы читаете, статья на тему Получение водорода
Производство водорода в промышленности — Знаешь как
Производство водорода
Содержание статьи
 Что такое производство водорода это процесс получения газа из водород содержащих веществ (вода). Один из самых востребованных это ее электролиз, в результате получается химически чистый водород.
Что такое производство водорода это процесс получения газа из водород содержащих веществ (вода). Один из самых востребованных это ее электролиз, в результате получается химически чистый водород.
В лабораторных условиях технический водород может быть получен реакцией кислот на металлы или электролизом воды.
Большие количества водорода применяются как сырье для синтеза аммиака и метанола, гидрогенизации жиров, производства бензина из угля, для селективного автоклавного восстановления цветных металлов из аммиачных растворов, восстановления руд и др. Кроме того, водород применяют для создания необходимой атмосферы в печах, для резки и сварки металлов, в качестве охлаждающего реагента в мощных генераторах электрического тока и т. д.
Промышленные способы получения водорода подразделяются на физические, химические и электрохимические.
Электрохимический способ получения водорода основан на электролитическом разложении воды. Этот метод может иметь преимущества перед другими методами там, где по условиям технологии требуется газ высокой чистоты, не содержащий каталитических ядов, либо при наличии дешевой электроэнергии. Малые количества водорода, требуемые постоянно или периодически, целесообразно во всех случаях получать электролизом, как наиболее простым из известных способов.
Впервые процесс электролиза воды наблюдали Труствик и Диманн в 1789 г. Первые конструкции промышленных электролизов с моно- и биполярными электродами, а также работающих при повышенных давлениях, были разработаны в 1888 г. Д. А. Лачиновым.
Электролит для получения водорода
При электролизе чистой воды на катоде выделяется водород, а на аноде — кислород. Однако удельная электропроводность чистой воды столь незначительна, что ее электролиз будет сопровождаться огромным расходом энергии. Следовательно, для практических целей в воду необходимо ввести электропроводящую добавку — кислоту, соль или щелочь. По электропроводности кислоты и щелочи имеют преимущество перед солями. Кислоты более электропроводны чем щелочи, а соли обладают меньшей удельной электропроводностью, чем кислоты и щелочи.
В щелочных растворах простые конструкционные материалы железо и обычные стали —оказываются вполне стойкими. Поэтому в промышленности для электролиза воды применяют исключительно щелочные электролиты.
Недостатком щелочных электролитов является снижение их электропроводности со временем, связанное с превращением гидроокиси в карбонат под действием СО2 воздуха.
К материалам для электродов предъявляется еще одно требование — перенапряжение выделения водорода и кислорода на них должно быть по возможности мало. Наилучший катодный материал — платинированная или гладкая платина. Однако, из-за высокой стоимости платину в качестве электродного материала не применяют. Металлы группы железа, устойчивые в щелочах, обладают и невысоким перенапряжением. Перенапряжение на железе и кобальте на несколько десятков милливольт меньше, чем на никеле.
Катодные процессы получения
В щелочных растворах выделение водорода происходит за счет присоединения электрона к молекуле воды:
2Н2О+2е→ Н2+2ОН—
Зависимость скорости этой реакции (силы тока I) от перенапряжения (η>0) выражается уравнением:
η = a + ((RT):(αF))lnI
где а — постоянная; R — газовая постоянная; Т — температура, °К; F — постоянная Фарадея; α — коэффициент переноса.
Из уравнения следует, что при прочих равных условиях перенапряжение пропорционально константе а, зависящей от материала электрода. Влияние материала электрода уже было рассмотрено выше. Здесь необходимо отметить следующее. Константа а по физическому смыслу есть перенапряжение при плотности тока, равной единице (1 а/см2). Но плотность тока мы относим к единице видимой поверхности электрода («габаритная» плотность тока), а в формулу входит истинная плотность тока. Следовательно, качество поверхности должно существенно сказываться на величине перенапряжения. Если поверхность имеет развитый рельеф, то каждой единице видимой поверхности будет соответствовать значительно большая истинная поверхность и при той же габаритной плотности тока истинная плотность тока будет в соответствующее число раз меньше.
Существует несколько способов получения высокоразвитой поверхности катодов. Увеличить истинную поверхность можно наждачной обработкой. Такая обработка стального катода снижает перенапряжение выделения водорода при плотности тока 1000 а/м2 и температуре 60—80° С на 0,2 в.
Вторым способом увеличения истинной поверхности является гальваническое осаждение на электроды металлов в виде губки. Этим удается снизить перенапряжение примерно на 0,3—0,4 в. Впрочем, катоды электролизных ванн спустя некоторое время работы самопроизвольно покрываются слоем губчатого железа, осаждаемого током в. процессе электролиза, так как вследствие коррозии аппаратуры в растворе появляются ионы железа, хотя и в очень малых количествах. Было предложено также гальванически покрывать катоды никелем, причем вести электролиз из раствора с добавкой роданистой соли. При этом в катодном осадке оказывается до 20% серы, которая затем выщелачиваясь в раствор, создает высокоразвитую поверхность электрода. Перенапряжение выделения водорода в результате этого может быть снижено в условиях опытов на 0,3—0,4 в.
Перенапряжение пропорционально логарифму плотности тока, т.с. с ростом плотности тока оно сперва растет быстро, а затем все медленнее и медленнее. Следовательно, рост напряжения на ванне с увеличением плотности тока в области малых плотностей тока будет большим, чем в области больших плотностей тока.
Повышение температуры снижает перенапряжение и увеличивает скорость электродной реакции. В реальных условиях возрастание температуры на 1 град снижает перенапряжение примерно на 2—3 мв.
В щелочном электролите нет катионов, которые могли бы разряжаться на катоде и приводить к появлению других электродных реакций, кроме реакции образования газообразного водорода. Единственной побочной реакцией, которая может протекать на катоде, является реакция электровосстановления растворенного кислорода:
О2+2Н2О + 4е → 4ОН—
Эта реакция протекает при значительно более положительных потенциалах, чем реакция катодного образования водорода. Однако ее скорость ограничивается малой растворимостью кислорода в щелочных растворах особенно при высоких температурах. На нее обычно тратятся всего лишь доли процента тока. Поэтому естественно, что электролизные ванны всегда работают с очень высокими катодными выходами по току (порядка 97—98% с учетом утечек тока).
Анодный процесс
Процесс выделения кислорода на аноде сопровождается окислением материала анода. Поэтому при длительном электролизе разряд анионов идет не на металле, а на окисленной поверхности электрода. На величину перенапряжения выделения кислорода оказывает влияние природа поверхностных окислов и прочность связи кислород — металл. С течением времени перенапряжение выделения кислорода несколько повышается пока не достигнет через длительный промежуток времени постоянного значения. Поэтому величина анодного потенциала в промышленной, длительно работающей ванне, более положительна, чем та, которую определяют в лабораторных условиях. По данным Я. И. Турьяна, эта разница для промышленных плотностей тока составляет 0,15—0,18 в.
Побочные реакции на аноде отсутствуют.
Электролит электроды диафрагмы
Для выбора оптимальной концентрации щелочи необходимо знать зависимость удельной электропроводности растворов от концентрации при различных температурах. Кривые, выражающие эту зависимость, при всех температурах проходят через максимум. С повышением температуры максимумы сдвигаются в сторону больших концентраций щелочи. При 70° С, что близко к температуре электролита в промышленных ваннах, максимальной электропроводностью обладают 22% раствор NaOH и соответственно 32% раствор КОН. Однако применяют 16—18% растворы NaOH и 25—29% растворы КОН. Этим, не снижая существенно удельную электропроводность раствора, уменьшают расход щелочи на приготовление электролита и восполнение потерь, а также достигают некоторого снижения агрессивности среды, ибо в концентрированных растворах щелочей коррозия хотя и невелика, но все же более заметна. Для еще большего подавления коррозии в электролит обычно добавляют пассиватор —K2Cr2O7, из расчета ~2 г/л электролита, заливаемого в ванну.
Максимальная электропроводность раствора КОН больше, чем NaOH, но стоимость NaOH меньше. Поэтому как КОН, так и NaOH одинаково могут быть использованы в электролизных ваннах.
Оно оказывается прямо пропорционально силе тока, проходящего через электролит, или плотности тока. Эта величина сильно зависит от материала электрода и высоты электродов.
Величину газонаполнения нельзя рассчитать теоретическим путем. Поэтому приходится определять газонаполнение экспериментально в каждом конкретном случае и затем рассчитывать значение К по формуле. При конструировании электролизеров стремятся создать условия, обеспечивающие величину газонаполнения не выше 15—20%.
Снижение напряжения на ванне при работе с кобальтированными железными катодами объясняется не только меньшим перенапряжением выделения водорода на кобальте, но и меньшим газонаполнением катодного пространства.
При электролизе щелочных растворов с электродами из металлов группы железа анодное пространство оказывается мало заполненным пузырьками газа. Наоборот, на катоде образуются очень мелкие пузыри, которые пронизывают всю толщу раствора, резко повышая его сопротивление. Это явление не может быть объяснено тем, что на катоде выделяется водорода в 2 раза больше, чем на аноде кислорода. Объясняется это явление тем, что в условиях электролиза с никелевыми или железными электродами потенциал катода более удален от потенциала нулевого заряда поверхности металла электрода, чем потенциал анода. Поэтому смачиваемость катода больше, чем анода и на катоде дипольные молекулы воды более интенсивно выталкивают пузырьки с поверхности.
Методы борьбы с газонаполнением электролита различны. В некоторой степени снижение газонаполнения удается осуществить повышением температуры. Целесообразно, несмотря на высокую стоимость кобальта, железные катоды гальванически покрывать слоем кобальта. Но эти способы не дают радикального решения вопроса. Поэтому снижение газонаполнения в основном проводят по линии создания таких конструкций электродов, которые позволяли бы удалять газы из межэлектродного пространства.
Если вести электролиз между двумя плоскими электродами, то весь объем выделяющихся газов будет проходить между электродами и повышать сопротивление электролита, находящегося между ними. Электролиз с такими электродами удается вести при невысоких катодных плотностях тока (200—300 а/м2).
Было предложено много различных конструкций электродов, позволяющих газам уходить из межэлектродного пространства . Однако все они не получили большого распространения.
Эффективное удаление газа происходит при циркуляции электролита внутри ячейки, основанной на разности плотностей электролита с газовыми пузырьками и без них. Такую циркуляцию можно создать, применяя «двойные электроды», состоящие из двух плоских листов, скрепленных друг с другом с небольшим зазором. Работающими сторонами электрода являются только наружные поверхности. Внутренние поверхности не работают, и электролит между листами остается свободным от газовых пузырьков. Плотность электролита с наружной стороны электрода, благодаря наличию газовых пузырьков, оказывается меньше плотности электролита между листами. Поэтому электролит между листами, опускаясь вниз, выталкивает электролит с газовыми пузырьками наверх. Образуется довольно интенсивная циркуляция электролита, способствующая выносу газовых пузырьков и, следовательно, снижению газонаполнения.
Наибольшее распространение получили вынесенные вперед перфорированные или сетчатые (однослойные и многослойные) электроды, работающие по принципу двойных электродов.
Во всех типах промышленных ванн для разделения газов применяются диафрагмы, которые изготовляют из асбестовой ткани. Роль диафрагмы — воспрепятствовать смешению газов. Разделение азов должно быть достаточно полным, ибо при смешении газов не только теряются продукты электролиза, но и образуются взрывоопасные, смеси. Смеси оказываются взрывоопасными, если в кислороде содержится более 5% водорода, или в водороде более 5,7% кислорода. Вместе с тем диафрагма должна быть достаточно пориста для того, чтобы падение напряжения в ней было незначительно.
Электролиз воды под давлением
Во многих случаях промышленной практики (синтез аммиака, заполнение баллонов сжатым газом и др.) желательно получать газы под давлением. Получение компримированных газов непосредственно из электролизеров значительно сокращает стоимость оборудования, так как делает ненужным применение отдельных компрессорных установок. Предельное, теоретически возможное, давление при электролизе воды составляет около 1860 атм. При этом давлении объем газов равняется объему воды, из которой они получены.
С ростом давления напряжение разложения увеличивается. Действительно, зависимость равновесных потенциалов водородного и кислородного электродов от давления.
Исследования электролиза воды под давлением показали, что такой процесс возможен. При этом было обнаружено, что напряжение на ванне, работающей под давлением, не увеличивалось, а, наоборот, в ряде случаев при повышении давления до 50 атм несколько снижалось. Это явление, согласно исследованиям В. В. Ипатьева с сотрудниками, объясняется тем, что, при электролизе под давлением, объем, занимаемый выделяющимися газами, уменьшается, а это снижает газонаполнение электролита и диафрагмы и уменьшает их сопротивление. Последний фактор перекрывает рост напряжения разложения с повышением давления. На практике оказывается затруднительным вести электролиз при давлениях выше 10—20 атм. Для работы при этих давлениях используются тщательно выполненные и надежно собранные фильтрпрессные электролизеры.
Статья на тему Производство водорода и кислорода
Урок 26. Получение водорода и его применение – HIMI4KA
В уроке 26 «Получение водорода и его применение» из курса «Химия для чайников» узнаем о получении водорода в лабораториях и в промышленности, а также выясним в каких отраслях промышленности его применяют.


Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
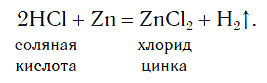
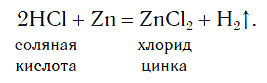
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
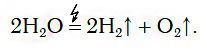
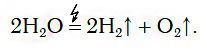
Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
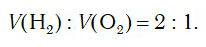
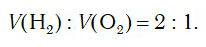
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
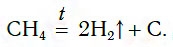
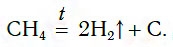
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
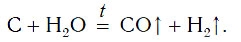
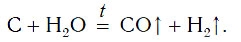
Существуют и другие промышленные способы получения водорода.
Применение водорода
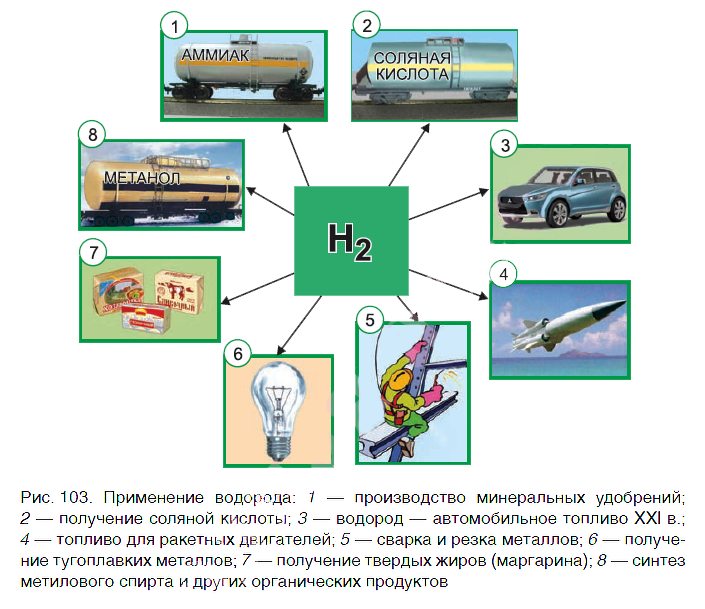
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 оС. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.

В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
- В лаборатории водород получают действием кислот на металлы.
- В промышленности для получения водорода используют доступное и дешевое сырье — природный газ, воду.
- Водород — это перспективный источник энергии XXI в.
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Конкурс — Получение водорода тремя способами
Получить водород! До недавнего времени это была моя мечта 🙂 . И я твёрдо решил осуществить ее.
В магазине я приобрёл все необходимые реактивы:
Далее заперся в своей комнате и начал творить! В итоге я в домашних условиях смог повторить все нижеописанные способы получения водорода. И я просто обязан поделиться с вами своими знаниями. Итак, три способа получения водорода.
Способ №1 и все необходимые для него реактивы.
1 Сульфат меди (медный купорос ) его можно купить в любом цветочном магазине ( внимание не путайте с лавками где продоются только цветы нужен магазин с удобрениями ) просто зайдите и скажите что вам нужен медный купорос
2 Обычная пищевая соль
3 фольга (если честно то подойдёт любое алюминиевое изделие будь то ложка или проволока)
Вот собственно и все реактивы. Теперь немного о посуде в которой мы всё это будем делать.
Your ads will be inserted here by
Easy AdSense Pro.
Please go to the plugin admin page to paste your ad code.
1 Бутылка из толстого стекла ( отлично подойдёт из под вина, пива или шампанского )
2 Кострюля с холодной водой .
Для чего нужно было именно из толстого стекла и с холодной водой? А нужно это поскольку при данной реакции выделяется большоё количество тепла и бутылка может треснуть или вовсе лопнуть.
А теперь начнём!!!! Насыпаем в бутылку примерно четыре ложки сульфата меди и столько же соли ( соли желательно брать немного больше ) добавим воды и всё это тщательно перемешиваем. Если всё сделано правильно то раствор должен стать зелёным, если нет, то добавьте ещё соли. Раствор готов! Начнём кидать туда алюминий ИИИИИИИ УРА-УРА начал выделяться водород, при этом алюминий начнёт ржаветь , а вода начнёт пузыриться.
Но как-же это происходит, как идёт реакция??? Дело в том что образующися хлорид меди смывает защитную пленку с алюминия и на равне с восстановлением меди идет образование водорода.
Способ № 2 и реактивы.
- Гидроксид натрия. Раньше я незнал где его купить, но потом узнал что он продоётся как средство для прочистки труб — крот в любом магазине бытовой химии.
- Алюминий ( ну вы поняли).
Ну бутылка и вода как в способе №1
Нальём крота в бутылку(если у вас сухой и в гранулах, то разбавьте водой ) . Добавим алюминий (его лучше обжечь на костре перед добавлением). Через минуты две начнётся очень бурная реакция с выделением водорода в больших количествах.
Внимание!!!!!!!! Второй способ ООООчень опасный, советую проделывать его в перчатках( Гидроксид натрия сильно разъедает кожу!!!). Перчаток у меня не нашлось и я делал без них. Потом сильно пожалел. К вечеру у меня все руки были КРАСНЫМИ! и безумно болели. Но самая большая опасность в этой реакции это ВОДОРОД!!!!Его выделяется много!!!! И вообще я не советую проводить этот способ в домашних условиях!!!!
Тут всё тоже самое, только едкая щелочь намного быстрее смывает защитную плёнку с алюминия и далее идёт реакция с выделением водорода
Способ №3.
В этом способе не нужно реактивов. Ну кроме поваренной соли. Этот опыт будет проводится с помощью электролиза. Всё что нужно это пропустить через раствор поваренной соли электричество.Ток должен быть постоянным. ( Водород будет выделяться на аноде, а на катоде небольшие количества кислорода
ПОДЕЛИТЕСЬ С ДРУЗЬЯМИ!
Получение водорода электролизом воды / Статьи и обзоры / Элек.ру
Получение чистого водорода путем электролиза воды — самая очевидная и эффективная технология, и один из наиболее перспективных способов получения альтернативного топлива. Водород добывают из любого водного раствора, а при сгорании он превращается обратно в воду.
По сравнению с прочими методами получения водорода, электролиз воды отличается целым рядом преимуществ. Во-первых, в ход идет доступное сырье — деминерализованная вода и электроэнергия. Во-вторых, во время производства отсутствуют загрязняющие выбросы. В-третьих, процесс целиком автоматизирован. Наконец, на выходе получается достаточно чистый (99,99%) продукт. Из всех методов электролиза наиболее перспективным считают высокотемпературный электролиз (себестоимость водорода от 2,35 до 4,8 $/кг). Его следует иметь на технологическом вооружении, поскольку при определенных экономических условиях он может быть использован в крупнопромышленном масштабе.
Электролизом воды называется физико-химический процесс, при котором под действием постоянного электрического тока дистиллированная вода разлагается на кислород и водород. В результате разделения на части молекул воды, водорода по объему получается вдвое больше, чем кислорода. Эффективность электролиза такова, что из 500 мл воды получается около кубометра обоих газов с затратами около 4 квт/ч электрической энергии.
Технологический ток для протекания процесса электролиза воды для получения водорода и кислорода получается, как правило, при помощи промышленного выпрямителя с необходимыми рабочими параметрами, Обычно это напряжение до 90В и силой тока до 1500 А. Подходящим агрегатом является Пульсар СМАРТ.
На электронном дисплее выпрямителя Пульсар СМАРТ или в специальном ПО для компьютера можно контролировать все стадии процесса производства, что позволяет оператору следить за параметрами, и круглосуточно журналировать протекание технологического процесса. Полностью автоматическая работа, включающая непрерывный мониторинг всех параметров для безаварийного функционирования без надзора оператора. Все параметры, касающиеся напряжения и силы тока постоянно измеряются и контролируются микропроцессором выпрямителя. Более того, все контролируемые параметры фиксируются устройством, которое в случае сбоя или отклонения может автоматически остановить процесс и сигнализирует об этом при помощи световой колонны.
Выпрямители тока серии Пульсар СМАРТ разработаны в соответствии с самыми высокими требованиями промышленной эффективности и международными стандартами. При этом технологическое программное обеспечение допускает гибкую адаптацию к требованиям Заказчика, и постоянно совершенствуется.
Получение водорода. Установки получения (производства) водорода.
Общее описание
- Генератор водорода
- Установка оборудована 2 пакетами элементов для производства водорода 30 нм³/ч
- Контейнер модернизирован и подготовлен для увеличения производительности в будущем до 45 нм³/ч. Так же если в будущем потребуется дополнительно увеличить мощность, то контейнер рассчитан на увеличение до 60 нм³/ч.
- Модуль хранения объемом 50 м³ по воде для хранения 450 нм³ водорода при 10 бар.
Предложенная нами система включает стандартные встроенные системы безопасности, стандартное заводское приемочное испытание и комплект технической документации.
Услуги на месте включают: пуск системы, ввод в эксплуатацию и обучение на месте. Строительные работы и подготовка площадки, выполняемые на месте, осуществляются заказчиком в соответствии с требованиями.
Энергоисточники (вода, электричество, азот, воздух КИП,…) должны быть доступны на месте.
Характеристики электролизера:
- Полностью автоматическая работа
- Полный контроль получения водорода
- Производство под давлением (10 бар изб.) без установки компрессора
- Высокая эффективность и надежность
- Очень низкие затраты на техническое обслуживание (ограниченное число подвижных деталей, без насоса для электролита)
- Водород не содержит углерода – без вредных выбросов
- Производственный процесс сертифицирован по ISO 9001, 14001
- Услуги по пуску и пост-продажному обслуживанию
Введение
Установка производства водорода в контейнерном исполнении для установки снаружи представляет собой комплексную установку производства водорода с производительностью по водороду 60 нм³/ч при чистоте 99,998% и давлении 10 бар (изб.)
Разработан модифицированный ISO контейнер повышенной вместимости для размещения генератора водорода и всего его питающего оборудования.
Ввод оборудования для наружного размещения в эксплуатацию на площадке заказчика тем самым значительно облегчен по сравнению с установкой в существующее помещение генератора на базе скида.
Надежность
Используя принцип внедрения технологического уровня эксплуатационной безопасности оборудования каждая установка помимо прочего обладает следующими характеристиками:
- минимальное присутствие газа в системе
- определение минимального давления для предотвращения попадания воздуха
- система непрерывного мониторинга/обнаружения водорода в атмосфере
- система защитной вентиляции зона II (только с кожухом или корпусом (каркасом) для наружного размещения)
- надежная логическая схема для всех параметров
- Система бесперебойного питания, обеспечивающая безопасное отключение в случае аварийного отключения питания
- Система постоянного мониторинга, чистота производства О2 газа
- Системы множественного / параллельного управления
- Многократное резервирование параметров, которые являются критичными в рамках безопасности системы
Автоматизация
Надежность – это одно из наиболее значимых требований для наших заказчиков. Установка разработана для полностью непрерывной эксплуатации с минимальной потребностью в присутствии оператора, обеспечивая константный поток водорода.
- Система контроля давления: Человеко-машинный интерфейс на панели управления позволяет операторы выбрать требуемое давление газа (между 8 и 10 бар изб.). Установка автоматически регулирует свою производительность с тем, чтобы обеспечить установленное давление.
- Автоматизация охлаждения: охлаждающая вода поступает в теплообменники через клапан, регулируемый ПЛК. При повышении температуры клапан открывается, тем самым подавая большее количество охлаждающей воды в контур. В результате этого – стабильная производственная температура.
- Автоматическая продувка азотом: следуя принципам системы, продувка азотом требуется перед запуском установки при внутреннем давлении ниже 15 кПа. Процесс продувки регулируется ПЛК системы путем активации клапана в последовательном процессе.
- Удаленный I/O: используя современное соединение PROFIBUS, мы значительно уменьшили количество соединительных кабелей и соответственно время, необходимое на установку. Внедрение прокола в комбинации с безопасным ПЛК и безопасным I/O позволяет системе полностью соответствовать самым строгим актуальным нормам и стандартам безопасности. ПЛК автоматически диагностирует любые ошибки передачи данных, не только делая систему безопаснее, но также сокращая время и силы на устранения неполадок.
Объем поставки
Сенсорный экран с человеко-машинным интерфейсом (HMI)
Экран HMI расположен на панели управления и позволяет оператору контролировать и эксплуатировать электролизер либо с экрана, либо с удаленного соединения, через защищенное соединение VPN. Система мониторинга включает в себя запись данных на компактную флэш карту. Она также позволяет нашим техническим специалистам подключаться к электролизеру, для диагностики и исправления случаев неисправностей и тревожной сигнализации при необходимости.
Исполнение контейнера
ISO 40’ футовый контейнер спроектирован и модифицирован для размещения водородной установки 60 нм³/ч и включает:
- изолированные стенки и перекрытия
- пол из металлических листов
- запираемые двери во внешних стенках
- Освещение во всех отсеках
- Все устройства полностью оснащены и установлены на место вкл. трубную обвязку и кабели, что значительно сокращает время и затраты на установку / межсоединения на месте.
- Два вытяжных вентилятора, которые вытягивают воздух через технологическое помещение из помещения общего назначения. Первый обеспечивает минимальный поток и работает постоянно. Поток проверяется между помещением общего назначения и технологическим помещением и подается аварийный сигнал, если минимум не достигнут.
Второй вентилятор активируется, когда температура окружающего воздуха в технологическом помещении находится вне пределов спецификации или когда обнаружен водород.

Технологический скид
Ключевым компонентов электролизного скида является пакет биполярных ячеек для электролиза воды под давлением. Пакет ячеек состоит из кольцевых электролизных ячеек, в каждой из которых содержатся два электрода и одна щелочная неорганическая ионообменная мембрана.
Генерация H2 и O2 происходит при подаче тока на пакет ячеек. Газы затем направляются на газовый сепаратор, который представляет собой двойной сосуд под давление из нержавеющей стали, после которого они промываются в специально спроектированном напорном сосуде, расположенном над газосепаратором.
Технологическая часть поставляется как полностью собранный скид, в который включено оборудование, например:
- Пакеты ячеек
- Газосепарторы, установка промывки газообразного водорода и коалесцирующие фильтры
- Теплообменники для электролита и системы газового охлаждения
- Лоток детектора утечек с реле уровня
- Детектор водорода , панель анализатора для водорода в кислороде
- Приборы кип и распределительные коробки: датчики, трансмиттеры, реле и т.д.
- Клапаны и вентиляционные коллекторы (H2 и O2)
Блок управления
Шкаф панели управления включает в себя ПЛК и все соответствующее оборудования для обеспечения автоматической и надежной эксплуатации установки. Панель управления с помощью кабелей будет подсоединена как к технологической части, так и к силовой стойке. Характеристики:
- Утвержденный электрический кожух с 2 запираемыми дверцами
- Вентиляторы охлаждения + система фильтрации воздуха
- ПЛК (Siemens S-7 программное обеспечение)
- Снаружи: терминал с дисплеем для визуализации и HMI
- Аварийный останов на дверце кожуха
- Блок бесперебойного питания для безопасного отключения
- Источник питания 24 В пост. тока
- Автоматические выключатели и трансформаторы
- Печатные платы и звуковая сигнализация
Блок питания

Блок питания конвертирует входящей 3х фазный переменный ток в стабилизированный постоянный ток, требуемый для процесса электролиза.
Каждый блок питания может питать до 2 пакетов элементов и состоит из:
- Кожух с запираемой дверцей
- Охлаждающие вентиляторы + система фильтрации воздуха
- Защитная блокировка дверного переключателя
- ПЛК контролируется тиристорами
- Трансформатор
- Выпрямительный диод
- Автоматические выключатели, контакторы
- Измерительный пакет элементов на дверце амперметр и вольтметр
- Устройство проверки фазы
Система очистки водорода

Система очистки водорода спроектирована для дальнейшей очистки водорода до минимального уровня в размере 99.998%. Данная чистота достигается в 2 этапа:
Этап 1. Деоксидизация: для уменьшения содержания O2 в потоке газообразного H2 с помощью каталитической реакции. Выход O2 в H2 составляет менее 10 ppm или опционально менее 2 ppm.
Этап 2. Осушка: для удаления влажности в 2 колоннах осушки. Одна колонна находится в работе, в то время как вторая находится в режиме резерва / регенерации. Водород на выходе будет иметь атмосферную точку росы менее -60 °C или опционально менее -75 °C.
Система очистка водорода сконструирована на скиде и располагается в технологическом помещении. Система очистки водорода управляется с помощью центрального ПЛК в панели управления и имеет следующие особенности:
- Сосуд деокисидзации с катализатором для удаления О2 в H2 (с обогревом и изоляцией)
- Теплообменник
- Коалесцирующий фильтр
- Система дренажного сосуда для удаления воды
- Оборудование КИП
- Две колонны осушки с молекулярным ситом (с обогревом и изоляцией) (с временной регенерацией)
- Соединения до контура охлаждения газа
- Соединение до вентиляционных коллекторов технологической части (H2 и O2)
Холодильник (охлаждение газа)

Холодильник подает охлаждающую воду низкой температуры в замкнутый контур газообразного водорода и кислорода в сторону теплообменников при температуре 15 °C, вне зависимости от температуры окружающей среды. Охлажденная вода охлаждает газообразный водород и кислород, превращая водяной пар, появляющийся в процессе электролиза, в конденсат. Затем он фильтруется и удаляется из потока газа. Холодильник устанавливается внутри кожуха для применения внутри помещения и включает насос и расширительный бак.
Спецификация на чиллер
Система охлаждения электролита

Данная система охлаждения, включающая в себя насосный скид и сухой охладитель, выводит тепло в окружающий воздух.
Охлаждающая вода, как правило, водный раствор этиленгликоль, циркулирует в закрытом контуре, через высокопроизводительный теплообменник по типу «электролит-вода», установленный в технологической части установки производства водорода.
Благодаря системе охлаждения закрытого цикла гарантируется полная выходная способность установки по водороду в диапазоне температуры окружающей среды от -40 до +40°C. Сухой охладитель и насосный скид регулируются с помощью центрального ПЛК в панели управления.
Спецификация на сухой охладитель
Система подготовки питательной воды

Система подготовки питательной воды превращает водопроводную воду в чистую деминерализованную воду, необходимую для процесса электролиза. Осуществляется постоянный мониторинг за качеством воды, прежде чем она сможет поступить в процесс. Размеры ВхШхГ – 1,5х1,0х0,5 м
Система включает в себя такие фильтрационные очистные этапы как:
- Мембрана обратного осмоса
- Ионообменная система смешанного типа со смолой (2 резервуара, наполненные смолой)
- Система смягчения воды с цифровым дозирующим насосом (анти-накипь)
- Измеритель электропроводности
- Активированный уголь и предварительные фильтры для улавливания частиц
- Указатели давления и реле
Спецификация на питательную воду
Техническая спецификация
Вышеуказанные данные представлены только для информации и не могут быть использованы для гарантийных целей.
Общий вид
Дополнительные опции (по запросу)
Улучшение чистоты -75 °C 2ppm O2
Данная опция снижает атмосферную точку росы произведенного H2 с -60 °C до -75 °C, а содержание О2 в произведенном H2 с 10ppm до 2 ppm.
Уменьшенное содержание N2 – распылительный разбрызгиватель
Распылительный разбрызгиватель – это устройство, устанавливаемое на входе деминерализованной воды установки производства водорода для уменьшения содержания N2 менее 2 ppm произведенного H2.
Замер чистоты в режиме реального времени
Производится непрерывный мониторинг произведенного H2 в реальном времени как по содержанию воды («точка росы»), так и по содержанию кислорода. Данная опция может быть выбрана только в сочетании с системой очистки водорода.
Спускной клапан (только в комбинации с системой замера чистоты в режиме реального времени)
Данное устройство автоматически выпускает H2 в атмосферу, в случае если его качество не соответствует спецификации. Данная опция может быть выбрана только в комбинации с системой замера чистоты H2 в режиме реального времени.
Использование кислорода
Стандартно О2 сбрасывается в атмосферу. Производитель может обеспечить опциональную систему для очистки О2 и его подготовки для дальнейшего использования / очистки со стороны заказчика.
Система кондиционирования воздуха на панели управления
Это модульная установка кондиционирования воздуха, устанавливаемая на электропанелях. Данное устройство рекомендовано для систем, часто эксплуатируемых в температурах окруж. среды более +40 °C
Массовый расходомер
Массовый расходомер – это непосредственный замер объема H2, идущего в линию заказчика.
Содержание кислорода в детекторе атмосферы
Трансмиттер кислорода в атмосфере может быть реализован в технологическом помещении для непрерывного мониторинга уровня O2 в атмосфере технологического помещения. Система сигнализации срабатывает, если уровень кислорода падает ниже или поднимается выше безопасных предельных значений.
Автоматический перезапуск
Данная функция позволяет установке непрерывно определять актуальное давление в линии заказчика. Если установка находится в резервном режиме, то с помощью данной функции установка может быть автоматически повторно запущена, как только давление линии заказчика окажется ниже заданного порогового значения.
Опции по каркасу для наружной установки
Низкотемпературная опция:
Будут предприняты специальные действия, чтобы допустить работу при температуре окружающей среды до -40 °C. Например, адоптированная система охлаждения с закрытым контуром и усиленная система обогрева.
Аварийные огни:
В случае отключения сетевого питания аварийные огни в помещении с приборами управления будут светить до 30 минут.
Внешние огни:
Огни снаружи контейнера при входе в помещение с приборами управления / для инженерного оборудования и технологического помещения.
Вентиляционные трубы:
Две трубы из высококачественной нержавеющей стали с колпачками от дождя для безопасной вентиляции H2 и О2. Длина данных вентиляционных труб соответствует спецификации, для каркаса для наружного размещения, который установлен в зоне без прилегающих конструкций. Вентиляционные трубы должны быть вертикально соединены на месте к специально определенным фланцам на боковой стороне контейнера. Кабели обогрева для защиты труб от нулевых температур (точка замерзания) включены в данный объем.
Границы объема поставки
Границей установка электролиза является каркас для наружного размещения. На внешних стенках каркаса для наружного размещения имеются металлические пластины, которые включают следующие соединения:
- Пользователь водородного газа
- Вход питательной воды
- Вход воздуха КИП
- Вентиляционное отверстие кислорода (вентиляционная линия не включена)
- Вентиляционное отверстие водорода (вентиляционная линия не включена)
- Соединение дренажа конденсата
- Вход инертного газа (азот)
- Электрические межсоединения: включены внутри контейнера
- Механические межсоединения: включены внутри контейнера
- Энергопитание: автоматический прерыватель на стороне электролиза.
- Охлаждающая вода (2 контура):
Сухой охладитель (охлаждение электролита)
- Сухой охладитель поставляется в отдельной коробке. Он спроектирован для установки на крыше каркаса для наружного размещения, а объем поставки включает технические условия на крыше контейнера для их установки.
- Трубка обвязки и кабели для соединения контейнера к внутренней части контейнера включены, но монтаж сухого охладителя на крыше и осуществление соединений на месте осуществляются заказчиком.
Холодильник (охлаждение газа):
- Холодильник поставляется с полностью выполненными соединениями в каркасе для наружного размещения
Установка водоподготовки:
- Установка водоподготовки поставляется с полностью выполненными соединениями в каркасе для наружного размещения.
Центр данных по альтернативным видам топлива: производство и распределение водорода
Несмотря на то, что водород присутствует в большом количестве на Земле как элемент, он почти всегда присутствует в составе другого соединения, такого как вода (H 2 O) или метан (CH 4 ), и должен быть разделен на чистый водород (H 2 ) для использования в электромобилях на топливных элементах. Водородное топливо соединяется с кислородом воздуха через топливный элемент, создавая электричество и воду в результате электрохимического процесса.
Производство
Водород можно производить из различных внутренних источников, включая ископаемое топливо, биомассу и электролиз воды с помощью электричества. Воздействие водорода на окружающую среду и энергоэффективность зависят от того, как он производится. Реализуется несколько проектов по снижению затрат, связанных с производством водорода.
Есть несколько способов производства водорода:
Риформинг / газификация природного газа: Синтез-газ, смесь водорода, окиси углерода и небольшого количества двуокиси углерода, образуется в результате реакции природного газа с высокотемпературным паром.Окись углерода реагирует с водой с образованием дополнительного водорода. Это самый дешевый, эффективный и распространенный способ. На конверсию природного газа с использованием пара приходится большая часть водорода, ежегодно производимого в Соединенных Штатах.
Синтез-газ можно также создать путем реакции угля или биомассы с высокотемпературным паром и кислородом в газификаторе под давлением, который преобразуется в газообразные компоненты — процесс, называемый газификация . Полученный синтез-газ содержит водород и монооксид углерода, который реагирует с водяным паром для отделения водорода.
Электролиз: Электрический ток расщепляет воду на водород и кислород. Если электричество производится из возобновляемых источников, таких как солнце или ветер, образующийся водород также будет считаться возобновляемым и имеет множество преимуществ по выбросам. Набирают обороты проекты по производству водорода, когда избыточная возобновляемая электроэнергия, если таковая имеется, используется для производства водорода посредством электролиза.
Возобновляемый жидкий риформинг: Возобновляемое жидкое топливо, такое как этанол, реагирует с высокотемпературным паром с образованием водорода вблизи точки конечного использования.
Ферментация: Биомасса превращается в сырье, богатое сахаром, которое можно сбраживать для получения водорода.
Ряд методов производства водорода находятся в стадии разработки:
Основными производителями водорода являются Калифорния, Луизиана и Техас. Сегодня почти весь водород, производимый в Соединенных Штатах, используется для очистки нефти, обработки металлов, производства удобрений и обработки пищевых продуктов.
Основной задачей производства водорода является снижение стоимости технологий производства, чтобы сделать получаемый водород конкурентоспособным по стоимости по сравнению с обычным транспортным топливом.Государственные и промышленные научно-исследовательские и опытно-конструкторские проекты снижают стоимость, а также воздействие на окружающую среду технологий производства водорода. Узнайте больше о производстве водорода в Управлении технологий водорода и топливных элементов.
Распределение
Большая часть водорода, используемого в Соединенных Штатах, производится там или поблизости от того места, где он используется, обычно на крупных промышленных предприятиях. Инфраструктура, необходимая для распределения водорода по общенациональной сети заправочных станций, необходимых для широкого использования электромобилей на топливных элементах, все еще нуждается в развитии.Первоначальное развертывание транспортных средств и станций сосредоточено на построении этих распределительных сетей, прежде всего в южной и северной Калифорнии.
В настоящее время водород распределяется тремя способами:
Трубопровод: Этот наименее затратный способ доставки больших объемов водорода ограничен, поскольку в настоящее время доступно только около 1600 миль трубопроводов США для доставки водорода. Эти трубопроводы расположены недалеко от крупных нефтеперерабатывающих и химических заводов в Иллинойсе, Калифорнии и на побережье Мексиканского залива.
Трубные прицепы высокого давления: Транспортировка сжатого водородного газа грузовиком, железнодорожным вагоном, кораблем или баржей в трубчатых прицепах высокого давления является дорогостоящей и используется в основном на расстояния до 200 миль или меньше.
Цистерны для сжиженного водорода: Криогенное сжижение — это процесс, при котором водород охлаждается до температуры, при которой он становится жидкостью. Хотя процесс сжижения является дорогостоящим, он позволяет транспортировать водород более эффективно (по сравнению с использованием трубных прицепов высокого давления) на большие расстояния грузовиком, железнодорожным вагоном, кораблем или баржей.Если сжиженный водород не используется с достаточно высокой скоростью в точке потребления, он выкипает (или испаряется) из резервуаров для хранения. В результате необходимо тщательно согласовывать скорость доставки и потребления водорода.
Создание инфраструктуры для распределения и доставки водорода на тысячи будущих заправочных станций представляет собой множество проблем. Поскольку водород содержит меньше энергии на единицу объема, чем все другие виды топлива, его транспортировка, хранение и доставка к месту конечного использования обходятся дороже в пересчете на галлоновый эквивалент бензина (на ГПЭ).Строительство новой сети водородных трубопроводов связано с высокими начальными капитальными затратами, а свойства водорода создают уникальные проблемы для материалов трубопроводов и конструкции компрессора. Однако, поскольку водород можно производить из самых разных ресурсов, региональное или даже местное производство водорода может максимально использовать местные ресурсы и минимизировать проблемы с распределением.
Необходимо учитывать компромисс между централизованным и распределенным производством. Производство водорода централизованно на крупных заводах снижает производственные затраты, но увеличивает затраты на сбыт.Производство водорода в точке конечного использования — например, на заправочных станциях — снижает затраты на сбыт, но увеличивает производственные затраты из-за затрат на создание производственных мощностей на месте.
Государственные и промышленные научно-исследовательские проекты преодолевают препятствия на пути эффективного распределения водорода. Узнайте больше о распределении водорода в Управлении технологий водорода и топливных элементов.
.
Производство водорода | Водород
Метод: Электролиз
Вкратце: Процесс, при котором вода (h3O) расщепляется на водород (h3) и кислород (O2) газ с подводом энергии и тепла в случае высокотемпературного электролиза.
На практике: Электрический ток разделяет воду на составные части. Если используется возобновляемая энергия, газ имеет нулевой углеродный след и известен как зеленый водород.
Метод: Риформинг — в первую очередь риформинг природного газа, но также и биогаза
Вкратце: Основные способы превращения природного газа, в основном метана, в водород включают реакцию либо с паром (паровой риформинг или паровой риформинг метана, когда используется метан), кислородом (частичное окисление) или с обоими последовательно (автотермический риформинг)
На практике: Паровой риформинг: в качестве окислителя используется чистый водяной пар.Реакция требует введения тепла («эндотермический»).
Метод: Водород из других промышленных процессов, которые создают водород в качестве побочного продукта.
Вкратце: Электрохимические процессы, такие как промышленное производство каустической соды и хлора, производят водород как побочный продукт.
На практике: Производство хлора и каустической соды сводится к пропусканию электрического тока через рассол (раствор соли — хлорида натрия — в воде).Рассол диссоциирует и рекомбинирует посредством обмена электронов (доставляемых током) на газообразный хлор, растворенную каустическую соду1 и водород. По характеру химической реакции хлор, каустическая сода и водород всегда производятся в фиксированном соотношении: 1,1 тонны каустика и 0,03 тонны водорода на тонну хлора.
риформинг
Паровой риформинг метана (SMR):

Как уже было описано выше, в настоящее время большая часть производимого сегодня водорода производится посредством процесса с интенсивным выбросом CO2, который называется паровым риформингом метана.
Высокотемпературный пар (700–1000 ° C) используется для производства водорода из источника метана, например природного газа. При паровом риформинге метана метан реагирует с паром под давлением 3–25 бар (1 бар = 14,5 фунтов на кв. Дюйм) в присутствии катализатора с образованием водорода, монооксида углерода и относительно небольшого количества диоксида углерода. Паровой риформинг эндотермический , то есть для протекания реакции в процесс необходимо подвести тепло.
Затем в так называемой «реакции конверсии водяного газа» монооксид углерода и водяной пар реагируют с использованием катализатора с образованием диоксида углерода и большего количества водорода.На заключительном этапе процесса, называемом «адсорбция при переменном давлении», диоксид углерода и другие примеси удаляются из газового потока, оставляя практически чистый водород. Паровой риформинг также можно использовать для производства водорода из других видов топлива, таких как этанол, пропан или даже бензин.
Для химиков:
Реакция парового риформинга метана
Ch5 + h3O (+ тепло) → CO + 3h3
Реакция конверсии водяного газа
CO + h3O → CO2 + h3 (+ небольшое количество тепла)
Частичное окисление
При частичном окислении метан и другие углеводороды в природном газе реагируют с ограниченным количеством кислорода (обычно из воздуха), которого недостаточно для полного окисления углеводородов до диоксида углерода и воды.При доступном количестве кислорода меньше стехиометрического, продукты реакции содержат в основном водород и монооксид углерода (и азот, если реакция проводится с воздухом, а не с чистым кислородом), а также относительно небольшое количество диоксида углерода и других соединений. Впоследствии в реакции конверсии водяного газа монооксид углерода реагирует с водой с образованием диоксида углерода и большего количества водорода.
Частичное окисление — это экзотермический процесс , при котором выделяется тепло.Этот процесс обычно намного быстрее, чем паровой риформинг, и требует меньшего размера реактора. Как видно из химических реакций частичного окисления, в этом процессе первоначально образуется меньше водорода на единицу входящего топлива, чем получается при паровом риформинге того же топлива.
Для химиков:
Реакция частичного окисления метана
Ch5 + ½O2 → CO + 2h3 (+ тепло)
Реакция конверсии водяного газа
CO + h3O → CO2 + h3 (+ небольшое количество тепла)
Источник: энергетика.gov
Паровой риформинг метана (SMR) для биогаза
Процесс SMR можно также использовать для производства водорода из биогаза.
Электролиз

Несмотря на то, что водород можно получить множеством способов, наиболее интересной, но и многообещающей частью является получение водорода путем электролиза воды.
В этом процессе электролиз расщепляет воду на водород и кислород с помощью электричества.Если используемое электричество поступает из возобновляемых источников энергии, таких как ветер или солнце, а произведенный водород используется в топливных элементах, то весь энергетический процесс не будет создавать чистых выбросов. В данном случае речь идет о «зеленом водороде».
Электролизер состоит из источника постоянного тока и двух электродов с покрытием из благородного металла, разделенных электролитом. Электролит или ионный проводник может быть жидкостью, например проводящим раствором едкого калия (гидроксид калия, КОН) для щелочного электролиза.
В щелочном электролизере катод (отрицательный полюс) теряет электроны в водном растворе.
Вода диссоциирует, что приводит к образованию водорода (h3) и гидроксид-ионов (OH —
Носители заряда движутся в электролите к аноду. На аноде (положительный полюс) электроны поглощаются отрицательными анионами OH -. Анионы ОН — окисляются с образованием воды и кислорода. Кислород поднимается на аноде. Мембрана предотвращает смешивание продуктовых газов h3 и O2, но пропускает ионы OH -.Электролизеры состоят из отдельных ячеек и узлов центральной системы (баланс завода). Комбинируя электролитические ячейки и батареи, производство водорода можно адаптировать к индивидуальным потребностям.
Электролизеры различаются по материалам электролита и температуре, при которой они работают: низкотемпературный электролиз (LTE), включая щелочной электролиз (AE) , электролиз с протонообменной мембраной (PEM ) и анионообменная мембрана ( AEM) электролиз (также известный как щелочной PEM) и высокотемпературный электролиз (HTE).Последняя группа, в первую очередь, включает электролиз твердого оксида (SOE ), но он все еще находится на продвинутой стадии исследований и разработок, и продукты еще не коммерчески доступны. Ожидается, что по достижении рыночной зрелости его преимущества будут включать повышенную эффективность преобразования и возможность производства синтез-газа непосредственно из пара и CO 2 для использования в различных приложениях, таких как синтетическое жидкое топливо (E4tech 2014, IEA 2015b).
Высокотемпературный электролиз особенно интересен, когда рядом с электролизером есть источник тепла (как это часто бывает на промышленных предприятиях или), более экономически эффективен, чем традиционный электролиз при комнатной температуре.Действительно, часть энергии поставляется в виде тепла, которое либо бесплатно, либо дешевле, чем электричество, а также потому, что реакция электролиза более эффективна при более высоких температурах.
Выбор той или иной технологии электролиза зависит от потребностей использования и местных условий.
Водород похож на электричество в том смысле, что его использование не вызывает никаких выбросов. Его углеродный след связан с его производственным режимом. В случае водорода, полученного путем электролиза, его углеродный след водорода напрямую связан с источником электричества.Таким образом, водород, производимый из безуглеродных возобновляемых источников или атомной энергии, не содержит углерода. Водород, произведенный с помощью сетки, имеет ту же углеродную интенсивность, что и смесь сетки.
Водород как побочный продукт
Как объяснено выше, водород получают путем отделения от его соединения.
Если производство водорода может быть первой целью процесса разделения, то также может быть, что процесс разделения направлен в первую очередь на производство другой молекулы и получение водорода в качестве побочного продукта.
Производство хлора и каустической соды сводится к пропусканию электрического тока через рассол (раствор соли — хлорида натрия — в воде). Рассол диссоциирует и рекомбинирует посредством обмена электронов (доставляемых током) на газообразный хлор, растворенную каустическую соду и водород. По характеру химической реакции хлор, каустическая сода и водород всегда производятся в фиксированном соотношении: 1,1 тонны каустика и 0,03 тонны водорода на тонну хлора.
Ряд исследований был направлен на определение количества доступного промышленного остаточного водорода.В рамках проекта ЕС «Дороги 2 HyCom» (Maisonnier et al. 2007) среди прочих результатов была получена карта, показывающая места производства водорода в Европе. На этой карте источники водорода разбиты на три категории: категория «коммерсант» поставляет водород другим промышленным потребителям, а категория «зависимая» сохраняет водород на месте для собственного использования. Только «побочный продукт» водород больше не используется в процессе или на месте; только эта категория может быть доступна для других приложений, таких как электромобили на топливных элементах.
Водород в качестве побочного продукта представляет собой интересный и дешевый источник водорода, необходимый для развертывания применения водорода в области его производства. Неудивительно, что регионы с большим количеством водорода в качестве побочного продукта являются одними из самых продвинутых в своей стратегии использования водорода.
.
8. Технологии производства водорода | Водородная экономика: возможности, затраты, препятствия и потребности в исследованиях и разработках
часов потребления за счет использования накопленного водорода для выработки дополнительной энергии; этот водород может генерироваться в непиковые часы.
Технологические опции
Современные технологии электролиза делятся на две основные категории: (1) твердый полимер с использованием протонообменной мембраны (PEM) и (2) жидкий электролит, чаще всего гидроксид калия (KOH).В обеих технологиях вода вводится в реакционную среду и подвергается воздействию электрического тока, вызывающего диссоциацию, после чего образующиеся атомы водорода и кислорода пропускаются через механизм ионного переноса, который заставляет водород и кислород накапливаться в отдельных физических потоках.
Электролизер PEM — это буквально топливный элемент PEM, работающий в обратном режиме. Когда вода вводится в ячейку электролизера PEM, ионы водорода (протоны) втягиваются внутрь и через мембрану, где они рекомбинируют с электронами с образованием молекул водорода.Газообразный кислород остается в воде. Поскольку эта вода рециркулирует, кислород накапливается в резервуаре для разделения и затем может быть удален из системы. Газообразный водород отдельно отводится от батареи ячеек и улавливается.
В системах с жидким электролитом обычно используется щелочной раствор для выполнения функций, аналогичных функциям электролизера PEM. В таких системах ионы кислорода мигрируют через электролитический материал, оставляя газообразный водород растворенным в потоке воды. Этот водород легко извлекается из воды, когда его направляют в разделительную камеру.
Полная стоимость водорода из систем PEM и KOH сегодня примерно сопоставима. Эффективность реакции обычно выше для систем КОН, потому что ионное сопротивление жидкого электролита ниже, чем сопротивление нынешних мембран PEM. Но преимущество систем КОН по эффективности реакции по сравнению с системами ПЭМ нивелируется более высокими требованиями к очистке и сжатию, особенно при малых масштабах (от 1 до 5 кг в час). Более подробная информация представлена в Приложении G.
Электролиз может особенно хорошо подходить для удовлетворения начальных потребностей в топливе на рынке транспортных средств на топливных элементах. Электролизеры достаточно хорошо масштабируются; эффективность реакции электролиза не зависит от размера задействованных элементов или стопок элементов. Компактный размер электролизеров делает их пригодными для размещения на существующих заправочных станциях или рядом с ними, и они могут использовать существующую инфраструктуру воды и электричества, сводя к минимуму потребность в новой инфраструктуре.
Будущее усовершенствование технологии электролиза
Целью Министерства энергетики США для электролиза является капитальные затраты в размере 300 долларов США / кВт для установки мощностью 250 кг / день (при 5000 фунтов на квадратный дюйм [фунт / кв. Дюйм] с КПД системы 73%, базис более низкой теплотворной способности [DOE, 2003b, стр. 3- 15]). Такую установку можно было бы интегрировать с возобновляемым источником энергии для производства водорода по цене 2,50 доллара за кг к 2010 году. Тогда большая центральная станция могла бы производить водород по цене 2 доллара за кг (DOE, 2003b, стр.3-16). Программа исследований Министерства энергетики США фокусируется на способах снижения затрат, повышения эффективности и интеграции электролизных заводов с возобновляемыми источниками электроэнергии. Министерство энергетики также продолжает разработку материалов для обратимых твердооксидных электролизеров, которые могут работать при более высоких температурах, чем PEM, и с потенциально очень высокой эффективностью. Министерство энергетики сообщило, что его бюджетный запрос на 2004 финансовый год включал примерно 3,2 миллиона долларов на исследования электролиза в водород. 5 , 6
Комитет считает правдоподобным, что капитальные затраты на электролизеры PEM могут снизиться в восемь раз — с 1000 долларов США / кВт в ближайшем будущем до 125 долларов США / кВт в течение следующих 15-20 лет, в зависимости от аналогичного снижения затрат, происходящего в топливных элементах PEM.Если капитальные затраты снизятся до этого уровня, по оценке комитета, водород можно будет производить примерно по 4 доллара за кг с использованием электроэнергии из сети и электролиза, что делает его привлекательным в переходный период 2010–2030 годов, пока не будут построены централизованные объекты и необходимая система распределения. Многолетний план исследований, разработок и демонстрации Министерства энергетики (DOE, 2003b) включает технический план топливных элементов, в котором рассматриваются технологические и ценовые барьеры — барьеры, преодоление которых также пойдет на пользу электролизерам.Элементы плана топливных элементов включают, например: разработку высокотемпературных мембран для топливных элементов PEM, разработку более дешевых полимерных мембран, имеющих более высокую ионную проводимость, и разработку альтернативных рецептур и структур катализаторов.
Кроме того, КПД системы электролизера может вырасти с нынешних 63,5 процентов до 75 процентов (более низкая теплотворная способность) в будущем. Среди приоритетов исследований, которые могут повысить эффективность и / или снизить стоимость будущих электролизных заправочных устройств и которые могут стать частью программы электролиза Министерства энергетики, следующие:
Снижение других (паразитных) потерь энергии в системе. Множество паразитных нагрузок, таких как регулировка мощности, можно уменьшить за счет модернизации и оптимизации системы.
Уменьшение плотности тока. Эффективность преобразования зависит от плотности электрического тока, поэтому замена электролита или большей площади поверхности элемента приводит к снижению общих требований к мощности на единицу производимого водорода.
Разработка гибридов электролиза / окисления .Гибридная концепция использует окисление природного газа как средство усиления миграции ионов кислорода через электролит и, таким образом, снижения эффективного количества электроэнергии, необходимой для переноса иона кислорода. Концепт
.
Новый метод эффективного получения водорода из воды
Исследователи WSU нашли способ создать большое количество недорогих катализаторов из нано-пены, которые могут способствовать генерации водорода в больших масштабах за счет расщепления молекул воды. Предоставлено: Университет штата Вашингтон.
Исследователи из Университета штата Вашингтон нашли способ более эффективно производить водород из воды — важный ключ к повышению жизнеспособности экологически чистой энергии.
Используя недорогие никель и железо, исследователи разработали очень простой пятиминутный метод создания больших количеств высококачественного катализатора, необходимого для химической реакции расщепления воды.
Они описывают свой метод в февральском номере журнала Nano Energy .
Преобразование и хранение энергии — ключ к чистой энергии. Поскольку солнечные и ветряные источники вырабатывают электроэнергию только с перерывами, существует острая потребность в способах хранения и экономии электроэнергии, которую они создают.Одна из самых многообещающих идей для хранения возобновляемой энергии — использовать избыток электроэнергии, произведенной из возобновляемых источников, для разделения воды на кислород и водород. Водород находит множество применений в промышленности и может быть использован в автомобилях с водородными топливными элементами.
Однако
Industries не использовала широко процесс разделения воды из-за непомерно высокой стоимости требуемых катализаторов из драгоценных металлов — обычно платины или рутения. Многие методы расщепления воды также требуют слишком большого количества энергии, или требуемые материалы катализатора разрушаются слишком быстро.
В своей работе исследователи под руководством профессора Юэ Линя из Школы машиностроения и материаловедения использовали два широко доступных и дешевых металла для создания пористой нано-пены, которая работала лучше, чем большинство катализаторов, которые используются в настоящее время, в том числе изготовленные из драгоценные металлы. Созданный ими катализатор выглядит как крошечная губка. Обладая уникальной атомной структурой и множеством открытых поверхностей по всему материалу, нано-пена может катализировать важную реакцию с меньшими затратами энергии, чем другие катализаторы.Катализатор показал очень небольшую потерю активности при 12-часовом испытании стабильности.
«Мы выбрали очень простой подход, который можно легко использовать в крупномасштабном производстве», — сказал Шаофан Фу, доктор философии WSU. студент, который синтезировал катализатор и провел большую часть тестирования активности.
Юэ Линь (слева) и Шаофан Фу, доктор философии WSU. студент, в лаборатории материаловедения WSU Линь Фото: Университет штата Вашингтон
Исследователи WSU сотрудничали в этом проекте с исследователями из Advanced Photon Source в Аргоннской национальной лаборатории и Тихоокеанской северо-западной национальной лаборатории.
«Современное оборудование для определения характеристик материалов в национальных лабораториях позволило глубже понять состав и структуру катализаторов», — сказал Цзюньхуа Сун, другой доктор философии WSU. студент, который работал над характеристикой катализатора.
Теперь исследователи ищут дополнительную поддержку, чтобы расширить свою работу для крупномасштабного тестирования.
«Это всего лишь лабораторное тестирование, но оно очень многообещающее, — сказал Линь.
Улучшенное разделение воды способствует преобразованию возобновляемой энергии
Дополнительная информация:
Шаофанг Фу и др., Ультратонкие и сильно разупорядоченные нано-пены Ni 2 Fe 1 обеспечили возможность высокоэффективной реакции выделения кислорода в щелочном электролите, Nano Energy (2017).DOI: 10.1016 / j.nanoen.2017.12.010
Предоставлено
Вашингтонский государственный университет
Цитата :
Новый метод эффективного получения водорода из воды (2018, 1 февраля)
получено 1 октября 2020
с https: // физ.org / news / 2018-02-method-эффективно-водород.html
Этот документ защищен авторским правом. За исключением честных сделок с целью частного изучения или исследования, нет
часть может быть воспроизведена без письменного разрешения. Контент предоставляется только в информационных целях.
.
