Число нейтронов в атоме. Изотопы — урок. Химия, 8–9 класс.
Число нейтронов в атоме
Мы знаем, что масса атома определяется массой ядра. Ядро состоит из протонов и нейтронов, относительные массы которых равны \(1\). Масса ядра равна сумме масс протонов и нейтронов. Число протонов определяем по порядковому номеру элемента. Значит, число нейтронов в ядре можно найти, если от относительной атомной массы отнять порядковый номер.
Пример:
фтор — элемент № \(9\). Его относительная атомная масса равна \(19\).
В ядре атома фтора — \(9\) протонов и \(19\) \(–\) \(9\) \(=\) \(10\) нейтронов.
Рубидий — элемент № \(37\). Его относительная атомная масса равна \(85\).
В ядре атома рубидия — \(37\) протонов и \(85\) \(–\) \(37\) \(=\) \(48\) нейтронов.
Нуклиды
Вид атомов с определённым числом протонов и нейтронов в ядре называется нуклидом.
Нуклид обозначается следующим образом: внизу слева записывается число протонов \(Z\) (порядковый номер), вверху слева указывается массовое число \(A\) (сумма чисел протонов и нейтронов) — RZA, например: C612, Se3479.
Для обозначения нуклидов используют и другие способы записи:
углерод — \(12\), C — \(12\), C12;
селен — \(79\), Se — \(79\), Se79.
Изотопы
Атомы одного и того же химического элемента могут иметь разные массы. Существуют атомы водорода с массами \(1\), \(2\) и \(3\), атомы хлора с массами \(35\) и \(37\) и т. д.
Разновидности атомов одного химического элемента, имеющие разные атомные массы, называют изотопами.
С учётом знаний о строении ядра это определение можно сформулировать по-другому.
Изотопы — разновидности атомов с одинаковым числом протонов в ядре (зарядом ядра), но разным числом нейтронов.
Значит, изотопы отличаются только числом нейтронов.
Протоны определяют свойства атома, то есть придают ему индивидуальность. А нейтроны не влияют на свойства атома, а отражаются на его массе. Поэтому все изотопы одного и того же элемента химически неотличимы.
Химический элемент — это вид атомов с определённым зарядом ядра.
Относительная атомная масса элемента
Большинство химических элементов существуют в виде смеси изотопов. Приведённая в Периодической таблице относительная атомная масса элемента — это средняя величина атомных масс всех его изотопов.
Пример:
определим относительную атомную массу хлора. \(25\) % его атомов — это атомы с массой \(37\), а \(75\) % — с массой \(35\). Найдём среднее значение:
Ar(Cl)=(37
·25+35
·75)100 \(=\) 35,5.
| 1 | Найти число нейтронов | H | |
| 2 | Найти массу одного моля | H_2O | |
| 3 | Баланс | H_2(SO_4)+K(OH)→K_2(SO_4)+H(OH) | |
| 4 | Найти массу одного моля | H | |
| 5 | Найти число нейтронов | Fe | |
| 6 | Найти число нейтронов | Tc | |
| 7 | Найти конфигурацию электронов | H | |
| 8 | Найти число нейтронов | Ca | |
| 9 | Баланс | CH_4+O_2→H_2O+CO_2 | |
| 10 | Найти число нейтронов | C | |
| 11 | Найти число протонов | H | |
| 12 | Найти число нейтронов | O | |
| 13 | Найти массу одного моля | CO_2 | |
| 14 | Баланс | C_8H_18+O_2→CO_2+H_2O | |
| 15 | Найти атомную массу | H | |
| 16 | Определить, растворима ли смесь в воде | H_2O | |
| 17 | Найти конфигурацию электронов | Na | |
| 18 | Найти массу одного атома | H | |
| 19 | Найти число нейтронов | Nb | |
| 20 | Найти число нейтронов | Au | |
| 21 | Найти число нейтронов | Mn | |
| 22 | Найти число нейтронов | Ru | |
| 23 | Найти конфигурацию электронов | O | |
| 24 | Найти массовую долю | H_2O | |
| 25 | Определить, растворима ли смесь в воде | NaCl | |
| 26 | Найти эмпирическую/простейшую формулу | H_2O | |
| 27 | Найти степень окисления | H_2O | |
| 28 | Найти конфигурацию электронов | K | |
| 29 | Найти конфигурацию электронов | Mg | |
| 30 | Найти конфигурацию электронов | Ca | |
| 31 | Найти число нейтронов | Rh | |
| 32 | Найти число нейтронов | Na | |
| 33 | Найти число нейтронов | Pt | |
| 34 | Найти число нейтронов | Be | Be |
| 35 | Найти число нейтронов | Cr | |
| 36 | Найти массу одного моля | H_2SO_4 | |
| 37 | Найти массу одного моля | HCl | |
| 38 | Найти массу одного моля | Fe | |
| 39 | Найти массу одного моля | C | |
| 40 | Найти число нейтронов | Cu | |
| 41 | Найти число нейтронов | S | |
| 42 | Найти степень окисления | H | |
| 43 | Баланс | CH_4+O_2→CO_2+H_2O | |
| 44 | Найти атомную массу | O | |
| 45 | Найти атомное число | H | |
| 46 | Найти число нейтронов | Mo | |
| 47 | Найти число нейтронов | Os | |
| 48 | Найти массу одного моля | NaOH | |
| 49 | Найти массу одного моля | O | |
| 50 | Найти конфигурацию электронов | Fe | |
| 51 | Найти конфигурацию электронов | C | |
| 52 | Найти массовую долю | NaCl | |
| 53 | Найти массу одного моля | K | |
| 54 | Найти массу одного атома | Na | |
| 55 | Найти число нейтронов | N | |
| 56 | Найти число нейтронов | Li | |
| 57 | Найти число нейтронов | V | |
| 58 | Найти число протонов | N | |
| 59 | Упростить | H^2O | |
| 60 | Упростить | h*2o | |
| 61 | Определить, растворима ли смесь в воде | H | |
| 62 | Найти плотность при стандартной температуре и давлении | H_2O | |
| 63 | Найти степень окисления | NaCl | |
| 64 | Найти атомную массу | He | He |
| 65 | Найти атомную массу | Mg | |
| 66 | Найти число электронов | H | |
| 67 | Найти число электронов | O | |
| 68 | Найти число электронов | S | |
| 69 | Найти число нейтронов | Pd | |
| 70 | Найти число нейтронов | Hg | |
| 71 | Найти число нейтронов | B | |
| 72 | Найти массу одного атома | Li | |
| 73 | Найти эмпирическую формулу | H=12% , C=54% , N=20 | , , |
| 74 | Найти число протонов | Be | Be |
| 75 | Найти массу одного моля | Na | |
| 76 | Найти конфигурацию электронов | Co | |
| 77 | Найти конфигурацию электронов | S | |
| 78 | Баланс | C_2H_6+O_2→CO_2+H_2O | |
| 79 | Баланс | H_2+O_2→H_2O | |
| 80 | Найти конфигурацию электронов | P | |
| 81 | Найти конфигурацию электронов | Pb | |
| 82 | Найти конфигурацию электронов | Al | |
| 83 | Найти конфигурацию электронов | Ar | |
| 84 | Найти массу одного моля | O_2 | |
| 85 | Найти массу одного моля | H_2 | |
| 86 | Найти число нейтронов | K | |
| 87 | Найти число нейтронов | P | |
| 88 | Найти число нейтронов | Mg | |
| 89 | Найти число нейтронов | W | |
| 90 | Найти массу одного атома | C | |
| 91 | Упростить | na+cl | |
| 92 | Определить, растворима ли смесь в воде | H_2SO_4 | |
| 93 | Найти плотность при стандартной температуре и давлении | NaCl | |
| 94 | Найти степень окисления | C_6H_12O_6 | |
| 95 | Найти степень окисления | Na | |
| 96 | Определить, растворима ли смесь в воде | C_6H_12O_6 | |
| 97 | Найти атомную массу | Cl | |
| 98 | Найти атомную массу | Fe | |
| 99 | Найти эмпирическую/простейшую формулу | CO_2 | |
| 100 | Найти число нейтронов | Mt |
Как определить число протонов и нейтронов в атоме? Примеры.
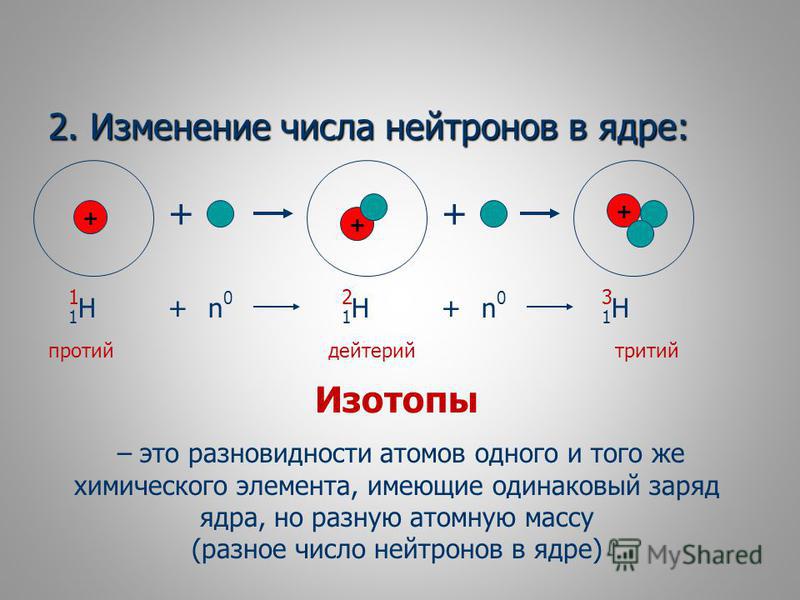
Как определить число нуклонов в ядре атома?
Число нуклонов в ядре атома равно массовому числу атома (относительная атомная масса химического элемента) или сумме протонов и нейтронов.
Как определить число протонов в атоме?
Число протонов в атоме равно заряду его ядра (обозначается как Z) или порядковому номеру элемента в периодической таблице Менделеева.
Как определить число нейтронов в атоме?
Очень просто!
N = A — Z
Где N — число нейтронов, A — атомная масса элемента (в целых числах), Z — заряд ядра атома или порядковый номер атома в периодической таблице Менделеева.
Развернутый ответ
Масса атома складывается из двух величин: масса протонов + масса нейтронов. Дело в том, что масса электронов пренебрежимо мала.
Масса нейтрона = 1,674 927 498 04(95)⋅10⁻²⁷ кг= 1,008 664 915 60(57) а.е.м.
Масса протона = 1,672 621 923 69(51)⋅10⁻²⁷ кг = 1,007276466621(53) а. е.м.
е.м.
Масса электрона = 9,109383 7015(28)⋅10⁻³¹ кг = 0,000548579909065 а.е.м.
То есть даже 100 электронов дадут в сумме всего 0,0548579909065 а.е.м.
Первоначально Д. И. Менделеев в построении своей периодической таблицы исходил из атомных весов элементов. Однако, дальнейшее развитие науки показало, что свойства химических элементов находятся в прямой зависимости не от атомной массы химического элемента, а от заряда ядра его атома. Таким образом, в периодической таблице химические элементы выстроены в порядке возрастания заряда ядра атома и номер элемента в таблице соответствует заряду его ядра. А заряд ядра равен сумме протонов. То есть № (элемента) = Z (заряд ядра или число протонов).
Остаток массы ядра приходится на нейтроны. Поэтому чтобы определить число нейтронов в атоме нужно всего лишь вычесть из атомной массы число протонов, которое равно заряду ядра или порядковому номеру элемента в таблице Менделеева.
Примеры
Сколько протонов и нейтронов в атоме натрия?
Ar (Na) = 23 а.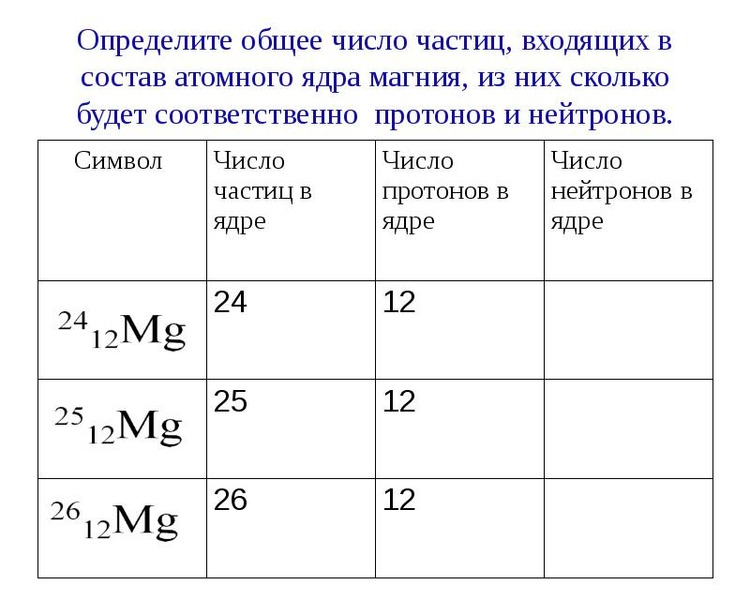 е.м.
е.м.
Z (Na) = 11 (протонов)
N = Ar (Na) — Z (Na) = 23 — 11 = 12 (нейтронов)
Ответ: число протонов в атоме натрия равно 11, а число нейтронов в атоме натрия равно 12.
Сколько протонов и нейтронов в атоме фосфора?
Ar (P) = 31 а.е.м.
Z (P) = 15 (протонов)
N = Ar (P) — Z (P) = 31 — 15 = 16 (нейтронов)
Ответ: число протонов в атоме фосфора равно 15, а число нейтронов в атоме фосфора равно 16.
Сколько протонов и нейтронов в атоме золота?
Ar (Au) = 197 а.е.м.
Z (Au) = 79 (протонов)
N = Ar (Au) — Z (Au) = 197 — 79 = 118 (нейтронов)
Ответ: число протонов в атоме золота равно 79, а число нейтронов в атоме золота равно 118.
Сколько протонов и нейтронов в атоме кремния?
Ar (Si) = 28 а.е.м.
Z (Si) = 14 (протонов)
N = Ar (Si) — Z (Si) = 28 — 14 = 14 (нейтронов)
Ответ: число протонов и нейтронов в атоме кремния равно 14.
Сколько протонов и нейтронов в атоме углерода?
Ar (C) = 12 а. е.м.
е.м.
Z (C) = 6 (протонов)
N = Ar (C) — Z (C) = 12 — 6 = 6 (нейтронов)
Ответ: число протонов и нейтронов в атоме углерода равно 6.
Сколько протонов и нейтронов в атоме калия?
Ar (K) = 39 а.е.м.
Z (K) = 19 (протонов)
N = Ar (K) — Z (K) = 39 — 19 = 20 (нейтронов)
Ответ: число протонов в атоме калия равно 19, а число нейтронов в атоме калия равно 20.
Сколько протонов и нейтронов в атоме железа?
Ar (Fe) = 39 а.е.м.
Z (Fe) = 19 (протонов)
N = Ar (Fe) — Z (Fe) = 56 — 26 = 30 (нейтронов)
Ответ: число протонов в атоме железа равно 19, а число нейтронов в атоме железа равно 30.
Сколько протонов и нейтронов в атоме алюминия?
Ar (Al) = 27 а.е.м.
Z (Al) = 13 (протонов)
N = Ar (Al) — Z (Al) = 27 — 13 = 14 (нейтронов)
Ответ: число протонов в атоме алюминия равно 13, а число нейтронов в атоме алюминия равно 14 .
Сколько протонов и нейтронов в атоме фтора?
Ar (F) = 19 а. е.м.
е.м.
Z (F) = 9 (протонов)
N = Ar (F) — Z (F) = 19 — 9 = 10 (нейтронов)
Ответ: число протонов в атоме фтора равно 9, а число нейтронов в атоме фтора равно 10.
Сколько протонов и нейтронов в атоме хлора?
Ar (Cl) = 35 а.е.м.
Z (Cl) = 17 (протонов)
N = Ar (Cl) — Z (Cl) = 35 — 17 = 18 (нейтронов)
Ответ: число протонов в атоме хлора равно 17, а число нейтронов равно 18.
Сколько протонов и нейтронов в атоме кислорода?
Ar (O) = 16 а.е.м.
Z (O) = 8 (протонов)
N = Ar (O) — Z (O) = 16 — 8 = 8 (нейтронов)
Ответ: число протонов и нейтронов в атоме кислорода равно 8.
Сколько протонов и нейтронов в атоме серы?
Ar (S) = 32 а.е.м.
Z (S) = 16 (протонов)
N = Ar (S) — Z (S) = 32 — 16 = 16 (нейтронов)
Ответ: число протонов и нейтронов в атоме серы равно 16.
Сколько протонов и нейтронов в атоме магния?
Ar (Mg) = 32 а.е.м.
Z (Mg) = 16 (протонов)
N = Ar (Mg) — Z (Mg) = 24 — 12 = 12 (нейтронов)
Ответ: число протонов в атоме магния равно 16, а число нейтронов равно 12.
Сколько протонов и нейтронов в атоме цинка?
Ar (Zn) = 65 а.е.м.
Z (Zn) = 30 (протонов)
N = Ar (Zn) — Z (Zn) = 65 — 30 = 35 (нейтронов)
Ответ: число протонов в атоме цинка равно 30, а число нейтронов в атоме цинка равно 35.
Похожие вопросы:
— Какие атомы имеют одинаковое число нейтронов?
— Как определить общее число электронов в атоме?
Как найти протоны, нейтроны и электроны
Как найти протоны, нейтроны и электроны
затвор шиберный для пескоструя
В попытке понять основную проектировании атомов, важно получить информацию о методологии, чтобы узнать, протонов, нейтронов и электронов. В данной статье рассматриваются основные методы, чтобы найти число субатомных частиц в атоме. Элементарная физика и химия дело с атомами, электронами и протонами. Понимание основных концепций этих основных частей атома может помочь нам расшифровать сложные химические процессы в этом мире. Кроме того, зная простые методы определения числа протонов, нейтронов и электронов, мы можем понять, из более близкой перспективой, как изменение количества этих частиц влияет на физические и химические свойства химических элементов.
Кроме того, зная простые методы определения числа протонов, нейтронов и электронов, мы можем понять, из более близкой перспективой, как изменение количества этих частиц влияет на физические и химические свойства химических элементов.
Электронов: это субатомная частица несет отрицательный заряд (-1). Он был обнаружен группой британских физиков, в том числе сэр J. Дж Томсон, в 1897 году.
Протон: положительно заряженная частица Протон (+1 заряд) — это просто как положительный ион водорода. Эрнест Резерфорд доказал существование протонов в 1918 году, отправив Альфа-частиц через газ азот.
Нейтрон: они нейтральные субатомные частицы найдены в центре ядра. Они были обнаружены Джеймс Чедвик в 1932 году.
Поиск протонов нейтронов и электронов в элементе
Будь то физики или химии учащимся элементарные науки должны быть осведомлены о способах, как находить протоны, нейтроны и электроны. Некоторые простые основы, которые студенты должны знать следующие:
Число протонов = Порядковый номер
Число электронов = число протонов = Порядковый номер
Количество нейтронов = масса Кол — атомный номер
Массовое число = сумма протонов и нейтронов
Находить протоны, нейтроны и электроны изотопы
Изотопы-это атомы одного элемента с одинаковым числом протонов, но различное число нейтронов. Например, углерод — 12, углерод — 13 и углерод — 14 являются три изотопов углерода, каждый из которых имеет 6 электронов. Однако количество нейтронов, 6, 7, и 8, соответственно, в каждом из этих изотопов углерода. Знать, как находить протоны, нейтроны и электроны в изотоп, давайте рассмотрим на примере изотопов хлора, хлор — 35 (17Cl35) и хлора — 37 (17Cl37)
Например, углерод — 12, углерод — 13 и углерод — 14 являются три изотопов углерода, каждый из которых имеет 6 электронов. Однако количество нейтронов, 6, 7, и 8, соответственно, в каждом из этих изотопов углерода. Знать, как находить протоны, нейтроны и электроны в изотоп, давайте рассмотрим на примере изотопов хлора, хлор — 35 (17Cl35) и хлора — 37 (17Cl37)
Хлора — 35 (17Cl35)
Число электронов = число протонов = Порядковый номер = 17
Массовое Число = 35
Количество нейтронов = масса Кол — атомный номер = 35 — 17 = 18
Если мы считаем, хлора — 37 (17Cl37)
Число электронов = число протонов = Порядковый номер = 17
Массовое Число = 37
Количество нейтронов = масса Кол — атомный номер = 37 — 17 = 20
Поиск протонов, нейтронов, электронов и ионов
Важно знать про катионы и анионы, прежде чем мы узнаем простой способ, чтобы найти количество протонов, электронов и нейтронов в них.
Катионов-Ионы, имеющие положительные заряды, называются катионами. Они потеряли после потери электронов в атоме.
Они потеряли после потери электронов в атоме.
Аниона: это отрицательно заряженные ионы, которые образуются в результате добавления дополнительных электронов в атоме.
Рассмотреть дело Nа+.
Согласно атомной структуры натрия, мы знаем, что атомное число натрия (na) составляет 11. Однако, поскольку ион натрия несет положительный заряд, должно быть, либо приобрели Протон, или потерял электрон. Так как это не возможно для НС, чтобы получить один Протон, так как он станет магния, должно быть, потеряла один электрон. Следовательно, исходное число электронов и протонов в натрия равен 11, но так как он потерял один электрон, число электронов = число протонов = Порядковый номер = 10.
Аналогичным образом, число нейтронов в na+ = массовое число — атомный номер = 23 — 10 = 13
Это просто, чтобы знать число протонов, электронов и нейтронов с помощью периодической таблицы. Эта Таблица имеет атомное и массовое число, написанное на нем. Пытаясь узнать больше о том, как найти эти субатомные частицы в несколько других элементов, студенты могут освоить эту простую технику.
Комментарии
Вера Константиновна — 20.01.2018 20:25:12
Так вот откуда я беру задания на урок…
§ 7. Химические реакции — гдз по химии для 8 класса О.С. Габриелян
Параграф №7, вопрос №1, стр 49
Условие:
Какие научные открытия доказали, что атом — сложная частица, что он делим?
Решение:
В 1910 г. в Кембридже, близ Лондона, Эрнест Резерфорд со своими учениками и коллегами изучал рассеивание α-частиц, проходящих через тоненькую золотую фольгу и попадавших на экран.
Советы:
Модель атома была названа планетарной. Напоминает строение нашей солнечной системы
Параграф №7, вопрос №2, стр 49
Условие:
Определите число протонов, электронов и нейтронов в атомах элементов: натрия, фосфора, золота.
Решение:
Na p+=11, e-=11, n0=12P p+=15, e-=15, n0=16Au p+=79, e-=79, n0=118
Советы:
число протонов и электронов=порядковому номеру.
Параграф №7, вопрос №3, стр 49
Условие:
Пользуясь этимологическим словарём, объясните, почему планетарную модель строения атома, предложенную Э. Резерфордом, называют также нуклеарной. Почему протоны и нейтроны вместе называют нуклонами?
Резерфордом, называют также нуклеарной. Почему протоны и нейтроны вместе называют нуклонами?
Решение:
Латинское nucleus — ядро, от этого входящие в состав ядра частицы протоны и нейтроны — «нуклоны», отсюда «нуклеарная модель» строения ядра атома, то есть «ядерная модель».
Резерфорд открыл и изучал строение ядра в атоме, поэтому и его теорию называют нуклеарной.
Советы:
Помни! протон положительно заряженная частица, влияющая на свойства атома, а нейтрон не имеет заряда, но влияет на массу атома химического элемента.
Параграф №7, вопрос №4, стр 49
Условие:
Порядковый номер элемента в таблице Д. И. Менделеева равен 35. Какой это элемент? Чему равен заряд ядра его атома? Сколько протонов, электронов и нейтронов в его атоме?
Решение:
Вром — это элемент с порядковым номером 35. Заряд ядра его атома будет равен 35, а следовательно, число протонов и электронов будут равны 35. Количество нейтронов будет равно 45.
Советы:
Чтобы найти нейтроны, необходимо от атомной массы элемента отнять заряд ядра. А количество протонов и электронов равно заряду ядра, то бишь, порядковому номеру элемента.
А количество протонов и электронов равно заряду ядра, то бишь, порядковому номеру элемента.
Параграф №7, вопрос №5, стр 49
Условие:
На уроках биологии вы рассматривали клетки растений, используя световой микроскоп. Каков принцип действия этого микроскопа?
Решение:
Главный принцип работы светового микроскопа состоит в том, что через прозрачный или полупрозрачный предмет (объект исследования), размещенный на предметном столике, проходят лучи света и попадают на систему линз объектива, которые увеличивают изображение.
Советы:
В световой микроскоп нельзя увидеть атом или молекулу
Параграф №7, вопрос №6, стр 49
Условие:
Что выступает в роли аналога света в сканирующем микроскопе? Каков принцип действия этого микроскопа?
Решение:
в роли аналога света выступает очень тонкая игла-щуп, которую ведут у самой поверхности исследуемого вещества, как сканер.
Неровности этой поверхности, создаваемые атомами (выпуклости и впадины), как бы прощупываются электрическим током, возникающим между иглой и частицами, которые образуют исследуемую поверхность.
В результате с помощью мощного компьютера полученное изображение поверхности, построенное из отдельных атомов, возникает на мониторе. На рисунке приведено изображение надписи «Peace», выложенное атомами ксенона.
Советы:
Сканирующий микроскоп позволяет видить мельчайшие частицы в отличии от светового.
Параграф №7, вопрос №7, стр 49
Условие:
Что такое нанотехнологии? Почему эта отрасль науки и производства получила такое название?
Решение:
Нанотехнология — это технология изучения нанометровых объектов, и работы с объектами порядка нанометра (миллионная доля миллиметра) что сравнимо с размерами отдельных молекул, и атомов.
нанотехнология — междисциплинарная отрасль прикладной науки и техники занимающаяся изучением, методам анализа и синтеза новых нанометровых материалов. название получила ( с греч. nanos — «карлик» + «техно» — искусство, + «логос» — учение, понятие) из-за того, что исследования проводятся на базе материалов не превышающих значения 100 нм.
Советы:
Всегда вникайте в состав слова. В нем отражается суть понятия.
Строение атома
Атом — это наименьшая частица химического элемента, сохраняющая все его химические свойства. Атом состоит из ядра и вращающихся вокруг него электронов. Ядро также имеет сложное строение и состоит из нейтронов и электронов.
Число электронов равно числу протонов в атоме и определяется порядковым номером. В связи с этим атом в целом электронейтрален, так как электроны заряжены отрицательно, а протоны положительно. Заряд ядра также равен порядковому номеру. Число нейтронов рассчитывается по формуле N = A — Z, где N — общее число нейтронов, А — массовое число, Z — заряд ядра. Число энергетических уровней в атоме определяется номером периода. Число электронов на последнем внешнем уровне равно номеру группы.
Максимальное число электронов на энергетическом уровне определяется формулой N = 2 * n^2 , где N — общее число электронов на энергетическом уровне, n — номер уровня. 2) и т.д.
2) и т.д.
Каждый энергетический уровень делится на подуровни. На первом уровне только один подуровень — s. На втором уровне два подуровня — s и p. на третьем — s, p и d. На четвертом — s, p, d и f.
Максимальное число электронов на подуровнях
- 2 — максимальное число электронов на s-подуровне.
- 6 — максимальное число электронов на p-подуровне.
- 10 — максимальное число электронов на d-подуровне.
- 14 — максимальное число электронов на f-подуровне.
Максимальное число электронов на подуровне не зависит от номера уровня.
Заполнение энергетических уровней
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s
Геометрия орбиталей
Примеры
Полезные ссылки
Источник материала
Электронная оболочка атома (видео)
Строение атома (Часть 1) (видео)
Строение атома (Часть 2) (видео)
Строение атома. Ядерные силы (видео)
Ядерные силы (видео)
Дополнительные материалы
Модели строения атома (видео)
Строение атома: Атомное ядро (видео)
Химия. Строение атома: Строение электронных оболочек (видео)
Строение атома (видео)
Урок 44. движение как качественное изменение. ядерные реакции — Естествознание — 10 класс
Естествознание, 10 класс.
Урок 44. Движение как качественное изменение. Ядерные реакции
Перечень вопросов, рассматриваемых в теме: Могут ли одни химические элементы превращаться в другие? Когда было открыто явление радиоактивности и как оно изучалось? Каковы особенности процесса радиоактивного распада? Как происходят ядерные реакции?
Глоссарий по теме:
Химический элемент – вид атомов с одинаковым зарядом ядра.
Нуклид (от лат. nucleus – ядро) – вид атомов с определенным значением заряда ядра Z (число протонов в ядре) и массового числа А (сумма числа протонов и нейтронов в ядре).
Изотопы (от греч. isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
Атомное ядро – положительно заряженная центральная часть атома, состоящая из протонов и нейтронов (нуклонов).
Ядерная физика – раздел физики, изучающий структуры и свойства атомных ядер и их превращений – процессов радиоактивного распада и ядерных реакций.
Радиоактивность (от лат. radio – испускаю, излучаю и actives – действенный) – свойство атомных ядер самопроизвольно изменять свой состав путем испускания элементарных частиц или ядер.
Радиоактивный распад – спонтанное изменение состава нестабильных атомных ядер путем испускания элементарных частиц или ядерных фрагментов.
Период полураспада – это время, в течение которого распадается половина исходного числа радиоактивных атомов.
Ядерные реакции – это превращение атомных ядер при взаимодействии их с элементарными частицами, гамма-квантами или друг с другом.
Деление ядер – процесс, при котором из одного ядра возникают два ядра близких по массе.
Цепные ядерные реакции – это ядерные реакции, в которых частицы, вызывающие их, образуются и как продукты этих реакций.
Основная и дополнительная литература по теме урока:
1. Естествознание. 10 класс: учебник для общеобразоват. организаций: базовый уровень / И.Ю. Алексашина, К.В. Галактионов, И.С. Дмитриев, А.В. Ляпцев и др. / под ред. И.Ю. Алексашиной. – 3-е изд. – М.: Просвещение, 2017. – С. 193-195.
2. Энциклопедия для детей. Том 16. Физика Ч. 1. Биография физики. Путешествие в глубь материи. Механическая картина мира / Глав. ред. В.А. Володин. – М.: Аванта+, 2000. – С. 243-257..
3. Энциклопедия для детей. Том 16. Физика. Ч. 2. Электричество и магнетизм. Термодинамика и квантовая механика. Физика ядра и элементарных частиц / Глав. ред. В.А. Володин. – М.: Аванта+, 2000. – С. 275-291.
Энциклопедия для детей. Том 16. Физика. Ч. 2. Электричество и магнетизм. Термодинамика и квантовая механика. Физика ядра и элементарных частиц / Глав. ред. В.А. Володин. – М.: Аванта+, 2000. – С. 275-291.
Открытые электронные ресурсы по теме урока:
Статья: Радиоактивный распад // Научно-популярный портал «Элементы». URL: http://elementy.ru/trefil/21197/Radioaktivnyy_raspad
Статья: Ядерный распад и синтез // Научно-популярный портал «Элементы». URL: http://elementy.ru/trefil/21178/Yadernyy_raspad_i_sintez
Теоретический материал для самостоятельного изучения
Столетиями алхимики, веря в трансмутацию, пытались найти средство, позволяющее превращать одни элементы в другие, но сделать это в ходе химических превращений оказалось невозможным. Превращать одни химические элементы в другие стало возможным только в XX столетии, когда человек научился осуществлять ядерные реакции. Изучением структуры и свойств атомных ядер и их превращений – процессов радиоактивного распада и ядерных реакций, занимается ядерная физика.
В конце XIX века французский физик Антуан Анри Беккерель (1852 – 1908), изучая флуоресценцию солей урана, обнаружил, что эти соединения испускают неизвестное излучение, засвечивающее завёрнутую в чёрную бумагу фотопластинку. При этом обнаруженное излучение соли урана испускали независимо от того облучались они светом или нет. Новым явлением заинтересовались французские учёные Пьер Кюри (1859 – 1906) и Мария Склодовская-Кюри (1867 – 1934). В 1897 – 1898 гг. они установили, что обнаруженное излучение является свойством урана, которое не зависит от того, в каком соединении этот элемент содержится. Исследуя в 1898 г. урановую руду, учёные открыли два новых химических элемента – полоний и радий, которые также обладали радиоактивностью – такое название они предложили для обнаруженного самопроизвольного испускания атомами излучения (от лат. radio – испускаю, излучаю и actives – действенный).
Изучение радиоактивного излучения позволило обнаружить его неоднородность. Так в 1899 г. английский физик Эрнест Резерфорд (1871 – 1937) установил, что магнитное поле разделяет излучение на две составляющие, обладающие положительными и отрицательными зарядами. Эти составляющие радиоактивного излучения получили название альфа-лучи и бета-лучи (по первым буквам греческого алфавита). В 1900 г. французский физик и химик Поль Виллар (1860 – 1934) сумел выделить еще одну составляющую, которая не отклонялась магнитным полем – гамма-лучи. Анри Беккерелем было установлено, что бета-лучи представляют собой поток электронов. В 1908 г. Э. Резерфордом совместно с немецким физиком Хансом Гейгером (1882 – 1945) было доказано, что альфа-частицы являются ядрами атома гелия (заряд Z = +2 и массовое число A = 4).
Эти составляющие радиоактивного излучения получили название альфа-лучи и бета-лучи (по первым буквам греческого алфавита). В 1900 г. французский физик и химик Поль Виллар (1860 – 1934) сумел выделить еще одну составляющую, которая не отклонялась магнитным полем – гамма-лучи. Анри Беккерелем было установлено, что бета-лучи представляют собой поток электронов. В 1908 г. Э. Резерфордом совместно с немецким физиком Хансом Гейгером (1882 – 1945) было доказано, что альфа-частицы являются ядрами атома гелия (заряд Z = +2 и массовое число A = 4).
Радиоактивное излучение свидетельствует о том, что ядра атомов претерпевают распад, в результате которого они превращаются в ядра новых химических элементов. Выяснилось, что радиоактивностью обладают многие элементы, присутствующие в земной коре. Более того, все химические элементы, расположенные в периодической системе за висмутом, радиоактивны: все их нуклиды нестабильны. Нуклидом (от лат. nucleus – ядро) называют вид атомов с определенным значением заряда ядра и массой. Для обозначения нуклида используют название химического элемента, к которому через дефис записываю массовое число (например, уран-238) или знак химического элемента, рядом с которым наверху указывают массовое число, а внизу заряд ядра (например, 23892U). Разные нуклиды одного элемента по отношению друг к другу являются изотопами. Изотопы (от греч. isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
Для обозначения нуклида используют название химического элемента, к которому через дефис записываю массовое число (например, уран-238) или знак химического элемента, рядом с которым наверху указывают массовое число, а внизу заряд ядра (например, 23892U). Разные нуклиды одного элемента по отношению друг к другу являются изотопами. Изотопы (от греч. isos – равный, одинаковый; topos – место) – это разновидности атомов одного и того же химического элемента, атомные ядра которого имеют одинаковое число протонов и различное число нейтронов.
На рубеже XIX –XX вв. было установлено, что существует три вида самопроизвольных ядерных превращений (позже были обнаружены и другие виды, но они менее распространены).
Альфа-распад (α-распад) – самопроизвольное (спонтанное) изменение состава нестабильных атомных ядер, сопровождающееся испусканием α-частиц, каждая из которых состоит из двух протонов и двух нейтронов (ядро атома гелия 42He). Примером такого распада может служить превращение радия-226 в радон-222: 22688Ra → 22286Rn + 42α (где 42α – альфа-частица или ядро атома гелия).
Примером такого распада может служить превращение радия-226 в радон-222: 22688Ra → 22286Rn + 42α (где 42α – альфа-частица или ядро атома гелия).
Бета-распад (β-распад) происходит в результате того, что один из нейтронов нестабильного атомного ядра превращается в протон, при этом ядро испускает электрон и легкую частицу, называемую антинейтрино. Записать процесс можно следующим образом: 10n → 11p + -1e + ~ν. Примером такого радиоактивного распада может быть превращение тория-234 в протактиний-234: 23490Th → 23491Pa + -1e + ~ν.
Гамма-распад (γ-распад) представляет собой процесс испускания возбужденным ядром атома излучения с очень малой длиной волны – гамма-квантов. При этом изменение заряда ядра атома не происходит.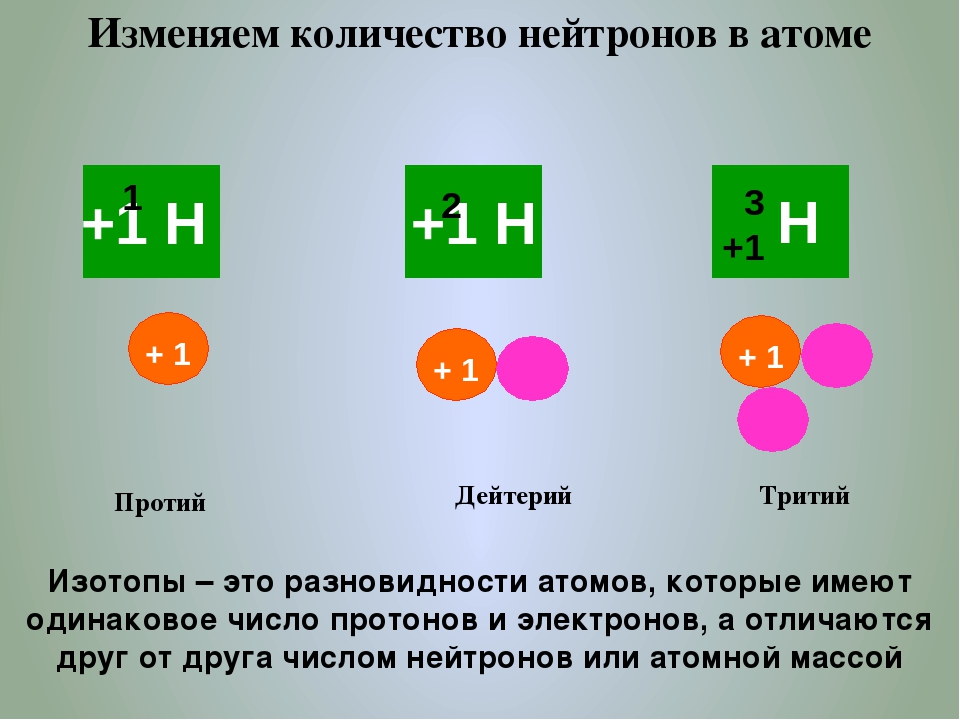
При всех этих распадах энергия ядра уменьшается. А что при этом происходит с зарядом ядра и массой? При α-распаде массовое число уменьшается на четыре единицы, а заряд ядра элемента – на две. При β-распаде атомный номер элемента увеличивается на единицу, а массовое число не изменяется. При γ-излучении, которое часто (но не всегда) сопутствует α- и β-распаду, ни атомный номер, ни массовое число не изменяются.
В ходе радиоактивного распада число имеющихся исходных атомов постепенно убывает. Изучая процессы радиоактивного распада во времени, Э. Резерфорд обнаружил, что через определенный промежуток времени – различающийся для разных элементов, количество того или иного радиоактивного элемента уменьшается в два раза. Этот промежуток времени, в течение которого распадается половина исходного числа радиоактивных атомов, был назван периодом полураспада Т1/2. Период полураспада характеризует скорость радиоактивного процесса и различается для разных радиоактивных изотопов. Если изотоп распадается быстро, то он называется короткоживущим. Значения Т1/2 для таких изотопов могут составлять 10-12 – 10-10 с и даже меньше. Примером может служить сверхлегкий изотоп кислорода-12, период полураспада которого составляет 10–21 с, или изотоп свинца-210 с периодом полураспада 1,5·10–4 с. Период полураспада долгоживущих, медленно распадающихся атомов, может достигать миллиардов лет. Так, например, для урана-238 период полураспада составляет 4,47·109 лет, для тория-232 – 1,405·1010 лет. Следует отметить, что скорость распада не зависит от внешних условий. Радиоактивный распад является статистическим процессом, поэтому нельзя определить, какой именно атом распадется в данный момент времени. Т.е ядро данного радиоактивного изотопа, родившееся только что, и ядро этого же изотопа, просуществовавшее миллионы лет имеют одинаковую вероятность распасться. Можно определить только среднее время жизни радиоактивного атома, если имеется большое число таких атомов.
Если изотоп распадается быстро, то он называется короткоживущим. Значения Т1/2 для таких изотопов могут составлять 10-12 – 10-10 с и даже меньше. Примером может служить сверхлегкий изотоп кислорода-12, период полураспада которого составляет 10–21 с, или изотоп свинца-210 с периодом полураспада 1,5·10–4 с. Период полураспада долгоживущих, медленно распадающихся атомов, может достигать миллиардов лет. Так, например, для урана-238 период полураспада составляет 4,47·109 лет, для тория-232 – 1,405·1010 лет. Следует отметить, что скорость распада не зависит от внешних условий. Радиоактивный распад является статистическим процессом, поэтому нельзя определить, какой именно атом распадется в данный момент времени. Т.е ядро данного радиоактивного изотопа, родившееся только что, и ядро этого же изотопа, просуществовавшее миллионы лет имеют одинаковую вероятность распасться. Можно определить только среднее время жизни радиоактивного атома, если имеется большое число таких атомов. Изменение числа атомов в процессе радиоактивного распада описывается законом радиоактивного распада: N = N0 2–t/T1/2, где N0 – число радиоактивных атомов в начальный момент времени t=0, N – число нераспавшихся атомов к моменту времени t, Т1/2 – период полураспада.
Изменение числа атомов в процессе радиоактивного распада описывается законом радиоактивного распада: N = N0 2–t/T1/2, где N0 – число радиоактивных атомов в начальный момент времени t=0, N – число нераспавшихся атомов к моменту времени t, Т1/2 – период полураспада.
В 1919 г. изучая воздействие альфа-излучения на различные газы, Э. Резерфорд обнаружил, что в результате бомбардировки альфа-частицами атомов азота получаются атомы кислорода. Этот процесс можно описать следующим образом: 147N + 42α → 178O + 11p (где 11p – протон или ядро атома водорода 11H). Таким образом, Резерфордом было осуществлено первое искусственное превращение элементов – ядерная реакция. Напомним, что ядерной реакцией называются превращение атомных ядер при взаимодействии их с элементарными частицами, гамма-квантами или друг с другом. От химической ядерная реакция отличается тем, что в ходе её изменяются ядра атомов, т.е. атомы одних элементов, превращаются в атомы других химических элементов. И ядерная реакция, и радиоактивный распад являются превращением одного атомного ядра (химического элемента) в другое ядро. Но если радиоактивный процесс происходит самопроизвольно и не зависит от внешнего воздействия, то ядерная реакция, наоборот, вызывается воздействием на атомное ядро других частиц (ядер, протонов, нейтронов, гамма-квантов).
От химической ядерная реакция отличается тем, что в ходе её изменяются ядра атомов, т.е. атомы одних элементов, превращаются в атомы других химических элементов. И ядерная реакция, и радиоактивный распад являются превращением одного атомного ядра (химического элемента) в другое ядро. Но если радиоактивный процесс происходит самопроизвольно и не зависит от внешнего воздействия, то ядерная реакция, наоборот, вызывается воздействием на атомное ядро других частиц (ядер, протонов, нейтронов, гамма-квантов).
Бомбардировкой альфа-частицами ядер различных атомов удалось осуществить множество ядерных превращений. В 1932 г. при бомбардировке альфа-частицами атомов бериллия английским физиком Джеймсом Чедвиком (1891 – 1974) был открыт нейтрон. Происходящий ядерный процесс можно изобразить следующим образом: 94Ве + 42α → 126С + 10n (где 10n – нейтрон). В 1934 г. французскими физикам Ирен Жолио-Кюри (1897 – 1956) и Фредериком Жолио-Кюри (1900 – 1958) была открыта искусственная радиоактивность – самопроизвольный распад нестабильных атомных ядер, полученных в ходе ядерных реакций. При облучении альфа-частицами алюминия им удалось получить не существующий в природе радиоактивный изотоп фософра-30. Уравнение, протекающей ядерной реакции можно представить следующим образом: 2713Al + 42α → 3015P + 10n. Период полураспада изотопа фосфора-30 составляет около 2,5 минут, при этом в ядре этого изотопа один из протонов превращается в нейтрон с испусканием позитрона (античастица электрона +1e) и нейтрино: 11p → 10n + +1e + ν. Процесс, происходящий с ядрами изотопа фосфора-30 можно записать следующим образом: 3015Р → 3014Si + +1e + ν.
французскими физикам Ирен Жолио-Кюри (1897 – 1956) и Фредериком Жолио-Кюри (1900 – 1958) была открыта искусственная радиоактивность – самопроизвольный распад нестабильных атомных ядер, полученных в ходе ядерных реакций. При облучении альфа-частицами алюминия им удалось получить не существующий в природе радиоактивный изотоп фософра-30. Уравнение, протекающей ядерной реакции можно представить следующим образом: 2713Al + 42α → 3015P + 10n. Период полураспада изотопа фосфора-30 составляет около 2,5 минут, при этом в ядре этого изотопа один из протонов превращается в нейтрон с испусканием позитрона (античастица электрона +1e) и нейтрино: 11p → 10n + +1e + ν. Процесс, происходящий с ядрами изотопа фосфора-30 можно записать следующим образом: 3015Р → 3014Si + +1e + ν.
Дальнейшие исследования показали, что с помощью ядерных реакций можно не только одни химические элементы превращать в другие, но и синтезировать новые элементы. Так в 1937 г. при облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые искусственно получен, а не выделен из природных соединений, химический элемент технеций Тс, получивший свое название от греческого слова «techne» – искусство, ремесло. В 1940 г. предсказанный Д.И. Менделеевым «экаиод» – химический элемент астат At, был получен искусственным путем в ходе ядерной реакции 20983Bi + 42α → 21185At + 2 10n.
Положительно заряженные частицы (протон, альфа-частица и др.), используемые в ядерных реакциях, испытывают сильное отталкивание при приближении к ядрам атомов, с которыми они должны взаимодействовать. Чтобы преодолеть это отталкивание альфа-частицы, протоны и т.д. должны обладать достаточно большой энергией, для этого их разгоняют с помощью специальных устройств – ускорителей. Первый ускоритель (циклотрон) был создан в 1931 году американским физиком Эрнестом Орландо Лоуренсом (1901 – 1958). С помощью циклотрона стало возможным проводить разнообразные ядерные реакции. Так, в 1932 г. Джоном Кокрофтом и Эрнестом Уолтоном была проведена первая ядерная реакция на быстрых протонах. Бомбардируя протонами литий, учёным удалось расщепить его на две альфа-частицы: 73Li + 11H → 42He + 42He.
Первый ускоритель (циклотрон) был создан в 1931 году американским физиком Эрнестом Орландо Лоуренсом (1901 – 1958). С помощью циклотрона стало возможным проводить разнообразные ядерные реакции. Так, в 1932 г. Джоном Кокрофтом и Эрнестом Уолтоном была проведена первая ядерная реакция на быстрых протонах. Бомбардируя протонами литий, учёным удалось расщепить его на две альфа-частицы: 73Li + 11H → 42He + 42He.
Наибольший интерес представляют реакции, проводимые с использованием нейтронов. Лишенные заряда нейтроны не испытывают отталкивания атомных ядер и легко в них проникают. Потоки нейтронов получают в результате ядерных реакций в ускорителях и в ядерных реакторах. Приведем несколько примеров ядерных реакций, вызываемых нейтронами: 2311Na + 10n → 2411Na + γ,
5927Co + 10n → 6027Co + γ. Подобные реакции применяются для получения новых изотопов: 3517Cl + 10n → 3516S + 11p или 2713Al + 10n → 2411Na + 42He.
Подобные реакции применяются для получения новых изотопов: 3517Cl + 10n → 3516S + 11p или 2713Al + 10n → 2411Na + 42He.
Большой практический интерес представляют реакции, вызываемые бомбардировкой нейтронами ядер урана-235 23592U. После поглощения нейтрона 23592U + 10n → 23692U ядро урана испытывает вынужденное деление, что приводит к образованию двух новых ядер и одновременно освобождается 2 или 3 нейтрона 10n. В результате такой реакции образуется смесь изотопов с массовыми числами равными приблизительно половине массового числа делящегося урана (смесь изотопов 9236Kr, 14156Ba и др.). Например: 23592U + 10n→ 23692U*→14456Ва + 8936Kr + 3 10n. При делении каждого ядра урана выделяется энергии порядка 200 МэВ. Процесс, при котором из одного атомного ядра возникает два близких по массе ядра, называют делением ядер.
При делении каждого ядра урана выделяется энергии порядка 200 МэВ. Процесс, при котором из одного атомного ядра возникает два близких по массе ядра, называют делением ядер.
Ядерный реактор оказался настоящей фабрикой радиоактивных изотопов.
Ядра изотопа 23592U могут захватывать нейтроны с небольшой энергией около 5 – 10 эВ (500 – 1000 кДж) – так называемые тепловые нейтроны, а нейтроны, образующиеся при делении ядра 23692U, обладают в миллионы раз большей энергией. Поэтому, чтобы реакция шла дальше за счет вылетающих при делении ядра нейтронов, их необходимо замедлить. Тогда пойдет цепная реакция деления урана – выделившиеся нейтроны, после замедления, будут захватываться другими ядрами 23592U и т. д. Ядерные реакции, в которых частицы, вызывающие их, образуются и как продукты этих реакций называются цепными ядерными реакциями. Осуществление таких реакций сопровождается выделением энергии и имеет большое практическое значение.
Резюме теоретической части.
1. В природе существуют разновидности атомов одного и того же элемента – изотопы, отличающиеся массами из-за разного содержания в ядрах их атомов нейтронов. В природе существуют радиоактивные изотопы, способные самопроизвольно изменять состав своих ядер. Все изотопы химических элементов, следующих за висмутом Bi в периодической системе химических элементов, являются радиоактивными. Многие химические элементы были получены искусственным путем в ходе ядерных реакций.
2. Превращение атомов одних химических элементов в другие возможно входе процессов радиоактивного распада и ядерных реакций. Изучением этих процессов занимается ядерная физика, зарождение которой началось на рубеже XIX – XX веков.
3. Процессы радиоактивного распада протекают самопроизвольно. В результате у ядер атомов изменятся состав и испускаются элементарные частицы, гамма-кванты или ядерные фрагменты. Наиболее распространенными являются α-распад, β-распад и γ-распад. Скорость радиоактивного процесса не зависит от внешних условий и характеризуется периодом полураспада, который сильно различается для радиоактивных изотопов разных химических элементов. Радиоактивный распад является статистическим процессом, который количественно описывается законом радиоактивного распада.
Скорость радиоактивного процесса не зависит от внешних условий и характеризуется периодом полураспада, который сильно различается для радиоактивных изотопов разных химических элементов. Радиоактивный распад является статистическим процессом, который количественно описывается законом радиоактивного распада.
4. Ядерные реакции, в отличие от процессов радиоактивного распада, протекают под внешним воздействием – атомные ядра бомбардируют другими ядрами, элементарными частицами или гамма-квантами. Бомбардирующие частицы чаще всего разгоняют с помощью специальных устройств – ускорителей. Наибольший интерес представляют ядерные реакции, проводимые с использованием нейтронов, потоки которых получают в результате ядерных реакций в ускорителях и в ядерных реакторах. Открытие деления ядер урана привело к осуществлению цепных ядерных реакций, которые имеют большое практическое значение.
5. Качественные изменения, происходящие с атомными ядрами в ходе процессов радиоактивного распада и ядерных реакций, можно рассматривать как одну из форм движения материи.
Примеры и разбор решения заданий тренировочного модуля:
1. Укажите верные утверждения:
Утверждение | Правильный ответ и пояснение |
А. Ядерные реакции приводят к превращению атомов одних химических элементов в другие. | Правильное утверждение. Химический элемент – это вид атомов с одинаковым зарядом ядра. В ходе ядерных реакций происходят изменения ядер атомов, в большинстве случаев меняется число протонов в ядре. Следовательно, в этих случаях происходит превращение атомов одних химических элементов в другие. |
Б. Радиоактивность атома химического элемента зависит от того, в каком химическом соединении он находится. | Неправильное утверждение. Радиоактивность – это свойство атомного ядра химического элемента, поэтому это свойство никак не зависит от того, в каком химическом соединении атом данного элемента находится. |
В. | Правильное утверждение. Альфа-распад сопровождается испусканием атомным ядром альфа-частиц – ядер атома гелия 42He, состоящих из двух протонов и двух нейтронов. Испустив альфа-частицу и потеряв два протона и два нейтрона, образовавшееся атомное ядро будет иметь массу на четыре единицы, а заряд на две единицы меньше, чем исходное ядро. |
2. Установление соответствие между элементами двух множеств. К каждой позиции первого столбца подберите соответствующую позицию второго.
Описание процесса | Вид явления |
1. При облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые был искусственно получен химический элемент технеций Тс. | А. Явление радиоактивности Б. |
2. В результате испускания ядром изотопа радия-226 альфа-частицы образуется изотоп радона-222. | |
3. При захвате ядром алюминия-27 нейтрона образуется ядро натрия-24 и альфа-частица. |
Правильный ответ:1 – Б; 2 – А; 3 – Б.
Описание процесса | Вид явления |
1. При облучении молибдена ядрами тяжёлого изотопа водорода дейтерия 21H был впервые был искусственно получен химический элемент технеций Тс. | Б. Ядерная реакция |
2. В результате испускания ядром изотопа радия-226 альфа-частицы образуется изотоп радона-222. | А. Явление радиоактивности |
3. При захвате ядром алюминия-27 нейтрона образуется ядро натрия-24 и альфа-частица. | Б. Ядерная реакция |
4.8: Изотопы — когда количество нейтронов меняется
Все атомы одного и того же элемента имеют одинаковое количество протонов, но некоторые могут иметь разное количество нейтронов. Например, у всех атомов углерода есть шесть протонов, и у большинства также шесть нейтронов. Но некоторые атомы углерода имеют семь или восемь нейтронов вместо обычных шести. Атомы одного и того же элемента, различающиеся числом нейтронов, называются изотопами . Многие изотопы встречаются в природе. Обычно один или два изотопа элемента являются наиболее стабильными и распространенными.Различные изотопы элемента обычно имеют одинаковые физические и химические свойства, потому что они имеют одинаковое количество протонов и электронов.
Например, у всех атомов углерода есть шесть протонов, и у большинства также шесть нейтронов. Но некоторые атомы углерода имеют семь или восемь нейтронов вместо обычных шести. Атомы одного и того же элемента, различающиеся числом нейтронов, называются изотопами . Многие изотопы встречаются в природе. Обычно один или два изотопа элемента являются наиболее стабильными и распространенными.Различные изотопы элемента обычно имеют одинаковые физические и химические свойства, потому что они имеют одинаковое количество протонов и электронов.
Пример: изотопы водорода
Водород — это пример элемента, имеющего изотопы. Три изотопа водорода смоделированы на рисунке \ (\ PageIndex {1} \). Большинство атомов водорода имеют только один протон, один электрон и не имеют нейтрона. Эти атомы просто называются водородом. Некоторые атомы водорода также имеют один нейтрон. Эти атомы представляют собой изотоп под названием дейтерий.У других атомов водорода есть два нейтрона. Эти атомы представляют собой изотоп под названием тритий.
Эти атомы представляют собой изотоп под названием тритий.
Рисунок \ (\ PageIndex {1} \): Три наиболее стабильных изотопа водорода: протий (A = 1), дейтерий (A = 2) и тритий (A = 3). (CC SA-BY 3.0; Баладжиджагадеш).
Для большинства элементов, кроме водорода, изотопы названы по их массовому числу. Например, атомы углерода с обычными 6 нейтронами имеют массовое число 12 (6 протонов + 6 нейтронов = 12), поэтому их называют углеродом-12. Атомы углерода с 7 нейтронами имеют атомную массу 13 (6 протонов + 7 нейтронов = 13).Эти атомы представляют собой изотоп под названием углерод-13.
Пример \ (\ PageIndex {1} \): изотопы лития
- Какой атомный номер и массовое число изотопа лития, содержащего 3 нейтрона?
- Какой атомный номер и массовое число у изотопа лития, содержащего 4 нейтрона?
Решение
Атом лития содержит в своем ядре 3 протона независимо от количества нейтронов или электронов.
а.
\ [\ begin {align} \ text {атомный номер} = \ left (\ text {количество протонов} \ right) & = 3 \ nonumber \\ \ left (\ text {количество нейтронов} \ right ») & = 3 \ nonumber \ end {align} \ nonumber \]
\ [\ begin {align} \ text {массовое число} & = \ left (\ text {количество протонов} \ right) + \ left (\ text {количество нейтронов} \ right) \ nonumber \\ \ text { массовое число} & = 3 + 3 \ nonumber \\ & = 6 \ nonumber \ end {align} \ nonumber \]
г.
\ [\ begin {align} \ text {атомный номер} = \ left (\ text {количество протонов} \ right) & = 3 \ nonumber \\ \ left (\ text {количество нейтронов} \ right ») & = 4 \ nonumber \ end {align} \ nonumber \]
\ [\ begin {align} \ text {массовое число} & = \ left (\ text {количество протонов} \ right) + \ left (\ text {количество нейтронов} \ right) \ nonumber \\ \ text { массовое число} & = 3 + 4 \ nonumber \\ & = 7 \ nonumber \ end {align} \ nonumber \]
Обратите внимание, что поскольку атом лития всегда имеет 3 протона, атомный номер лития всегда равен 3.Однако массовое число равно 6 в изотопе с 3 нейтронами и 7 в изотопе с 4 нейтронами. В природе существуют только определенные изотопы. Например, литий существует как изотоп с 3 нейтронами и как изотоп с 4 нейтронами, но он не существует как изотоп с 2 нейтронами или как изотоп с 5 нейтронами.
Стабильность изотопов
Атомам необходимо определенное соотношение нейтронов и протонов, чтобы иметь стабильное ядро. Слишком много или слишком мало нейтронов по сравнению с протонами приводит к нестабильному или радиоактивному ядру, которое рано или поздно распадется до более стабильной формы.Этот процесс называется радиоактивным распадом. Многие изотопы имеют радиоактивные ядра, и эти изотопы называются радиоизотопами. Когда они распадаются, они выделяют частицы, которые могут быть вредными. Вот почему радиоактивные изотопы опасны и почему работа с ними требует специальных защитных костюмов. Изотоп углерода, известный как углерод-14, является примером радиоизотопа. Напротив, изотопы углерода, называемые углеродом-12 и углеродом-13, стабильны.
Все это обсуждение изотопов возвращает нас к атомной теории Дальтона.Согласно Дальтону, атомы данного элемента идентичны. Но если в атомах одного элемента может быть разное количество нейтронов, значит, у них также может быть разная масса! Как Далтон это пропустил? Оказывается, что элементы, встречающиеся в природе, существуют как постоянные однородные смеси их встречающихся в природе изотопов. Другими словами, кусок лития всегда содержит оба типа встречающегося в природе лития (тип с 3 нейтронами и тип с 4 нейтронами). Более того, он всегда содержит оба в одинаковых относительных количествах (или «относительном количестве»).В куске лития \ (93 \% \) всегда будет литий с 4 нейтронами, а оставшийся \ (7 \% \) всегда будет литием с 3 нейтронами.
Дальтон всегда экспериментировал с большими кусками элемента — кусками, которые содержали все встречающиеся в природе изотопы этого элемента. В результате, когда он проводил свои измерения, он фактически наблюдал усредненные свойства всех различных изотопов в образце. Для большинства наших целей в химии мы будем делать то же самое и иметь дело со средней массой атомов.К счастью, помимо разной массы, большинство других свойств разных изотопов схожи.
Есть два основных способа, которыми ученые часто показывают массовое число интересующего их атома. Важно отметить, что массовое число — , а не , указанное в периодической таблице. Эти два способа включают запись символа ядра или указание имени элемента с записанным массовым числом.
Для записи ядерного символа массовое число помещается в верхнем левом углу (верхний индекс) химического символа, а атомный номер помещается в нижний левый (нижний индекс) символа.{238} _ {92} U} \]
В представленном выше ядре никеля атомный номер 28 указывает, что ядро содержит 28 протонов, и, следовательно, оно должно содержать 31 нейтрон, чтобы иметь массовое число 59. Ядро урана имеет 92 протона, как и все ядра урана. ; и это конкретное ядро урана имеет 146 нейтронов.
Другой способ представления изотопов — добавление дефиса и массового числа к химическому названию или символу. Таким образом, двумя ядрами будут никель-59 или Ni-59 и уран-238 или U-238, где 59 и 238 — массовые числа двух атомов, соответственно.{40} _ {19} \ ce {K} \)?
Решение
\ [\ text {атомный номер} = \ left (\ text {количество протонов} \ right) = 19 \]
Для всех атомов без заряда количество электронов равно количеству протонов.
\ [\ text {количество электронов} = 19 \]
Массовое число 40 представляет собой сумму протонов и нейтронов.
Чтобы найти количество нейтронов, вычтите количество протонов из массового числа.
\ [\ text {количество нейтронов} = 40 — 19 = 21.\]
Пример \ (\ PageIndex {3} \): Zinc-65
Сколько протонов, электронов и нейтронов содержится в атоме цинка-65?
Решение
\ [\ text {число протонов} = 30 \]
Для всех атомов без заряда количество электронов равно количеству протонов.
\ [\ text {количество электронов} = 30 \]
Массовое число 65 — это сумма протонов и нейтронов.
Чтобы найти количество нейтронов, вычтите количество протонов из массового числа.{45} _ {20} \ ce {Ca} \)
- Ответ:
- 27 протонов, 27 электронов, 33 нейтрона
- Ответ b:
- 11 протонов, 11 электронов, 13 нейтронов
- Ответ c:
- 20 протонов, 20 электронов, 25 нейтронов
- Ответ d:
- 38 протонов, 38 электронов, 52 нейтрона
вопросов и ответов — Как узнать количество протонов, электронов и нейтронов в атоме элемента?
Сколько протонов, электронов и нейтронов содержится в атоме криптона, углерода, кислорода, неона, серебра, золота и т. Д…?
Чтобы узнать количество протонов, электронов и нейтронов в атоме, просто выполните следующие простые шаги:
Шаг 1 — Сбор информации
Первое, что вам нужно сделать, это найти некоторую информацию о вашем элементе. Перейдите к Периодической таблице элементов и щелкните свой элемент. Если это упростит задачу, вы можете выбрать свой элемент из алфавитного списка.
Используйте Таблицу элементов, чтобы найти атомный номер и атомный вес вашего элемента. Атомный номер — это число, расположенное в верхнем левом углу, а атомный вес — это число, расположенное внизу, как в этом примере для криптона:
Шаг 2 — Число протонов равно…
Атомный номер — это количество протонов в атоме элемента. В нашем примере атомный номер криптона 36. Это говорит нам о том, что атом криптона имеет в своем ядре 36 протонов.
Здесь интересно то, что каждые атома криптона содержат 36 протонов. Если в атоме нет 36 протонов, это не может быть атом криптона. Добавление или удаление протонов из ядра атома создает другой элемент. Например, удаление одного протона из атома криптона создает атом брома.
Шаг 3 — Число электронов …
По определению, атомы не имеют полного электрического заряда. Это означает, что должен быть баланс между положительно заряженными протонами и отрицательно заряженными электронами. Атомы должны иметь равное количество протонов и электронов . В нашем примере атом криптона должен содержать 36 электронов, так как он содержит 36 протонов.
Электроны особым образом расположены вокруг атомов. Если вам нужно знать, как электроны расположены вокруг атома, взгляните на «Как мне читать таблицу конфигурации электронов?» страница.
Атом может приобретать или терять электроны, превращаясь в так называемый ион . Ион — это не что иное, как электрически заряженный атом. Добавление или удаление электронов из атома не меняет его элемент, только его чистый заряд.
Например, при удалении электрона из атома криптона образуется ион криптона, который обычно записывается как Kr + . Знак плюс означает, что это положительно заряженный ион. Он заряжен положительно, потому что из атома был удален отрицательно заряженный электрон.Число оставшихся 35 электронов было меньше 36 положительно заряженных протонов, что привело к заряду +1.
Шаг 4 — Число нейтронов …
Атомный вес в основном является мерой общего числа частиц в ядре атома . На самом деле все не так чисто. Атомный вес на самом деле является средневзвешенным значением всех встречающихся в природе изотопов элемента по отношению к массе углерода-12. Не понял этого? Неважно.Все, что вам действительно нужно найти, это массовое число . К сожалению, массовое число не указано в Таблице элементов. К счастью, чтобы найти массовое число, все, что вам нужно сделать, это округлить атомный вес до ближайшего целого числа . В нашем примере массовое число криптона равно 84, поскольку его атомный вес 83,80 округляется до 84.
Массовое число — это количество частиц в ядре атома. Помните, что ядро состоит из протонов и нейтронов.Итак, если мы хотим, мы можем написать:
Массовое число = (Число протонов) + (Число нейтронов)
Для криптона это уравнение принимает следующий вид:
84 = (Число протонов) + (Число нейтронов)
Если бы мы только знали, сколько протонов у криптона, мы могли бы выяснить, сколько в нем нейтронов. Подождите … Мы с по знаем, сколько протонов в криптоне! Мы сделали это еще в Step 2 ! Атомный номер (36) — это количество протонов в криптоне.Подставляя это в уравнение, мы получаем:
84 = 36 + (количество нейтронов)
Какое число, добавленное к 36, дает 84? Надеюсь, вы сказали 48. Это количество нейтронов в атоме криптона.
Здесь интересно то, что добавление или удаление нейтронов из атома не создает другого элемента. Скорее, он создает более тяжелую или более легкую версию этого элемента. Эти разные версии называются изотопами, и большинство элементов на самом деле представляют собой смесь разных изотопов.
Если бы вы могли захватить атомы криптона и подсчитать количество нейтронов, которые у каждого из них, вы бы обнаружили, что у большинства из них будет 48, у других — 47, у некоторых — 50, у некоторых — 46, у некоторых — 44 и очень немногие будут иметь 42. Вы бы посчитали разное количество нейтронов, потому что криптон представляет собой смесь шести изотопов.
Вкратце …
Для любого элемента:
Количество протонов = атомный номер
Количество электронов = количество протонов = атомный номер
Количество нейтронов = массовое число — атомный номер
Для криптона:
Число протонов = атомный номер = 36
Число электронов = Число протонов = атомный номер = 36
Число нейтронов = массовое число — атомный номер = 84 — 36 = 48
Связанные страницы:
Математическая игра с элементами
Все об атомах
Видео — Как нарисовать атом!
Периодическая таблица элементов
Сколько электронов умещается в каждой оболочке атома?
Как прочитать таблицу электронной конфигурации?
Как определить, сколько протонов, нейтронов и электронов в атоме?
2.4: Нейтроны: изотопы и расчеты массовых чисел
Задачи обучения
- Опишите расположение, заряд и относительную массу нейтрона.
- Определите изотоп и массовое число.
- Определите количество протонов, нейтронов и электронов в определенном изотопе элемента.
- Представляет отдельный изотоп элемента с использованием трех основных элементных символизмов.
Последняя субатомная частица не была открыта до 1932 года. Чтобы учесть нейтральный заряд атома в целом, количество положительно заряженных протонов и отрицательно заряженных электронов в атоме должно быть одинаковым.Следовательно, любые оставшиеся субатомные частицы должны быть незаряженными, чтобы не нарушить этот установленный баланс заряда. В самом деле, нейтронов , названные по их нейтральному заряду, не обладают никакими электрическими свойствами. Следовательно, эти субатомные частицы, которые обозначены обозначением «n 0 », было невероятно трудно обнаружить. Нейтроны также находятся в ядре атома, а масса нейтрона оказалась на , всего на немного больше, чем масса протона.
Каждая субатомная частица существует для определенной цели. Как было сказано в предыдущем разделе, количество валентных электронов, присутствующих в атоме, определяет реакционную способность этого элемента. Число протонов, обнаруженных в атоме, определяет идентичность этого атома, и все протоны атома коллективно притягивают окружающие электроны, удерживая последние связанные с атомом. Напомним, однако, что все протоны, каждый из которых несет заряд +1, плотно упакованы в центральную область атома.Следовательно, каждый положительно заряженный протон должен сильно отталкиваться каждым другим протоном в ядре, и, кроме того, общая сила этих сил отталкивания достаточно существенна, чтобы расколоть ядро. Однако нейтроны эффективно действуют как «ядерный клей» и позволяют протонам существовать в непосредственной физической близости друг от друга. Другими словами, нейтроны — это субатомная частица, ответственная за поддержание структурной целостности ядра.
Наконец, напомним, что каждый атом определенного элемента должен иметь определенное количество протонов и электронов.Каждый атом углерода C, который существует в известной вселенной, равен , определенному как , чтобы содержать 6 протонов, потому что его атомный номер равен 6, и он также должен содержать 6 электронов, чтобы атом сохранял общий чистый нейтральный заряд. Однако количество нейтронов в атоме элемента составляет , а не , определяемое атомным номером этого элемента. Фактически, количество нейтронов, присутствующих в элементе, может варьироваться от атома к атому. «Клеевую» аналогию, приведенную в предыдущем абзаце, можно расширить, чтобы объяснить это явление.Хотя для приклеивания одного объекта к другому требуется минимальное количество клея, небольшое количество излишка клея не помешает этим объектам слипаться, но большой избыток клея может оказаться проблематичным. Точно так же каждый элемент должен содержать минимальное количество нейтронов, чтобы удерживать ядро вместе, но может содержать небольшое количество дополнительных нейтронов без ущерба для структурной целостности ядра. Однако ядро, содержащее слишком много нейтронов, станет нестабильным и подвергнется радиоактивному распаду , который будет обсуждаться в главе 9 этого текста.
Массовое число
Массовое число атома равно общему количеству протонов и нейтронов, содержащихся в его ядре. Это определение можно представить в виде уравнения, как показано ниже.
Массовое число = количество протонов + количество нейтронов
Истинная масса атома — невероятно малая величина. Для упрощения используемых численных значений массе отдельного протона присвоено значение 1 атомных единиц массы или а.е.м. .Поскольку масса нейтрона примерно такая же, как масса протона, каждому присутствующему нейтрону также дается значение 1 а.е.м. Поскольку масса электрона составляет 1/2 000 или массы протона, любой вклад, который электроны вносят в общую массу атома, незначителен. Следовательно, количество электронов, присутствующих в атоме, игнорируется при вычислении массового числа этого атома.
Пример \ (\ PageIndex {1} \)
Воспользуйтесь периодической таблицей, чтобы вычислить массовое число атома водорода, содержащего 2 нейтрона.
Решение
Массовое число атома рассчитывается путем сложения количества протонов и нейтронов, находящихся в этом атоме. Дано количество нейтронов, но количество протонов должно определяться по атомному номеру элемента. В этом случае водород (H) имеет атомный номер 1 и, следовательно, каждый атом водорода будет содержать 1 протон. Уравнение, показанное выше, может быть применено следующим образом.
Массовое число = количество протонов + количество нейтронов
Массовое число = 1 + 2
Следовательно, этот конкретный атом водорода будет иметь массовое число 3 .
Обратите внимание, что массовое число, вычисленное в примере \ (\ PageIndex {1} \), не совпадает с числом под символом элемента и названием водорода в периодической таблице. Это несоответствие можно объяснить тонкой, но невероятно важной информацией: вычисление, выполненное в примере \ (\ PageIndex {1} \), было выполнено для одиночного атома и водорода. Однако периодическая таблица предназначена для представления всех атомов водорода в известной Вселенной.Поскольку на каждые существующих атомов водорода должны содержать 1 протон, атомный номер, написанный над символом элемента водорода, действительно представляет на каждые атома водорода.
Однако помните, что количество нейтронов, содержащихся в элементе, может варьироваться от атома к атому. Изменение количества нейтронов, присутствующих в атоме, в свою очередь, приведет к тому, что эти отдельные атомы водорода будут иметь разные расчетные массовые числа. Эти отдельные «версии» элемента называются изотопами , которые определяются как атомы элемента, которые имеют одинаковые атомные номера и, следовательно, содержат одинаковое количество протонов, но разные массовые числа и, следовательно, содержат разные числа нейтронов.Три изотопа водорода смоделированы на рисунке \ (\ PageIndex {1} \). Большинство атомов водорода имеют один протон, один электрон и не содержат нейтронов, но менее распространенные изотопы водорода могут содержать один или два нейтрона. Водород уникален тем, что его изотопам даны специальные имена, которые также показаны ниже на рисунке \ (\ PageIndex {1} \).
Рисунок \ (\ PageIndex {1} \): три самых стабильных изотопа водорода.
По пространственным причинам перечисление массовых чисел для всех изотопов элемента в одном прямоугольнике периодической таблицы нецелесообразно.Вместо этого вычисляется средневзвешенное значение, называемое средневзвешенным значением . Средневзвешенное значение учитывает не только массовое число каждого изотопа, но также то, насколько распространен или распространен этот изотоп в природе по отношению к каждому из других изотопов этого элемента. Следовательно, средняя атомная масса — это величина, которая действительно представляет всех изотопов данного элемента, что делает его подходящим для включения в периодическую таблицу.
Пример \ (\ PageIndex {2} \)
Используйте периодическую таблицу, чтобы определить следующую информацию для атома с атомным номером 74 и массовым числом 186.
- Символ элемента
- Название элемента
- Число протонов, содержащихся в атоме
- Количество электронов в атоме
- Количество нейтронов в атоме
Решения
- Атомный номер элемента находится над символом элемента в рамке периодической таблицы. Элемент с атомным номером 74 обозначен как W .
- Элемент с атомным номером 74 называется tungsten .
- Количество протонов, присутствующих в атоме, определяется атомным номером элемента. Следовательно, каждый атом вольфрама содержит 74 протонов .
- Поскольку атом должен иметь общий нейтральный заряд, количество протонов и электронов в атоме элемента должно быть одинаковым. Следовательно, каждый атом вольфрама также содержит 74 электронов .
- Массовое число атома рассчитывается путем сложения количества протонов и нейтронов, обнаруженных в этом атоме, как показано ниже.
Массовое число = количество протонов + количество нейтронов
Поскольку массовое число было предоставлено, это уравнение можно изменить, чтобы определить количество нейтронов, содержащихся в этом конкретном изотопе вольфрама.
186 = 74 + количество нейтронов
186-74 = количество нейтроновСледовательно, этот конкретный атом вольфрама содержит 112 нейтронов .
Символизм стихий
Всего выделено 252 стабильных изотопа для 80 различных элементов.Фактор количества наблюдаемых нестабильных изотопов приводит к значительному увеличению общего количества известных элементарных изотопов. Хотя каждый из трех наиболее распространенных изотопов водорода имеет уникальное имя, в конечном итоге было бы крайне непрактично устанавливать разные имена для на каждый изотоп, на на каждый элемент , существование которого было доказано. Таким образом, ученые используют три различных элементарных символа для обозначения конкретных изотопов элементов.Первые два символа очень похожи в том, что каждый включает имя элемента или символ элемента, за которым следует тире и числовое значение, которое соответствует массовому числу конкретного изотопа этого элемента. В третьем типе элементарного символизма, который называется ядерным символом , массовое число изотопа размещается как надстрочный индекс перед символом элемента, а атомный номер элемента записывается непосредственно под массовым числом.Важно отметить разницу между изотопом и символикой элемента . Рисунок \ (\ PageIndex {2} \) моделирует эти три различных элементарных символов , которые все представляют один и тот же изотоп , поскольку каждый из них имеет идентичное массовое число .
Рисунок \ (\ PageIndex {2} \): три элементарных символа для одного изотопа никеля. Пример \ (\ PageIndex {3} \)
Запишите ядерный символ изотопа, описанный в примере \ (\ PageIndex {2} \).{40} _ {19} \ ce {K} \)
Решения
- Этот изотоп обозначен ядерным символом. В этих обозначениях атомный номер изотопа записывается в виде нижнего индекса. Поскольку атомный номер указывает как количество протонов, так и количество электронов, присутствующих в атоме, этот изотоп содержит 19 протонов и 19 электронов . Количество нейтронов в изотопе можно рассчитать по его массовому числу, которое записывается в виде верхнего индекса в символе ядра.
Массовое число = количество протонов + количество нейтронов
40 = 19 + количество нейтронов
40-19 = количество нейтроновСледовательно, в этом изотопе калия (K) 21 нейтрон .
Этот изотоп представлен вторым символом, показанным на рисунке \ (\ PageIndex {2} \). При использовании этого обозначения необходимо использовать имя элемента, чтобы найти его атомный номер. Поскольку цинк (Zn) имеет атомный номер 30, этот изотоп содержит 30 протонов и 30 электронов .Число нейтронов в изотопе можно снова рассчитать по его массовому числу, которое представляет собой числовое значение, записанное после тире в обоих представлениях, показанных на рисунке \ (\ PageIndex {2} \).
Массовое число = количество протонов + количество нейтронов
65 = 30 + количество нейтронов
65-30 = количество нейтроновСледовательно, в этом изотопе цинка (Zn) 35 нейтронов .
Упражнение \ (\ PageIndex {1} \)
Определите, сколько протонов, электронов и нейтронов присутствует в атоме каждого из следующих изотопов.{60} _ {27} \ ce {Co} \)
- Ответьте на
- Этот изотоп обозначен ядерным символом. В этих обозначениях атомный номер изотопа записывается в виде нижнего индекса. Поскольку атомный номер указывает как количество протонов, так и количество электронов, присутствующих в атоме, этот изотоп содержит 27 протонов и 27 электронов . Количество нейтронов в изотопе можно рассчитать по его массовому числу, которое записывается в виде верхнего индекса в символе ядра.
Массовое число = количество протонов + количество нейтронов
60 = 27 + количество нейтронов
60-27 = количество нейтроновСледовательно, в этом изотопе кобальта (Co) 33 нейтронов .
- Ответ б
- Этот изотоп представлен вторым символом, показанным на рисунке \ (\ PageIndex {2} \). При использовании этого обозначения необходимо использовать имя элемента, чтобы найти его атомный номер. Поскольку уран (U) имеет атомный номер 92, этот изотоп содержит 92 протонов и 92 электрона .Число нейтронов в изотопе можно снова рассчитать по его массовому числу, которое представляет собой числовое значение, записанное после тире в обоих представлениях, показанных на рисунке \ (\ PageIndex {2} \).
Массовое число = количество протонов + количество нейтронов
238 = 92 + количество нейтронов
238 — 92 = количество нейтроновСледовательно, в этом изотопе урана (U) содержится 146 нейтронов и нейтронов.
- Ответ c
- Этот изотоп представлен с использованием первого символа, показанного на рисунке \ (\ PageIndex {2} \).При использовании этого обозначения необходимо использовать символ элемента, чтобы найти его атомный номер. Поскольку у натрия (Na) атомный номер 11, этот изотоп содержит 11 протонов и 11 электронов . Число нейтронов в изотопе можно снова рассчитать по его массовому числу, которое представляет собой числовое значение, записанное после тире в обоих представлениях, показанных на рисунке \ (\ PageIndex {2} \).
Массовое число = количество протонов + количество нейтронов
25 = 11 + количество нейтронов
25-11 = количество нейтроновСледовательно, в этом изотопе натрия (Na) 14 нейтронов .
Как определить количество нейтронов, протонов и электронов для атомов, ионов и изотопов
Обновлено 9 марта 2020 г.
Автор Рити Гупта
Рецензент: Lana Bandoim, B.S.
Когда вы пытаетесь определить количество нейтронов, протонов или электронов, которые имеют различные химические соединения, периодическая таблица станет вашим лучшим другом. Посмотрите, как использовать периодическую таблицу, а также ядерную нотацию, чтобы найти количество субатомных частиц, связанных с любым химическим веществом.
Чтение периодической таблицы
Периодическая таблица сообщает много того, что вам нужно знать о каждом элементе, включая количество электронов, протонов и нейтронов.
Взгляните на запись для углерода в периодической таблице (см. Раздел Ресурсы). Какую информацию дает вам запись о углероде?
1. Самый большой компонент — это химический символ для элемента. Для углерода это C.
2. Над символом находится атомный номер (Z), который равен количеству протонов в ядре и количеству электронов в электронном облаке (при условии, что атом нейтрален).Для углерода Z = 6.
3. Под символом указана атомная масса. Хотя это число представляет собой средневзвешенное значение масс всех изотопов элемента, округлив его до ближайшего целого числа, вы найдете массовое число наиболее распространенного изотопа. Для углерода массовое число (M) равно 12. Это число является суммой количества протонов и нейтронов.
Теперь вы знаете, что для нейтрального атома углерода число электронов равно шести, число протонов — шесть, но каково число нейтронов? Вы можете использовать массовое число, чтобы найти это.Просто возьмите M и вычтите Z. Для углерода это означает, что существует шесть нейтронов.
Определение числа субатомных частиц в ионах
Ионы образуются, когда атом теряет или приобретает электроны. Число в надстрочном индексе скажет вам величину этого изменения. Допустим, у вас есть Cl — . Сколько электронов, протонов и нейтронов у этого иона?
Процесс поиска этих значений очень похож на то, что было сделано выше. Однако теперь нужно учитывать тот факт, что атом не является нейтральным.
Из периодической таблицы Менделеева вы можете сказать, что у хлора 17 протонов и 18 нейтронов (обозначены буквами M-Z или 35-17).
Учитывая, что суммарный заряд отрицательный, электронов должно быть больше, чем протонов. Вы можете использовать следующее уравнение:
Подсоединение 17 для протонов (p +) и -1 для заряда дает:
Таким образом, ион хлора имеет 18 электронов.
Определение числа субатомных частиц в изотопах
Изотопы — это формы одного и того же элемента с различным числом нейтронов.Число протонов не может быть изменено, так как, как только это число (Z) изменится, изменится и элемент. Когда речь идет об изотопах, часто может оказаться полезным ядерное обозначение .
Используя ядерную нотацию, можно записать углерод-12 12 6 C.
Ядерная нотация сообщает вам три вещи:
1. Химический символ элемента (C для углерода в примере выше)
2. Массовое число или количество нейтронов и протонов в ядре является верхним индексом (12 в примере выше).Массовое число = # нейтронов + # протонов. Подсказка: это число, на которое следует обращать внимание при исследовании изотопов.
3. Атомный номер или число протонов (Z) является нижним индексом. Для элемента это всегда одно и то же. (6 для углерода в примере выше).
Например, углерод-12 будет записан в ядерной нотации 12 6 C, а изотоп углерода-13 будет записан 13 6 C. Итак, сколько электронов, протонов и нейтронов образует углерод. -13 есть?
Число протонов и электронов — это индекс (6).
Чтобы найти количество нейтронов, используйте следующее уравнение:
Подключив то, что вы знаете, дает:
Углерод-13 имеет семь нейтронов, а углерод-12 — шесть.
Массовое число | Химия для неосновных специалистов
Цели обучения
- Определите массовое число.
- Рассчитайте массовое число, если задано количество протонов и нейтронов.
- Вычислить количество нейтронов при заданном атомном номере.
Как определить массу химического вещества?
Часто студенту необходимо взвесить химическое вещество для эксперимента.Если он или она использует часовое стекло (маленький круглый предмет, который будет удерживать твердый химикат), сначала необходимо определить вес часового стекла. Затем в стекло добавляют твердое вещество и измеряют вес стекла и твердого вещества. Показание весов — это сумма стакана плюс химикат.
История определения атомной массы
В рамках своего исследования атомов Джон Дальтон определил ряд атомных масс элементов в начале 1800-х годов. Атомные веса были основой периодической таблицы, которую разработал Менделеев.Первоначально все атомные веса были основаны на сравнении с водородом, атомный вес которого равен единице. После открытия протона ученые предположили, что вес атома по существу равен весу протонов — электроны, как известно, почти ничего не вносят в атомный вес элемента.
Этот подход работал до тех пор, пока мы не научились определять количество протонов в элементе. Затем мы увидели, что атомный вес элемента часто вдвое превышает количество протонов (или больше).Открытие нейтрона дало недостающую часть картины. Атомная масса, как теперь известно, складывается из протонов и нейтронов в ядре.
Массовое число
Резерфорд показал, что большая часть массы атома сосредоточена в его ядре, которое состоит из протонов и нейтронов. Массовое число определяется как общее количество протонов и нейтронов в атоме. Рассмотрим Таблицу ниже, которая показывает данные из первых шести элементов периодической таблицы.
| Имя | Символ | Атомный номер | Протоны | Нейтроны | Электроны | Массовое число |
| Водород | H | 1 | 1 | 0 | 1 | 1 |
| Гелий | He | 2 | 2 | 2 | 2 | 4 |
| Литий | Ли | 3 | 3 | 4 | 3 | 7 |
| Бериллий | Be | 4 | 4 | 5 | 4 | 9 |
| Бор | B | 5 | 5 | 6 | 5 | 11 |
| Углерод | С | 6 | 6 | 6 | 6 | 12 |
Рассмотрим элемент гелий.Его атомный номер 2, поэтому в его ядре есть два протона. Его ядро также содержит два нейтрона. Поскольку 2 + 2 = 4, мы знаем, что массовое число атома гелия равно 4. Наконец, атом гелия также содержит два электрона, поскольку количество электронов должно равняться количеству протонов. Этот пример может заставить вас поверить, что атомы имеют одинаковое количество протонов и нейтронов, но дальнейшее изучение приведенной выше таблицы покажет, что это не так. Литий, например, имеет три протона и четыре нейтрона, поэтому его массовое число составляет 7.
Зная массовое число и атомный номер атома, вы можете определить количество нейтронов, присутствующих в этом атоме, путем вычитания.
Количество нейтронов = массовое число — атомный номер
Атомы элемента хрома (Cr) имеют атомный номер 24 и массовое число 52. Сколько нейтронов находится в ядре атома хрома? Чтобы определить это, вы должны вычесть, как показано:
52-24 = 28 нейтронов в атоме хрома
Состав любого атома можно проиллюстрировать сокращенными обозначениями с использованием атомного номера и массового числа.{52} _ {24} \ text {Cr} [/ latex].
Другой способ обозначить конкретный атом — написать массовое число атома после имени, разделенное дефисом. Вышеупомянутый атом можно было бы записать как хром-52.
Сводка
- Массовое число определяется как общее количество протонов и нейтронов в атоме.
- Количество нейтронов = массовое число — атомный номер.
Практика
Воспользуйтесь ссылкой ниже, чтобы ответить на следующие вопросы:
http: // education.jlab.org/qa/pen_number.html
- Какие данные в периодической таблице показывают количество протонов в атоме?
- Как определить количество нейтронов в атоме?
- Какое массовое число у атома?
Обзор
- Кто первым определил атомный вес элементов?
- На чем основывались первоначальные атомные веса?
- Почему расчеты, основанные на количестве протонов, не годились для определения атомного веса?
- Атом олова имеет атомный номер 50 и массовое число 118.Сколько нейтронов присутствует в этом атоме?
- Каково массовое число атома кобальта, содержащего 27 протонов и 30 нейтронов?
Глоссарий
- массовое число: Общее количество протонов и нейтронов в атоме.
Атомный номер и массовое число
Цель обучения
- Определите соотношение между массовым числом атома, его атомным номером, его атомной массой и количеством субатомных частиц
Ключевые моменты
- Нейтральные атомы каждого элемента содержат равное количество протонов и электронов.
- Число протонов определяет атомный номер элемента и используется, чтобы отличить один элемент от другого.
- Количество нейтронов варьируется, в результате чего образуются изотопы, которые представляют собой разные формы одного и того же атома, которые различаются только количеством нейтронов, которыми они обладают.
- Вместе количество протонов и количество нейтронов определяют массовое число элемента.
- Поскольку изотопы элемента имеют несколько разные массовые числа, атомная масса рассчитывается путем получения среднего массового числа его изотопов.
Условия
- атомная масса Средняя масса атома с учетом всех его встречающихся в природе изотопов.
- Сумма количества протонов и нейтронов в атоме.
- Число протонов в атоме.
Массовое число
Атомный номер
Атомный номер
Нейтральные атомы элемента содержат равное количество протонов и электронов. Число протонов определяет атомный номер элемента (Z) и отличает один элемент от другого.Например, атомный номер углерода (Z) равен 6, потому что у него 6 протонов. Количество нейтронов может изменяться для получения изотопов, которые представляют собой атомы одного и того же элемента, имеющие разное количество нейтронов. Число электронов также может быть различным в атомах одного и того же элемента, в результате чего образуются ионы (заряженные атомы). Например, железо Fe может существовать в нейтральном состоянии или в ионных состояниях +2 и +3.
Массовое число
Массовое число элемента (A) — это сумма количества протонов и количества нейтронов.Небольшой вклад массы электронов не учитывается при вычислении массового числа. Это приближение массы можно использовать, чтобы легко вычислить, сколько нейтронов имеет элемент, просто вычтя количество протонов из массового числа. Протоны и нейтроны весят около одной атомной единицы массы или а.е.м. Изотопы одного и того же элемента будут иметь одинаковый атомный номер, но разные массовые числа.
Атомный номер, химический символ и массовое число Углерод имеет атомный номер шесть и два стабильных изотопа с массовыми числами двенадцать и тринадцать соответственно.Его средняя атомная масса 12,11.
Ученые определяют атомную массу, вычисляя среднее значение массовых чисел естественных изотопов. Часто полученное число содержит десятичную дробь. Например, атомная масса хлора (Cl) составляет 35,45 а.е.м., потому что хлор состоит из нескольких изотопов, некоторые (большинство) с атомной массой 35 а.е.м. (17 протонов и 18 нейтронов), а некоторые с атомной массой 37 а.е.м. (17 протонов и 20 нейтронов).
Зная атомный номер (Z) и массовое число (A), вы можете найти количество протонов, нейтронов и электронов в нейтральном атоме.Например, атом лития (Z = 3, A = 7 а.е.м.) содержит три протона (находится из Z), три электрона (поскольку количество протонов равно количеству электронов в атоме) и четыре нейтрона (7 — 3 = 4).
Показать источники
Boundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
атомов и элементов
Атомная структура
Атомы — это основные строительные блоки всего, что нас окружает.Они бывают разных видов, называемых элементами, но каждый атом имеет определенные общие характеристики. Все атомы имеют плотное центральное ядро, называемое атомным ядром. Ядро образуют частицы двух типов: протоны с положительным электрическим зарядом и нейтроны без заряда. У всех атомов есть по крайней мере один протон в их ядре, и количество протонов определяет, какой из элементов типа и является атом. Например, у атома кислорода 8 протонов. Если бы вы каким-то образом смогли изменить протонное число этого атома на 7, , даже если бы все остальное осталось прежним, , это больше не был бы атом кислорода, это был бы азот.По этой причине мы перечисляем различные элементы по их протонным или атомным номерам. Периодическая таблица элементов — это таблица всех элементов, которые были обнаружены до сих пор, в порядке их атомного номера.
Помимо протонов и нейтронов, все атомы имеют электроны, отрицательно заряженные частицы, которые перемещаются в пространстве, окружающем положительно заряженное ядро ядра. Электроны обычно изображаются на рисунках намного меньшими, чем протоны или нейтроны, потому что их масса намного меньше.На самом деле масса электрона настолько мала, что не учитывается в массе атома. Однако сила заряда отдельного электрона равна силе заряда одиночного протона, и, несмотря на свою небольшую массу, электроны важны для уравновешивания заряда атома. Если специально не указано иное, атомы всегда имеют то же количество электронов, что и протоны; следовательно, вы можете узнать номер электрона, посмотрев на атомный номер. Но в отличие от протонов, количество электронов может измениться и действительно изменится на , не влияя на тип элемента, которым является атом!
Теперь мы знаем, как найти число протонов и число электронов для данного атома, но как насчет нейтронов? Сколько нейтронов у атомов данного элемента? Это НЕ всегда то же самое, что количество протонов и электронов.Например, у водорода есть один протон и один электрон, но у него вообще нет нейтронов! Мы определяем это, глядя на атомную массу. Несмотря на то, что атом настолько мал, что вам потребуется почти миллион, чтобы увидеть даже крошечную точку на экране вашего компьютера, каждый крошечный атом определенно имеет массу и занимает пространство. Эта масса исходит от ядра. Каждый протон и нейтрон имеют примерно одинаковую массу, измеряемую в дальтонах или атомных единицах массы (амус). Поскольку единица измерения определяется одним протоном, 1 протон = 1 нейтрон = 1 дальтон = 1 а.е.м.У электронов есть масса, но она почти в 2000 раз меньше массы протона. Ни в одном из известных нам атомов не хватает электронов, чтобы повлиять на общую массу; следовательно, полная масса равна сумме протонов и нейтронов в атоме.
Поскольку мы можем найти количество протонов и атомную массу атома, глядя на информацию о его элементе в периодической таблице, мы можем вычислить количество нейтронов в этом атоме, вычитая количество протонов из атомной массы.
Когда количество нейтронов различно для отдельных атомов одного и того же элемента, каждый атом называется изотопом. Когда вы читаете периодическую таблицу, указанная атомная масса представляет собой среднюю атомную массу для всех изотопов этого элемента, встречающихся в природе. Например, атомная масса углерода в периодической таблице составляет 12,01. Углерод не может содержать 6,01 нейтрона, потому что у вас не может быть части нейтрона. Это значение превышает 6, потому что, хотя большинство атомов углерода имеют 6 нейтронов, некоторые атомы углерода находятся с 7 нейтронами, а другие — с 8 нейтронами.Для наших целей мы округляем атомную массу до ближайшего целого числа, чтобы вычислить количество нейтронов.
Атомная структура
Это видео показывает, как атомы и их компоненты работают вместе.
Валентные электроны
Теперь, когда у вас была возможность поработать с атомами в целом, давайте копнем немного глубже. Электроны остаются в атоме из-за их притяжения к положительному заряду протонов, но они не так тесно связаны с атомом, как протоны или нейтроны.Электроны — сложные частицы, потому что им нужно много места в атоме, и, тем не менее, они также привязаны к определенной области внутри этого атома. Хотя рисунки, с которыми мы работали, показывают ядро как видимый объект среднего размера в центре атома, на самом деле оно очень крошечное, и большая часть атома — это пространство вокруг ядра, в котором движутся электроны.
Из-за общего отрицательного заряда электроны отталкиваются друг от друга, если подходят слишком близко. В то же время электроны притягиваются к положительному заряду ядра.Детали энергии и положения электронов могут быть очень сложными, но мы сосредоточимся только на том, что нам нужно понять для изучения молекул жизни.
Электроны расположены в энергетических оболочках (также известных как электронные оболочки) вокруг ядра атома. Хотя у электронов много места, все они хотят быть как можно ближе к притягивающему их положительному заряду ядра. В то же время электроны отталкиваются друг от друга из-за своего отрицательного заряда, и лишь немногие из них могут приблизиться к ядру в любой момент времени.Фактически, только два электрона могут поместиться в трехмерном пространстве, ближайшем к ядру. Это пространство называется первой энергетической оболочкой. Если в атоме три электрона, первые два будут находиться в первой энергетической оболочке. Третий электрон должен будет обосноваться на второй энергетической оболочке, трехмерном пространстве немного дальше от ядра, где он будет один. В этом примере одинокий электрон называется валентным электроном, а внешняя энергетическая оболочка, содержащая любые электроны, называется валентной оболочкой.
Вторая энергетическая оболочка достаточно велика, чтобы удерживать до восьми электронов, сгруппированных парами внутри четырех электронных орбиталей или пространств, где электроны проводят большую часть своего времени. Это означает, что если во второй энергетической оболочке есть только один электрон, остается много дополнительного места.
Когда энергетическая оболочка заполнена не полностью, электрон (ы) в этой оболочке не так стабилен и с большей вероятностью вступит в реакцию. По этой причине атомы имеют тенденцию реагировать с другими атомами способами, которые заполняют или опустошают их валентную оболочку, чтобы получить стабильность полной внешней энергетической оболочки.Атомы могут делать это, приобретая или теряя электроны, превращаясь в ионы, или разделяя электроны с другими атомами для образования стабильных ассоциаций.
Используя число электронов и энергетические оболочки, мы можем определить количество валентных электронов для любого данного атома и его ожидаемый уровень реактивности. Работая с приведенным ниже примером, вы должны помнить, что, хотя мы рисуем энергетические оболочки в виде кругов вокруг атомного ядра, это не означает, что это реальный путь электрона. Стиль концентрического круга рисования энергетических оболочек предназначен для обозначения среднего расстояния, на котором электроны в этой энергетической оболочке вращаются вокруг ядра.На самом деле электроны не движутся по круговой орбите, как показано на рисунке, а перемещаются по гораздо более сложным путям вокруг атомного ядра.
Постройте атом
Используйте это упражнение, чтобы попрактиковаться в чтении таблицы Менделеева для создания нескольких атомов.
Что такое валентность?
В этом упражнении вы рассчитаете количество валентных электронов в атомах, используя периодическую таблицу элементов.

 В ходе альфа-распада образуется атомное ядро с зарядом на две единицы и массой на четыре единицы меньше, чем у исходного атомного ядра.
В ходе альфа-распада образуется атомное ядро с зарядом на две единицы и массой на четыре единицы меньше, чем у исходного атомного ядра. Ядерная реакция
Ядерная реакция