| 1 | Найти число нейтронов | H | |
| 2 | Найти массу одного моля | H_2O | |
| 3 | Баланс | H_2(SO_4)+K(OH)→K_2(SO_4)+H(OH) | |
| 4 | Найти массу одного моля | H | |
| 5 | Найти число нейтронов | Fe | |
| 6 | Найти число нейтронов | Tc | |
| 7 | Найти конфигурацию электронов | H | |
| 8 | Найти число нейтронов | Ca | |
| 9 | Баланс | CH_4+O_2→H_2O+CO_2 | |
| 10 | Найти число нейтронов | C | |
| 11 | Найти число протонов | H | |
| 12 | Найти число нейтронов | O | |
| 13 | Найти массу одного моля | CO_2 | |
| 14 | Баланс | C_8H_18+O_2→CO_2+H_2O | |
| 15 | Найти атомную массу | H | |
| 16 | Определить, растворима ли смесь в воде | H_2O | |
| 17 | Найти конфигурацию электронов | Na | |
| 18 | Найти массу одного атома | H | |
| 19 | Найти число нейтронов | Nb | |
| 20 | Найти число нейтронов | Au | |
| 21 | Найти число нейтронов | Mn | |
| 22 | Найти число нейтронов | Ru | |
| 23 | Найти конфигурацию электронов | O | |
| 24 | Найти массовую долю | H_2O | |
| 25 | Определить, растворима ли смесь в воде | NaCl | |
| 26 | Найти эмпирическую/простейшую формулу | H_2O | |
| 27 | Найти степень окисления | H_2O | |
| 28 | Найти конфигурацию электронов | K | |
| 29 | Найти конфигурацию электронов | Mg | |
| 30 | Найти конфигурацию электронов | Ca | |
| 31 | Найти число нейтронов | Rh | |
| 32 | Найти число нейтронов | Na | |
| 33 | Найти число нейтронов | Pt | |
| 34 | Найти число нейтронов | Be | Be |
| 35 | Найти число нейтронов | Cr | |
| 36 | Найти массу одного моля | H_2SO_4 | |
| 37 | Найти массу одного моля | HCl | |
| 38 | Найти массу одного моля | Fe | |
| 39 | Найти массу одного моля | C | |
| 40 | Найти число нейтронов | Cu | |
| 41 | Найти число нейтронов | S | |
| 42 | Найти степень окисления | H | |
| 43 | Баланс | CH_4+O_2→CO_2+H_2O | |
| 44 | Найти атомную массу | O | |
| 45 | Найти атомное число | H | |
| 46 | Найти число нейтронов | Mo | |
| 47 | Найти число нейтронов | Os | |
| 48 | Найти массу одного моля | NaOH | |
| 49 | Найти массу одного моля | O | |
| 50 | Найти конфигурацию электронов | Fe | |
| 51 | Найти конфигурацию электронов | C | |
| 52 | Найти массовую долю | NaCl | |
| 53 | Найти массу одного моля | K | |
| 54 | Найти массу одного атома | Na | |
| 55 | Найти число нейтронов | N | |
| 56 | Найти число нейтронов | Li | |
| 57 | Найти число нейтронов | V | |
| 58 | Найти число протонов | N | |
| 59 | Упростить | H^2O | |
| 60 | Упростить | h*2o | |
| 61 | Определить, растворима ли смесь в воде | H | |
| 62 | Найти плотность при стандартной температуре и давлении | H_2O | |
| 63 | Найти степень окисления | NaCl | |
| 64 | Найти атомную массу | He | He |
| 65 | Найти атомную массу | Mg | |
| 66 | Найти число электронов | H | |
| 67 | Найти число электронов | O | |
| 68 | Найти число электронов | S | |
| 69 | Найти число нейтронов | Pd | |
| 70 | Найти число нейтронов | Hg | |
| 71 | Найти число нейтронов | B | |
| 72 | Найти массу одного атома | Li | |
| 73 | Найти эмпирическую формулу | H=12% , C=54% , N=20 | , , |
| 74 | Найти число протонов | Be | Be |
| 75 | Найти массу одного моля | Na | |
| 76 | Найти конфигурацию электронов | Co | |
| 77 | Найти конфигурацию электронов | S | |
| 78 | Баланс | C_2H_6+O_2→CO_2+H_2O | |
| 79 | Баланс | H_2+O_2→H_2O | |
| 80 | Найти конфигурацию электронов | P | |
| 81 | Найти конфигурацию электронов | Pb | |
| 82 | Найти конфигурацию электронов | Al | |
| 83 | Найти конфигурацию электронов | Ar | |
| 84 | Найти массу одного моля | O_2 | |
| 85 | Найти массу одного моля | H_2 | |
| 86 | Найти число нейтронов | K | |
| 87 | Найти число нейтронов | P | |
| 88 | Найти число нейтронов | Mg | |
| 89 | Найти число нейтронов | W | |
| 90 | Найти массу одного атома | C | |
| 91 | Упростить | na+cl | |
| 92 | Определить, растворима ли смесь в воде | H_2SO_4 | |
| 93 | Найти плотность при стандартной температуре и давлении | NaCl | |
| 94 | Найти степень окисления | C_6H_12O_6 | |
| 95 | Найти степень окисления | Na | |
| 96 | Определить, растворима ли смесь в воде | C_6H_12O_6 | |
| 97 | Найти атомную массу | Cl | |
| 98 | Найти атомную массу | Fe | |
| 99 | Найти эмпирическую/простейшую формулу | CO_2 | |
| 100 | Найти число нейтронов | Mt |
НАЧАЛА ФИЗИКИ
Таким образом для превращения ядра в ядро должны произойти 8 α и 6 β-распадов.
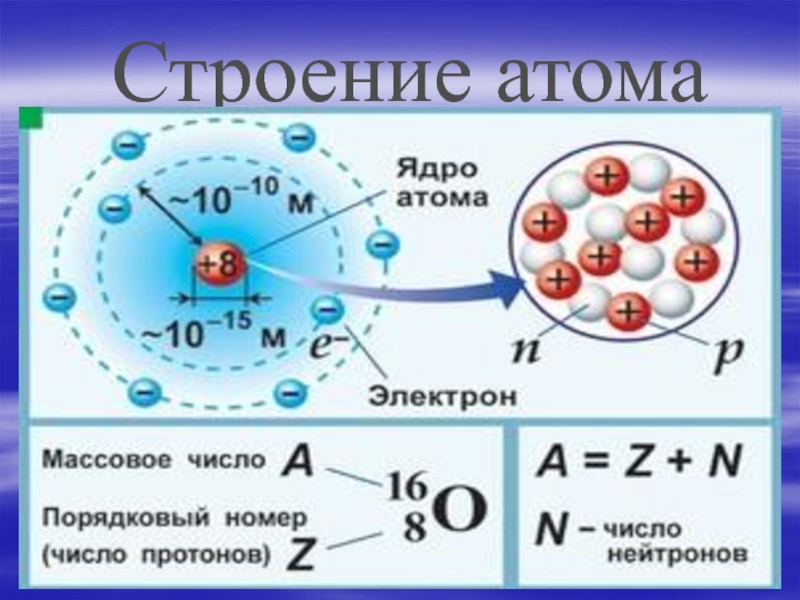
Пример 36.6. Сколько нейтронов и протонов содержится в ядре атома золота ?
Решение. Нижний индекс у символа ядра определяет число протонов, верхний – суммарное число протонов и нейтронов. Отсюда заключаем, что в ядре атома золота содержится 79 протонов и 118 нейтронов. При этом все ядра, содержащие 79 протонов и разное количество нейтронов, будут ядрами атомов золота (различными изотопами золота). Ядра же, содержащие 118 нейтронов и разное количество протонов, будут ядрами разных химических элементов.
Пример 36.7. Ядро свинца поглотило один нейтрон. Какое ядро образовалось в результате этого процесса?
Решение. При поглощении нейтрона ядром число нейтронов в ядре увеличивается на единицу, число протонов не изменяется. Поэтому в результате этого процесса образуется ядро свинца .
Как указывалось выше, некоторые атомы могут самопроизвольно испускать определенные частицы – электроны, α-частицы, γ-кванты. Поскольку энергии радиоактивных частиц на несколько порядков превосходят характерные энергии электронов в атомах, то, очевидно, источником радиоактивных излучений являются атомные ядра. Обсудим, какие процессы приводят к радиоактивным распадам.
Поскольку энергии радиоактивных частиц на несколько порядков превосходят характерные энергии электронов в атомах, то, очевидно, источником радиоактивных излучений являются атомные ядра. Обсудим, какие процессы приводят к радиоактивным распадам.
α-Излучение представляет собой поток ядер атомов гелия , состоящих их двух протонов и двух нейтронов. Благодаря большой энергии связи α-частицы формируются внутри распадающегося ядра из его «собственных» протонов и нейтронов, а затем вылетают из ядра. После этого атом теряет два внешних электрона и становится электрически нейтральным атомом элемента, ядро которого содержит на два нейтрона и два протона меньше, чем распавшееся ядро. Этот процесс можно схематически записать в виде уравнения, которое называется уравнением ядерной реакции:
36.14
565/597
Как найти количество нейтронов в атоме — Наука и Техника — Каталог статей
Каждое атомное ядро, кроме водорода, содержит как протоны, так и нейтроны. Ядра слишком малы, чтобы их можно было увидеть даже под микроскопом, а нуклоны (это общий термин для протонов и нейтронов) еще меньше. Это позволяет подсчитать количество нейтронов, но ученые все еще знают, сколько в ядрах каждого изотопа каждого элемента. Откуда они знают? Они используют такие методы, как масс-спектрометрия, для измерения общей массы атомов конкретного элемента. Как только они узнают общую массу, остальное легко.
Ядра слишком малы, чтобы их можно было увидеть даже под микроскопом, а нуклоны (это общий термин для протонов и нейтронов) еще меньше. Это позволяет подсчитать количество нейтронов, но ученые все еще знают, сколько в ядрах каждого изотопа каждого элемента. Откуда они знают? Они используют такие методы, как масс-спектрометрия, для измерения общей массы атомов конкретного элемента. Как только они узнают общую массу, остальное легко.
Общая масса атома — это сумма всех его протонов, нейтронов и электронов, но электроны настолько легки, что для всех практических целей они не имеют значения. Это означает, что масса элемента является суммой масс его нуклонов. Число протонов одинаково для каждого атома определенного элемента, а протоны и нейтроны имеют одинаковую массу, поэтому все, что вам нужно сделать, это вычесть количество протонов из атомной массы, измеренное в единицах атомной массы (amu), и вы остались с количеством нейтронов.
Используйте периодическую таблицу
Периодическая таблица перечисляет все элементы, увеличивая число протонов, поэтому место, которое элемент занимает в таблице, автоматически сообщает вам, сколько протонов находится в его ядре. Это атомный номер элемента, и он отображается прямо под символом для элемента. Рядом с ним другое число, которое является атомной массой. Это число всегда больше атомного номера и часто содержит дробь, потому что это среднее от атомных масс всех естественных изотопов этого элемента. Вы можете использовать его для определения среднего количества протонов в ядре этого элемента.
Это атомный номер элемента, и он отображается прямо под символом для элемента. Рядом с ним другое число, которое является атомной массой. Это число всегда больше атомного номера и часто содержит дробь, потому что это среднее от атомных масс всех естественных изотопов этого элемента. Вы можете использовать его для определения среднего количества протонов в ядре этого элемента.
Процедура не может быть проще. Округлите атомную массу до ближайшего целого числа, затем вычтите из нее атомный номер элемента. Разница равна количеству нейтронов.
пример
1. Сколько в среднем нейтронов в ядре урана?
Уран является 92-м элементом в периодической таблице, поэтому его атомный номер 92, и в его ядре 92 протона. Периодическая таблица перечисляет атомную массу как 238.039 amu. Округлите атомную массу до 238, вычтите атомный номер, и у вас останется 146 нейтронов. Уран имеет большое количество нейтронов по отношению к числу протонов, поэтому все его изотопы радиоактивны.
Количество нейтронов в изотопе
Количество нейтронов в ядре конкретного элемента может варьироваться, и каждый вариант элемента с его характерным числом нейтронов известен как изотоп. Все элементы, кроме 20, имеют более одного изотопа, а некоторые имеют много. Олово (Sn) возглавляет список с десятью изотопами, сопровождаемыми ксеноном (Xe) с девятью.
Каждый изотоп элемента состоит из целого числа протонов и нейтронов, поэтому его атомная масса представляет собой простую сумму этих нуклонов. Атомная масса для изотопа никогда не бывает дробной. У ученых есть два способа обозначить изотоп. Взяв в качестве примера изотоп углерода, вы можете записать его как C-14 или 14C. Число — это атомная масса. Вычтите атомный номер элемента из атомной массы изотопа, и в результате получите число нейтронов в ядре этого изотопа.
В случае С-14 атомное число углерода равно 6, поэтому в ядре должно быть 8 нейтронов. Это на два больше, чем у более распространенного сбалансированного изотопа С-12.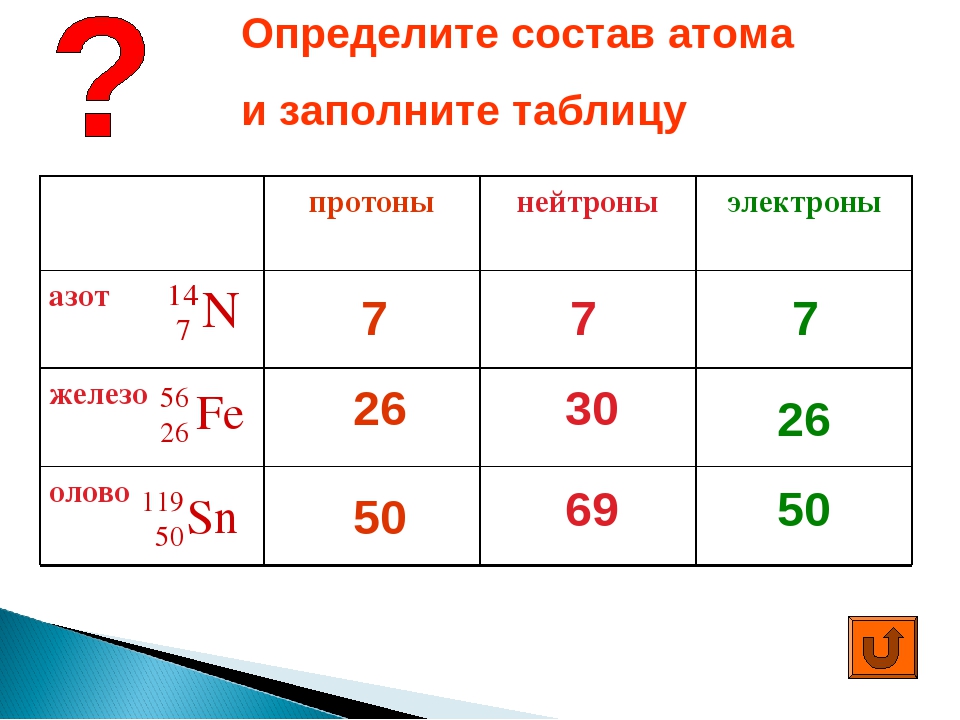 Дополнительная масса делает С-14 радиоактивным.
Дополнительная масса делает С-14 радиоактивным.
Оказывается, многие умные люди совершенно не представляют, как…: akuklev — LiveJournal
Оказывается, многие умные люди совершенно не представляют, как работают атомные реакторы! А ведь чтобы разобраться, нужно немножко школьной физики и буквально пять минут времени. В книге А. С. Дятлова «Чернобыль. Как это было» приводится описание реактора РБМК-1000, оно занимает всего 4 страницы текста, и в то же время содержит достаточно технических деталей, чтобы понимать принципы работы всех других реакторов. Не поленитесь потратить пару минут времени, всё-таки в наше время это должен знать каждый.
Напомню, что атомы состоят из тяжёлого ядра и облачка очень лёгких электронов. Ядро состоит из положительно заряженных протонов и электронейтральных нейтронов. Заряд ядра (то есть количество протонов) определяет, сколько электронов оно может притянуть и насколько сильно — а соответственно, в какие химические связи атом может вступать. Поэтому все химические свойства атома зависят только от количества протонов.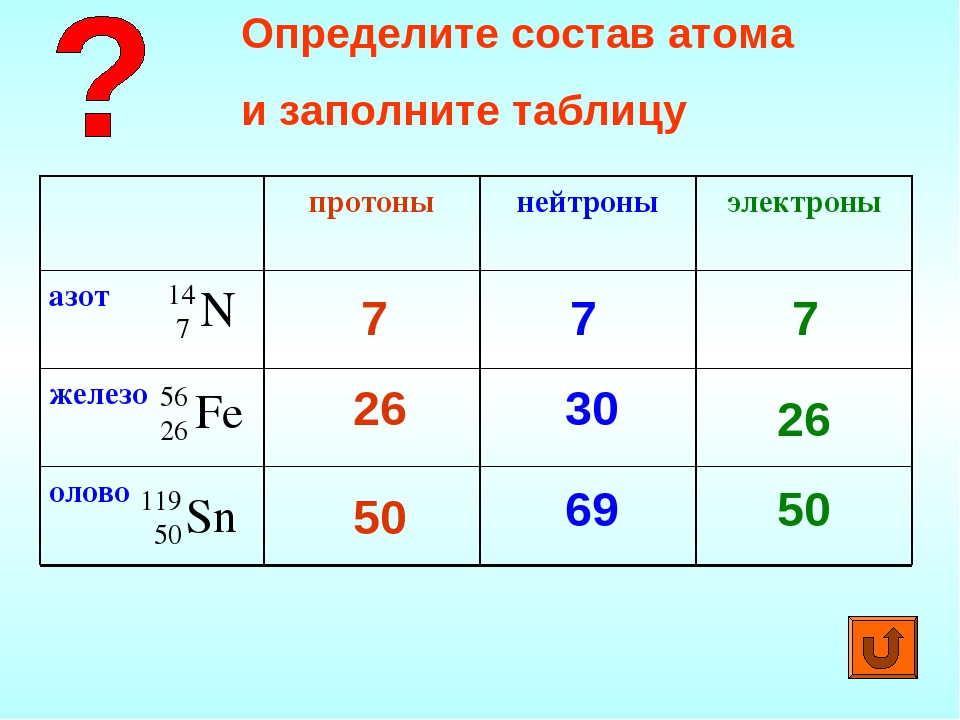 Водород — один протон в ядре, гелий два (изображение справа) и так далее.
Водород — один протон в ядре, гелий два (изображение справа) и так далее.
Итак, количество протонов обнаруживается по химическим свойствам, а чтобы узнать количество нейтронов нужно просто взвесить атом: электроны практически ничего не весят, а протоны и нейтроны весят примерно одинаково — по одной этомой единице веса u. В виду сказанного, атомы маркируют так: название химического элемента и масса. Например, водород-1 (1H) имеет ядро из одного протона, водород-2 (2H) ядро из одного протона и одного нейтрона. А уран-235 (235U) имеет ядро с 92 протонами и общим весом 235 u, стало быть там (235 − 92 =) 143 нейтрона.
Атомы, у которых число протонов одинаково, а число нейтронов разное, называют изотопами. В природе часто встречаются разные изотопы каждого их элементов. В частности водород-1 и водород-2 (дейтерий) оба встречаются в природе, оба абсолютно стабильные.
Ядра крепкие и надёжные только если соотношение протонов и нейтронов в них правильное. Если оно неправильное, ядро получается кривое-косое и со временем разваливается:
Если оно неправильное, ядро получается кривое-косое и со временем разваливается:
– Ядра урана-235, например, разваливаются на два куска солидных размеров, это называется спонтанное деление.
– От менее «кривых» ядер, например, от урана-238 откалываются маленькие стабильные осколки по два нейтрона и два протона (то есть, ядра гелия-4) — это называется альфа-распадом.
– Ещё может случиться превращение нейтрона в протон или наоборот. Естественно при таком превращении нужно куда-то деть разницу зарядов:
– При превращении нейтрона (заряд = 0) в протон (заряд = 1) выделяется электрон (заряд = -1). Это называется β—-распад.
– При превращении протона в нейтрон соответственно выделяется позитрон (β+-распад) либо поглощается один из электронов из электронного облачка вокруг ядра (e-захват).
Всё это добро в придачу сопровождается выделением γ-излучения, то очень-очень крепкого рентгена. Им конечно можно в некоторых случаях лечить раковых больных, но в общем случае попадение излучения в человека здоровью мягко говоря не способствует. Сами же распады представляют опасность только если происходят внутри человеческого тела или совсем близко (в пределах 20–30 сантиметров) от тела. Из сказанного следует, что кушать и дышать склонными к распадам атомами – последнее дело, но с другой стороны, при соблюдении должных мер предосторожности с ними вполне можно безопасно работать. Бывают вещи и поопаснее.
Сами же распады представляют опасность только если происходят внутри человеческого тела или совсем близко (в пределах 20–30 сантиметров) от тела. Из сказанного следует, что кушать и дышать склонными к распадам атомами – последнее дело, но с другой стороны, при соблюдении должных мер предосторожности с ними вполне можно безопасно работать. Бывают вещи и поопаснее.
Так вот. При всех этих распадах выделяется офигительная энергия. Выражается это в основном в том, что образовавшиеся куски разлетаются друг от друга с адской скоростью. А скорость движения молекул имеет, как известно, самое прямое отношение к температуре. Иначе говоря, в результате распадов, материал греется. Очень заманчиво использовать это дармовое тепло с целью обогрева и выработки электричества. Однако встречающиеся в природе ядра распадаются очень редко, потому что те которые распадаются быстро уже давно на земле распались. Поэтому тепла с них никакого почти и не получишь, если только не подстегнуть распад. А это как раз можно, если по ядру хорошенько стукнуть чем-нибудь сравнимого размера, например пролетающим нейтроном. Именно этот механизм используется в ядерных реакторах.
Именно этот механизм используется в ядерных реакторах.
“Атомный реактор электростанций — это аппарат для преобразования ядерной энергии в тепловую. Топливом в подавляющем большинстве реакторов служит слабообогащенный уран. В природе химический элемент уран состоит из двух его изотопов: 0,7% изотоп с атомным весом 235, остальное — изотоп с атомным весом 238. Топливом является только изотоп урана-235. При захвате (поглощении) нейтрона ядром урана-235 оно становится неустойчивым и по житейским меркам мгновенно распадается на две, в основном неравные, части с выделением большого количества энергии. В каждом акте деления ядра энергии выделяется в миллионы раз больше, чем при сгорании молекулы нефти или газа. В таком большом реакторе, как Чернобыльский, при работе на полной мощности «сгорает» около четырех килограммов урана за сутки.
Устройство твэла реактора РБМК: 1 — заглушка; 2 — таблетки диоксида урана;
3 — оболочка из циркония; 4 — пружина; 5 — втулка; 6 — наконечник.
Выделяемая при каждом делении ядра урана энергия реализуется следующим образом: основная часть — в виде кинетической энергии «осколков» деления, которые в процессе торможения передают ее практически всю в ТВЭЛе (тепловыделяющем элементе) реактора и в его конструктивной оболочке. Выход за оболочку сколько-нибудь заметной части осколков недопустим. Если посмотрим на таблицу Менделеева, то увидим, что ядра осколков деления имеют явный избыток нейтронов для того, чтобы быть стабильными. Поэтому в результате цепочки β-распадов, претерпевая радиационные превращения, они по таблице химических элементов сдвигаются вправо до стабильного состояния. Этот процесс, сопровождающийся испусканием β-частиц и γ-излучением, для каждого вида осколков имеет свою биографию и свои периоды полураспада. Именно осколки деления и составляют большую часть радиационного загрязнения территории при аварии после разрушения и выброса при взрыве ТВЭЛов.
Выход за оболочку сколько-нибудь заметной части осколков недопустим. Если посмотрим на таблицу Менделеева, то увидим, что ядра осколков деления имеют явный избыток нейтронов для того, чтобы быть стабильными. Поэтому в результате цепочки β-распадов, претерпевая радиационные превращения, они по таблице химических элементов сдвигаются вправо до стабильного состояния. Этот процесс, сопровождающийся испусканием β-частиц и γ-излучением, для каждого вида осколков имеет свою биографию и свои периоды полураспада. Именно осколки деления и составляют большую часть радиационного загрязнения территории при аварии после разрушения и выброса при взрыве ТВЭЛов.
При нормальной работе реактора β-частицы также не выходят за пределы ТВЭЛов и там теряют свою энергию; γ-излучения большей частью поглощаются также внутри реактора. После прекращения цепной реакции, при остановке реактора, остаточные тепловыделения от распада продуктов деления еще длительное время вынуждают охлаждать ТВЭЛы.
При каждом делении ядра урана испускается два-три, в среднем около двух с половиной, нейтрона. Их кинетическая энергия поглощается замедлителем, топливом и конструктивными элементами реактора, затем передается теплоносителю.
Их кинетическая энергия поглощается замедлителем, топливом и конструктивными элементами реактора, затем передается теплоносителю.
Как раз нейтроны-то и делают возможным осуществлять цепную реакцию деления ядер урана-235. Если один нейтрон от каждого деления вызовет новое деление, то интенсивность реакции сохранится на одном уровне.
Большая часть нейтронов испускается немедленно при делении ядра. Это мгновенные нейтроны. Малая часть, около 0,7%, через небольшой промежуток времени, через секунды и десятки секунд, — запаздывающие нейтроны. Они позволяют управлять интенсивностью реакции деления урана и регулировать мощность реактора. В противном случае существование энергетических реакторов становилось бы проблематичным — только атомная бомба. Остальная часть энергии деления — мгновенное γ-излучение, выделяемое непосредственно при делении, и энергия нейтрино, которую мы никак не улавливаем и не видим.
Обычно в энергетических реакторах используют не природный, а несколько обогащенный изотопом-235 уран. Но все-таки большая часть — это уран-238 и потому значительное количество нейтронов поглощается им. Ядро урана-238, после поглощения нейтрона, неустойчиво и через двойной β-распад превращается в химический элемент плутоний-239, также способный делиться при поглощении тепловых нейтронов, как и уран-235. Свойства плутония как топлива отличаются от урана и при достаточном его накоплении после длительной работы реактора несколько изменяют физику реактора. Выброшенный при аварии плутоний также вносит свою лепту в загрязнение территории. Причем надежды на его распад нет никакой (период полураспада плутония-239 более 24 тыс. лет), только миграция вглубь земли. Присутствуют и другие изотопы плутония.
Но все-таки большая часть — это уран-238 и потому значительное количество нейтронов поглощается им. Ядро урана-238, после поглощения нейтрона, неустойчиво и через двойной β-распад превращается в химический элемент плутоний-239, также способный делиться при поглощении тепловых нейтронов, как и уран-235. Свойства плутония как топлива отличаются от урана и при достаточном его накоплении после длительной работы реактора несколько изменяют физику реактора. Выброшенный при аварии плутоний также вносит свою лепту в загрязнение территории. Причем надежды на его распад нет никакой (период полураспада плутония-239 более 24 тыс. лет), только миграция вглубь земли. Присутствуют и другие изотопы плутония.
Свойства урана-235:
• делиться при поглощении его ядром теплового (с малой энергией) нейтрона;
• выделять при этом большое количество энергии;
• испускать при делении нейтроны, необходимые для самоподдерживающейся реакции.
Уран-235 является основой создания атомных энергетических реакторов. Почти все реакторы АЭС работают на тепловых нейтронах, т.е. нейтронах с малой кинетической энергией. Нейтроны после деления урана или плутония претерпевают стадии замедления, диффузии и захвата ядрами топлива и конструктивных материалов. Часть нейтронов вылетает за пределы активной зоны — утечка. Одновременно происходит большое количество делений, и, следовательно, в работающем реакторе всегда в наличии большое количество нейтронов, составляющих нейтронный поток, нейтронное поле. Выгорание ядер топлива происходит медленно, и поэтому в достаточно длительный промежуток времени количество топлива в реакторе можно считать неизменным. Тогда число поглощенных топливом нейтронов, а при этом и число разделившихся ядер и количество получаемой энергии, будет прямо пропорционально нейтронному потоку в активной зоне. Фактически задача операторов сводится к измерению и поддержанию нейтронного потока согласно требованиям по поддержанию мощности.
Почти все реакторы АЭС работают на тепловых нейтронах, т.е. нейтронах с малой кинетической энергией. Нейтроны после деления урана или плутония претерпевают стадии замедления, диффузии и захвата ядрами топлива и конструктивных материалов. Часть нейтронов вылетает за пределы активной зоны — утечка. Одновременно происходит большое количество делений, и, следовательно, в работающем реакторе всегда в наличии большое количество нейтронов, составляющих нейтронный поток, нейтронное поле. Выгорание ядер топлива происходит медленно, и поэтому в достаточно длительный промежуток времени количество топлива в реакторе можно считать неизменным. Тогда число поглощенных топливом нейтронов, а при этом и число разделившихся ядер и количество получаемой энергии, будет прямо пропорционально нейтронному потоку в активной зоне. Фактически задача операторов сводится к измерению и поддержанию нейтронного потока согласно требованиям по поддержанию мощности.
Если условно разбить нейтроны деления на последовательные поколения (условность в следующем — поскольку деление происходит несогласованно, то это аналогично движению неорганизованной толпы, а не шагам армейской колонны) с количеством нейтронов № 1, № 2 и так далее, то при равенстве числа нейтронов каждого поколения мощность реактора будет постоянной, такой реактор будет называться критичным и коэффициент размножения нейтронов, равный отношению числа нейтронов последующего поколения к предыдущему, равен единице. При коэффициенте размножения больше единицы число нейтронов и мощность непрерывно возрастают — реактор надкритичный. Чем больше коэффициент размножения, тем больше скорость нарастания мощности, причем мощность нарастает со временем не линейно, а по экспоненте.
При коэффициенте размножения больше единицы число нейтронов и мощность непрерывно возрастают — реактор надкритичный. Чем больше коэффициент размножения, тем больше скорость нарастания мощности, причем мощность нарастает со временем не линейно, а по экспоненте.
В оперативной работе пользуются, как правило, не величиной коэффициента размножения К, а величиной так называемой реактивности ρ, которая при К, незначительно отличающихся от единицы, с достаточной точностью представляется равной (К − 1). В обычной практике оператор имеет дело с реактором, надкритичность или положительная реактивность которого составляет не более одной десятой процента. При большей реактивности скорость нарастания мощности становится слишком большой, опасной для целостности реактора и обслуживающих систем. Все энергетические реакторы имеют автоматическую A3 (аварийную защиту), глушащую реактор при большой скорости увеличения мощности. На использовавшемся на Чернобыльской АС реакторе РБМК АЗ срабатывала при скорости возрастания мощности в два раза за время 20 с.
Важнейший момент. При делении ядра урана примерно 0,7% нейтронов рождаются не при делении, а с некоторым запаздыванием. Они входят в общее число нейтронов данного поколения и тем самым увеличивают время жизни поколения нейтронов. Доля запаздывающих нейтронов обычно обозначается β. Если избыточная (положительная) реактивность достигает (и больше) величины β, то реактор становится критичным только на мгновенных нейтронах, скорость сменяемости поколений которых велика — определяется временем замедления и диффузии нейтронов, и поэтому скорость увеличения мощности очень большая. Защиты в этом случае нет — только разрушение реактора может прервать цепную реакцию. Так было 26 апреля 1986 г. на четвертом блоке Чернобыльской АЭС. Фактически из-за наработки в активной зоне плутония и различия в свойствах мгновенных и запаздывающих нейтронов в реакторе РБМК величина β-эффективная равнялась не 0,7, а 0,5%.
Топливная кассета
Реактор РБМК-1000 — это реактор канального типа, замедлитель нейтронов — графит, теплоноситель — обычная вода. Топливная кассета набирается из 36 ТВЭЛов по три с половиной метра длиной. ТВЭЛы с помощью дистанционирующих решеток, закрепленных на центральном несущем стержне, размещаются на двух окружностях: на внутренней 6 штук и на внешней 12 штук. Каждая кассета состоит из двух ярусов по высоте. Таким образом, активная зона имеет высоту семь метров. Каждый ТВЭЛ набирается из таблеток диоксида урана UO2, размещенных в герметичной трубе из сплава циркония с ниобием. В отличие от корпусных реакторов, где все топливные кассеты располагаются в общем корпусе, рассчитанном на полное рабочее давление, в реакторе РБМК каждая кассета размещена в отдельном технологическом канале, представляющем собой трубу диаметром 80 мм.
Топливная кассета набирается из 36 ТВЭЛов по три с половиной метра длиной. ТВЭЛы с помощью дистанционирующих решеток, закрепленных на центральном несущем стержне, размещаются на двух окружностях: на внутренней 6 штук и на внешней 12 штук. Каждая кассета состоит из двух ярусов по высоте. Таким образом, активная зона имеет высоту семь метров. Каждый ТВЭЛ набирается из таблеток диоксида урана UO2, размещенных в герметичной трубе из сплава циркония с ниобием. В отличие от корпусных реакторов, где все топливные кассеты располагаются в общем корпусе, рассчитанном на полное рабочее давление, в реакторе РБМК каждая кассета размещена в отдельном технологическом канале, представляющем собой трубу диаметром 80 мм.
Активная зона реактора РБМК высотой 7 и диаметром 11,8 м набрана из 1888 графитовых колонн с центральными отверстиями каждая, куда установлены каналы. Из этого числа 1661 — технологические каналы с топливными кассетами, остальные — каналы СУЗ (системы управления и защиты), где размещены 211 поглощающих нейтроны стержней и 16 датчиков контроля. Каналы СУЗ равномерно распределены по активной зоне в радиальном и азимутальном направлениях. Снизу к технологическим каналам подводится теплоноситель — обычная вода под высоким давлением, охлаждающая ТВЭЛы. Вода частично испаряется и в виде пароводяной смеси сверху отводится в барабан-сепараторы, где пар отделяется и поступает на турбины. Вода из барабан-сепараторов при помощи ГЦН (главных циркуляционных насосов) вновь подается на вход в технологические каналы. Пар после отработки в турбинах конденсируется и возвращается в контур теплоносителя. Таким образом, замыкается контур циркуляции воды.
Каналы СУЗ равномерно распределены по активной зоне в радиальном и азимутальном направлениях. Снизу к технологическим каналам подводится теплоноситель — обычная вода под высоким давлением, охлаждающая ТВЭЛы. Вода частично испаряется и в виде пароводяной смеси сверху отводится в барабан-сепараторы, где пар отделяется и поступает на турбины. Вода из барабан-сепараторов при помощи ГЦН (главных циркуляционных насосов) вновь подается на вход в технологические каналы. Пар после отработки в турбинах конденсируется и возвращается в контур теплоносителя. Таким образом, замыкается контур циркуляции воды.
Если принять конструкцию активной зоны заданной, посмотрим куда деваются нейтроны деления. Часть нейтронов уходит за пределы активной зоны и теряется безвозвратно. Часть нейтронов поглощается замедлителем, теплоносителем, конструкционными материалами и продуктами деления топливных ядер. Это бесполезная утрата нейтронов. Остальные поглощаются топливом. Для поддержания постоянной мощности количество поглощаемых топливом нейтронов также должно быть неизменным.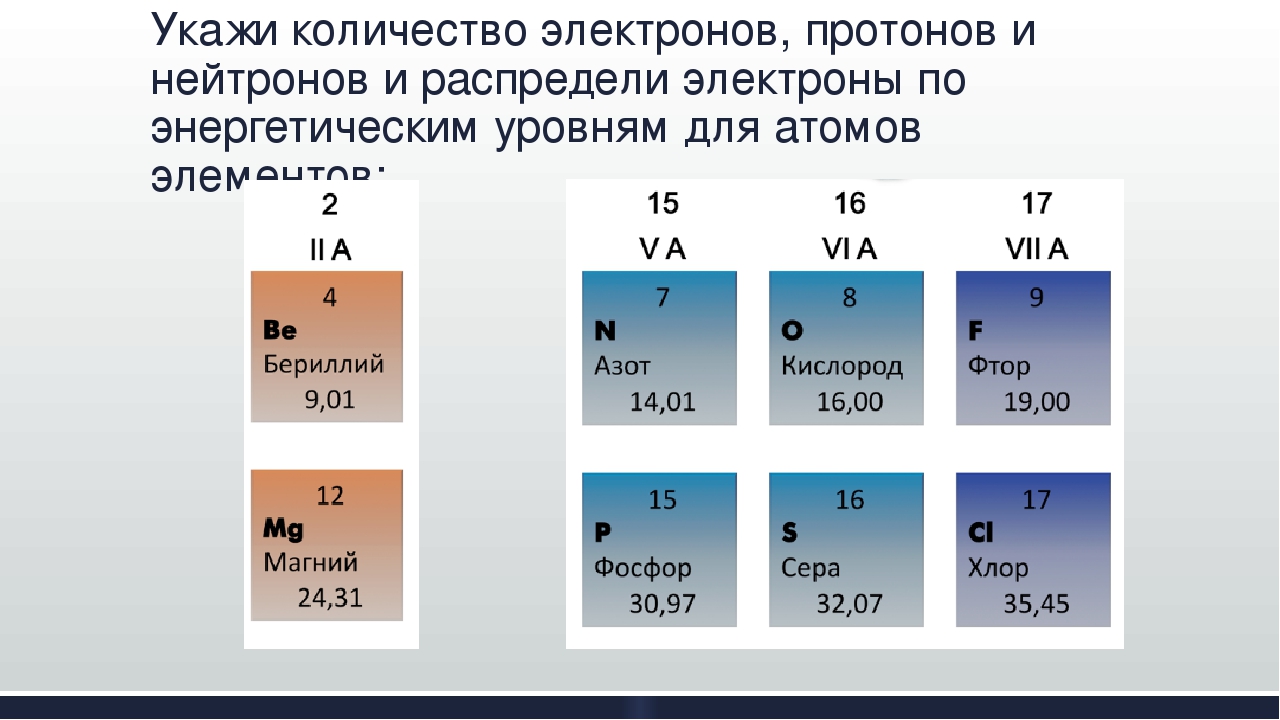 Следовательно, из испускаемых при каждом делении топливного ядра двух с половиной (в среднем) нейтронов на утечку и захват неделящимися материалами мы можем терять полтора нейтрона.
Следовательно, из испускаемых при каждом делении топливного ядра двух с половиной (в среднем) нейтронов на утечку и захват неделящимися материалами мы можем терять полтора нейтрона.
Это будет критичный реактор. Такой реактор работать не может, хотя бы по следующей причине: при делении урана образуются ядра различных химических элементов и среди них в значительном количестве ксенон с атомным весом 135, обладающий очень большим сечением поглощения нейтронов. При подъеме мощности начинает образовываться ксенон, и реактор заглохнет. Так и было с первым американским реактором. Э. Ферми посчитал сечение захвата нейтронов ядром ксенона и в шутку сказал, что ядро получается величиной с апельсин.
Для компенсации этого и других эффектов топливо в реактор загружают с избытком, что при постоянной утечке нейтронов и поглощении их неделящимися материалами увеличивает долю поглощения топливом. Чтобы не происходило постоянного наращивания мощности такого реактора, в активную зону вводят так называемые органы воздействия на реактивность, содержащие материалы, интенсивно поглощающие нейтроны. Методы компенсации могут быть различные, мы рассмотрим их только на примере РБМК.
Методы компенсации могут быть различные, мы рассмотрим их только на примере РБМК.
В каналах СУЗ размещаются стержни, содержащие сильный поглотитель нейтронов — бор, с помощью которого и поддерживается нужный баланс нейтронов и, следовательно, мощность реактора. При необходимости увеличения мощности часть стержней выводится полностью или частично из активной зоны, в результате чего увеличивается доля нейтронов, поглощаемых топливом, мощность возрастает и стержни по достижении нужного уровня мощности вновь вводятся в активную зону. Как правило, новое положение стержней управления не идентично исходному — это зависит от изменения реактивности активной зоны при изменении мощности — от мощностного коэффициента реактивности.
При необходимости уменьшения мощности в активную зону вводят стержни, т.е. вводят отрицательную реактивность, реактор становится подкритичным и мощность начинает уменьшаться. На новом уровне мощность стабилизируется изменением положения стержней. Все это осуществляется автоматическим регулятором. Оператор нажатием кнопки изменяет уровень заданной мощности, а остальное — дело регулятора. Правда, в случае с реактором РБМК это не совсем так, а иногда и совсем не так, — оператор вынужден своим вмешательством корректировать работу регулятора в основном по установлению энерговыделения в той или иной части зоны.
Оператор нажатием кнопки изменяет уровень заданной мощности, а остальное — дело регулятора. Правда, в случае с реактором РБМК это не совсем так, а иногда и совсем не так, — оператор вынужден своим вмешательством корректировать работу регулятора в основном по установлению энерговыделения в той или иной части зоны.
Во вновь построенном реакторе технологические каналы загружаются свежими невыгоревшими топливными кассетами. Если все 1661 канал загрузить кассетами, то коэффициент размножения будет столь велик, что погасить его имеющимися стержнями управления будет невозможно. Поэтому около 240 технологических каналов вместо топливных кассет загружаются специальными стержнями-поглотителями нейтронов. И еще несколько сотен поглотителей размещаются в отверстиях центральных несущих стержней топливных кассет. По мере выгорания топлива эти поглотители постепенно извлекаются и заменяются топливными кассетами. При извлечении всех поглотителей поддержание нужной реактивности активной зоны осуществляется заменой наиболее выгоревших кассет свежими. Наступает режим стационарных перегрузок.
Наступает режим стационарных перегрузок.
В реакторе РБМК топливные кассеты заменяются при работе реактора на мощности специальной разгрузочно-загрузочной машиной. В это время активная зона содержит полностью выгоревшие кассеты, свежие и с промежуточным выгоранием. Вот на этот режим и рассчитано количество стержней управления и защиты.
Каждый стержень СУЗ вносит какую-то реактивность, что зависит от его местоположения в зоне и формы нейтронного поля. В реакторе РБМК реактивность принято измерять в стержнях, эффективность одного стержня условно принята 0,05%. Как уже пояснялось, скорость увеличения мощности реактора тем больше, чем больше его положительная реактивность. Скорость уменьшения мощности также больше при большей внесенной отрицательной реактивности.
В результате нарушений режима и неисправностей в системах возникает необходимость во избежание повреждений быстро заглушить реактор. Поэтому количество стержней СУЗ всегда должно быть с избытком для приведения реактора в состояние с нужной подкритичностью. Когда реактор находится в критическом состоянии (критическое значит не катастрофическое, а что его коэффициент размножения равен единице и, соответственно, реактивность равна нулю), обязательно должно быть не менее какого-то количества стержней выведено из активной зоны и готово к немедленному вводу в зону для прекращения цепной реакции деления. И чем больше стержней выведено из активной зоны, тем
Когда реактор находится в критическом состоянии (критическое значит не катастрофическое, а что его коэффициент размножения равен единице и, соответственно, реактивность равна нулю), обязательно должно быть не менее какого-то количества стержней выведено из активной зоны и готово к немедленному вводу в зону для прекращения цепной реакции деления. И чем больше стержней выведено из активной зоны, тем
больше уверенности, что реактор при необходимости будет заглушен быстро, с большой подкритичностью. Это верно для всех реакторов, спроектированных согласно требованиям норм и правил безопасности.
Во всех реакторах тем или иным путем часть органов воздействия на реактивность введена в реактор — это необходимо для маневрирования мощностью. К примеру, при вынужденном частичном снижении мощности временно увеличивается количество ксенона (говорят, что реактор отравлен ксеноном), увеличение количества поглотителя нейтронов нужно скомпенсировать выводом из зоны части оперативно извлекаемого поглотителя. Иначе реактор придется заглушить и ждать распада ксенона.
Иначе реактор придется заглушить и ждать распада ксенона.
В реакторе РБМК при работе часть стержней СУЗ находится частично или полностью в активной зоне и подавляет (компенсирует) какую-то избыточную реактивность. Теперь определимся с понятием ОЗР: Оперативный запас реактивности — это положительная реактивность, которую реактор имел бы при всех извлеченных стержнях СУЗ.
Как и нормальным реакторам, реактору РБМК запас реактивности также необходим для маневра мощностью. Еще после аварии в 1975 г. на первом блоке Ленинградской АЭС для РБМК был определен минимальный запас реактивности в 15 стержней исходя из необходимости регулирования энерговыделения в активной зоне. А после чернобыльской аварии была найдена совершенная дикость, абсурд — при малом запасе A3 не глушит, а разгоняет реактор. Чем меньше запас реактивности, тем более ядерноопасен РБМК?! Знай наших!.. Мы не как другие прочие. Еще реакторов с такими свойствами нет. Можно понять, что A3 не справилась с глушением реактора, но чтобы сама разгоняла реактор — такого и в кошмарном сне не привидится.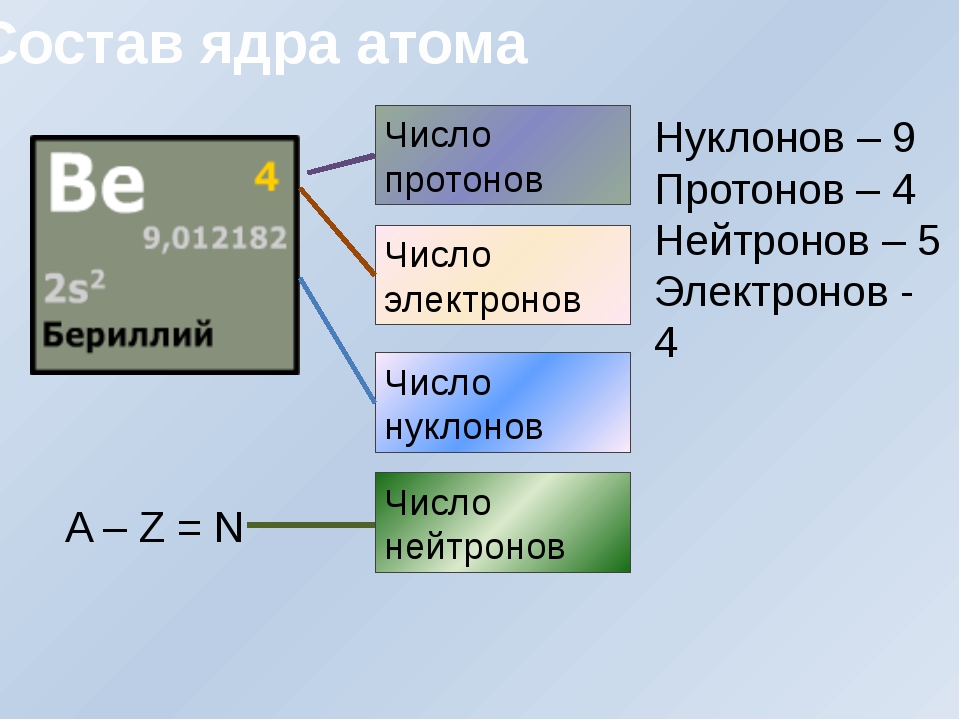
Как и ОЗР, в тексте часто будут упоминаться паровой эффект реактивности и мощностной коэффициент реактивности. Уясним понятия.
Пусть реактор работает на какой-то мощности при неизменном расходе теплоносителя. В технологическом канале вода нагревается до кипения и появляется пар. По мере продвижения в канале все больше воды, отбирающей тепло у ТВЭЛов, превращается в пар. Таким образом, в стационарном режиме имеем в пределах активной зоны какое-то количество пара. Теперь увеличим мощность реактора. Количество тепла возрастает и, следовательно, будет в активной зоне больше водяного пара.
Каким образом это повлияет на реактивность активной зоны — в сторону уменьшения или увеличения — зависит от соотношения в зоне ядер замедлителя и топлива. Вода также является замедлителем нейтронов, как и графит, и с увеличением количества пара в активной зоне становится меньше воды. Проектанты, видимо, исходя из экономических соображений, выбрали соотношение ядер замедлителя и топлива в РБМК таким, чтобы полная замена воды паром вела к увеличению реактивности на пять-шесть β.
Чем это страшно? К примеру, при разрыве трубы теплоносителя диаметром 800 мм обезвоживание наступает через несколько секунд и тихоходная A3 не справилась бы с выделившейся реактивностью.
Взрыв, как и 26 апреля. Это не все. При увеличении мощности температура топлива всегда возрастает и это ведет к уменьшению реактивности. В реакторе РБМК при изменении мощности, в основном, два фактора влияют на реактивность: отрицательный температурный эффект топлива и положительный паровой эффект. Они и составляют быстрый мощностной коэффициент реактивности — изменение реактивности при изменении мощности на один мегаватт (или киловатт). Другие эффекты изменения реактивности в зависимости от мощности: температурный эффект графита и отравление реактора ксеноном, хотя и имеют существенную величину, проявляются с большим запаздыванием и на динамику не влияют. У правильно сконструированного реактора мощностной коэффициент должен быть отрицательным. Это означает, что при каком-либо возмущении возрастает реактивность, с ней начинает увеличиваться мощность, а это ведет к уменьшению реактивности и мощность стабилизируется, хотя и на более высоком уровне. У реактора РБМК мощностной коэффициент был положительным в большом диапазоне мощностей — в нарушение требований нормативных документов.
У реактора РБМК мощностной коэффициент был положительным в большом диапазоне мощностей — в нарушение требований нормативных документов.
Это прямо повлияло на возникновение аварии 26 апреля.”
— Анатолий Степанович Дятлов «Чернобыль. Как это было», страницы 14–17.
Как определить количество протонов, нейтронов и электронов в изотопах
Материя бывает разных размеров, форм и цветов. Рассмотрим хлор, желтоватый газ, или свинец, серо-черное твердое вещество, или ртуть, серебристую жидкость. Три очень разных элемента, каждый из которых состоит только из одного вида атомов. Различия в материи сводятся к мельчайшим различиям в атомной структуре.
TL; DR (слишком длинный; Не читал)
Поймите, что изотопы элемента имеют разные массовые числа, но одинаковое количество протонов. Используя Периодическую таблицу, найдите атомный номер элемента. Атомный номер равен количеству протонов. В сбалансированном атоме количество электронов равно количеству протонов. В несбалансированном атоме количество электронов равно количеству протонов плюс противоположный заряд иона. Вычислите количество нейтронов, вычтя атомный номер из массового числа. Если массовое число определенного изотопа неизвестно, используйте округленную атомную массу из Периодической таблицы. к ближайшему целому числу минус атомный номер, чтобы найти среднее количество нейтронов для элемент.
В несбалансированном атоме количество электронов равно количеству протонов плюс противоположный заряд иона. Вычислите количество нейтронов, вычтя атомный номер из массового числа. Если массовое число определенного изотопа неизвестно, используйте округленную атомную массу из Периодической таблицы. к ближайшему целому числу минус атомный номер, чтобы найти среднее количество нейтронов для элемент.
Структура атомов
Каждый атом состоит из трех основных частиц. Протоны и нейтроны группируются в ядре в центре атома. Электроны образуют вращающееся облако вокруг ядра. Протоны и нейтроны составляют массу атомов. Электроны, крошечные по сравнению с протонами и нейтронами, вносят очень небольшой вклад в общую массу атомов.
Атомы и изотопы
Атомы одного и того же элемента имеют одинаковое количество протонов. Все атомы меди состоят из 29 протонов. У всех атомов гелия есть 2 протона. Изотопы возникают, когда атомы одного и того же элемента имеют разные массы. Поскольку количество протонов элемента не меняется, разница в массе возникает из-за разного количества нейтронов. Медь, например, имеет два изотопа: медь-63 и медь-65. Медь-63 имеет 29 протонов и массовое число 63. Медь-65 имеет 29 протонов и массовое число 65. Гелий имеет 2 протона и почти всегда имеет массовое число 4. Очень редко гелий образует изотоп гелий-3, который все еще имеет 2 протона, но имеет массовое число 3.
Медь, например, имеет два изотопа: медь-63 и медь-65. Медь-63 имеет 29 протонов и массовое число 63. Медь-65 имеет 29 протонов и массовое число 65. Гелий имеет 2 протона и почти всегда имеет массовое число 4. Очень редко гелий образует изотоп гелий-3, который все еще имеет 2 протона, но имеет массовое число 3.
Один из методов написания формулы для изотопа показывает имя элемента или символ, за которым следует массовое число, например, гелий-4 или He-4. Другая сокращенная идентификация изотопов показывает массовое число как верхний индекс и атомный номер как нижний индекс, оба показаны перед атомным символом. Например, 42Он указывает изотоп гелия с массовым числом 4.
Периодическая таблица элементов
Расположение Периодической таблицы элементов предоставляет важную информацию для определения количества протонов, нейтронов и электронов в атомах. В современной Периодической таблице элементы расположены в порядке их протонов. Первый элемент в таблице, водород, имеет один протон. Последний элемент (по крайней мере, на данный момент) в таблице, Оганессон или Унуноктиум, имеет 118 протонов.
Последний элемент (по крайней мере, на данный момент) в таблице, Оганессон или Унуноктиум, имеет 118 протонов.
Сколько протонов?
Атомный номер в Периодической таблице определяет количество протонов в любом атоме этого элемента. Медь с атомным номером 29 состоит из 29 протонов. Определение атомного номера элемента показывает количество протонов.
Сколько нейтронов?
Разница между изотопами элемента зависит от количества нейтронов. Чтобы узнать количество нейтронов в изотопе, найдите массовое число изотопа и атомный номер. Атомный номер или количество протонов находится в Периодической таблице. Атомная масса, также найденная в Периодической таблице, является средневзвешенным значением всех изотопов элемента. Если изотоп не идентифицирован, атомную массу можно округлить до ближайшего целого числа и использовать для определения среднего числа нейтронов.
Например, атомная масса ртути составляет 200,592. У Меркурия есть несколько изотопов с массовыми числами от 196 до 204. Используя среднюю атомную массу, вычислите среднее количество нейтронов, сначала округлив атомную массу от 200,592 до 201. Теперь вычтите количество протонов, 80, из атомной массы, 201-80, и найдите среднее количество нейтронов, 121.
Используя среднюю атомную массу, вычислите среднее количество нейтронов, сначала округлив атомную массу от 200,592 до 201. Теперь вычтите количество протонов, 80, из атомной массы, 201-80, и найдите среднее количество нейтронов, 121.
Если массовое число изотопа известно, можно вычислить фактическое количество нейтронов. Используйте ту же формулу, массовое число минус атомный номер, чтобы вычислить количество нейтронов. В случае ртути наиболее распространенным изотопом является ртуть-202. Используйте уравнение 202-80 = 122, чтобы найти, что ртуть-202 имеет 122 нейтрона.
Сколько электронов?
Нейтральный изотоп не имеет заряда, а это означает, что положительный и отрицательный заряды уравновешиваются в нейтральном изотопе. В нейтральном изотопе количество электронов равно количеству протонов. Как и определение количества протонов, определение количества электронов в нейтральном изотопе требует определения атомного номера элемента.
В ионе, изотопе с положительным или отрицательным зарядом, количество протонов не равно количеству электронов. Если протонов больше, чем электронов, изотоп имеет больше положительных зарядов, чем отрицательных. Другими словами, количество протонов превышает количество электронов на то же число, что и положительный заряд. Если количество электронов превышает количество протонов, заряд иона будет отрицательным. Чтобы найти количество электронов, добавьте к количеству протонов противоположность дисбаланса зарядов.
Если протонов больше, чем электронов, изотоп имеет больше положительных зарядов, чем отрицательных. Другими словами, количество протонов превышает количество электронов на то же число, что и положительный заряд. Если количество электронов превышает количество протонов, заряд иона будет отрицательным. Чтобы найти количество электронов, добавьте к количеству протонов противоположность дисбаланса зарядов.
Например, если изотоп имеет заряд -3, как у фосфора (атомный номер 15), то количество электронов на три больше, чем количество протонов. При вычислении количества электронов получается 15 + (- 1) (- 3), или 15 + 3 = 18, или 18 электронов. Если изотоп имеет заряд +2, как у стронция (атомный номер 38), то количество электронов на два меньше, чем количество протонов. В этом случае расчет становится 38 + (- 1) (+ 2) = 38-2 = 36, так что у иона 36 электронов. Обычное сокращение для ионов показывает дисбаланс заряда в виде верхнего индекса, следующего за атомным символом. В примере с фосфором ион будет записан как P-3.
3.4: Атомная масса и атомный номер
Результаты обучения
- Определение атомных и массовых чисел.
- Определить количество протонов, нейтронов и электронов в атоме.
- Определите заряд и относительную массу субатомных частиц.
- Обозначьте расположение субатомных частиц в атоме.
- Определите массу атома на основе его субатомных частиц.
- Напишите A/Z и формат символа-массы для атома.
Атомы являются фундаментальными строительными блоками всей материи и состоят из протонов, нейтронов и электронов. Поскольку атомы электрически нейтральны, количество положительно заряженных протонов должно быть равно количеству отрицательно заряженных электронов. Поскольку нейтроны не влияют на заряд, количество нейтронов не зависит от количества протонов и будет различаться даже среди атомов одного и того же элемента.
Атомный номер
Атомный номер (представленный буквой Z) элемента представляет собой число протонов в ядре каждого атома этого элемента .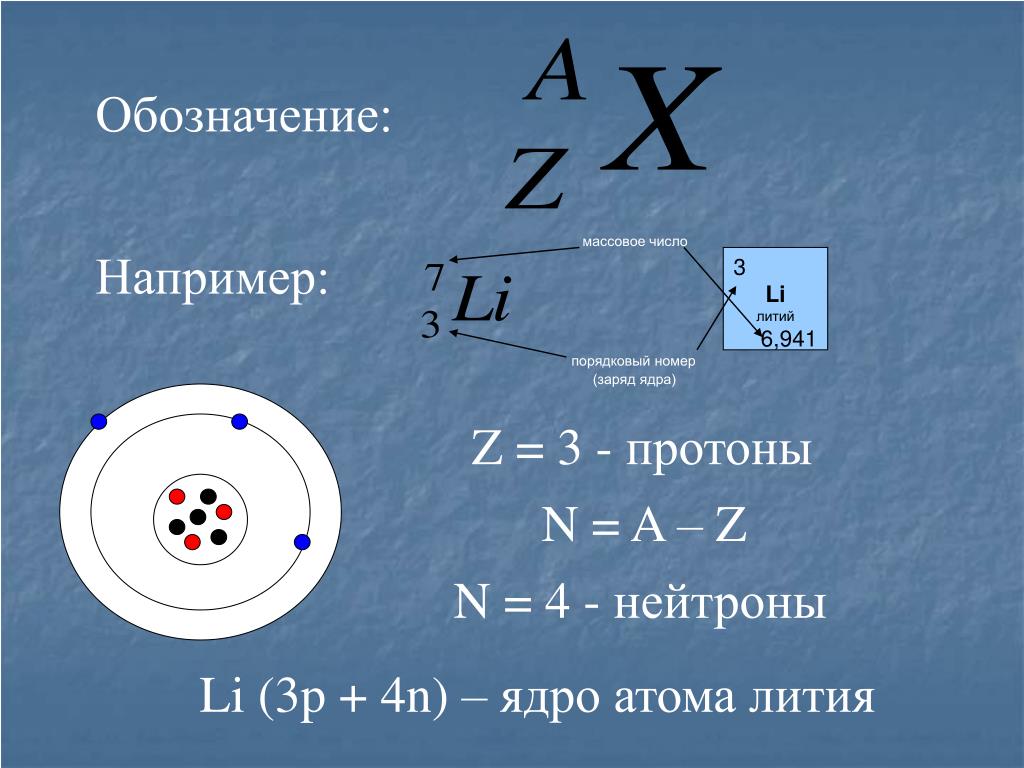 Атом может быть классифицирован как конкретный элемент исключительно на основании его атомного номера. Например, любой атом с атомным номером 8 (его ядро содержит 8 протонов) является атомом кислорода, а любой атом с другим числом протонов будет другим элементом. Периодическая таблица (см. рисунок ниже) отображает все известные элементы и расположена в порядке возрастания атомного номера. В этой таблице атомный номер элемента указан над символом элемента. Водород в левом верхнем углу таблицы имеет атомный номер 1.Каждый атом водорода имеет в ядре один протон. Следующим на столе стоит гелий, атомы которого имеют два протона в ядре. Атомы лития имеют три протона, атомы бериллия — четыре и так далее.
Атом может быть классифицирован как конкретный элемент исключительно на основании его атомного номера. Например, любой атом с атомным номером 8 (его ядро содержит 8 протонов) является атомом кислорода, а любой атом с другим числом протонов будет другим элементом. Периодическая таблица (см. рисунок ниже) отображает все известные элементы и расположена в порядке возрастания атомного номера. В этой таблице атомный номер элемента указан над символом элемента. Водород в левом верхнем углу таблицы имеет атомный номер 1.Каждый атом водорода имеет в ядре один протон. Следующим на столе стоит гелий, атомы которого имеют два протона в ядре. Атомы лития имеют три протона, атомы бериллия — четыре и так далее.
Рисунок \(\PageIndex{1}\): Субатомный номер социального страхования — протон.
Поскольку атомы нейтральны, количество электронов в атоме равно количеству протонов. Все атомы водорода имеют один электрон, занимающий пространство вне ядра. Гелий с двумя протонами будет иметь два электрона. В классе химии количество протонов всегда будет эквивалентно атомному номеру. Это значение не изменится, если ядро не распадется или не подвергнется бомбардировке (ядерная физика).
В классе химии количество протонов всегда будет эквивалентно атомному номеру. Это значение не изменится, если ядро не распадется или не подвергнется бомбардировке (ядерная физика).
Рисунок \(\PageIndex{3}\): Периодическая таблица элементов. (CC BY-SA 4.0 International; DePiep через Википедию).
Массовый номер
Экспериментальные данные показали, что подавляющая часть массы атома сосредоточена в его ядре, которое состоит из протонов и нейтронов. Массовое число (обозначенное буквой А) определяется как общее количество протонов и нейтронов в атоме. Рассмотрим приведенную ниже таблицу, в которой показаны данные первых шести элементов периодической таблицы.
| Имя | Символ | Атомный номер (Z) | Протоны | Нейтроны | Электроны | Массовый номер (А) (округленный до двух знаков после запятой) |
|---|---|---|---|---|---|---|
| водород | \(\се{Н}\) | 1 | 1 | 0 | 1 | 1. 01 01 |
| гелий | \(\ce{He}\) | 2 | 2 | 2 | 2 | 4,00 |
| литий | \(\ce{Li}\) | 3 | 3 | 4 | 3 | 6,94 |
| бериллий | \(\ce{Be}\) | 4 | 4 | 5 | 4 | 9.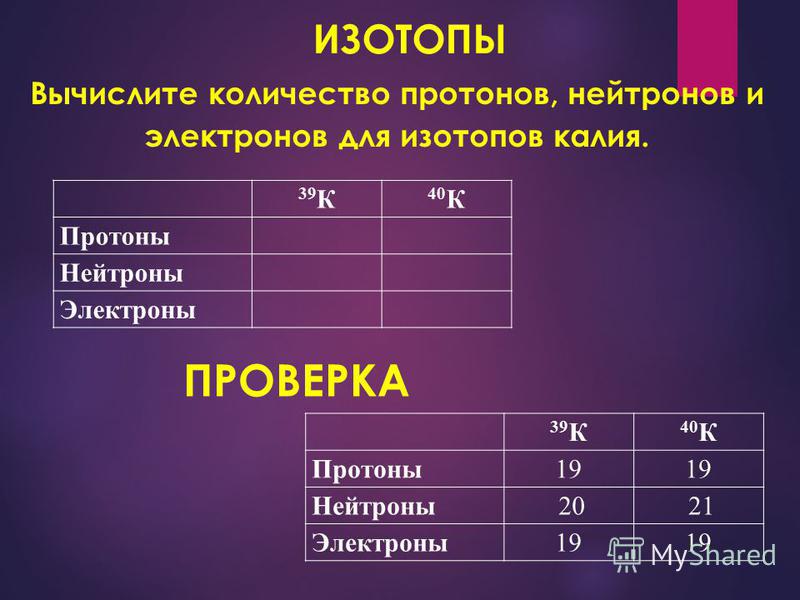 01 01 |
| бор | \(\ce{B}\) | 5 | 5 | 6 | 5 | 10,18 |
| уголь | \(\се{С}\) | 6 | 6 | 6 | 6 | 12.01 |
Рассмотрим элемент гелий.Его атомный номер равен 2, поэтому в его ядре два протона. Его ядро также содержит два нейтрона. Поскольку \(2 + 2 = 4\), мы знаем, что массовое число атома гелия равно 4. Наконец, атом гелия также содержит два электрона, так как число электронов должно равняться числу протонов. Этот пример может привести вас к мысли, что атомы имеют одинаковое количество протонов и нейтронов, но дальнейшее изучение приведенной выше таблицы покажет, что это не так. Литий, например, имеет три протона и четыре нейтрона, что дает ему массовое число 7.
Этот пример может привести вас к мысли, что атомы имеют одинаковое количество протонов и нейтронов, но дальнейшее изучение приведенной выше таблицы покажет, что это не так. Литий, например, имеет три протона и четыре нейтрона, что дает ему массовое число 7.
Рисунок \(\PageIndex{4}\): Формат A/Z и поиск субатомов для elementChromium (Авторское право; Элизабет Р. Гордон)
Зная массовое число и атомный номер атома, вы можете определить количество нейтронов, присутствующих в этом атоме, путем вычитания.
\[\text{Число нейтронов} = \text{массовое число с округлением} — \text{атомный номер}\]
Атомы элемента хрома \(\left( \ce{Cr} \right)\) имеют атомный номер 24 и массовое число 52.Сколько нейтронов в ядре атома хрома? Чтобы определить это, вы должны вычесть, как показано:
\[52 — 24 = 28 \: \text{нейтроны в атоме хрома}\]
Состав любого атома можно проиллюстрировать с помощью сокращенной записи, называемой форматом A/Z. И атомный номер, и масса записываются слева от химического символа.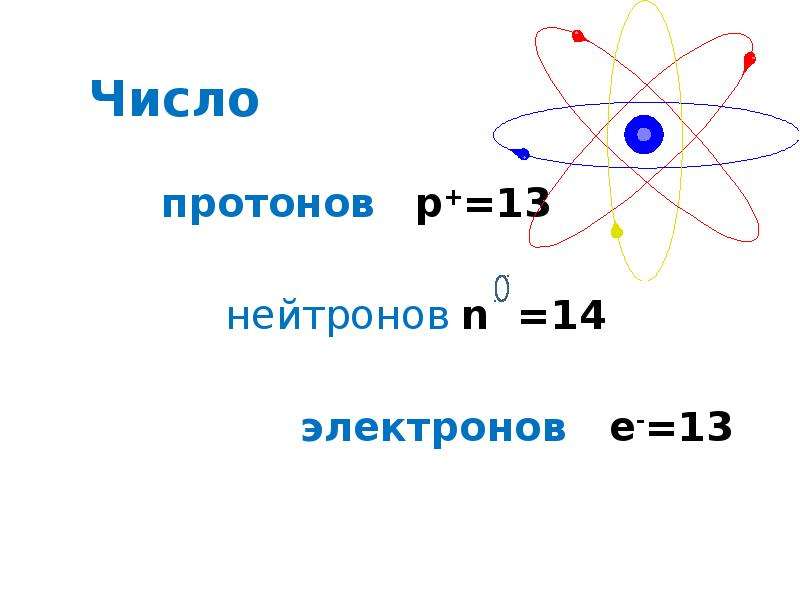 {52}_{24}Cr}\]
{52}_{24}Cr}\]
Другим способом обозначения конкретного атома является запись массового числа атома после названия, разделенного дефисом.Формат символа-массы для вышеуказанного атома будет записан как Cr-52. В этом обозначении атомный номер не включен. Вам нужно будет обратиться к периодической таблице для значений протонов.
Пример \ (\ PageIndex {1} \)
Рассчитайте каждую из трех субатомных частиц и дайте конкретные названия групп или периодов для каждого атома.
- ртуть
- платина
- бром
Решения
- Hg (переходный металл) – имеет 80 электронов, 80 протонов и 121 нейтрон
- Pt (переходный металл) — имеет 78 электронов, 78 протонов и 117 нейтронов
- Br (галоген) — имеет 35 электронов, 35 протонов и 45 нейтронов
Пример \ (\ PageIndex {2} \)
Запишите атомы в формате A/Z и символьной массы в примере \(\PageIndex{1}\). {80}_{35}Бр}\) и Бр-80
{80}_{35}Бр}\) и Бр-80
Пример \ (\ PageIndex {3} \)
Определите элементы на основе приведенных ниже утверждений.
- Какой элемент имеет 25 протонов?
- Какой элемент имеет 0 нейтронов?
- Какой элемент имеет 83 электрона?
Решения
а. марганец
г. водород
г. висмут
Нужно больше практики?
- Откройте раздел 3.E данного ООР и ответьте на вопросы №1–№2, №4 и №8.
Авторы и авторство
Фонд CK-12 Шэрон Бьюик, Ричарда Парсонса, Терезы Форсайт, Шонны Робинсон и Джин Дюпон.
Эллисон Сульт, доктор философии. (Кафедра химии, Университет Кентукки)
Атомная структура — Годзимо
Во-первых, атомы являются строительными блоками материи — мы это ясно понимаем.
Однако даже атомы состоят из вещества, а вещество меньшего размера известно как субатомные частицы.
В этом разделе мы сосредоточимся на этих субатомных частицах. Субатомные частицы состоят из протонов, нейтронов и электронов, которые удерживаются вместе сильными ядерными силами.
Пока все хорошо!
Неудивительно, что масса этих частиц очень и очень мала — я имею в виду крошечная!
И протоны, и нейтроны имеют массу в одну атомную единицу массы. Все они находятся в ядре вместе, но не могут отталкиваться друг от друга из-за сильного ядерного взаимодействия, создаваемого протонами и нейтронами.
Вы можете знать или не знать, но атомы имеют нейтральный заряд, потому что они несут одинаковое количество протонов и электронов, которые компенсируют друг друга.
Протоны несут один положительный заряд, а электроны несут один отрицательный заряд, поэтому в нейтральном атоме всегда одинаковое количество протонов и электронов.
Электроны имеют один отрицательный заряд и весят примерно 0,005 атомной единицы массы. Так что если вы думали, что нейтроны и протоны маленькие — электроны еще меньше!
Ионы образуются, когда атомы либо теряют, либо приобретают электроны, чтобы достичь полной внешней оболочки. Неметаллы приобретают электроны и превращаются в отрицательные ионы. Атомы металлов теряют электроны и превращаются в положительные ионы.
Неметаллы приобретают электроны и превращаются в отрицательные ионы. Атомы металлов теряют электроны и превращаются в положительные ионы.
Атомы также имеют то, что называется изотопами. Это атомы определенного элемента и имеют определенное количество нейтронов.
Другими словами, изотопы — это атомы элемента, которые имеют разное количество нейтронов в ядре, но одинаковое количество протонов, поэтому они имеют одинаковый атомный номер, но разные атомные массы.
Большинство элементов имеют несколько изотопов, некоторые из которых стабильны, а другие самопроизвольно распадаются, выделяя радиоактивность.
Чтобы найти массовое число атома, нужно просто сложить количество протонов и электронов.
Например, атом имеет семь нейтронов и семь протонов, его массовое число (А) равно 14.
Чтобы найти атомный номер, мы смотрим на протоны в атоме.
Например, посмотрите на хлор, у него 17 протонов, поэтому его атомный номер (Z) равен 17.
Вы также можете рассчитать количество протонов, электронов и нейтронов..PNG) Возьмем в качестве примера натрий.
Возьмем в качестве примера натрий.
Атомный номер, то есть количество протонов, равен 11. Количество протонов равно количеству электронов. Итак, натрий имеет 11 протонов и 11 электронов. Массовое число равно 23. Количество нейтронов = массовое число – атомный номер. Количество нейтронов = 23 – 11 = 12,
Связанные
Атомный
Структура
A. Атомный номер равен электронам или протонам
Каждый элемент имеет атомный номер.Атомные номера указаны вместе с названиями и символами элементов на внутренней стороне обложки текста. Атомный номер равен заряду ядра. Следовательно, оно также равно числу протонов в ядре, а также численно равно числу электронов в нейтральном атоме. Атомный номер имеет символ Z.
Разные элементы имеют разные атомные номера; поэтому атомы разных элементов содержат разное количество протонов (и электронов).Кислород имеет атомный номер 8; его атомы содержат 8 протонов и 8 электронов.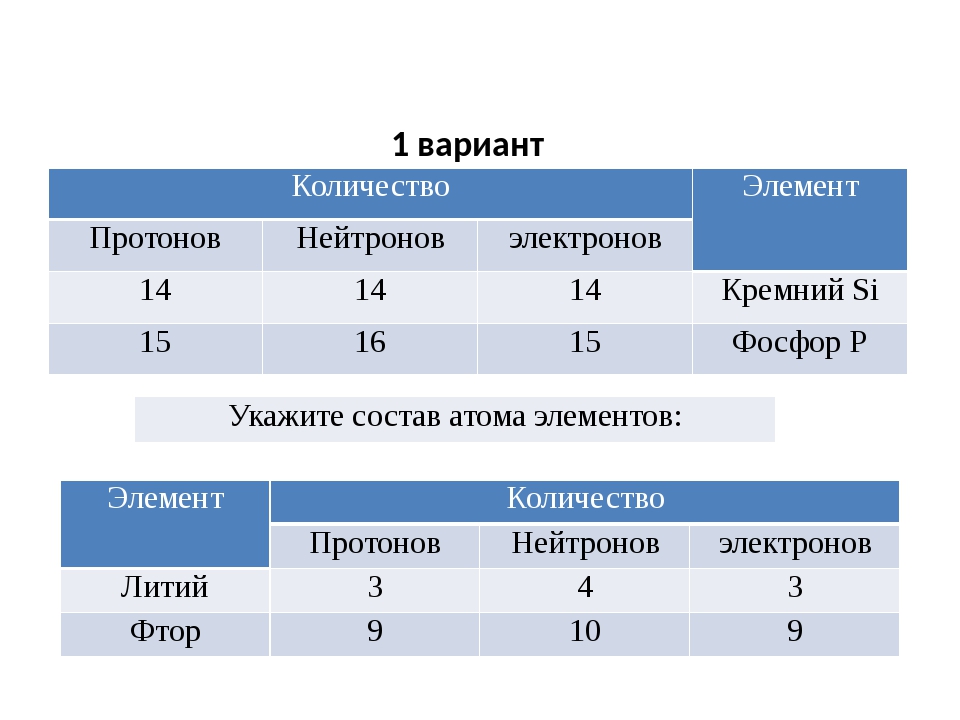 Уран имеет атомный номер 92; его атомы содержат 92 протона и 92 электрона.
Уран имеет атомный номер 92; его атомы содержат 92 протона и 92 электрона.
Связь между атомным номером и количеством протонов или электронов можно сформулировать следующим образом:
| Атомный номер | = количество протонов на атом |
| = число электронов на нейтральный атом |
Б.Массовое число равно количеству протонов плюс нейтронов
Каждый атом также имеет массовое число, обозначаемое символом А. Массовое число атома равно количеству протонов плюс количество нейтронов, которые он содержит. Другими словами, количество нейтронов в любом атоме равно его массовому числу минус его атомный номер.
Количество нейтронов = массовое число — атомный номер
или
Массовое число = количество протонов + количество нейтронов
Атомный номер и массовое число атома элемента можно показать, написав перед символом элемента массовое число в виде верхнего индекса и атомный номер в виде нижнего индекса:
| массовый номер атомный номер | Символ элемента | или | А З | Х |
Например, атом золота (символ Au) с атомным номером 79 и массовым числом 196 обозначается как:
С. Изотопы
Изотопы
Хотя все атомы данного элемента должны иметь одинаковый атомный номер, не обязательно, чтобы все они имели одинаковое массовое число. Например, некоторые атомы углерода (атомный номер 6) имеют массовое число 12, другие имеют массовое число 13, а третьи имеют массовое число 14. Эти разные виды одного и того же элемента называются изотопами.
Изотопы — это атомы с одинаковым атомным номером (и, следовательно, из одного и того же элемента), но с разными массовыми числами.Состав атомов встречающихся в природе изотопов углерода показан в таблице 4.2.
| ТАБЛИЦА 4.2 Природные изотопы углерода | |||
| Изотоп | протонов | Электроны | Нейтроны |
|---|---|---|---|
| 6 | 6 | 6 | |
| 6 | 6 | 7 | |
| 6 | 6 | 8 | |
Различные изотопы элемента могут быть обозначены с помощью надстрочных и нижних индексов, чтобы показать массовое число и атомный номер. Их также можно идентифицировать по названию элемента с массовым числом конкретного изотопа. Например, в качестве альтернативы
Их также можно идентифицировать по названию элемента с массовым числом конкретного изотопа. Например, в качестве альтернативы
мы можем написать углерод-12, углерод-13 и углерод-14.
В природе на Земле встречается около 350 изотопов, еще 1500 были получены искусственно. Изотопы данного элемента отнюдь не одинаково распространены. Например, 98,89 % всего углерода, встречающегося в природе, — это углерод-12, 1,11 % — углерод-13 и лишь незначительное количество — углерод-14.Некоторые элементы имеют только один встречающийся в природе изотоп. В таблице 4.3 перечислены встречающиеся в природе изотопы нескольких распространенных элементов, а также их относительная распространенность.
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
D. Внутренняя структура атома
До сих пор мы обсуждали электроны, протоны и нейтроны и способы определения
сколько каждого конкретного атома содержит. Остается вопрос: эти
Остается вопрос: эти
частицы, беспорядочно распределенные внутри атома, как черника в булочке,
или у атома есть какая-то организованная внутренняя структура? В начале
ХХ века ученые пытались ответить на этот вопрос. Различные теории
были предложены, но ни один из них не был проверен экспериментально. В нашем обсуждении
истории науки мы предположили, что на различных этапах ее развития
наука топталась на месте, пока кто-нибудь не провел ключевой эксперимент, который дал
новые идеи.В истории изучения атомов был поставлен ключевой эксперимент
в 1911 году Эрнестом Резерфордом и его коллегами.
1. Силы между телами
Наше понимание выводов, сделанных из эксперимента Резерфорда, зависит от знания сил, действующих между телами. Поэтому, прежде чем обсуждать его эксперимент, уместно сделать краткий обзор этих сил. Во-первых, это сила
сила тяжести, существующая между всеми телами. Его величина зависит от соответствующих масс и от расстояния между центрами тяжести двух взаимодействующих тел. Вы знакомы с гравитацией; он удерживает ваши ноги на земле, а луну на орбите.
Вы знакомы с гравитацией; он удерживает ваши ноги на земле, а луну на орбите.
Электрические силы также существуют между заряженными частицами. Величина электрической силы между двумя заряженными телами зависит от заряда каждого тела и от расстояния между их центрами. Если заряды одного знака (положительные или отрицательные), тела отталкиваются друг от друга; если заряды разного знака, то тела притягиваются друг к другу.
Магнитные силы, третий тип, аналогичны электрическим силам.Каждый магнит имеет два полюса — северный полюс и южный полюс. Когда два магнита соединяются вместе, между одноименными полюсами возникает сила отталкивания, а между разноименными полюсами — сила притяжения. В заряженном теле могут взаимодействовать магнитные и электрические силы. Эти три силы были известны в конце девятнадцатого века, когда интенсивно изучалась структура атома.
2. Опыт Резерфорда
Опишем опыт Резерфорда.
В 1911 году было общепризнано, что атом содержит электроны и протоны, но они, вероятно, не расположены по какому-либо определенному образцу. Резерфорд хотел установить, существует ли закономерность. Он надеялся получить эту информацию, изучая, как протоны в атоме отклоняют траекторию движения другой заряженной частицы, проходящей сквозь атом. В качестве второй частицы он выбрал альфа
Резерфорд хотел установить, существует ли закономерность. Он надеялся получить эту информацию, изучая, как протоны в атоме отклоняют траекторию движения другой заряженной частицы, проходящей сквозь атом. В качестве второй частицы он выбрал альфа
() частицы. Альфа-частица содержит два протона и два нейтрона, что придает ей относительную массу 4 а.е.м. и заряд +2. Альфа-частица настолько близка по массе и заряду к протону, что ее траектория изменилась бы, если бы она прошла рядом с протоном.В эксперименте пучок альфа-частиц направлялся на кусок золотой фольги, настолько тонкой, что становилась полупрозрачной, и, что более важно для Резерфорда, толщиной всего в несколько атомов. Фольга была окружена экраном из сульфида цинка, который вспыхивал каждый раз, когда в него попадала альфа-частица. Построив расположение вспышек, можно было бы определить, как путь альфа-частиц через атом был изменен протонами в атоме.
Три пути, показанные на рисунке 4.2 (пути A, B и C) являются репрезентативными для наблюдаемых. Большинство альфа-частиц следовали по пути А; они прошли прямо сквозь фольгу, как будто ее и не было. Некоторые были слегка отклонены от своего первоначального пути, как на пути B; и еще меньшее число отскочило от фольги, как будто они ударились о твердую стену (путь C).
Большинство альфа-частиц следовали по пути А; они прошли прямо сквозь фольгу, как будто ее и не было. Некоторые были слегка отклонены от своего первоначального пути, как на пути B; и еще меньшее число отскочило от фольги, как будто они ударились о твердую стену (путь C).
| РИСУНОК 4.2 (a) Поперечное сечение аппарата Резерфорда. |
| РИСУНОК 4.2 (б) Увеличенное сечение золотой фольги в аппарате, показывающее отклонение альфа-частиц ядрами атомов золота. |
Хотя вы можете быть удивлены, что какие-либо альфа-частицы прошли через золотую фольгу, Резерфорд этого не сделал. Он ожидал, что многие пройдут прямо (путь А). Он также ожидал, что из-за наличия в атоме положительно заряженных протонов некоторые альфа-частицы будут следовать по слегка отклоненному пути (путь В).Тот факт, что некоторые альфа-частицы отскочили назад (путь С), поразил Резерфорда и его коллег.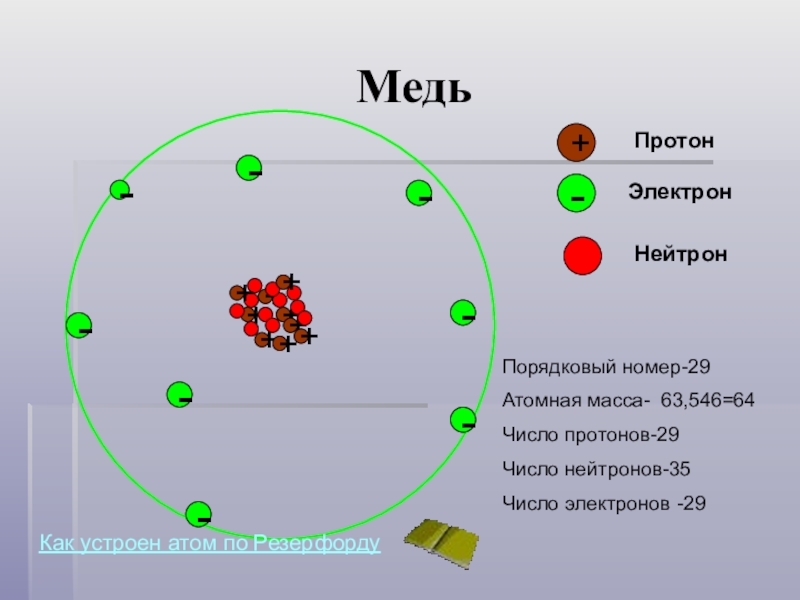 Путь C предполагал, что частицы врезались в область плотной массы и отскочили назад. Если использовать аналогию Резерфорда, возможность такого отскока была столь же маловероятной, как пушечное ядро, отскакивающее от куска папиросной бумаги.
Путь C предполагал, что частицы врезались в область плотной массы и отскочили назад. Если использовать аналогию Резерфорда, возможность такого отскока была столь же маловероятной, как пушечное ядро, отскакивающее от куска папиросной бумаги.
3. Результаты эксперимента
Тщательное рассмотрение результатов и особенно пути С убедило Резерфорда (и научное сообщество) в том, что атом содержит очень маленькое плотное ядро и большое количество внеядерного пространства.Согласно теории Резерфорда, ядро атома содержит всю массу атома и, следовательно, все протоны. Протоны придают ядру положительный заряд. Поскольку одноименные заряды отталкиваются друг от друга, положительно заряженные альфа-частицы, пролетая близко к ядру, отклоняются (путь В). Ядро, содержащее все протоны и нейтроны, массивнее альфа-частицы; следовательно, альфа-частица, ударившаяся в ядро атома золота, отскакивает от столкновения, как и те, что следовали по пути С.
Вне ядра, в относительно огромном внеядерном пространстве атома, находятся крошечные электроны.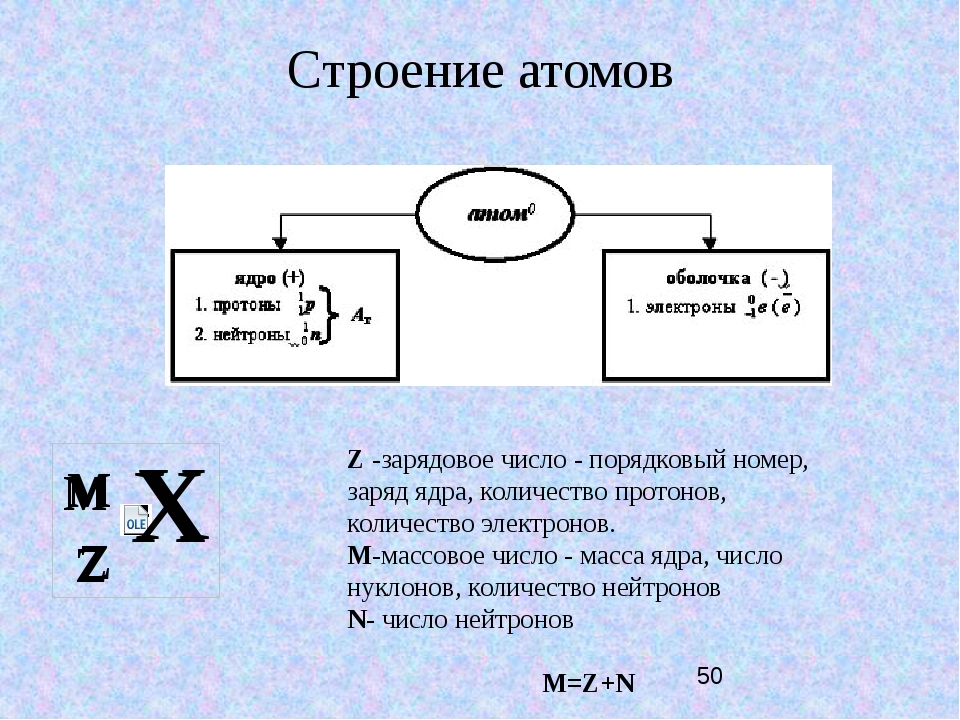 Поскольку электроны настолько малы по сравнению с занимаемым ими пространством, внеядерное пространство атома практически пусто. В эксперименте Резерфорда альфа-частицы, сталкиваясь с этой частью атомов в золотой фольге, проходили через фольгу неотклоняясь (путь А).
Поскольку электроны настолько малы по сравнению с занимаемым ими пространством, внеядерное пространство атома практически пусто. В эксперименте Резерфорда альфа-частицы, сталкиваясь с этой частью атомов в золотой фольге, проходили через фольгу неотклоняясь (путь А).
Если ядро содержит практически всю массу атома, оно должно быть чрезвычайно плотным.Его диаметр составляет около 10 90 716 -12 90 717 см, что составляет примерно 1/10 000 диаметра всего атома. Учитывая эту модель, если бы ядро было размером с мрамор, атом с его внеядерными электронами имел бы диаметр 300 мкм. Если бы шарик имел такую же плотность, как ядро атома, он весил бы 3,3 х 10 10 кг.
Эта модель ядра требует введения силы, отличной от тех, которые обсуждались ранее, силы, которая позволит протонам с их взаимно отталкивающими положительными зарядами плотно упаковываться в ядре, разделенные только незаряженными нейтронами.Эти ядерные силы, по-видимому, зависят от взаимодействия между протонами и нейтронами. Некоторые слабые, а некоторые очень сильные. Вместе они скрепляют ядро, но они еще не изучены.
Некоторые слабые, а некоторые очень сильные. Вместе они скрепляют ядро, но они еще не изучены.
Модель атома, основанная на работах Резерфорда, конечно, не более чем модель; мы не можем видеть эти субатомные частицы или их расположение внутри атома. Однако эта модель дает нам представление об атоме, которое совпадает с наблюдениями, сделанными в отношении его свойств.Теперь мы можем определить не только то, какие субатомные частицы содержит тот или иной атом, но и то, находятся ли они в его ядре. Например, атом углерода-12
содержит 6 протонов и 6 нейтронов в ядре и 6 электронов вне ядра.
У нас есть две отдельные части атома — ядро и внеядерное пространство. Ядро атома не играет никакой роли в химических реакциях, но участвует в радиоактивных реакциях.(Такие реакции обсуждаются далее в этой главе.) Химия атома зависит от его электронов — сколько их и как они расположены во внеядерном пространстве.
Назад На главную
  Далее
Радиационные исследования — CDC: The Ionized Atom
Атом — Мельчайшая частица элемента, которая может вступать в химическую реакцию.
Электрон — Элементарная частица с отрицательным электрическим зарядом и массой 1/1837 массы протона.Электроны окружают ядро атома из-за притяжения между их отрицательным зарядом и положительным зарядом ядра. В стабильном атоме будет столько электронов, сколько протонов. Количество электронов, вращающихся вокруг атома, определяет его химические свойства. См. также нейтрон
Ионизирующее излучение — Любое излучение, способное вытеснять электроны из атомов с образованием ионов. Высокие дозы ионизирующего излучения могут вызвать серьезное повреждение кожи или тканей. См. также альфа-частица, бета-частица, гамма-луч, нейтрон, рентгеновское излучение.
Изотоп — Нуклид элемента, имеющий одинаковое количество протонов, но разное количество нейтронов.
Нейтрон — Небольшая атомная частица, не обладающая электрическим зарядом, обычно присутствующая в ядре атома. Нейтроны, как следует из названия, нейтральны по своему заряду. То есть у них нет ни положительного, ни отрицательного заряда. Нейтрон имеет примерно ту же массу, что и протон. См. также альфа-частица, бета-частица, гамма-луч, нуклон, рентгеновское излучение.
Нейтроны, как следует из названия, нейтральны по своему заряду. То есть у них нет ни положительного, ни отрицательного заряда. Нейтрон имеет примерно ту же массу, что и протон. См. также альфа-частица, бета-частица, гамма-луч, нуклон, рентгеновское излучение.
Ядро — Центральная часть атома, содержащая протоны и нейтроны. Ядро — самая тяжелая часть атома.
Протон — небольшая атомная частица, обычно находящаяся внутри ядра атома, обладающая положительным электрическим зарядом. Несмотря на то, что протоны и нейтроны примерно в 2000 раз тяжелее электронов, они крошечные. Количество протонов уникально для каждого химического элемента. См. также нуклон.
Излучение — Энергия, движущаяся в форме частиц или волн. Знакомые излучения — это тепло, свет, радиоволны и микроволны. Ионизирующее излучение — это очень высокоэнергетическая форма электромагнитного излучения.
Радиоактивный распад — Распад ядра нестабильного атома под действием излучения.
Радиоактивность — Процесс самопроизвольного преобразования ядра, обычно с испусканием альфа- или бета-частиц, часто сопровождаемый гамма-лучами.Этот процесс называется распадом или распадом атома.
Радионуклид — нестабильная и, следовательно, радиоактивная форма нуклида.
[Вернуться к началу]
Атомная структура | Группа Грандинетти
Атомная структура
Атом состоит из трех типов субатомных частиц: протона , нейтрона и электрона .
| Частица | Масса/г | Заряд/$q_e$ | |||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Протон | 1.{-19}$ кулонов. Протроны и нейтроны имеют одинаковые массы, а электроны намного легче (более чем в 1000 раз легче). Протоны и электроны имеют одинаковые и противоположные заряды, а нейтроны не имеют заряда. У нас есть следующая простая картина атома . Атом состоит из положительно заряженного ядра, состоящего из протонов и нейтронов. Это маленькое ядро окружено вращающимися электронами.Поскольку протоны и нейтроны намного массивнее электронов, практически вся масса атома сосредоточена в ядре . Легкие отрицательно заряженные электроны движутся по орбите в пространстве вокруг ядра. Мы используем следующий символ для описания атома: A= Z + N, где N — число нейтронов. Если вы добавите или вычтете протона из ядра, вы создадите новый элемент . Если вы добавите или вычтете нейтрона из ядра, вы создадите новый изотоп того же элемента, с которого вы начали. В нейтральном атоме количество положительно заряженных протонов в ядре равно количеству вращающихся вокруг электронов . Атом водородаДавайте посмотрим на простейший пример атома, атом водорода . Атом состоит из протона и электрона, удерживаемых вместе электромагнитной силой между положительно заряженным протоном и отрицательно заряженным электроном. Электрон вращается вокруг протона, потому что это более легкая частица, подобно тому, как Земля вращается вокруг Солнца. Однако существуют большие различия в представлении Земли, вращающейся вокруг Солнца, и электрона, вращающегося вокруг ядра.1_1$H мы можем получить изотопа водорода. Вот три общих изотопа водорода. Если мы добавим протона к ядру водорода, мы получим гелий (другой элемент). Вот два распространенных изотопа гелия. Другим примером является углерод. Поскольку символ элемента и атомный номер избыточны, вы часто будете видеть изотопы, написанные без атомного номера. Например, вы увидите только 12 C. Количество протонов определяется атомным номером , нижним номером, поэтому количество протонов равно 17. Это нейтральный атом , поэтому будет равное количество отрицательно заряженных электронов, чтобы уравновесить положительно заряженные электроны. заряженных протонов, таким образом, количество электронов также равно 17. Мы знаем, что атомная масса равна . А = Z + N , где N — количество нейтронов. Переставляя уравнение получаем Н = А — Я Подставляем уже известные нам числа, получаем N = 35 — 17 = 18 = количество нейтронов Теперь вы можете подумать, что атомное ядро с большим количеством протонов (например, 12 C ) разлетелось бы на части из-за электрического отталкивания между положительно заряженными протонами.Оказывается, эти силы электрического отталкивания преодолеваются силой притяжения между протонами и нейтронами, называемой сильной ядерной силой. Атомная массаграмма не очень удобная единица измерения атомной массы, поэтому определена новая единица, называемая единицей атомной массы (u) . 1 и = 1.66053904 x 10 -24 г Перевыражая массы субатомных частиц через атомные единицы массы, мы имеем
Используя прибор под названием масс-спектрометр , мы можем очень точно измерить массу атомов и молекул.
То, что 12 C имеет массу ровно 12 000 000 единиц, не является совпадением. Масс-спектрометр может точно измерять только массу различий .Для решения этой проблемы определено, что изотоп 12 C имеет массу ровно 12 единиц. Как и следовало ожидать, разные изотопы одного и того же элемента будут иметь разные массы. Однако, если вы посмотрите на периодическую таблицу, вы заметите, что для массы каждого элемента указано только одно число. Как можно иметь только одну массу, если существует более одного изотопа каждого элемента? Ответ состоит в том, что масса каждого элемента равна средневзвешенному значению масс всех изотопов этого элемента.В этом средневзвешенном веса представляют собой процент содержания каждого изотопа в природе. Например, если вы проанализируете кусок чистого углерода с планеты Земля, вы обнаружите, что
Итак, средневзвешенная масса углерода равна (0,9889)(12,000000 u 12 С ) + (0. Вполне возможно, что на планете в далекой галактике естественное содержание изотопов углерода может быть другим, и поэтому они будут иметь немного разные числа под углеродом в своей периодической таблице. Однако массы изотопов везде одинаковы. Природное содержание 63 Cu составляет 69,09 %, а 65 Cu составляет 30,19 %. Если атомный вес 63 Cu равен 62,93 ед., а 65 Cu равен 64.93 u, каков средний атомный вес природной меди? (0,6909)(62,93 ед. 63 Cu ) + (0,3091)(64,93 ед. 65 Cu ) = 63,55 ед. Домашнее задание из
2,15, 2,19, 2,21, 2,23, 2,25, 2,27, 2,33, 2,35, 2,37, 2,47, 2,49 Структура ядра, богатого нейтронами, бросает вызов существующим теориям — ScienceDaily Чуть более десяти лет назад ученые довели атомы магния до новых пределов, запихивая в их ядра дополнительные нейтроны, приближаясь – и, возможно, достигая – максимального предела для этого элемента. Теперь международная группа под руководством ученых из Национальной лаборатории Лоуренса в Беркли Министерства энергетики (Berkeley Lab) воспроизвела эту экзотическую систему, известную как магний-40, и получила новые и неожиданные сведения о ее ядерной структуре. «Магний-40 находится на перекрестке, где возникает много вопросов о том, как он выглядит на самом деле», — сказала Хизер Кроуфорд, штатный научный сотрудник отдела ядерных наук в лаборатории Беркли и ведущий автор этого исследования, опубликованного в Интернете 19 февраля.7 в журнале Physical Review Letters . «Это чрезвычайно экзотический вид». В то время как количество протонов (имеющих положительный электрический заряд) в его атомном ядре определяет атомный номер элемента — его положение в периодической таблице — количество нейтронов (не имеющих электрического заряда) может различаться. Самый распространенный и стабильный тип атома магния, встречающийся в природе, имеет 12 протонов, 12 нейтронов и 12 электронов (имеющих отрицательный заряд). Атомы одного и того же элемента с разным числом нейтронов известны как изотопы.Изотоп магния-40 (Mg-40), который изучали исследователи, имеет 28 нейтронов, что может быть максимумом для атомов магния. Для данного элемента максимальное количество нейтронов в ядре называется «линии нейтронного капельного полива» — если вы попытаетесь добавить еще один нейтрон, когда он уже заполнен, лишний нейтрон немедленно «стечет» из ядро. «Он чрезвычайно богат нейтронами», — сказал Кроуфорд. «Неизвестно, находится ли Mg-40 на линии капельного полива, но он определенно очень близок. Это один из самых тяжелых изотопов, который в настоящее время можно экспериментально получить вблизи линии капельного полива.» Форма и структура ядер вблизи границы стока особенно интересны физикам-ядерщикам, потому что они могут научить их фундаментальным вещам о том, как ядра ведут себя в экстремальных условиях существования. «Интересный вопрос, который постоянно возникает у нас в голове, когда вы подходите так близко к линии капельного полива, звучит так: «Изменяется ли способ расположения нейтронов и протонов?», — сказал Пол Фэллон, старший научный сотрудник отдела ядерных наук лаборатории Беркли. Такое фундаментальное понимание может дать информацию о теориях взрывных процессов, таких как создание тяжелых элементов при слиянии звезд и взрывах, сказал он. Исследование основано на экспериментах на японском заводе по производству пучков радиоактивных изотопов (RIBF), расположенном в Центре ускорительных исследований RIKEN Nishina в Вако, Япония.Исследователи объединили мощность трех циклотронов — типа ускорителя частиц, впервые разработанного основателем Berkeley Lab Эрнестом Лоуренсом в 1931 году — для получения пучков частиц очень высокой энергии, движущихся со скоростью около 60 процентов от скорости света. Исследовательская группа использовала мощный пучок кальция-48, стабильного изотопа кальция с магическим числом протонов (20) и нейтронов (28), чтобы поразить вращающийся диск из углерода толщиной в несколько миллиметров. Некоторые ядра кальция-48 столкнулись с ядрами углерода, в некоторых случаях образовав изотоп алюминия, известный как алюминий-41.Ядерно-физический эксперимент отделил эти атомы алюминия-41, которые затем были направлены на попадание в пластиковую мишень толщиной в несколько сантиметров (Ch3). Удар этой вторичной мишенью выбил протон из некоторых ядер алюминия-41, создав ядра Mg-40. Эта вторая мишень была окружена детектором гамма-излучения, и исследователи смогли исследовать возбужденные состояния Mg-40 на основе измерений гамма-лучей, испускаемых при взаимодействии луча с мишенью. В дополнение к Mg-40 измерения также зафиксировали энергии возбужденных состояний в других изотопах магния, включая Mg-36 и Mg-38. «Большинство моделей говорят, что Mg-40 должен быть очень похож на более легкие изотопы, — сказал Кроуфорд. «Но это не так. Когда мы видим что-то, что выглядит совсем по-другому, задача состоит в том, чтобы новые теории зафиксировали все это». Поскольку теперь теории расходятся с тем, что было замечено в экспериментах, необходимы новые расчеты, чтобы объяснить, что меняется в структуре ядер Mg-40 по сравнению с Mg-38 и другими изотопами. Фэллон сказал, что многие расчеты предполагают, что ядра Mg-40 сильно деформированы и, возможно, имеют форму футбольного мяча, поэтому два добавленных нейтрона в Mg-40 могут жужжать вокруг ядра, формируя так называемое ядро гало, а не встраиваясь в него. форма, которую демонстрируют соседние изотопы магния. «Мы размышляем о некоторых физических аспектах, но это должно быть подтверждено более подробными расчетами», — сказал он. Кроуфорд сказал, что дополнительные измерения и теоретическая работа над Mg-40 и что близлежащие изотопы могут помочь точно определить форму ядра Mg-40 и объяснить, что вызывает изменение в ядерной структуре. Исследователи отметили, что центр ядерной физики для пучков редких изотопов, новый объект управления науки Министерства энергетики США, который строится в Мичиганском государственном университете, в сочетании с массивом отслеживания энергии гамма-излучения (GRETA), строящимся в лаборатории Беркли, позволит дальнейшие исследования других элементов вблизи ядерной границы. Изотоп — обзор | ScienceDirect TopicsРавновесное и кинетическое фракционирование изотопов Фракционирование изотопов обычно обсуждается с точки зрения того, являются ли они равновесными или кинетическими процессами.Эти два обозначения охватывают большинство фракционирования, при этом кинетическое фракционирование относится к широкому кругу неравновесных процессов, таких как испарение и диффузия. Равновесное фракционирование изотопов происходит в первую очередь из-за различий в частотах колебаний изотопологов и, как таковое, зависит от температуры. Следствием этого является то, что более тяжелые изотопы образуют более прочные связи, чем легкие изотопы, и в равновесии более тяжелый изотоп разделится на фазу с более прочной связью (White, 2015).Изотопное фракционирование велико при температурах поверхности Земли и уменьшается с повышением температуры до тех пор, пока α не приблизится к 1 при магматических температурах. Эта температурная зависимость лежит в основе геотермометрии стабильных изотопов и палеотермометрии. Кинетическое фракционирование изотопов обусловлено однонаправленными реакциями, такими как дистилляция, испарение, диффузия, кристаллизация и окислительно-восстановительные реакции.В этих реакциях более легкие изотопы, поскольку они образуют более слабые связи, которые легче разрываются, реагируют быстрее, чем более тяжелые изотопы. Биологические реакции, в частности, могут демонстрировать большие эффекты кинетического фракционирования, и эти крупные фракционирования можно использовать в качестве индикаторов биологической активности и специфических метаболических процессов. Фракционирование также зависит от того, является ли система открытой, и продукт удален или не может дать обратную реакцию, или закрыт, и продукты могут дать обратную реакцию. (6)R=R0⋅fα−1 где R изотопный состав фазы является функцией начального соотношения изотопов R 0 , доля материала f , оставшихся в пласте, и коэффициент фракционирования α . На рис. 1 показано фракционирование воды по Рэлею при испарении — кинетический процесс, который можно описать уравнением Рэлея. По мере испарения воды с R 0 = 0‰ (кривая A) остаточная вода становится тяжелее из-за удаления легкого изотопа, согласно уравнению.6. δ 18 O мгновенного пара (кривая B) на 10 ‰ легче остаточной воды, но также становится тяжелее по мере протекания реакции. Рис. 1. В открытой системе, описываемой фракционированием по Рэлею, водяной пар удаляется по мере его испарения.Когда жидкая вода A с δ 18 O = 0 испаряется, δ 18 O мгновенного водяного пара B на 10 ‰ легче воды. По мере развития реакции оставшийся резервуар с жидкой водой A становится все более истощенным по 18 O, как и образующийся пар B. Если реакция идет до конца и не остается жидкой воды, накопленный пар C имеет то же значение δ 18 O в качестве исходной жидкости. Пунктирные линии D и E описывают двухфазную замкнутую систему. A, B и C также описывают кинетическое фракционирование изотопов в замкнутой системе (в которой имеется конечный источник реагента), где A — реагент, B — мгновенный продукт, а C — накопленный продукт. Перерисовано из Gat JR and Gonfiantini R (1981) Гидрология стабильных изотопов. Дейтерий и кислород-18 в круговороте воды . В: Гат Дж.Р. и Гонфиантини Р. (ред.), Международное агентство по атомной энергии: Вена, опубликовано в Международном агентстве по атомной энергии, Гидрология стабильных изотопов, Серия технических отчетов № 210, Вена: МАГАТЭ. Большая часть фракционирования изотопов зависит от массы. Когда существует более двух стабильных изотопов элемента, например кислорода или серы, фракционирование изотопов между разными парами изотопных отношений (т.g., 16 O/ 17 O и 16 O/ 18 O) можно предсказать на основе относительной разности масс между изотопами, и поэтому они называются фракционированием изотопов, зависящим от массы. Когда фракционирование значительно отклоняется от этого соотношения, оно называется масс-независимым фракционированием (MIF). Например, массовое фракционирование между тремя изотопами кислорода можно предсказать по соотношению δ 17 O ≈ 0,5 δ 18 O, отражающему относительную разницу масс между 16 O, 17 O и 18 О. |

 985
985 76
76 47
47

 {35}_{17}$Cl?
{35}_{17}$Cl?  На малых расстояниях внутри ядра эта сила сильнее электромагнитных сил отталкивания, но на больших
На малых расстояниях внутри ядра эта сила сильнее электромагнитных сил отталкивания, но на больших Вот некоторые измеренные массы изотопов с помощью масс-спектрометра .
Вот некоторые измеренные массы изотопов с помощью масс-спектрометра . Затем все остальное измеряется относительно 12 С.
Затем все остальное измеряется относительно 12 С. 0111)(13,0039 ед. 13 С ) = 12,011 ед.
0111)(13,0039 ед. 13 С ) = 12,011 ед.

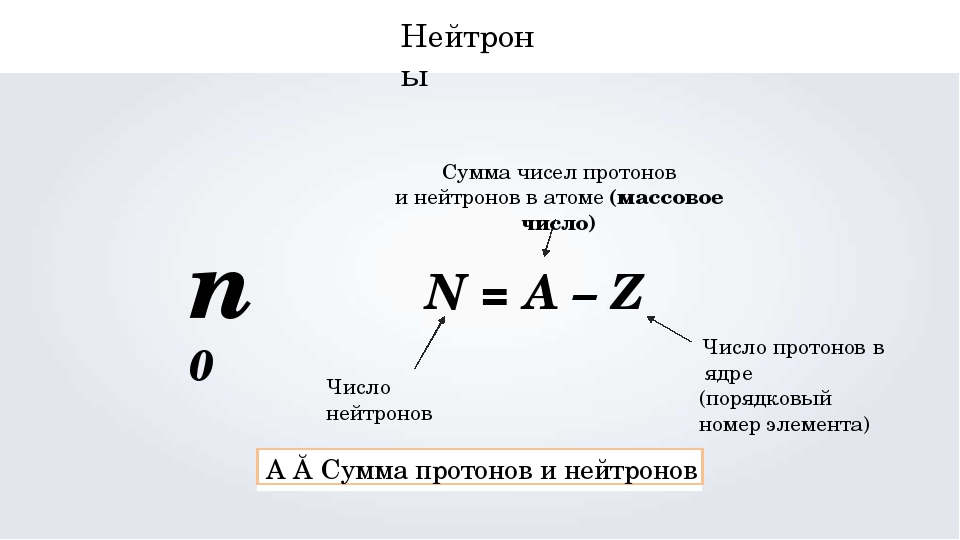 Отдел и соавтор исследования.«Одной из основных целей в области ядерной физики является понимание структуры от ядра элемента до линии капельного полива».
Отдел и соавтор исследования.«Одной из основных целей в области ядерной физики является понимание структуры от ядра элемента до линии капельного полива».


 Факторы равновесного фракционирования можно предсказать с помощью квантовой статистической механики (Chacko et al., 2001), хотя большинство факторов фракционирования в геохимии стабильных изотопов также были определены экспериментально.
Факторы равновесного фракционирования можно предсказать с помощью квантовой статистической механики (Chacko et al., 2001), хотя большинство факторов фракционирования в геохимии стабильных изотопов также были определены экспериментально. Рэлеевское фракционирование или дистилляция описывает равновесное фракционирование в открытой системе и кинетическое фракционирование с помощью однонаправленных реакций с конечным источником реагента, что функционально аналогично равновесным реакциям в открытой системе, когда продукты удаляются и не могут вступать в обратные реакции.Фракционирование Рэлея можно выразить в виде уравнения:
Рэлеевское фракционирование или дистилляция описывает равновесное фракционирование в открытой системе и кинетическое фракционирование с помощью однонаправленных реакций с конечным источником реагента, что функционально аналогично равновесным реакциям в открытой системе, когда продукты удаляются и не могут вступать в обратные реакции.Фракционирование Рэлея можно выразить в виде уравнения: Накопленный пар (кривая С) не превышает фракционирования, обусловленного равновесным коэффициентом фракционирования между водой и водяным паром при данной температуре. Равновесное фракционирование в закрытой системе показано линиями D и E.
Накопленный пар (кривая С) не превышает фракционирования, обусловленного равновесным коэффициентом фракционирования между водой и водяным паром при данной температуре. Равновесное фракционирование в закрытой системе показано линиями D и E.