Поверхностные явления на электролитических газовых пузырьках при электролизе воды в магнитном поле Текст научной статьи по специальности «Физика»
Поверхностные явления на электролитических газовых пузырьках при электролизе воды в магнитном поле
*В. Н. Зайченко, И. А. Слободянюк
Институт общей и неорганической химии им. В.И. Вернадского Национальной Академии наук Украины, пр. Палладина, 32/34, Киев-142, 03680, Украина, e-mail: [email protected]
Известно, что воздействие внешнего постоянного магнитного поля (ПМП) на процесс электролиза воды при определенной ориентации векторов электрического и магнитного полей снижает перенапряжение выделения водорода и кислорода. Механизм такого действия за счет образования магнитогидродинамических микровихрей электролита вокруг пузырьков, облегчающих их отрыв от электродов, то есть удаление продуктов электролиза, может иметь место, но он не согласуется с полученными нами результатами. Нами обнаружено, что под действием ПМП в момент отрыва от электрода и на начальном участке траектория движения пузырьков близка к параболической, которая далее сменяется прямолинейным вертикальным движением. Согласно закону Лоренца, определено, что пузырьки водорода несут отрицательный заряд, а кислорода -положительный во всем интервале рН, в том числе и при рН = 2,5, когда заряд пузырьков за счет адсорбции ионов из электролита равен нулю. Известно, что однородное ПМП действует только на движущиеся заряды. Высказано предположение, что такими движущимися по поверхности пузырьков зарядами могут быть эмитированные с катода электроны.
Ключевые слова: гидратированные электроны, магнитное поле, перенапряжение, сила Лоренца, электролиз.
УДК 544.636/638
ВВЕДЕНИЕ
Инжекция электронов из газовой фазы в водные растворы электролитов в условиях низкотемпературного плазменного электролиза (НТПЭ) хорошо известна [1]. Идея НТПЭ, которую впервые осуществил Я. Губкин, принадлежит Е. Варбургу [2]. Далее она была развита в [3, 4] и последующими исследователями доведена до создания новой ветви технической электрохимии [1].
Эмитированные с катода электроны, попадая в водную среду, гидратируются, образуя очень активные гидратированные электроны. Гидрати-рованные электроны образуются также при воздействии на водную среду ионизирующего излучения. Например, в [5] показано, что в поверхностных слоях морской воды под действием солнечного света возникают стационарные концентрации гидратированных электронов.
Возможность образования гидратированных электронов в условиях обычного электролиза водных растворов отмечена в обзоре [6]. Доказательства эмиссии электронов с катода в электролит приведены в [7], где авторами показано, что обнаруженное в [8] восходящее струйное течение электролита, образуемое на микрокатоде, расположенном в вертикальном капилляре, которое отклоняется при действии однородного ПМП от вертикали в соответствии с законом Лоренца, является потоком эмитированных электронов с микрокатода. Эти электроны мгновенно гидра-
тируются и образуют восходящую струю диаметром на порядок меньше диаметра капилляра. Подобные струи наблюдали также в [4]. Некоторые экспериментальные факты, косвенно подтверждающие образование гидратированных электронов в процессе электролиза, приведены
в [9].
Цель настоящей работы — получение дополнительных экспериментальных данных в подтверждение данной гипотезы.
МЕТОДИКА ЭКСПЕРИМЕНТА
В работе использовались следующие электролиты: 30% раствор КОН (1), 0,05М раствор серной кислоты (2), раствор серной кислоты с рН 2,5 (3) и раствор медного купороса (200 г/л) с серной кислотой (50 г/л) (4).
Ячейкой служила прямоугольная кювета из органического стекла с внутренним сечением 16^135 и высотой 90 мм. В качестве электродов использовались капилляры из нержавеющей стали с наружным и внутренним диаметрами соответственно 0,5 и 0,3 мм, рабочей поверхностью являлись торцы капилляров площадью 1,26-10-3 см2. Электроды вмонтированы в дно ячейки без выступающих поверхностей на дистанции 4 мм относительно друг друга и размещены параллельно и перпендикулярно оси магнитопровода (оси магнитного поля). К нижним торцам капилляров через штуцеры подведены силиконовые трубки для автономной подачи
© Зайченко В.Н., Слободянюк И.А., Электронная обработка материалов, 2016, 52(3), 88-93.
газов. Источником стабилизированного питания служил прибор ТЕС-14. Однородное ПМП индукцией до 0,8 Тл создавали лабораторным электромагнитом с регулируемым питанием постоянным током. Сечение полюсов электромагнита и зазор между ними составляли 70^100 и 20 мм соответственно. Калибровку электромагнита производили с помощью тесла амперметра Ф 4354/1. Разница в величине индукции ПМП в центре зазора и на его краях составляла не более 2%.
Опыт 1.
Заполнили ячейку электролитом (1). Ток регулировали таким образом, чтобы скорость выделения пузырьков водорода на катоде составляла не более 10^15 с-1, при этом плотность анодного и катодного токов равнялась 40 мА/см2. При отсутствии ПМП пузырьки водорода и кислорода под действием архимедовой силы всплывают строго вертикально (рис. 1а). Под действием ПМП индукцией 0,8 Тл траектории движения пузырьков водорода и кислорода в начальный период отклоняются в противоположные стороны в плоскостях, перпендикулярных вектору магнитной индукции В- (рис. 1б). При изменении направления вектора В- на противоположное изменяется на противоположное и отклонение траекторий (рис. 1в).
©
® в ® Е В ®
е е е
(а) (б) (в)
Рис. 1. Траектория движения пузырьков водорода (о) и кислорода (•): (а) — в отсутствие магнитного поля; (б), (в),
(г) — при воздействии магнитного поля с различной ориентацией векторов магнитного В— и электрического Е— полей;
(д) — схема движения эмитированных электронов с катода, вектор В— направлен по лучу зрения.
Данные опыта 1 говорят о том, что по поверхности пузырьков водорода и кислорода движутся заряды противоположного знака, на которые действует сила Лоренца, отклоняющая их траектории ортогонально векторам скорости движения зарядов и и магнитной индукции В-. Электрической составляющей силы Лоренца (д-Е-), согласно уравнению ¥л = д-Е- + д(^Б^), пренебрегаем, так как в отсутствие ПМП траектории движения пузырьков не отклоняются. При этом направление отклонения пузырьков соот-
ветствует отрицательному заряду на пузырьках водорода, создаваемому движущимися по их поверхности от катода отрицательными частицами, и положительному заряду на пузырьках кислорода. Существенно, что на начальном участке траектория движения пузырьков близка к параболической, которая далее сменяется прямолинейным вертикальным движением. Это говорит о том, что заряды на пузырьках нейтрализуются.
Опыт 2.
Аналогично опыту 1, но при условии перпендикулярности векторов В~* и Е-. В данном случае также наблюдается отклонение движения пузырьков водорода и кислорода от вертикали в направлениях, соответствующих закону Лоренца (правило левой руки), причем траектории движения пузырьков не смещаются вдоль вектора В-(рис. 1г). Пузырьки водорода в этом случае также заряжены отрицательно, а кислорода — положительно.
Опыт 3.
Аналогично опыту 1, но в 0,05М растворе И2804. Пузырьки водорода и кислорода движутся по таким же траекториям, как и в щелочном растворе. Это свидетельствует о том, что пузырьки водорода заряжены отрицательно, а кислорода — положительно.
Опыт 4.
Аналогично опыту 3, но в растворе И2804 с рН 2,5. Траектория движения пузырьков такая же, как в опыте 3. Значит, заряжены пузырьки аналогично.
Опыт 5.
Заполнили ячейку электролитом (4), при электролизе которого при плотности тока ниже 20 мА/см2 отсутствует газовыделение. Через капиллярный катод барботировали с помощью микрокомпрессора пузырьки воздуха. В начальный период диаметр пузырьков воздуха, выходящих из капиллярного катода, составлял ~ 0,5 мм. При включении ПМП вплоть до индукции 0,8 Тл отклонение траектории движения пузырьков не наблюдалось.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Согласно результатам опытов 1-4, выделяющиеся на катоде пузырьки водорода при электролизе воды заряжены отрицательно, кислорода — положительно как в щелочных, так и в кислых растворах. В опытах 1, 3, 4 кондукци-онное воздействие на электролит, как проводник с током, отсутствует, так как векторы В- и Е-параллельны. Поэтому объяснить ход траектории движения пузырьков вследствие возникающих вихрей электролита нельзя из-за отсутствия
последних. В опыте 2 при перпендикулярных В и Е^ возникновение такого вихря возможно, но в силу малой объемной плотности тока в электролите он не возникает, иначе траектория движения пузырьков сместилась бы относительно плоскости, перпендикулярной вектору В~., проходящей через капиллярные электроды.
Известно, что ПМП действует только на движущиеся электрические заряды.
В [10] показано, что в отсутствие ПАВ электролитические пузырьки водорода и кислорода заряжены отрицательно при рН > 3 и положительно при рН < 2, при этом точка нулевого заряда лежит в интервале рН 2^3, то есть пузырьки не заряжены. Из этого следует, что при движении под действием ПМП пузырьки водорода и кислорода отклонялись бы в одну сторону. Это противоречит результатам опытов 1-3, которые демонстрируют, что пузырьки водорода и кислорода отклоняются в противоположные стороны, что возможно только в том случае, если они несут противоположные заряды. А это противоречит данным [10]. Значит, траектории движения пузырьков при их отрыве от электродов отклоняются от движения по вертикали не за счет неподвижных зарядов, образованных адсорбированными ионами, а за счет динамических зарядов. Подтверждением этому служит опыт 4, выполненный в растворе Н2804 при рН 2,5, когда поверхность пузырьков не заряжена, то есть находится в точке нулевого заряда, а они отклоняются так же, как в опытах 1-3.
Существенным является факт действия силы Лоренца на пузырьки в момент отрыва их от электродов, когда скорость их всплытия равна нулю. Значит, равна нулю и скорость стационарных зарядов, образованных за счет адсорбированных ионов. Поэтому причиной возникновения силы Лоренца могут быть только динамические заряженные частицы. Такими частицами на катоде, вероятнее всего, являются эмитированные электроны. Поскольку эмиссия электронов с катода в объем электролита в данных условиях электролиза мало вероятна, мы полагаем, что эмитированные электроны движутся в пузырьке по границе раздела газ-электролит (рис. 1д). Расчетные данные показали, что в таких условиях возможен выигрыш полной энергии 333,4 кДж/моль и свободной энергии -334,0 кДж/моль. Такая модель требует совершенствования, и численные значения величин могут измениться. Электроны, двигаясь по поверхности пузырьков в направлении, ортогональном ПМП, сообщают пузырькам начальный импульс, который совместно с архимедовой силой заставляет их двигаться в начальный период по параболической траектории, а далее, в
связи с высокой реакционной способностью гид-ратированных электронов, пузырьки теряют заряд и движутся по вертикали (рис. 1 д). На аноде генерируемыми положительно заряженными частицами предположительно могут быть Н20 .
Сказанное не противоречит теории возникновения стационарных зарядов на электролитических пузырьках благодаря адсорбции ионов. Но ПМП, как уже сказано, на прилипшие пузырьки с такими зарядами не действует и не может сообщить им начальный импульс, который наблюдается в опытах 1-4. Кроме того, переход траекторий в прямолинейный участок свидетельствовал бы о десорбции таких зарядов, что трудно объяснить. Поэтому адсорбированные заряды в условиях выполненных опытов не могут играть существенную роль. Об этом свидетельствуют и результаты опытов 1-4, когда при переходе из щелочной области в кислую, согласно адсорбционной теории, изменяется знак заряженных пузырьков и траектории их движения должны были бы измениться на противоположные, но этого не происходит. Более того, при рН 2,5 (опыт 4), когда пузырьки не заряжены, траектории их движения остаются такими же, как в опытах 1-3.
В [11] доказано, что внешнее ПМП при электролизе воды снижает перенапряжение выделения водорода и кислорода, что очень важно для практики получения экологически чистого энергоносителя. Такое снижение перенапряжения авторы объясняют возникновением на вертикальных электродах принудительной конвекции за счет градиента плотности раствора и магнитогидродинамических потоков.
Авторы [12] отмечают образование вокруг выделяющихся электролитических пузырьков микровихрей при воздействии ПМП за счет искривления силовых линий тока у поверхности пузырьков и возникновения составляющей вектора тока, перпендикулярной вектору В~7 Однако они не отмечают, что ниже экватора пузырьков должны образовываться микровихри противоположного направления (рис. 2).
Такие микровихри могут способствовать отрыву пузырьков от поверхности электродов и снижать перенапряжения выделения электролитических газов, но траектории движения пузырьков не могут носить упорядоченный характер, как это имеет место в нашем случае (опыты 1-4). Поэтому они играют менее существенную роль.
В некотором согласии с полученными результатами находятся данные работ Э. Фукса с сотрудниками, опубликованные в обзоре [13].
В 1893 г. сэр В. Армстронг выполнил такой опыт: два стеклянных стакана наполнил химически чистой водой, соединил их хлопковым шну-
ром, опустил в стаканы две металлические пластинки и после подачи на них высокого постоянного напряжения наблюдал образование по шнуру между стаканами водяного мостика. Спустя некоторое время шнур перескакивал из одного стакана в другой, а между стаканами образовывался водяной мостик. Изучение этого явления продолжил Э. Фукс с сотрудниками.
t
Рис. 2. Образование МГД-микровихрей вокруг электролитического пузырька; 1г — горизонтальная составляющая вектора тока.
Э. Фукс показал [13], что перемычка из воды образуется и без хлопкового шнура, причем ее длина при раздвижении стаканчиков может достигать более 30 мм, а время до разрушения -десятков минут. Он назвал эту перемычку «floating water bridge» (висячий водяной мостик).
Однако некоторые экспериментальные данные в публикациях Э. Фукса и других ученых пока не нашли удовлетворительного объяснения.
В этой связи полезно рассмотреть висячий водяной мостик как элемент электрохимической системы. Действительно, два стаканчика, наполненные доверху очень чистой дистиллированной водой с начальной электропроводимостью порядка 0,06 мкСм/см, с опущенными в них платиновыми электродами и соединенными водяным мостиком, возникающим при поляризации их постоянным напряжением до 25 кВ, образуют электрохимическую систему, хотя и в экстремальном варианте (рис. 3). Поэтому некоторые явления, возникающие в такой системе, можно объяснить с позиций электрохимии.
В [14] обнаружено, что после включения напряжения в катодном пространстве рН повышается до 9 единиц, в анодном уменьшается до 4, причем авторы, на наш взгляд, ошибочно утверждают, что электролиз при этом не протекает. При прохождении тока до 5 мА, обнаруженного Фуксом, в электрохимической системе обязательно протекает электролиз, в данном случае электролиз воды, а продукты электролиза
(водород и кислород) при такой малой плотности тока растворяются в воде и визуально не обнаруживаются.
Рис. 3. Висящий водяной мостик, образующийся при поляризации платиновых электродов постоянным напряжением до 25 кВ.
Увеличение рН в прикатодном пространстве легко объяснить как протеканием электролиза, так и весьма вероятной при такой напряженности электрического поля холодной эмиссией электронов с отрицательно поляризованного электрода (катода). Здесь полезно вспомнить опыты М. Розенберг, выполненные в 1922 г. [4], и, по ее мнению, прямо доказывающие, что с платинового или медного катода, поляризованного от катушки Румкорфа, электроны эмитируют через воздушный зазор толщиной 2 мм в 0,25М раствор иодида калия. При добавлении в раствор крахмала или фенолфталеина наблюдается окрашенная струя, проникающая с большой скоростью в глубь кюветы на расстояние до 9-10 см (рис. 4).
Ук
и
III
Рис. 4. Траектория движения электронов, эмитированных с катода (К) в водном растворе [4].
При помещении кюветы между полюсами постоянного магнита траектория струи отклоняется в сторону в соответствии с воздействием магнитного поля на движущиеся отрицательно заряженные частицы (рис. 5). М. Розенберг утверждает, что с помощью окрашенных струй «мы видим пути и движение электронов в растворе».
Рис. 5. Отклонение траектории электронов, эмитированных с катода (К) в водном растворе, под действием магнитного поля [4].
В соответствии с современными взглядами эмитированные электроны, попадая в воду, образуют так называемые гидратированные электроны еач». Они обладают очень высокой реакционной способностью, и так как в очень чистой воде, кроме молекул воды, ионов Н+ и ОН-, ничего нет, то они реагируют с протонами, образуя Н и Н2О, либо, взаимодействуя между собой, образуют Н2 и 2ОН-. При этом в катодном пространстве повышается относительная концентрация ионов ОН-, что приводит к увеличению рН.
Далее в прикатодном пространстве зафиксировано понижение температуры. Объяснить этот факт можно протеканием эндотермических реакций. Большинство реакций с участием гидрати-рованных электронов езд- в воде протекают с высокой скоростью и являются экзотермическими [15]. И только две реакции протекают с поглощением тепла. Это исключительно медленная реакция гидратированного электрона с водой:
еач» + Н20 = Нач + 0НЗЧ» , Н0 = 35 кДж/моль (1) и ионизация гидратированного атома водорода: Нщ = Нач+ + еач» , Н0 = 46 кДж/моль (2)
(Н0 — стандартная энтальпия реакции).
Возможно, именно эти эндотермические реакции и понижают температуру в катодном стаканчике, что является косвенным подтверждением эмиссии электронов.
В начальный период происходит перетекание воды по мостику из анодного стаканчика в катодный, затем уровни воды стабилизируются благодаря встречному потоку за счет гидростатического давления, как в сообщающихся сосудах. Это связано с тем, что присутствующие в воде заряженные частицы, в том числе электроны, при миграции в электрическом поле переносят с собой гидратную оболочку. Так как они связаны с различным количеством молекул воды, обладают различной подвижностью, то и коли-
чество переносимой воды в разных направлениях различно.
Э. Фукс с соавторами наблюдали также повышение температуры в мостике, что связано, вероятно, с выделением джоулева тепла благодаря тому, что плотность тока в мостике из-за малого сечения больше, чем в стаканчиках.
С помощью трассера, в качестве которого использовали порошок полиамида со средним размером частиц 5 мкм, авторы обнаружили вращение наружного слоя воды в мостике по часовой стрелке (если смотреть со стороны анодного стаканчика) с тангенциальной скоростью 0,3 м/с при диаметре мостика 2^3 мм. Аксиальная скорость при этом составляла 0,2 м/с. Объяснить такое вращение можно только с помощью магнитной гидродинамики. Если в однородном электрическом поле заряженные частицы движутся прямолинейно, то для вращательного движения или движения по спирали необходимо наличие магнитного поля. Источниками такого поля в опытах Э. Фукса с сотрудниками могли быть геомагнитное поле, собственное магнитное поле электрохимической системы или техногенные поля от других источников.
Известно, что в Центральной Европе усредненная индукция вертикальной составляющей геомагнитного поля равна примерно 0,5-10-4 Тл. Диаметр окружности, по которой вращается гид-ратированный электрон, движущийся с аксиальной скоростью 0,2 м/с, обладающий зарядом 1,6-10-19 Кл и массой вместе с гидратной оболочкой из 4 молекул воды 1,2-10-25 кг, составляет 6 мм. Это величина такого же порядка, как и диаметр мостика. Следует отметить, что гидра-тированные протоны (Н3О-3Н2О)+, имея противоположный знак заряда и мигрируя в противоположном направлении, вращаются аналогично электронам по окружности диаметром 6,05 мм, а гидроксид-ионы (ОН-3Н2О)- — по окружности диаметром 5,04 мм.
Если на катоде происходит эмиссия электронов, то на аноде, в силу принципа электронейтральности объема воды, должно образовываться эквивалентное количество положительных частиц. Такими частицами могут быть заряженные молекулы воды Н2О+ (то есть ОН + Н) [15]. Они реагируют с другими частицами, что аналогично захвату положительной дырки. При этом в воде сохраняется баланс по заряженным частицам и принцип электронейтральности не нарушается. Не нарушается также и первый закон Фарадея.
Рассмотрение висячего водяного мостика с таких позиций позволит стимулировать как дальнейшие исследования роли гидратирован-ных электронов в электрохимических процессах, так и структуры воды.
ЗАКЛЮЧЕНИЕ
Показано, что в момент роста и отрыва пузырьков водорода и кислорода от поверхности электродов при электролизе воды под воздействием внешнего постоянного магнитного поля с индукцией 0,1—0,8 Тл на них действует сила Лоренца, которая совместно с архимедовой силой в начальный период придает траекториям движения пузырьков параболический вид. Это указывает на то, что по поверхности пузырьков в этот период движутся заряженные частицы. Далее пузырьки движутся вертикально, что свидетельствует о нейтрализации таких зарядов.
Характер траектории движения не меняется при переходе из щелочной области в кислую. Более того, характер траектории не меняется при рН = 2,5 в точке нулевого заряда поверхности пузырьков. Следовательно, адсорбированные из электролита ионы не играют существенной роли в динамике процесса.
Сделано предположение, что на катоде движущимися по поверхности пузырьков заряженными частицами могут быть эмитированные электроны, которые гидратируются и взаимодействуют с другими частицами, присутствующими в растворе. При этом теряется заряд на пузырьках, о чем свидетельствует дальнейшее их движение по вертикали.
Природа движущихся зарядов на пузырьках кислорода пока не выяснена. Такими носителями заряда могут быть, например, h3O+.
Показано также, что ПМП действует только на генерируемые на электродах пузырьки. Траектории движения барботируемого воздуха через поляризованные капиллярные электроды не отклоняются от вертикали.
ЛИТЕРАТУРА
1. Кравченко А.В., Кублановский В.С., Пивоваров А.А., Пустовойтенко В.П. Низкотемпературный плазменный электролиз: теория и практика. Днепропетровск: ООО «Акцент ПП», 2013. 230 с.
2. Gubkin Y. Elektrolytische Metallabscheidung an der freien Oberfläche einer Salzlösung. Annalen der Physik und Chemie. 1887, 32, 114-115.
3. Makowetsky A. Über die Bildung von Wasserstoffsuperoxyd, Salpetersäure und Ammoniak bei der Glimmbogenentladung, unter Verwendung von Wasser als einer Elektrode. Z. Elektrochem. 1911. 17(6), 217-235.
4. Писаржевский Л.В., Розенберг М.А. Электрон в химии растворов и в электрохимии. Харьков: Гос. из-во Украины, 1923. 128 с.
5. Пармон В.Н. Проблема фотокаталитического разложения воды. В кн.: Фотокаталитическое преобразование солнечной энергии. Ч. 2. Молекулярные системы для разложения воды. Замараев К.И. Ред. Новосибирск: Наука, 1985, 6-107.
6. Антропов Л.И. Сольватированные электроны и их возможная роль в электродных процессах. В Сб.: Итоги науки. Серия «Химия». Т.6. Электрохимия. Горбунова К.М. Ред. М: ВИНИТИ, 1971, 5-64.
7. Сколунов А.В., Томилов А.П. О возможном участии гидратированных электронов в процессе электролиза водных растворов. Электрохимия. 1992, 28(6), 887-892.
8. Шорыгин А.П., Казарян Э.В., Алимова Р.З. Действие магнитного поля на струйные течения в электрохимической ячейке с микроэлектродом в канале. Электрохимия. 1979, 15(5), 678-680.
9. Зайченко В.Н. Движение электролита и газовых пузырьков при электролизе в магнитном поле. Журнал прикладной химии. 2012, 85(11), 1888-1891.
10. Brandon N.P., Kelsall G.H., Levine S., Smith A.L. Interfacial Electrical Properties of Electrogenerated Bubbles. J. Appl. Electrochem. 1985, 15(4), 485-493.
11. Iida T., Matsushima H., Fukunaka Y. Water Electrolysis under a Magnetic Field. J. Electrochem. Soc. 2007, 154(8), 112-115.
12. Koza J.A., Muhlenhoff S., Zabinski P., Nikrityuk P.A., Eckert K., Uhlemann M., Gebert A., Weier T., Schultz L., Odenbach S. Hydrogen Evolution under the Influence of a Magnetic Field. Electrochim. Acta. 2011, 56(6), 2665-2675.
13. Fuchs E.C., Wexler A.D., Paulitsch-Fuchs A.H., Agostinho L.L.F., Yntema D., Woisetschlager J. The Armstrong experiment revisited. Eur. Phys. J. Special Topics. 2014, 223(5), 959-977.
14. Woisetschlager J., Gatterer K., Fuchs E.C. Experiments in a Floating Water Bridge. Experiments in Fluids. 2010, 48(1), 121-131.
15. Харт Э., Анбар М. Гидратированный электрон. М.: Мир, 1973. 280 с.
Поступила 22.01.15 После доработки 09.07.15 Summary
It is known that an effect of an external constant magnetic field (CMF) on the process of electrolysis of water at a certain orientation of the vectors of the electric and magnetic fields reduces the overvoltage of the release of hydrogen and oxygen. The mechanism of this action due to the formation of magneto-hydrodynamic micro vortices of the electrolyte around the bubbles, which facilitates their separation from the electrodes, i.e. removal of electrolysis products, could take place, but it is not consistent with our results. We have found that due to the influence of a CMF in the moment of the separation of bubbles from the electrode and within the initial section, the trajectory of the bubble is close to a parabolic one, which is then changed by a straight vertical motion. According to the Lorentz law, it has been found that hydrogen bubbles are negatively charged and those of oxygen are positive in the entire range of pH, including pH of 2.5, when the charge of bubbles due to adsorption of ions from the electrolyte is zero. It is known that a homogeneous CMF influences only the moving charges. It is suggested that such charges moving over the surface of the bubbles may be emitted by electrons from the cathode.
Keywords: hydrated electrons, magnetic field, overvoltage, Lorentz force, electrolysis.
Электролиз униполярным генератором.: afhh723 — LiveJournal
довольно очевидное применение униполярного генератора, так как он обладает достаточно малым сопротивлением, что дает ему способность вырабатывать большие токи (сотни килоАмпер), что очень неплохо ввиду закономерности выведеной тем же Фарадем. Как известно закон Фарадея для электролиза
m – масса выделяющегося вещества, г;
n – количество электронов, переносимых в электродном процессе;
F – число Фарадея (F=96485 Кл/моль)
I – сила тока, А;
t – время, с;
M – молярная масса выделяющегося вещества, г/моль.
как видно нам нужен большой ток.
стоит еще заметить что нужен некий минимальный потенциал при котором электролиз будет ити.
безхитросно сделанный на коленке генератор способен выдовать несколько десятков ампер
от себя хочу заметить что напряжение на таком генераторе удвоенное. вобще говря ЭДС = nBS
n — оброты в секунду
B — магнитная индукция
S — площадь пронизываемая потоком B
т.е. делайте правильные выводы. ну и напоследок схема генератора:
диски изготавливаются из электротехнической сталитолшиной где-то 1 мм. вал тогда имет делать смысл из нержавейки, диски должны иметь не только прочное механическое соединение с валом, но и иметь надежный электрический контакт с ним.
и еще одно соображения по поводу электролиза: горе «СЕ-шники» как правило занимаются изготовление гремучего газа со всеми вытикающими… наверное в целях безопасности они переименовали его в газ брауна, но как показывает практика — сути это меняет мало.
элетрод для электролиза изготавливается следующим образом:
берутся два листа нержавеющей стали толшиной не более ~1мм. на один лист надо наклеить небольшие кусочки изоляции в слоев 5 — т.е. надо изготовить такую полосу из изоляци в 5 слоев, потом наклеить на длинные края и по-середине одного листа квадратики примерно 15×15 из «многослойной изоляции» по всей длине листа, наложить сверху второй и свернуть в «трубку».
как уже отмечалось газы в этом случае разделить трудно, но если по каким-то причинам вы получите в установке гремучий газ — вы об этом узнаете по следующим признакам — оторванные взрывом конечности или голова.
вот и вся технология.
вращающийся электролизер для получения водорода и кислорода — патент РФ 2379379
Изобретение относится к конструкциям электролизеров для получения водорода и кислорода путем электролиза воды. Устройство для электролитического получения водорода и кислорода содержит технологические линии подачи воды и электролита и отвода продуктов электролиза, электролизер, включающий корпус с верхней и нижней крышками, установленный на соединенном с приводом вращения валу, и короткозамкнутые электроды, один из которых расположен на валу, а другой образован внутренней поверхностью корпуса. Линия отвода продуктов электролиза содержит последовательно соединенные устройство откачивания продуктов электролиза, газовый анализатор и сепаратор, а линия подачи воды и электролита содержит емкости для воды и электролита, устройство регулирования расхода воды, вентили, смеситель и теплообменник. Устройство снабжено магнитной системой, включающей механически соединенные магнитопроводом постоянные неподвижные магниты в виде дисков, расположенных параллельно над верхней и нижней крышками корпуса, а также двумя электрически соединенными с валом и корпусом токоведущими дисками, соответствующими ширине неподвижных магнитов, покрывающими верхнюю и нижнюю крышки. В токоведущих дисках выполнены радиальные прорези, а крышки выполнены из электроизоляционного материала. Изобретение позволяет снизить рабочую скорость вращения электролизера, увеличить производительность и сократить потребляемую электроэнергию. 2 ил.
Формула изобретения
Устройство для электролитического получения водорода и кислорода, содержащее технологические линии подачи воды и электролита и отвода продуктов электролиза, электролизер, включающий корпус с верхней и нижней крышками, установленный на соединенном с приводом вращения валу с каналами подвода раствора электролита и отвода продуктов электролиза, короткозамкнутые электроды, один из которых расположен на валу, а другой образован внутренней поверхностью корпуса, при этом линия отвода продуктов электролиза содержит последовательно соединенные устройство откачивания продуктов электролиза и сепаратор, а линия подачи воды и электролита содержит емкости для воды и электролита, устройство регулирования расхода воды, вентили, смеситель и теплообменник, на линии отвода продуктов электролиза установлен газовый анализатор, вход которого соединен с выходом устройства откачивания продуктов электролиза, а выход соединен с устройством регулирования расхода воды, при этом короткозамкнутый электрод, расположенный на валу, выполнен в виде цилиндра с радиальными каналами, отличающееся тем, что оно снабжено магнитной системой, включающей механически соединенные магнитопроводом постоянные неподвижные магниты в виде дисков, расположенных параллельно над верхней и под нижней крышками корпуса, а также двумя электрически соединенными с валом и корпусом токоведущими дисками, покрывающими верхнюю и нижнюю крышки, с выполненными в них радиальными прорезями, соответствующими ширине неподвижных магнитов, при этом крышки выполнены из электроизоляционного материала.
Описание изобретения к патенту
Предлагаемое техническое решение относится к области электрохимии, а именно к конструкциям электролизеров для получения водорода и кислорода путем электролиза воды. Известна «Установка для разложения воды электролизом» (патент РФ № 2224051, опубл. 20.02.2004), содержащая технологические линии подачи воды и электролита и отвода продуктов электролиза, электролизер, включающий корпус, установленный на соединенном с приводом вращения валу с каналами подвода раствора электролита и отвода продуктов электролиза, канал отвода раствора электролита, короткозамкнутые электроды, один из которых расположен на валу, а другой образован внутренней поверхностью корпуса, и теплообменник, а также верхний и нижний подшипниковые узлы, в которых вертикально расположен вал. Внешний контур циркуляции раствора электролита содержит кольцевую камеру раствора электролита с внутренней поверхностью в форме улитки, установленную на верхнем подшипниковом узле неподвижно, датчик наличия раствора электролита и смеситель раствора электролита, соединенный с линиями подачи электролита и воды и каналом подвода раствора электролита, корпус электролизера выполнен из токопроводящего материала и снабжен нижней и верхней крышками, выполненными из токопроводящего материала, канал отвода раствора электролита выполнен в верхней крышке и снабжен регулируемым клапаном, сообщающимся с кольцевой камерой раствора электролита, внутренняя поверхность корпуса снабжена, по меньшей мере, одной направляющей канавкой, линия подачи воды снабжена устройством регулирования расхода воды, линия отвода продуктов электролиза снабжена устройством для откачивания продуктов электролиза, теплообменник расположен во внешнем контуре циркуляции раствора электролита, а датчик наличия раствора электролита соединен с устройством регулирования расхода воды и приводом вращения вала. К недостаткам известной установки относится необходимость в больших рабочих скоростях вращения электролизера, что делает устройство малопригодным для промышленного применения. Сюда же можно отнести сложность конструкции, малую производительность.
Наиболее близким к предлагаемому техническому решению является «Устройство для электролитического получения водорода и кислорода» (патент РФ № 2309198, опубл. 27.10.2007, БИ № 30), содержащее технологические линии подачи воды и отвода продуктов электролиза, электролизер, включающий корпус с верхней и нижней крышками, выполненными из электропроводящего материала, установленный на соединенном с приводом вращения валу с каналами подвода раствора электролита и отвода продуктов электролиза, короткозамкнутые электроды, один из которых расположен на валу, а другой образован внутренней поверхностью корпуса. При этом линия отвода продуктов электролиза содержит последовательно соединенные устройство откачивания продуктов электролиза и сепаратор, а линия подачи воды и электролита содержит емкости для воды и электролита, устройство регулирования расхода воды, вентили, смеситель и теплообменник. Устройство снабжено электромагнитной системой, включающей неподвижные магниты в виде дисков, установленные параллельно над верхней и под нижней крышками корпуса, механически соединенный с ними магнитопровод с обмоткой возбуждения, электрически соединенной с генератором импульсов и преобразователем напряжения, на линии отвода продуктов электролиза установлен газовый анализатор, вход которого соединен с выходом устройства откачивания продуктов электролиза, а выход соединен с устройством регулирования расхода воды, при этом короткозамкнутый электрод, расположенный на валу, выполнен в виде цилиндра с радиальными каналами.
К недостаткам данного устройства относится также требование высоких рабочих скоростей вращения электролизера, малая производительность и значительное потребление электроэнергии, необходимое для питания электромагнитной системы.
Технической задачей, решаемой предлагаемым техническим решением, является упрощение конструкции, снижение рабочей скорости вращения электролизера, увеличение производительности и сокращение потребляемой электроэнергии.
Поставленная задача решается тем, что известное устройство для электролитического получения водорода и кислорода, содержащее технологические линии подачи воды и электролита и отвода продуктов электролиза, электролизер, включающий корпус с верхней и нижней крышками, установленный на соединенном с приводом вращения валу с каналами подвода раствора электролита и отвода продуктов электролиза, короткозамкнутые электроды, один из которых расположен на валу, а другой образован внутренней поверхностью корпуса, при этом линия отвода продуктов электролиза содержит последовательно соединенные устройство откачивания продуктов электролиза и сепаратор, а линия подачи воды и электролита содержит емкости для воды и электролита, устройство регулирования расхода воды, вентили, смеситель и теплообменник, на линии отвода продуктов электролиза установлен газовый анализатор, вход которого соединен с выходом устройства откачивания продуктов электролиза, а выход соединен с устройством регулирования расхода воды, при этом короткозамкнутый электрод, расположенный на валу, выполнен в виде цилиндра с радиальными каналами, согласно изобретению снабжено магнитной системой, включающей механически соединенные магнитопроводом постоянные неподвижные магниты в виде дисков, расположенных параллельно над верхней и под нижней крышками корпуса, а также двумя электрически соединенными с валом и корпусом токоведущими дисками, покрывающими верхнюю и нижнюю крышки с выполненными в них радиальными прорезями, соответствующими ширине неподвижных магнитов, при этом крышки выполнены из электроизоляционного материала.
Предлагаемое устройство схематично представлено на фиг.1. На фиг.2 представлено изображение токоведущего диска с радиальными прорезями.
Устройство содержит электролизер 1, включающий цилиндрический корпус 2, выполненный из электропроводящего немагнитного материала с верхней 3 и нижней 4 крышками, выполненными из электроизоляционного материала, установленный на вертикальном валу 5, выполненном из токопроводящего немагнитного материала и закрепленном в верхнем 6 и в нижнем 7 подшипниковых узлах. Вал 5 соединен с приводом вращения 8 и внутри имеет каналы подвода раствора электролита или воды 9 и отвода продуктов электролиза 10. К наружным поверхностям крышек 3 и 4 прилегают верхний 11 и нижний 12 токоведущие диски с радиальными прорезями. На валу 5 внутри электролизера расположен короткозамкнутый электрод 13 с радиально расположенными в нем каналами 14 (например, анод), выполненный из электропроводящего немагнитного материала. Внутренняя поверхность корпуса 2 образует другой электрод (например, катод). Канал подачи раствора электролита или воды 9 соединен с линией подачи воды и электролита 15, с теплообменником 16, смесителем 17, с вентилем 18, с емкостью для электролита 19, с вентилем 20, с устройством регулирования расхода воды 21 и с емкостью для воды 22. Теплообменник 16 соединен также со сливным вентилем 23. Канал отвода продуктов электролиза 10 соединен посредством технологической линии отвода продуктов электролиза 24 с устройством откачивания продуктов электролиза 25, соединенным с газовым анализатором 26, электрически соединенным с устройством регулирования расхода воды 21 и с сепаратором 27 для разделения кислородно-водородной смеси на кислород и водород. Электролизер снабжен магнитной системой, включающей верхний 28 и нижний 29 постоянные неподвижные магниты в виде дисков и механически соединенный с ними магнитопровод 30. На поверхности электролизера, контактирующей с электролитом, нанесены специальные покрытия, улучшающие электрические свойства электропроводящих частей и защищающие материалы от коррозии.
Устройство работает следующим образом. Электролит из емкости для электролита 19 через открытый вентиль 18 попадает в смеситель 17, затем в теплообменник 16, затем по технологической линии подачи электролита 15 — в канал подачи раствора электролита 9, расположенный в валу 5, и в электролизер 1. Вентиль 20 на линии подачи воды закрыт. После наполнения электролизера 1 раствором электролита вентиль 18 закрывают и включают привод вращения 8 вала 5, который приводит электролизер 1 во вращение, разгоняя его до начала процесса электролиза. При достаточно высокой производительности установки газовый анализатор 26 вырабатывает запирающий сигнал для устройства регулирования расхода воды 21, и технологическая линия подачи воды 15 в электролизер 1 перекрывается. Открывают вентиль 20. Устройство переходит в режим автоматического регулирования подачи воды из емкости для воды 22 через устройство регулирования расхода воды 21, открытый вентиль 20, смеситель раствора электролита 17, теплообменник 16 и канал подачи раствора электролита 9 в электролизер 1. Во вращающемся электролизере 1 в процессе выработки водорода и кислорода объем раствора электролита и соответственно его концентрация постоянно изменяются: концентрация раствора электролита повышается, а объем уменьшается. Граница раздела раствора электролита и газовой среды смещается к периферии электролизера 1. Электрод 13, расположенный на валу 5, оказывается в газовой среде, и электролиз прекращается. Газовый анализатор 26 подает сигнал на открытие устройства регулирования расхода воды 21. Из емкости для воды 22 по технологической линии подачи воды 15 в электролизер 1 поступает подогретая в теплообменнике 16 вода. Далее процесс повторяется. Каждый из электродов в электролизере 1 может выполнять функцию анода или катода в зависимости от химического состава используемого электролита.
В процессе вращения под действием центробежной силы в электролизере 1 создается поле искусственной силы тяжести, под воздействием которого катионы и анионы в виде гидратов, имеющих существенно отличающуюся собственную массу, разделяются. Более тяжелые ионы, например катионы, образуют около внутренней поверхности корпуса 2 (катода) отрицательный пространственный электрический заряд, который индуцирует в корпусе 2, выполненном из токопроводящего материала, адекватный заряд из электронов проводимости. Легкие ионы сконцентрируются в области между катодом и анодом 13, образуя свой пространственный положительный заряд, при этом, если величина его потенциала окажется достаточной для создания электрического поля, способного деформировать гидратные оболочки легких ионов, возникшее равновесие будет нарушено на аноде 13. Легкие ионы приблизятся к поверхности анода 13 и разрядятся. Тяжелые ионы также отдадут свой заряд катоду, и между электродами через верхний 11 и нижний 12 токоведущие диски с радиальными прорезями и вал 5, выполненные из токопроводящих материалов, как по короткозамкнутому контуру, потечет постоянный электрический ток. Ионы электролита восстановятся, образуя водород и кислород, а промежуточные продукты электролиза вступят с водой во вторичные реакции. Восстановленные водород и кислород вытесняются к центру электролизера 1 и в виде кислородно-водородной смеси через канал отвода продуктов электролизера 10, устройство откачивания продуктов электролиза 25 и газовый анализатор 26 отводят потребителю.
Для разделения кислородно-водородной смеси на кислород и водород в устройстве может быть предусмотрен сепаратор 27, из которого разделенные газы направляют к потребителям кислорода и водорода.
В подобных известных устройствах процесс электролиза происходит под действием только центробежного поля, что предполагает большие угловые частоты вращения электролизера (3000-5000 радиан в секунду). Технически это труднореализуемо. В подобных известных устройствах следующего поколения для снижения рабочих скоростей вращения электролизера и повышения производительности применяется электромагнитная система с электропитанием от внешнего источника.
В предлагаемом устройстве применена магнитная система с постоянными магнитами 28 и 29, что исключает потребление электроэнергии извне.
На движущуюся в постоянном магнитном поле электрически заряженную частицу воздействует сила Лоренца
F=B·V·q,
где В — магнитная индукция, Тл;
V -линейная скорость, м/с;
q -величина электрического заряда, К.
Векторы сил, действующих на отрицательные и положительные частицы, направлены противоположно и перпендикулярно к вектору линейной скорости так, что тяжелые ионы стремятся к периферии электролизера, а легкие — к центру.
Для увеличения возникающей разности потенциалов между электродами в предлагаемом устройстве применяются токоведущие диски 11 и 12 с радиальными прорезями. Диски прилегают к наружным поверхностям крышек 3 и 4 корпуса 2 и соединяют электрически корпус с валом 5 и соответственно с расположенными на них электродами. При вращении токоведущих дисков 11 и 12 в постоянном магнитном поле в них возникает ЭДС:
E= ·B(r2-r1),
где -угловая частота вращения диска, 1/с,
В — магнитная индукция, Тл,
r1 — расстояние от оси вала 5 до ближайшего края радиальной прорези,
r2 — расстояние от оси вала 5 до отдаленного края радиальной прорези.
Нужный знак ЭДС токоведущих дисков 11 и 12 реализуется либо изменением направления вращения электролизера 1, либо изменением полюсов магнитной системы, состоящей из магнитопровода 30 и постоянных магнитов 28, 29. В результате применения токоведущих дисков удается снизить рабочие скорости электролизера до 500÷700 радиан в секунду и значительно повысить производительность.
Процесс разложения воды на водород и кислород за счет восстановления их ионов сопровождается уменьшением энтальпии раствора электролита, в результате чего температура раствора постоянно снижается, и, если не восполнять теплопотери, то раствор замерзнет и процесс прекратится. По этой причине раствор необходимо подогревать. С этой целью в технологической линии подвода воды установлен теплообменник 16. Тепловую энергию к теплообменнику 16 могут подводить в виде выхлопных газов или антифриза от двигателя внутреннего сгорания или в ином виде. Для обеспечения техники безопасности устройство может быть снабжено защитным кожухом. В предлагаемом устройстве происходит преобразование механической, электрической и тепловой энергий в химическую энергию.
Газовый анализатор 26 может быть использован типа АВП-02 или АКПН-02, выполняющий и функцию датчика. В качестве устройства откачивания продуктов электролиза 25 можно задействовать электровакуумный насос, устройства регулирования расхода воды 21 — электромагнитный клапан.
Предлагаемое устройство позволяет повысить производительность установки, снизить рабочие угловые частоты вращения электролизера и упростить конструкцию и значительно снизить потребление электроэнергии. Устройство может быть изготовлено с использованием традиционных конструкционных материалов, комплектующих и известных электролитов и может быть использовано в агрегатах двигателей внутреннего сгорания транспортных средств, повышая их топливную экономичность, с паровыми турбинами тепловых и атомных электростанций, для утилизации промышленного тепла в металлургии и др.
Плазменный электролиз как модельная система для изучения ХЯС

Вадим Петрович Гончар, к.т.н.. химик.
Область интересов — Энергонива, ХЯС
Плазменный электролиз #ХЯС #LENR
Среди множества методов генерации плазменных образований, приводящих к возникновению трансмутации или других ХЯС-эффектов, плазменный электролиз видится нам наиболее удобным для репликации и проведения масштабных распределённых исследований, а также для приобретения первичных навыков работы с плазмой. К положительным сторонам работы именно с плазменным электролизом следует отнести простоту и дешевизну комплектующих для сборки экспериментальной установки, низкое энергопотребление, отсутствие мощных импульсных электрического и магнитного полей. Это позволяет широкому кругу энтузиастов собирать экспериментальные установки и работать с ними, не создавая особых неудобств (в виде электромагнитных помех, грохота разрядов и периодически выбиваемых пробок) для окружающих.
Кроме того, плазменный электролиз, как относительно маломощный источник плазмы, позволяет работать со статичными, непроточными ячейками, ограничиваясь только внешним охлаждением в водяной (или ледовой) бане. Отсутствие необходимости в сложной системе циркуляционного охлаждения не только существенно упрощает и удешевляет экспериментальную установку, но также позволяет избежать привнесения загрязнений, неизбежных в иных случаях.
Принципиальная электрическая схема простейшей экспериментальной ячейки приведена на рисунке 1. В качестве балластного сопротивления R1 целесообразно использовать электрочайник на 1,5…2кВт. Это не только сбережёт проводку в доме, но и позволит во время опытов освежаться ароматным чаем. Tr1 – это ЛАТР-2,5 -наиболее распространённая модель лабораторного автотрансформатора. D1 – выпрямительный мост с максимальным током 50А, желательно на радиаторе. С1 – сглаживающий конденсатор, желательно бумажный или другой, не чувствительный к импульсной нагрузке, ёмкостью 50…100мкФ.
В качестве собственно ячейки целесообразно использовать пластиковую ёмкость объемом 1…2 л. Стекло я не рекомендую по причине возможного разбития, металл будет корродировать, да и опасность непредусмотренного замыкания токоведущих частей резко возрастает.
Рабочий электролит – раствор соды в воде. Если подход серьёзный, и осадок планируется изучать, то вода должна быть дистиллированной, а сода (в таком случае её уже следует называть «карбонат натрия») должна иметь квалитет чистоты не ниже «чда».
Основное слабое место плазменного электролиза – быстрый нецелевой износ плазмирующего электрода (это тот электрод, площадь которого на несколько порядков меньше второго (обычно 10…20 мм2), и на котором зажигается «плазменная рубашка»). В случае плазмирующего анода это легко объяснимо – плазма из атомарного кислорода съедает даже платину. Но плазмирующий катод тоже быстро изнашивается. Мы полагаем, причина здесь в образовании летучих гидридов металлов.
В любом случае, наилучшим из доступных материалов для плазмирующего электрода является вольфрам. Второй электрод может быть либо графитовым (если это анод), либо из любого металла – если это катод.
На установке, аналогичной описанной выше, нами была проведена серия экспериментов по установлению факта трансмутации в таких мягких условиях. Сегодня мы расскажем об эксперименте с плазменным вольфрамовым катодом и графитовым анодом.
В качестве катода был использован вольфрамовый пруток диаметром 2 мм. Анодом служил тигель из химически-чистого графита. Эксперимент проводили в двух растворах карбоната натрия: 0,3М и 1М. В ходе эксперимента напряжение на ячейке плавно повышали ЛАТРом с 0 до 200 В для установления стабильной плазменной рубашки Ток при этом достигал 7А для 0,3М раствора и 10А для 1М раствора. По мере развития плазменной рубашки, ток падал, и достигал минимума при формировании псевдо-дугового разряда (о формах и стадиях плазменного катода мы, я надеюсь, ещё поговорим). Так как такая форма разряда приводит к быстрому выгоранию катода, после её достижения ячейка выключалась, электролит заменялся свежим и процесс повторялся. Осадок отделялся от обработанного электролита после каждой экспозиции фильтрованием на бумажном обеззоленом фильтре «белая лента». После наработки достаточного для анализа количества порошка катод был дополнительно освобождён от возможных отложений путем обработки в том же электролите переменным током. Полученный осадок отфильтрован на том же фильтре.
Итак, в ходе эксперимента были получены две пробы осадка. Сразу после осаждения осадок, полученный в 0,3М электролите, был чёрного цвета. Осадок из более концентрированного электролита, напротив, был светло-голубого цвета, почти белым. Этот признак и был положен в основу маркировки образцов.
После промывки дистиллированной водой, фильтры с образцами были кальцинированы до полного выгорания органической части. Масса полученных порошков составила 23 мг («чёрный» образец) и 19 мг («белый» образец) соответственно. Как видно, количество осадка крайне мало. Это является вторым существенным недостатком плазменного электролиза, так как требует от экспериментатора очень большой аккуратности в работе с образцами во избежание их потери или загрязнения. Но, тем не менее, это количество вполне достаточно для проведения анализа современными физико-химическими методами. Результаты такого анализа приведены на рисунках 2 и 3.
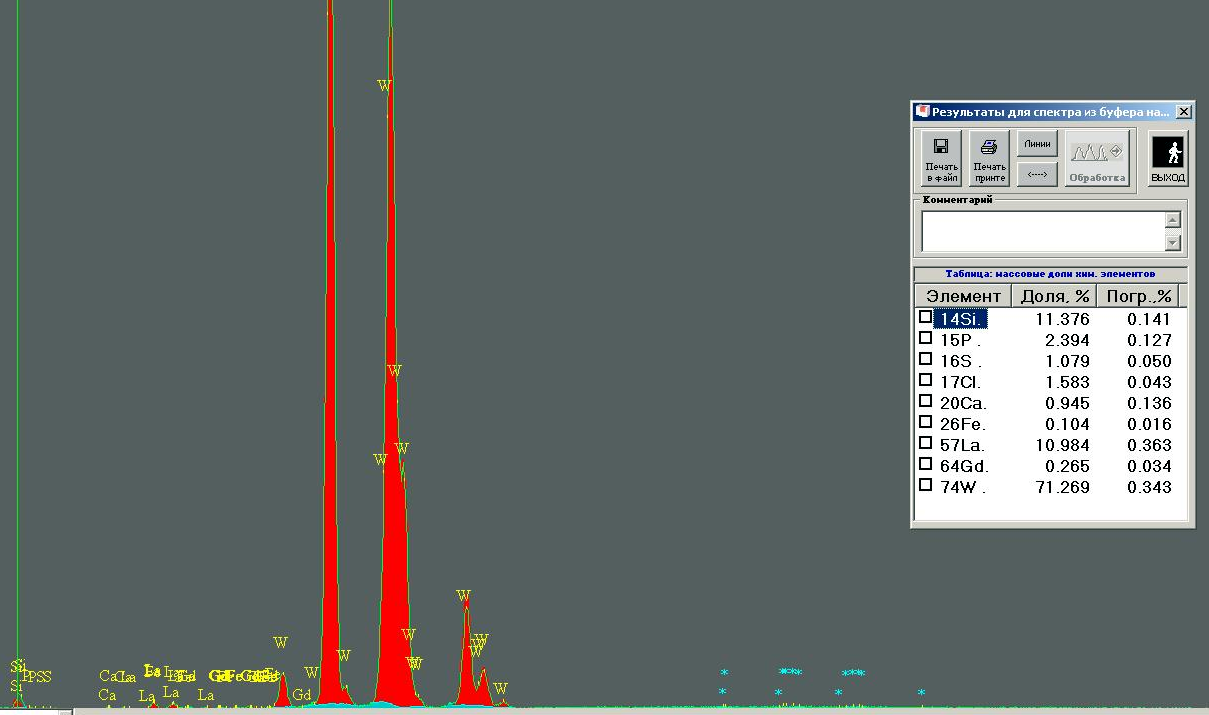
Рис 2. Белый осадок
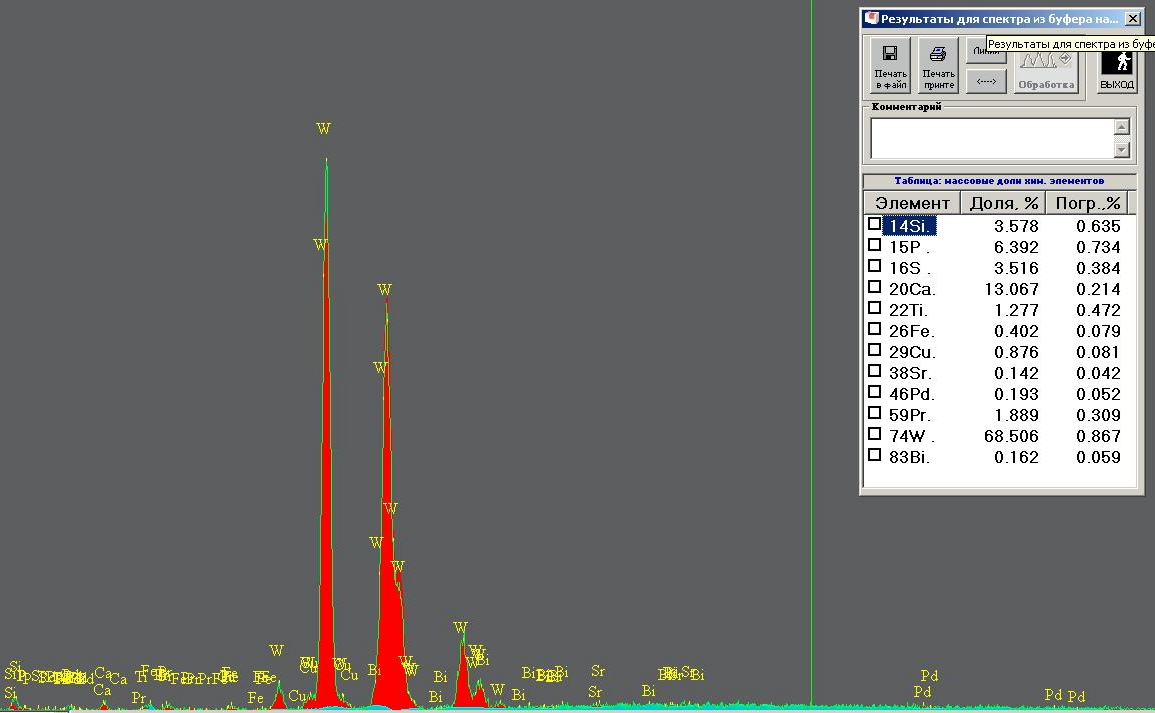
Рис.3 Черный осадок
Итак, результаты анализа вполне однозначно свидетельствуют о протекании процессов трансмутации при плазменном электролизе. В обеих случаях наработано значимое количество кремния, фосфора и серы. Эти элементы совершенно однозначно отсутствуют в вольфраме. В то же время, именно эти элементы, наряду с железом, наиболее часто упоминаются в качестве продуктов трансмутации. Кстати, железа в наших опытах обычно получается очень мало, в отличие от результатов, публикуемых другими исследователями. Также обращает на себя внимание высокое содержание кальция (13%) в образце «чёрный» и лантана (почти 11%) в образце «белый». Особо следует отметить, что практически все элементы, обнаруженные в осадке, находятся выше-левее вольфрама в периодической таблице элементов Д.И. Менделеева, что означает, что в ходе плазменного электролиза наиболее часто реализуются «распадные» каналы трансмутации. Единственным исключением является висмут в образце «чёрный». Следует подчеркнуть, что висмут, наряду со свинцом, наиболее часто встречающиеся представители «синтезных» каналов трансмутации в экспериментах с плазменным электролизом, независимо от условий проведения опытов.
что это такое, применение, сущность, правила, примеры
Вопрос о том, что такое электролиз, рассматривается еще в школьном курсе физике, и для большинства людей не является секретом. Другое дело – его важность и практическое применение. Этот процесс с большой пользой используется в различных отраслях и может пригодиться для домашнего мастера.

Что такое электролиз?
Электролиз представляет собой комплекс специфических процессов в системе электродов и электролита при протекании по ней постоянного электрического тока. Его механизм основывается на возникновении ионного тока. Электролит – это проводник 2-го типа (ионная проводимость), в котором происходит электролитическая диссоциация. Она связана с разложением на ионы с положительным (катион) и отрицательным (анион) зарядом.
Электролизная система обязательно содержит положительный (анод) и отрицательный (катод) электрод. При подаче постоянного электрического тока катионы начинают двигаться к катоду, а анионы – к аноду. Катионами в основном являются ионы металлов и водород, а анионами – кислород, хлор. На катоде катионы присоединяют к себе избыточные электроны, что обеспечивает протекание восстановительной реакции Men+ + ne → Me (где n – валентность металла). На аноде, наоборот, электрон отдается из аниона с протеканием окислительной реакции.
Таким образом, в системе обеспечивается окислительно-восстановительный процесс. Важно учитывать, что для его протекания необходима соответствующая энергия. Ее должен обеспечить внешний источник тока.
Законы электролиза Фарадея
Великий физик М.Фарадей своими исследованиями позволил не только понять природу электролиза, но и производить необходимые расчеты для его осуществления. В 1832 г. появились его законы, связавшие основные параметры происходящих процессов.
Первый закон
Первый закон Фарадея гласит, что масса восстанавливающегося на аноде вещества прямо пропорциональна электрическому заряду, наведенному в электролите: m = kq = k*I*t, где q — заряд, k – коэффициент или электрохимический эквивалент вещества, I – сила тока, протекающего через электролит, t – время прохождения тока.

Второй закон
Второй закон Фарадея позволил определить коэффициент пропорциональности k. Он звучит следующим образом: электрохимический эквивалент любого вещества прямо пропорционален его молярной массе и обратно пропорционален валентности. Закон выражается в виде:

k = 1/F*A/z, где F – постоянная Фарадея, А- молярная масса вещества, z – его химическая валентность.
С учетом обоих законов можно вывести окончательную формулу для расчета массы, оседающего на электроде вещества: m = A*I*t/(n*F), где n – количество электронов, участвующих в электролизе. Обычно n соответствует заряду иона. С практической точки зрения важна связь массы вещества с подаваемым током, что позволяет контролировать процесс, изменяя его силу.
Электролиз расплавов
Один из вариантов электролиза – использование в качестве электролита расплав. В этом случае в электролизном процессе участвуют только ионы расплава. В качестве классического примера можно привести электролиз солевого расплава NaCl (поваренная соль). К аноду устремляются отрицательные ионы, а значит, выделяется газ (Cl). На катоде будет происходить восстановление металла, т.е. оседание чистого Na, образующегося из положительных ионов, притянувших избыточные электроны. Аналогично можно получать другие металлы (К, Са, Li и т.д.) из расправа соответствующих солей.

При электролизе в расплаве электроды не подвергаются растворению, а участвуют только в качестве источника тока. При их изготовлении можно использовать металл, графит, некоторые полупроводники. Важно, чтобы материал имел достаточную проводимость. Один из наиболее распространенных материалов – медь.
Особенности электролиза в растворах
Электролиз в водном растворе существенно отличается от расплава. Здесь имеют место 3 конкурирующих процесса: окисление воды с выделением кислорода, окисление аниона и анодное растворение металла. В процессе задействованы ионы воды, электролита и анода. Соответственно, на катоде может происходить восстановление водорода, катионов электролита и металла анода.

Возможность протекания указанных конкурирующих процессов зависит от величины электрических потенциалов системы. Протекать будет только тот процесс, который требует меньше внешней энергии. Следовательно, на катоде будут восстанавливаться катионы, имеющие максимальный электродный потенциал, а на аноде – окисляться анионы с наименьшим потенциалом. Электродный потенциал водорода принят за «0». Для примера, у калия он равен (-2,93 В), натрия – (-2,71 В), свинца (-0,13 В), а у серебра – (+0,8 В).
Электролиз в газах
Газ может исполнить роль электролита только при наличии ионизатора. В этом случае ток, проходя через ионизированную среду, вызывает необходимый процесс на электродах. При этом законы Фарадея не распространяются на газовый электролиз. Для его осуществления необходимы такие условия:
- Без искусственной ионизации газа не поможет ни высокое напряжение, ни большой ток.
- Для электролиза подходят лишь кислоты, не содержащие кислорода и находящиеся в газообразном состоянии, и некоторые газы.
Важно! При выполнении необходимых условий процесс протекает аналогично электролизу в жидком электролите.
Особенности процессов, происходящих на катоде и аноде
Для практического применения электролиза важно понимать, что происходит на обоих электродах при подаче электрического тока. Характерны такие процессы:
- Катод. К нему устремляются положительно заряженные ионы. Здесь происходит восстановление металлов или выделение водорода. Можно выделить несколько категорий металлов по катионной активности. Такие металлы, как Li, K, Ba, St, Ca, Na, Mg, Be, Al, хорошо восстанавливаются только из расплава солей. Если используется раствор, то выделяется водород за счет электролиза воды. Можно обеспечить восстановление в растворе, но при достаточной концентрации катионов, у следующих металлов — Mn, Cr, Zn, Fe, Cd, Ni, Ti, Co, Mo, Sn, Pb. Процесс протекает наиболее легко для Ag, Cu, Bi, Pt, Au, Hg.
- Анод. К этому электроду поступают отрицательно заряженные ионы. Окисляясь, они отбирают электроны у металла, что приводит к их анодному растворению, т.е. переходу в положительно заряженные ионы, которые направляются к катоду. Анионы также подразделяются по своей активности. Только из расплавов могут разряжаться такие анионы PO4, CO3, SO4, NO3, NO2, ClO4, F. В водных растворах электролизу подвергаются не они, а вода с выделением кислорода. Наиболее легко реагируют такие анионы, как ОН, Cl, I, S, Br.

При обеспечении электролиза важно учитывать склонность материала электродов к окислению. В этом отношении выделяются инертные и активные аноды. Инертные электроды делаются из графита, угля или платины и не участвуют в снабжении ионами.
Факторы, влияющие на процесс электролиза
Процесс электролиза зависит от следующих факторов:
- Состав электролита. Значительное влияние оказывают различные примеси. Они подразделяются на 3 типа – катионы, анионы и органика. Вещества могут быть более или менее отрицательными, чем основной металл, что и мешает процессу. Среди органических примесей выделяются загрязнители (например масла) и ПАВ. Их концентрация имеет предельно допустимые значения.
- Плотность тока. В соответствии с законами Фарадея, масса осаждаемого вещества увеличивается с увеличением силы тока. Однако возникают неблагоприятные обстоятельства – концентрированная поляризация, повышенное напряжение, интенсивный разогрев электролита. С учетом этого существуют оптимальные значения плотности тока для каждого конкретного случая.
- рН электролита. Кислотность среды также выбирается с учетом металлов. Например оптимальное значение кислотности электролита для цинка – 140 г/куб.дм.
- Температура электролита. Она влияет неоднозначно. С увеличением температуры растет скорость электролиза, но повышается и активность примесей. Для каждого процесса есть оптимальная температура. Обычно она находится в пределах 38-45 градусов.
Важно! Электролиз можно ускорить или замедлить путем различных воздействий и выбора состава электролита. Для каждого варианта применения существует свой режим, который следует строго соблюдать.
Где применяется электролиз?
Электролиз применяется во многих сферах. Можно выделить несколько основных направлений использования для получения практических результатов.
Гальваническое покрытие
Тонкое, прочное гальваническое покрытие из металла можно наложить путем электролиза. Покрываемое изделие устанавливается в ванну в виде катода, а электролит содержит соль нужного металла. Так можно покрыть сталь цинком, хромом или оловом.

Электроочистка — рафинирование меди
Примером электроочистки может служить такой вариант: катод – чистая медь, анод – медь с примесями, электролит – водный раствор медного сульфата. Медь из анода переходит в ионы и оседает в катоде уже без примесей.

Добыча металлов
Для получения металлов из солей они переводятся в расплав, а затем обеспечивается электролиз в нем. Достаточно эффективен такой способ для получения алюминия из бокситов, натрия и калия.

Анодирование
При этом процессе покрытие выполняется из неметаллических соединений. Классический пример – анодирование алюминия. Алюминиевая деталь устанавливается, как анод. Электролит – раствор серной кислоты. В результате электролиза на аноде оседает слой из оксида алюминия, обладающего защитными и декоративными свойствами. Указанные технологии широко используются в различных отраслях промышленности. Можно осуществить процессы и своими руками с соблюдением техники безопасности.
Энергетические затраты
Электролиз требует больших энергетических затрат. Процесс будет иметь практическую ценность при достаточной величине анодного тока, а для этого необходимо приложить значительный постоянный ток от источника электроэнергии. Кроме того, при его проведении возникают побочные потери напряжения – анодное и катодное перенапряжение, потери в электролите за счет его сопротивления. Эффективность работы установки определяется путем отнесения мощности энергозатрат к единице полезной массы полученного вещества.
Электролиз давно и с высокой эффективностью используется в промышленности. Анодированные и гальванические покрытия стали обычным явлением в повседневной жизни, а добыча и обогащение материалов помогает добывать многие металлы из руды. Процесс можно запланировать и рассчитать, зная основные его закономерности.
Электролиз водопроводной воды с использованием электродов из различных материалов.
Готовим раствор повареной соли в обычной водопроводной воде. Будем использовать три вида электродов — стальные (бритвенные лезвия), медные (жала для паяльника), алюминиевые (уголок). В качестве источника питания используем зарядное устройство для автомобильных аккумуляторов (12-14 вольт постоянного тока).
Первыми будут бритвенные лезвия. Анод сразу начинает растворяться с образованием чёрно-зелёных хлопьев гидроокиси двухвалентного железа. Соль в данном случае только увеличивает электропроводность раствора (облегчает отрыв ионов анода и его разрушение).
Вот что мы получаем за пару минут работы на хорошем постоянном токе. На переменке 220 разрушаются оба электрода, но процесс идёт куда медленнее за счёт того, что медленные тяжёлые ионы раствора не успевают «раскачиваться» под действием достаточно быстрой переменки, а так же из-за низкого содержания солей в используемой Горожанином воде, здесь мы воду посолили чтобы снизить её электрическое сопротивление и ускорить процесс.
Теперь объясним, почему данная каша меняет цвет и бывает разных цветов. Потому что состоит она (в основном) из неустойчивого гидроксида двухвалентного железа, который очень легко окисляется кислородом воздуха до рыже-бурого гидроксида трёхвалентного железа. Для увеличения площади контакта с кислородом выливаем смесь на тарелочку.
Как видим, при контакте с воздухом чёрно-зелёная смесь гидроокиси железа быстро становится рыже-бурой.
Медные.
Как обычно, один электрод худеет, другой толстеет. Недолетевшие до катода ионы меди образуют неустойчивые сложные комплексы, с течением времени так же меняющие цвет.
Алюминий.
Видим смесь бело-серой окиси/гидроокиси алюминия с разрушенного анода.
Вот результат. Как видим, со временем гидроокись железа меняет цвет от зелёного в сторону рыже-бурого. Напоминаю, что при проведении электролиза при слабом токе или на переменке характер уже содержащихся в воде солей даже в малых количествах (в природе) будет оказывать большее влияние на окраску образующихся комплексных соединений. Но основная масса полученных веществ — это продукты разрушения анода.
Магнитный электролиз — Магнитный ток
Дорогой друг:
Как вы, наверное, знаете, я большой поклонник Эдварда Лидскалнина из Coral Castle. Книга Эда называлась «Магнитные токи». Вы можете прочитать все об Эде в моей книге «Электричество — производи, а не покупай», доступной на сайте www.electricitybook.com —
также в прошлом информационном бюллетене, посвященном секретам Кораллового Замка. Вот очень интересная статья из старого выпуска Popular Science, которая усиливает и поддерживает теорию Эда о том, что существует такая вещь, как магнитный ток.Я считаю следующую статью «Магия магнетизма» очень интересной — особенно в свете сегодняшних поисков более эффективного способа получения дешевого водорода. Это магнитный электролиз? …
Магия с магнетизмом (Феликс Эренхафт)
Если этот экспериментатор прав, его открытие опровергнет все наши общепринятые представления об этой знакомой силе.
от Олдена П.Арманьяк (Popular Science, июнь 1944 г.) 
Может ли магнит разрывать воду на части?
Нет, говорят учебники физики. Да, говорит профессор Феликс Эренхафт, бывший директор Физического института Венского университета, который сейчас продолжает свои исследования в Нью-Йорке. Если он окажется прав, его выводы
в сфере магнетизма обещают такие широкие практические применения, как динамо-машины, двигатели, трансформаторы, телефоны и радио, которые возникли в результате фундаментальных исследований Фарадея в области электричества.
За свое «невозможно»
В эксперименте доктор Эренхафт использует простейший аппарат. Два блестящих стержня из чистого шведского железа, запечатанные в отверстиях с противоположных сторон U-образной трубы, напоминают знакомую старшеклассникам установку для разрушения.
вода превращается в водород и кислород, пропуская через нее электричество. И это именно то, что произошло бы, если бы доктор Эренхафт прикрепил электрические провода от батареи к стержням. Но он этого не делает.
Вместо этого,
он использует железные стержни как полюсные наконечники или «северный» и «южный» концы магнита — либо электромагнита, либо постоянного магнита.Пузырьки газа поднимаются через двойные столбы подкисленной воды, чтобы собираться и анализироваться.
Как и следовало ожидать, почти весь газ представляет собой водород, высвобождаемый обычным химическим взаимодействием между железными стержнями и разбавленной серной кислотой (один процент по объему) в воде. Но феноменальная часть
эксперимент состоит в том, что кислород тоже появляется, доктор.Эренхафт недавно сообщил Американскому физическому обществу. В частности, он присутствует в четко измеряемых пропорциях от 2 до 12 процентов от общего объема газов.
Когда газы, полученные с помощью постоянного магнита, разделяются, большая часть кислорода находится над северным полюсом магнита. После принятия строгих мер предосторожности, включая короткое замыкание полюсов магнита проволокой,
так что полюса будут иметь одинаковый электрический потенциал, — д-р.Эренхафт приходит к выводу, что кислород может поступать только из одного места. И это от воды, разложенной магнитом! Без магнита чистый водород
развивается. 
У этого эксперимента есть интересная сторона. Сильный постоянный магнит типа Alnico претерпевает заметную потерю прочности.
— скажем, 10 процентов за 24 часа — после использования для разложения воды, — замечает доктор Эренхафт. Фактически, производители магнитов, которые, как предполагается, будут служить годами без существенных изменений, поняли, что с ними происходит.
удивление и тревога.Но их продукция не виновата. Энергия от электрической батареи расходуется на разложение воды, и было бы разумно ожидать, что энергия, накопленная в постоянном магните, будет истощена.
аналогично.
Что придает огромное значение описанному подвигу по разделению воды с помощью магнита, так это свежие доказательства, которые он предлагает в пользу существования «магнитного тока» или потока магнитно заряженных частиц,
что подозревалось известными пионерами и которое д-р.Эренхафт теперь утверждает, что доказал. Подтверждение этого удивительного открытия укажет на возможного будущего конкурента электрического тока, которого, возможно, можно будет обуздать.
невероятными способами.
Излишне говорить, что научному миру потребуется много убедительных доказательств, поскольку выводы доктора Эренхафта категорически противоречат давно устоявшимся убеждениям. Как учат каждого школьника, магнит
имеет северный полюс и южный полюс. Разбейте его на две части молотком, и у каждой части будет свой северный и южный полюсы.Ни один закон не запрещает вам представить магнит только с одним полюсом, и эта идея пригодится в некоторых случаях.
электрические и радио расчеты. Но что касается фактов, у вас не может быть одного полюса без другого, полагал экспериментатор по имени Питер Перегринус, он продемонстрировал это к своему удовлетворению, используя грузоподъемный камень в течение года.
1269 г., и с тех пор преобладающее мнение поддерживает его. (Как мы теперь знаем, груз, который он плавал на платформе в воде, просто поворачивался до тех пор, пока его северный полюс не оказался напротив южного магнитного полюса Земли, и наоборот.Он не показал наблюдаемого превышения северного или южного магнетизма — и отсюда вывод, что они всегда были равны.)
Но верен ли изречение «никаких отдельных магнитных полюсов» в гораздо более деликатном
тест — скажем, если вы заменили микроскопические частицы железа или других магнитных металлов, столь же крошечные, как частицы дыма, на массивный кусок камня размером  , который использовал Перегрин? Доктор Эренхафт попробовал это.В воздушном зазоре между северным и южным полюсами магнита он создает то, что он называет однородным магнитным полем, то есть с абсолютно силовыми магнитными линиями.
, который использовал Перегрин? Доктор Эренхафт попробовал это.В воздушном зазоре между северным и южным полюсами магнита он создает то, что он называет однородным магнитным полем, то есть с абсолютно силовыми магнитными линиями.
параллельно. Он обнаружил, что в этом поле частицы металла движутся к северному или южному полюсу, меняя свое направление в зависимости от направления магнитного поля. На частицах, заключает он, должен быть избыток
северного или южного магнитного заряда. Расширяя терминологию Фарадея, он называет частицы магнитными ионами.Это одиночные магнитные полюса, показанные в правом нижнем углу цветного рисунка. Вместо того, чтобы нести плюс или минус
электрические заряды, как и знакомые ионы, несут северный или южный магнитные заряды.
Так же, как бегущие электрические ионы образуют электрический ток, почему бы бегущим магнитным ионам не образовывать магнитный ток? Смотрите для
вы еще один из поразительных экспериментов доктора Эренхафта и делайте собственные выводы.
На этот раз сердцем устройства будет небольшая стеклянная ячейка, как и прежде, снабженная полюсными наконечниками из чистого железа, которые погружаются в
вода, содержащая один процент серной кислоты.Электромагнит, включенный или выключенный по желанию, питает полюса. Из проектора мощный луч света сходится в узком зазоре между полюсными наконечниками и маломощный
микроскоп, установленный горизонтально, показывает, что там происходит. Добавление камеры обеспечивает постоянную запись.
Вы начинаете с выключенным Магнитом. Глядя в окуляр микроскопа, вы видите потоки пузырьков.
поднимаясь от обоих полюсов. Они представляют собой газообразный водород, выделяющийся в результате того же химического воздействия, что и в первом эксперименте.
Бросьте выключатель, который включает магнит, и сцена резко изменится. Остановился мертвым в своих
следы, некоторые пузыри цепляются за полюсы. Другие покидают один полюс и переходят на другой. Доктор Эренхафт обращает особое внимание на пузырьки, движущиеся вниз вопреки их собственной плавучести под действием какой-то невидимой силы.
сильнее гравитации.
Тем временем развивается эффектное явление — миниатюрная карусель газовых пузырей между гранями полюсов и параллельно им.Невозможно адекватно показать в
Тем не менее, при временной выдержке эффект явно проявляется в виде белого размытия, когда верхнему магнитному полюсу для фотографических целей придается коническая форма. Визуальное наблюдение показывает поразительные детали. Если частицы меди, скажем,
были добавлены в подкисленную воду, они будут вращаться в той же плоскости, что и пузырьки водорода, но в противоположном направлении. Для обоих скорость завихрения зависит от силы магнитного поля.Обеспечить регресс
полярность магнита, и каждый набор частиц вращается в противоположном направлении.
Это не теории с безумными глазами, а совершенно очевидные факты. Любой скептически настроенный физик получит постоянное приглашение увидеть их
собственными глазами в лаборатории доктора Эренхафта, предоставленной в его распоряжение в квартале Нью-Йорка известной оптической фирмы Carl Zeiss. Как объяснить этот феномен остается проблемой для науки, если только д-р.Эренхафта
выводы должны быть приняты. Посмотрите, как аккуратно они проводят аналогию между хорошо известными электрическими эффектами и новыми магнитными эффектами:
Пузыри или частицы, которые перемещаются между полюсными наконечниками магнита, ведут себя
точно так же, как если бы они были магнитными ионами или их скоплениями, отталкиваемыми одинаковыми магнитными полюсами и притягиваемыми противоположно намагниченными полюсами. Это в точности соответствует тому, как «электрические» или обычные ионы взаимодействуют с положительными
и отрицательные электроды.Что касается розового цвета пузырьков водорода и частиц меди, доктор Эренхафт заключает, что это электрически заряженные частицы — обычные ионы — вращающиеся вокруг магнитного поля.
текущий. Это будет точным аналогом классической концепции, согласно которой магнетизм вращается вокруг проводника с током.
Теперь начинают разворачиваться ошеломляющие последствия наблюдений доктора Эренхафта.
Существование такой вещи, как магнитный ток, однажды установленное, проложит путь для таких гигантских отраслей, как те, к которым в свое время привело открытие электричества.«Золотая лихорадка» для практических приложений может быть
ожидается. Патенты на них будут стоить баснословных сумм, поскольку изобретения, использующие магнитный ток, будут основными.
Какую форму они могут принять, никто не может предвидеть, и доктор Эренхафт осторожно отказывается делать предположения.
Однако посетитель его лаборатории не может устоять перед искушением дать волю своему воображению. Новые виды двигателей и генераторов? Лучшие способы передачи энергии? Трансформаторы, которые будут работать на постоянном токе вместо переменного
текущий? Атомные сокрушители? Радикальные методы видеть вещи в темноте, через микроскопы и телескопы? Как извлечь энергию из магнетизма самой земли? А у вас дома замена магнитного тока — кто
когда-нибудь испытывал от этого шок? — для электрического тока? Чистые мечты, все они, сегодня — но некоторые из них, возможно, реалии 2044 года.
Прежде чем можно было обуздать магнитные токи, конечно, возникало множество вопросов о
их поведение еще предстоит изучить и ответить. Пока никто не знает, можно ли их проводить по проводам, например по электрическим токам, а также по проводящим жидкостям. Если да, то провода могут быть из совершенно разных материалов.
чем лучшие проводники по электричеству. Точно так же самые эффективные изоляторы для магнитного тока могут быть веществами, совершенно непохожими на те, которые используются для электрических изоляторов.Вся эта тема предлагает огромное поле для новаторства.
как электричество сто лет назад. И теперь, как и тогда, экспериментатор-любитель, возившийся у себя в подвале, имеет такой же шанс сделать эпохальное открытие, как и выдающиеся ученые в большой лаборатории.
С уважением,
Билл Андерсон
.
Определение, процесс, применение, электролиз воды
- БЕСПЛАТНАЯ ЗАПИСЬ КЛАСС
- КОНКУРСНЫЕ ЭКЗАМЕНА
- BNAT
- Классы
- Класс 1-3
- Класс 4-5
- Класс 6-10
- Класс 110003 CBSE
- Книги NCERT
- Книги NCERT для класса 5
- Книги NCERT, класс 6
- Книги NCERT для класса 7
- Книги NCERT для класса 8
- Книги NCERT для класса 9
- Книги NCERT для класса 10
- NCERT Книги для класса 11
- NCERT Книги для класса 12
- NCERT Exemplar
- NCERT Exemplar Class 8
- NCERT Exemplar Class 9
- NCERT Exemplar Class 10
- NCERT Exemplar Class 11
9plar
- RS Aggarwal
- RS Aggarwal Решения класса 12
- RS Aggarwal Class 11 Solutions
- RS Aggarwal Решения класса 10
- Решения RS Aggarwal класса 9
- Решения RS Aggarwal класса 8
- Решения RS Aggarwal класса 7
- Решения RS Aggarwal класса 6
- RD Sharma
- RD Sharma Class 6 Решения
- RD Sharma Class 7 Решения
- Решения RD Sharma класса 8
- Решения RD Sharma класса 9
- Решения RD Sharma класса 10
- Решения RD Sharma класса 11
- Решения RD Sharma Class 12
- PHYSICS
- Механика
- Оптика
- Термодинамика
- Электромагнетизм
- ХИМИЯ
- Органическая химия
- Неорганическая химия
- Периодическая таблица
- MATHS
- Статистика
- 9000 Pro Числа
- Числа
- 9000 Pro Числа Тр Игонометрические функции
- Взаимосвязи и функции
- Последовательности и серии
- Таблицы умножения
- Детерминанты и матрицы
- Прибыль и убытки
- Полиномиальные уравнения
- Деление фракций
- Microology
- 0003000
- Книги NCERT
- FORMULAS
- Математические формулы
- Алгебраические формулы
- Тригонометрические формулы
- Геометрические формулы
- КАЛЬКУЛЯТОРЫ
- Математические калькуляторы
- 0003000
- 000 Калькуляторы
- 000 Физические модели 900 Образцы документов для класса 6
- Образцы документов CBSE для класса 7
- Образцы документов CBSE для класса 8
- Образцы документов CBSE для класса 9
- Образцы документов CBSE для класса 10
- Образцы документов CBSE для класса 1 1
- Образцы документов CBSE для класса 12
- Вопросники предыдущего года CBSE
- Вопросники предыдущего года CBSE, класс 10
- Вопросники предыдущего года CBSE, класс 12
- HC Verma Solutions
- HC Verma Solutions Класс 11 Физика
- HC Verma Solutions Класс 12 Физика
- Решения Лакмира Сингха
- Решения Лахмира Сингха класса 9
- Решения Лахмира Сингха класса 10
- Решения Лакмира Сингха класса 8
9000 Класс
9000BSE 9000 Примечания3 2 6 Примечания CBSE
- Примечания CBSE класса 7
- Примечания CBSE класса 8
- Примечания CBSE класса 9
- Примечания CBSE класса 10
- Примечания CBSE класса 11
- Примечания 12 CBSE
Примечания
- Дополнительные вопросы по математике класса 8 CBSE
- Дополнительные вопросы по науке 8 класса CBSE
- Дополнительные вопросы по математике класса 9 CBSE
- Дополнительные вопросы по математике класса 9 CBSE Вопросы
- CBSE Class 10 Дополнительные вопросы по математике
- CBSE Class 10 Science Extra questions
- Class 3
- Class 4
- Class 5
- Class 6
- Class 7
- Class 8 Класс 9
- Класс 10
- Класс 11
- Класс 12
- Решения NCERT для класса 11
- Решения NCERT для класса 11 по физике
- Решения NCERT для класса 11 Химия
- Решения NCERT для биологии класса 11
- Решение NCERT s Для класса 11 по математике
- NCERT Solutions Class 11 Accountancy
- NCERT Solutions Class 11 Business Studies
- NCERT Solutions Class 11 Economics
- NCERT Solutions Class 11 Statistics
- NCERT Solutions Class 11 Commerce
- NCERT Solutions for Class 12
- Решения NCERT для физики класса 12
- Решения NCERT для химии класса 12
- Решения NCERT для биологии класса 12
- Решения NCERT для математики класса 12
- Решения NCERT, класс 12, бухгалтерия
- Решения NCERT, класс 12, бизнес-исследования
- NCERT Solutions Class 12 Economics
- NCERT Solutions Class 12 Accountancy Part 1
- NCERT Solutions Class 12 Accountancy Part 2
- NCERT Solutions Class 12 Micro-Economics
- NCERT Solutions Class 12 Commerce
- NCERT Solutions Class 12 Macro-Economics
- NCERT Solut Ионы Для класса 4
- Решения NCERT для математики класса 4
- Решения NCERT для класса 4 EVS
- Решения NCERT для класса 5
- Решения NCERT для математики класса 5
- Решения NCERT для класса 5 EVS
- Решения NCERT для класса 6
- Решения NCERT для математики класса 6
- Решения NCERT для науки класса 6
- Решения NCERT для класса 6 по социальным наукам
- Решения NCERT для класса 6 Английский язык
- Решения NCERT для класса 7
- Решения NCERT для математики класса 7
- Решения NCERT для науки класса 7
- Решения NCERT для социальных наук класса 7
- Решения NCERT для класса 7 Английский язык
- Решения NCERT для класса 8
- Решения NCERT для математики класса 8
- Решения NCERT для науки 8 класса
- Решения NCERT для социальных наук 8 класса ce
- Решения NCERT для класса 8 Английский
- Решения NCERT для класса 9
- Решения NCERT для класса 9 по социальным наукам
- Решения NCERT для математики класса 9
- Решения NCERT для математики класса 9 Глава 1
- Решения NCERT для математики класса 9, глава 2
- для математики класса 9, глава 3
- Решения NCERT для математики класса 9, глава 4
- Решения NCERT для математики класса 9, глава 5
- для математики класса 9, глава 6
- Решения NCERT для математики класса 9, глава 7
- для математики класса 9, глава 8
- Решения NCERT для математики класса 9, глава 9
- Решения NCERT для математики класса 9, глава 10
- для математики класса 9, глава 11
- NCERT для математики класса 9 Глава 12
- для математики класса 9 Глава 13
- NCER Решения T для математики класса 9 Глава 14
- Решения NCERT для математики класса 9 Глава 15
Решения NCERT
Решения NCERT
Решения NCERT
Решения NCERT
Решения
Решения NCERT
- Решения NCERT для науки класса 9
- Решения NCERT для науки класса 9 Глава 1
- Решения NCERT для науки класса 9 Глава 2
- Решения NCERT для науки класса 9 Глава 3
- Решения NCERT для науки класса 9 Глава 4
- Решения NCERT для науки класса 9 Глава 5
- Решения NCERT для науки класса 9 Глава 6
- Решения NCERT для науки класса 9 Глава 7
- Решения NCERT для науки класса 9 Глава 8
- Решения NCERT для науки класса 9 Глава 9
- Решения NCERT для науки класса 9 Глава 10
- Решения NCERT для науки класса 9 Глава 12
- Решения NCERT для науки класса 9 Глава 11
- Решения NCERT для науки класса 9 Глава 13
- для науки класса 9 Глава 14
- Решения NCERT для класса 9 по науке Глава 15
Решения NCERT
- Решения NCERT для класса 10
- Решения NCERT для класса 10 по социальным наукам
- Решения NCERT для математики класса 10
- Решения NCERT для класса 10 по математике Глава 1
- Решения NCERT для математики класса 10, глава 2
- Решения NCERT для математики класса 10, глава 3
- Решения NCERT для математики класса 10, глава 4
- Решения NCERT для математики класса 10, глава 5
- Решения NCERT для математики класса 10, глава 6
- Решения NCERT для математики класса 10, глава 7
- Решения NCERT для математики класса 10, глава 8
- Решения NCERT для математики класса 10, глава 9
- Решения NCERT для математики класса 10, глава 10
- Решения NCERT для математики класса 10 Глава 11
- Решения NCERT для математики класса 10 Глава 12
- Решения NCERT для математики класса 10 Глава ter 13
- Решения NCERT для математики класса 10 Глава 14
- Решения NCERT для математики класса 10 Глава 15
- Решения NCERT для науки класса 10
- Решения NCERT для класса 10 науки Глава 1
- Решения NCERT для класса 10 Наука, глава 2
- Решения NCERT для класса 10, глава 3
- Решения NCERT для класса 10, глава 4
- Решения NCERT для класса 10, глава 5
- Решения NCERT для класса 10, глава 6
- Решения NCERT для класса 10 Наука, глава 7
- Решения NCERT для класса 10, глава 8
- Решения NCERT для класса 10, глава 9
- Решения NCERT для класса 10, глава 10
- Решения NCERT для класса 10, глава 11
- Решения NCERT для класса 10 Наука Глава 12
- Решения NCERT для класса 10 Наука Глава 13
- NCERT S Решения для класса 10 по науке Глава 14
- Решения NCERT для класса 10 по науке Глава 15
- Решения NCERT для класса 10 по науке Глава 16
- Программа NCERT
- NCERT
- Class 11 Commerce Syllabus
- Учебный план класса 11
- Учебный план класса 11
- Учебный план экономического факультета 11
- Учебный план по коммерции класса 12
- Учебный план класса 12
- Учебный план класса 12
- Учебный план
- Класс 12 Образцы документов для торговли
- Образцы документов для предприятий класса 11
- Образцы документов для коммерческих предприятий класса 12
- TS Grewal Solutions
- TS Grewal Solutions Class 12 Accountancy
- TS Grewal Solutions Class 11 Accountancy
- Отчет о движении денежных средств 9 0004
- Что такое предпринимательство
- Защита прав потребителей
- Что такое основные средства
- Что такое баланс
- Что такое фискальный дефицит
- Что такое акции
- Разница между продажами и маркетингом
9100003
- ICC
- Образцы документов ICSE
- Вопросы ICSE
- ML Aggarwal Solutions
- ML Aggarwal Solutions Class 10 Maths
- ML Aggarwal Solutions Class 9 Maths
- ML Aggarwal Solutions Class 8 Maths
- ML Aggarwal Solutions Class 7 Maths Решения Математика класса 6
- Решения Селины
- Решения Селины для класса 8
- Решения Селины для класса 10
- Решение Селины для класса 9
- Решения Фрэнка
- Решения Фрэнка для математики класса 10
- Франк Решения для математики 9 класса
9000 4
- ICSE Class
- ICSE Class 6
- ICSE Class 7
- ICSE Class 8
- ICSE Class 9
- ICSE Class 10
- ISC Class 11
- ISC Class 12
- 900 Экзамен IAS
- Пробный тест IAS 2019 1
- Пробный тест IAS4
2
- Экзамен KPSC KAS
- Экзамен UPPSC PCS
- Экзамен MPSC
- Экзамен RPSC RAS
- TNPSC Group 1
- APPSC Group 1
- Экзамен BPSC
- Экзамен WPSC
- Экзамен JPSC
- Экзамен GPSC
- Ответный ключ UPSC 2019
- Коучинг IAS Бангалор
- Коучинг IAS Дели
- Коучинг IAS Ченнаи
- Коучинг IAS Хайдарабад
- Коучинг IAS Мумбаи
9000 JEE 9000 JEE 9000 Advanced
- Программа BYJU NEET
- NEET 2020
- NEET Eligibility
- NEET Eligibility
- NEET Eligibility 2020 Подготовка
- NEET Syllabus
- Support
- Разрешение жалоб
- Служба поддержки
- Центр поддержки
- GSEB
- GSEB Syllabus
GSEB Образец
003 GSEB Books
- MSBSHSE Syllabus
- MSBSHSE Учебники
- MSBSHSE Образцы статей
- MSBSHSE Вопросы
- 9000
- AP 2 Year Syllabus
- MP Board Syllabus
- MP Board Образцы документов
- MP Board Учебники
- Assam Board Syllabus
- Assam Board
- Assam Board
- Assam Board Документы
- Bihar Board Syllabus
- Bihar Board Учебники
- Bihar Board Question Papers
- Bihar Board Model Papers
- Odisha Board
- Odisha Board
- Odisha Board 9000
- ПСЕБ 9 0002
- PSEB Syllabus
- PSEB Учебники
- PSEB Вопросы и ответы
- RBSE
- Rajasthan Board Syllabus
- RBSE Учебники
- RBSE
- RBSE
- 000 HPOSE
- 000
- 000
- 000
000 HPOSE
000 HPOSE
000 HPOSE
000
0003 Контрольные документы
- JKBOSE Syllabus
- JKBOSE Образцы документов
- Экзаменационные образцы JKBOSE
900 .
электрического заряда | Свойства, примеры, единицы измерения и факты
Электрический заряд , основное свойство материи, переносимой некоторыми элементарными частицами, которое определяет, как на частицы влияет электрическое или магнитное поле. Электрический заряд, который может быть положительным или отрицательным, возникает в дискретных естественных единицах и не создается и не разрушается.
Подробнее по этой теме
гроза: электрификация грозы
В пределах одной грозы есть восходящие и нисходящие потоки, а также различные частицы облаков и осадки.Измерения показывают, что …
Электрические заряды бывают двух основных типов: положительные и отрицательные. Два объекта, у которых есть избыток заряда одного типа, оказывают друг на друга силу отталкивания, когда находятся относительно близко друг к другу. Два объекта с избыточными противоположными зарядами, один положительно заряженный, а другой отрицательно заряженный, притягиваются друг к другу, когда они относительно близко. ( См. Кулоновская сила.)
Многие фундаментальные, или субатомные, частицы материи обладают свойством электрического заряда.Например, электроны имеют отрицательный заряд, а протоны имеют положительный заряд, а нейтроны имеют нулевой заряд. Экспериментально установлено, что отрицательный заряд каждого электрона имеет одинаковую величину, которая также равна положительному заряду каждого протона. Таким образом, заряд существует в естественных единицах, равных заряду электрона или протона, фундаментальной физической постоянной. Прямое и убедительное измерение заряда электрона как естественной единицы электрического заряда было впервые выполнено (1909 г.) в эксперименте Милликена с каплей масла.Атомы вещества электрически нейтральны, потому что их ядра содержат столько же протонов, сколько электронов, окружающих ядра. Электрический ток и заряженные объекты предполагают разделение части отрицательного заряда нейтральных атомов. Ток в металлических проводах состоит из дрейфа электронов, из которых один или два от каждого атома связаны более слабо, чем остальные. Некоторые атомы в поверхностном слое стеклянного стержня, положительно заряженные при протирании его шелковой тканью, потеряли электроны, оставив чистый положительный заряд из-за ненейтрализованных протонов их ядер.Отрицательно заряженный объект имеет избыток электронов на поверхности.
Милликен, эксперимент с каплей масла Между 1909 и 1910 годами американский физик Роберт Милликен провел серию экспериментов с каплями масла. Сравнивая приложенную электрическую силу с изменениями в движении масляных капель, он смог определить электрический заряд на каждой капле. Он обнаружил, что все капли имеют заряды, кратные одному числу — фундаментальному заряду электрона. Encyclopædia Britannica, Inc.
Электрический заряд сохраняется: в любой изолированной системе, в любой химической или ядерной реакции чистый электрический заряд постоянен. Алгебраическая сумма основных зарядов остается прежней. ( См. Сохранение заряда .)
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской.
Подпишитесь сегодня
Единицей электрического заряда в системах метр – килограмм – секунда и системе СИ является кулон и определяется как количество электрического заряда, протекающего через поперечное сечение проводника в электрической цепи в течение каждой секунды, когда ток имеет значение одного ампера.Один кулон состоит из 6,24 × 10 18 естественных единиц электрического заряда, таких как отдельные электроны или протоны. По определению ампера, сам электрон имеет отрицательный заряд 1,602176634 × 10 −19 кулонов.
Электрохимическая единица заряда, фарадей, полезна при описании реакций электролиза, например, при нанесении металлического гальванического покрытия. Один фарадей равен 96485,332123 кулонам, заряду моля электронов (то есть числу Авогадро, 6.02214076 × 10 23 , электронов).
.
Электролитическая ячейка | устройство | Britannica
Электролитическая ячейка , любое устройство, в котором электрическая энергия преобразуется в химическую энергию или наоборот. Такая ячейка обычно состоит из двух металлических или электронных проводников (электродов), расположенных отдельно друг от друга и находящихся в контакте с электролитом ( q.v.), обычно растворенным или конденсированным ионным соединением. При подключении электродов к источнику постоянного электрического тока один из них заряжается отрицательно, а другой — положительно.Положительные ионы в электролите мигрируют к отрицательному электроду (катоду) и там объединяются с одним или несколькими электронами, теряя часть или весь свой заряд и становясь новыми ионами, имеющими более низкий заряд или нейтральными атомами или молекулами; в то же время отрицательные ионы мигрируют к положительному электроду (аноду) и переносят на него один или несколько электронов, также становясь новыми ионами или нейтральными частицами. Общий эффект двух процессов — перенос электронов от отрицательных ионов к положительным ионам, химическая реакция ( см. реакция окисления-восстановления).Примером может служить электролиз хлорида натрия (поваренная соль) с образованием металлического натрия и газообразного хлора; энергия, необходимая для протекания реакции, обеспечивается за счет электрического тока. Другие распространенные применения электролиза включают электроосаждение для рафинирования или нанесения покрытия на металлы и производство каустической соды.
Британская викторина
Гаджеты и технологии: факт или вымысел?
Голограммы часто встречаются на кредитных картах.
В случае веществ, которые генерируют энергию, а не потребляют ее, когда они реагируют друг с другом, часть или вся эта энергия может быть преобразована в электричество, если реакцию можно разделить на окисление и восстановление, которое может быть превращено в электричество. возникают на отдельных электродах. В свинцово-кислотной аккумуляторной батарее, например, диоксид свинца, металлический свинец и серная кислота реагируют с образованием сульфата свинца и воды; отдельными процессами являются окисление свинца до сульфата свинца на одном электроде и восстановление диоксида свинца до сульфата свинца на другом, в то время как электрический заряд переносится через электролит за счет миграции ионов водорода.Эти процессы создают движущую силу (напряжение или электрический потенциал), которая заставляет электричество течь через внешнюю цепь, соединяющую два электрода. В элементах и батареях используются многие другие химические комбинации.
Другие элементы для выработки электричества средствами, отличными от движения проводника в магнитном поле, включают солнечные элементы, в которых поток электронов между полупроводниками возникает в результате поглощения света, и топливные элементы, в которых непрерывная подача жидкого или газообразного окислителя , такой как кислород, удаляет электроны с катода, поскольку восстановитель, такой как водород, подает электроны на анод.
.
