как устроены, виды, срок службы, принцип работы и хранение
Автор Aluarius На чтение 8 мин. Просмотров 647 Опубликовано
Литий-ионный аккумулятор – описание, история создания
Литий-ионный аккумулятор – источник тока, основанный на преобразовании химических реакций, происходящих внутри источника, в электрическую энергию. Данный тип батареи наиболее распространён в современной жизни, в большинстве своём из-за повсеместного использования в электронике: сотовых телефонах, цифровых фотоаппаратах, ноутбуках и так далее. Кроме этого, литиевые аккумуляторы ставят в электромобили.
Первое упоминание современных литиевых аккумуляторных батарей относится к 70-м годам XX века и связано с именем Майкла Стэнли Уиттингема. Будучи химиком в нефтяной компании «Exon», он создал источник тока, в котором в качестве анода использовался сульфид титана, а катод был литиевым. Первая батарея обладала напряжением 2,3 Вольт и способностью перезаряжаться, однако была пожароопасной и ядовитой. При взрыве, который мог случиться внезапно, литий вступал в контакт с воздухом и горел, а дисфульд титана выделял сероводород, вдыхание которого как минимум неприятно. Помимо этого, титан обладает и всегда обладал высокой стоимостью, и из-за всех этих факторов проект Уиттенгема был закрыт.
Первая батарея обладала напряжением 2,3 Вольт и способностью перезаряжаться, однако была пожароопасной и ядовитой. При взрыве, который мог случиться внезапно, литий вступал в контакт с воздухом и горел, а дисфульд титана выделял сероводород, вдыхание которого как минимум неприятно. Помимо этого, титан обладает и всегда обладал высокой стоимостью, и из-за всех этих факторов проект Уиттенгема был закрыт.
Литий-ионная батарея, несмотря на свои недостатки, казалась достаточно привлекательной для продолжения развития, однако требовалась замена анодного материала, чем в 1978 году занялся Джон Гуденаф. Спустя некоторое время он обнаружил, что кобальтит лития (оксид лития-кобальта) обладает лучшими характеристиками, касающимися безопасности использования, а также напряжением, достигающим 4 Вольта. Однако использование лития в качестве катодного материала становилось причиной короткого замыкания аккумулятора. В 1980 году Рашид Язами указал на графит и назвал его наиболее подходящим в качестве анода материалом.
Однако потребовалось ещё одиннадцать лет, чтобы созданная и усовершенствованная батарея появилась в продаже под брендом компании «Sony».
СПРАВКА: Разработчик коммерческой версии аккумулятора Акиро Ёсино, а также Уиттенгем и Гуденаф в 2019 году получили Нобелевскую премию в области химии за равноценный вклад в создание литиево ионных аккумуляторов.
Принцип действия
Работа литионных аккумуляторов основана на электрохимическом потенциале, суть которого заключается в способности металлов отдавать отрицательные заряды. При подключении электрической цепи на аноде источника тока происходит химическая реакция, сопровождаемая образованием на его поверхности свободных электронов. По законам физики освобождённые электроны стремятся к положительной стороне – катоду, чтобы восстановить баланс, однако от движения их удерживает электролит, находящийся между анодом и катодом. Тем самым отрицательные заряды вынуждены двигаться к положительным «в обход» – через всю электрическую цепь, создавая ток.
Положительные ионы, образовавшиеся на стороне анода после «побега» электронов, проходят через электролит к катоду, чтобы удовлетворить потребность в отрицательных зарядах. В момент, когда все электроны переместятся на отрицательный электрод, аккумулятор будет разряжен.
Процесс зарядки запускает электрическую энергию в цепь, тем самым запуская в батарее обратную реакцию – скопление электронов на аноде. После полного перезаряда батарейки её можно заново подключать к цепи.
ВНИМАНИЕ: даже находясь в режиме ожидания, аккумуляторы теряют часть заряда. При этом они обладают такой характеристикой как старение – постепенно приходящая неспособность удерживать первоначальное количество заряда.
Устройство li-ion аккумулятора
В li-ion аккумуляторах в качестве отрицательного электрода служит алюминиевая фольга с нанесённым поверх слоем оксида лития. Анодом выступает медная фольга, и на её поверхность наносится графит. Между электродами располагается пористый разделитель, пропитанный электролитом.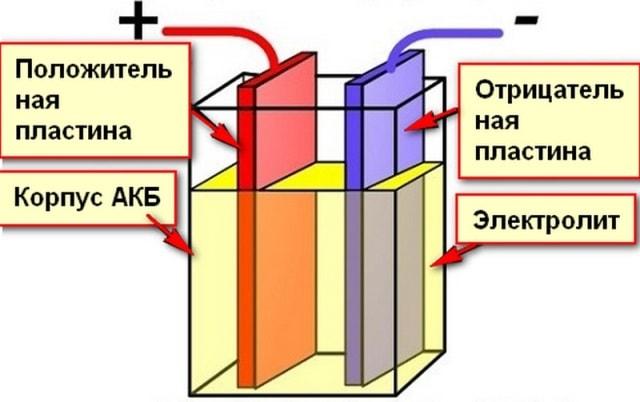 Все компоненты ради уменьшения занимаемого ими объёма сворачиваются в цилиндр или в пакет и помещаются в полностью герметичный корпус. При этом анод и катод присоединяются к токоснимающим клеммам. Герметичность конструкции обуславливается недопустимостью вытекания электролита. Кроме этого нельзя, чтобы внутрь батареи попали пары воды или кислорода, иначе произойдёт реакция между попавшим веществом и электролитом или электродами, и аккумулятор выйдет из строя.
Все компоненты ради уменьшения занимаемого ими объёма сворачиваются в цилиндр или в пакет и помещаются в полностью герметичный корпус. При этом анод и катод присоединяются к токоснимающим клеммам. Герметичность конструкции обуславливается недопустимостью вытекания электролита. Кроме этого нельзя, чтобы внутрь батареи попали пары воды или кислорода, иначе произойдёт реакция между попавшим веществом и электролитом или электродами, и аккумулятор выйдет из строя.
В батарейку в соображениях безопасности могут быть включены специальные элементы. Например, устройство, которое увеличит сопротивление аккумулятора при положительном температурном коэффициенте. А также устройство, которое в случае превышения давления газа допустимых значений разорвёт связь между катодом и положительной клеммой. Иногда корпус батареи может быть оснащён клапаном предохранения, основной задачей которого является сброс внутреннего давления в случае аварийной ситуации или нарушения эксплуатационных условий.
Некоторые особо важные источники таки могут обладать внешней электронной защитой, которая не позволяет перегреть или перезарядить батарейку, а также исключает возможность короткого замыкания.
По форме корпуса li-ion аккумуляторы делятся на цилиндрические и призматические, первые из которых изготавливаются путём сворачивания слоёв, из которых состоит батарея. Призматический тип аккумулятора li-ion, численно превосходящий из-за применения в ноутбуках и мобильных телефонах, создаётся путём плотного складывания пластин друг на друга.
Характеристики литиевых аккумуляторов
ИНТЕРЕСНО: собственные удельные характеристики обеспечили описываемым батареям лидирующие позиции среди всех выпускаемых химических источников тока.
Рабочее напряжение
Минимальное значение напряжения составляет 2,2-2,5 Вольт, а максимальное не превышает 4,25-4,35 Вольт. На данную характеристику в значительной степени влияет материал, используемый для электродов.
Ёмкость
На свойство батареи хранить заряд непосредственно влияет ток и температура, которая возникает при разряде. Вообще максимальная ёмкость аккумуляторов варьируется в широком диапазоне и зависит от типоразмера. Например, в наиболее распространённой батарее 18650 ёмкость обычно находится в пределах от 1000 до 3600 миллиампер-час.
СПРАВКА: 14500 аккумулятор, размеры которого сопоставимы с пальчиковой батарейкой (АА), также популярен среди пользователей и обладает номинальной ёмкостью 900 микроампер-час.
В общем, под ёмкостью подразумевается количество ионов лития, способных достигнуть анода или катода. Со временем после многочисленных зарядок электроды теряют свои свойства и могут вместить всё меньшее число зарядов, а аккумулятор тем временем не способен удерживать прежнее их количество. В результате батарея устаревает и постепенно утрачивает основополагающую функцию.
Рабочая температура
Предельные значения температуры находятся в диапазоне от -20°С до +50°С, однако работать в пограничных режимах аккумулятор долго не сможет, это скажется на его способности запасать энергию. Оптимальная температура для функционирования составляет примерно 20°С, а лучшие значения для хранения – от 0 до 10°С. При этом уровень заряда 30-50% считается наиболее щадящим для ёмкости при длительном хранении.
Оптимальная температура для функционирования составляет примерно 20°С, а лучшие значения для хранения – от 0 до 10°С. При этом уровень заряда 30-50% считается наиболее щадящим для ёмкости при длительном хранении.
ВНИМАНИЕ: если температура упадёт до +4°С объём вырабатываемой батареей энергии уменьшится на 5-7% в соответствии с максимальным значением. Более низкие значения приведут к потери 40-50% ёмкости и преждевременному исчерпанию ресурса.
Саморазряд
Данная характеристика варьируется от 6% до 10% в год.
Количество циклов заряд-разряд
Батарея литиевая не имеет эффекта памяти, а срок её годности рассчитан в зависимости от количества циклов полной разрядки.
| Процент оставшегося заряда, % | Количество циклов зарядки |
| 500 | |
| 50 | 1500 |
| 75 | 2500 |
| 90 | 4700 |
Так, для увеличения срока службы аккумулятора стоит чаще его заряжать.
Разновидности аккумуляторов
Наиболее распространены следующие виды литий-ионных батарей:
- Литий-кобальтовая. Популярный тип в ноутбуках, смартфонах и цифровых камерах. В состав входит катод из кобальтового оксида и графитовый анод. К преимуществам относят высокий показатель удельной энергоёмкости, а к недостаткам: низкий срок годности, ограниченную нагрузку и невысокую термическую стабильность.
- Литий-маргенцевая. Основная область применения – электроинструменты, медицинское оборудование и электрические силовые устройства. Катод представляет собой литий-марганцевую шпинель, обеспечивающей низкое сопротивление.
- Литий-никель-марганец-кобальт-оксидная. Сочетание металлов, входящих в состав, позволяет использовать сильные стороны каждого элемента. Применяется как в частных областях, так и в более крупных – промышленных, например, в системах безопасности и аварийного освещения.
- Литий-железно-фосфатная. Популярный вариант для стационарных специализированных устройств.
 К преимуществам относят стойкость к неправильным условиям эксплуатации, высокую безопасность и термическую стабильность, а к минусам причисляют малое значение ёмкости.
К преимуществам относят стойкость к неправильным условиям эксплуатации, высокую безопасность и термическую стабильность, а к минусам причисляют малое значение ёмкости. - Литий-никель-кобальт-алюминий-оксидная. Дороговизна оправдывается долговечностью и хорошими показателями энергоёмкости. Используют в промышленных целях и медицинском оборудовании.
- Литий-титановая. Можно встретить в сфере уличного освещения и автомобильных агрегатах. Дорогие и обладают низкой удельной энергоёмкостью, однако имеют долгий срок годности, работают в широком температурном диапазоне, производительны и безопасны.
Особенности хранения и утилизации
Хранить li-ion аккумуляторы необходимо в следующих условиях:
- Место хранения должно быть сухим и прохладным, причём батарейку следует предварительно извлечь из оборудования.
- Оптимальная температура должна находиться в диапазоне от +1°С до +25°С. При этом допускается хранение в холодильнике, но сначала аккумулятор нужно обернуть непромокаемым и не пропускающим влагу материалом.

- Заряд батарейки следует сохранить в районе 40%, это позволит избежать падения напряжения при саморазряде ниже допустимого.
После окончания срока годности использованный аккумулятор нужно сдать на переработку или утилизацию, причём этими вопросами занимаются специализированные службы, занимающиеся приёмом батарей.
Обычно процедура переработки включает в себя несколько этапов:
- Разбор корпуса.
- Избавление от электролита путём слива.
- Очищение электродов.
- Переработка корпуса и переплавление металлов.
ВАЖНО: литиевые батареи нельзя выбрасывать, как обычный мусор! Для их утилизации необходимо обращаться в специальные пункты сдачи.
Существует несколько способов для определения мест сбора использованных источников тока:
- Проект RecycleMap от «Гринпис», позволяющий после выбора и объекта утилизации города найти пункты приёма.
- Городской сайт администрации. На случай, если регион тщательно следит за подобным процессом.

- Сайты с объявлениями. Частные организации и подрядчики выкладывают в интернет информацию о сборе батарей.
- Магазины бытовой техники или крупные гипермаркеты. В последнее время в подобных местах стали появляться специальные контейнеры, куда можно выбросить неработающие батарейки.
Отличие аккумуляторов Li-ion от Ni-Cd аккумуляторов
Ёмкость литий-ионных источников тока значительно выше, чем тот же показатель у никель-кадмиевых аккумуляторов, вследствие чего требуется много меньшая по весу и габаритам батарея, чтобы обеспечить одно и то же время работы.
Также в процессе хранения ввиду низкой скорости саморазряда li-ion аккумуляторы разряжаются меньше, чем другие типы, и они более терпимы к постоянной зарядке, даже если заряд батареи не обнулён.
В плане экологичности рассматриваемые батарейки меньше вредят окружающей среде, чем никель-кадмиевые, как при изготовлении, так и в использовании материалов.
Однако по отношению к Ni-Cd аккумуляторами в литий-ионных используют более дорогостоящие технологии.
плюсы и минусы, срок службы, маркировка и обслуживание
Автор Aluarius На чтение 9 мин. Просмотров 336 Опубликовано
Что такое гелевый аккумулятор
Гелевый аккумулятор – это свинцово-кислотный источник питания, в котором электролит между пластинами находится в абсорбированном, гелевом состоянии. В гелевом аккумуляторе электролит загущен силикагелем.
Такие аккумуляторы чрезвычайно прочны и универсальны. Аккумуляторы этого типа выделяют мало дыма и могут использоваться в местах, где отсутствует достаточная вентиляция.
Устройство и принцип работы
И гелевые, и AGM-технологии основаны на концепции свинцово-кислотной технологии, которая была открыта еще в 1869 году. За все эти годы основная технология свинцово-кислотных систем практически не изменилась: электролит является кислотным, а пластины изготовлены из свинца.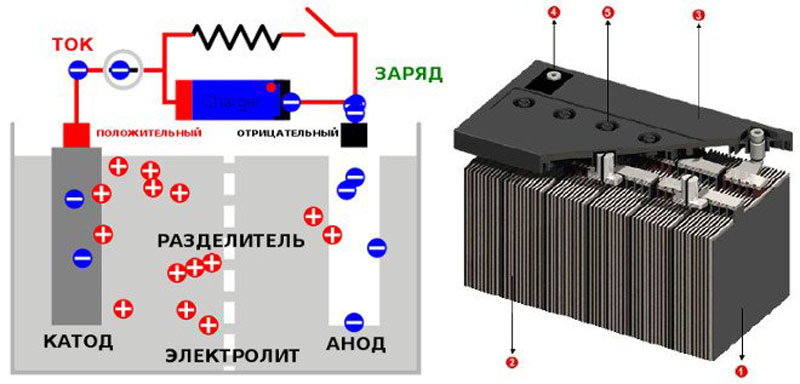
Справка! Когда они были впервые представлены, свинцово-кислотные батареи произвели революцию в концепции накопления энергии. Это были самые первые батареи с возможностью подзарядки. Хотя свинец был дорогим, базовая конструкция свинцово-кислотных батарей была пригодна для массового производства. Это позволило снизить расходы до уровня, доступного для многих приложений.
Использование тонких пластин означало, что его можно использовать для приложений, требующих сильных и быстрых скачков тока (пусковые электродвигатели в автомобилях), в то время как более толстая пластина делала его идеальным для применений с глубоким циклом (холодильники, силовое освещение и т. д.).
Разновидности аккумуляторов
Гелевые АКБ имеют тенденцию терять энергию быстрее, чем аккумуляторы AGM, особенно при более низких температурах. Это из-за гелеобразного тиксотропного состава батареи. Аккумуляторы AGM работают в экстремальных погодных условиях, что делает их пригодными для энергоемких зимних коммунальных служб, таких как снегоходы.
Когда дело доходит до глубины разряда (DoD), гелевые аккумуляторы используют кислоту лучше, чем аккумуляторы AGM. Кислота защищает пластины гелевых батарей, расширяя возможности их глубокого разряда. Тем не менее, гелевая батарея должна быть правильно заряжена, иначе это может привести к преждевременному выходу из строя. Шрам внутри желеобразного материала может создавать пакеты, которые разъедают пластины.
Каждый тип батареи имеет свое назначение и использование случай, так что давайте рассмотрим плюсы и минусы каждого.
В течение многих лет залитая свинцово-кислотная батарея была стандартом в солнечной промышленности. Этот тип батареи также используется в тележках для гольфа и вилочных погрузчиках. Они являются наиболее экономичными и долговечными из свинцово-кислотных аккумуляторов.
Герметичные свинцово-кислотные аккумуляторы
Герметичные свинцово-кислотные батареи очень похожи на затопленную версию, но нет доступа во внутренний отсек. Это означает, что вам не нужно добавлять дистиллированную воду. Электролит запечатан внутри, и его достаточно для того, чтобы аккумулятор проработал рассчитанное количество циклов.
Электролит запечатан внутри, и его достаточно для того, чтобы аккумулятор проработал рассчитанное количество циклов.
Маркировка
Стандартная маркировка аккумуляторов:
Характеристики гелевых аккумуляторов
Обе категории, относящиеся к герметичным свинцово-кислотным батареям , батарея AGM (абсорбирующее матовое стекло) и гелевая батарея, часто ошибочно принимают за одно и то же. Обе батареи обладают схожими характеристиками, такими как возможности глубокого цикла , неразрывная конструкция, и обе могут использоваться в разных ориентациях. Аккумуляторы двух типов также известны своими низкими саморазрядами, низкими эксплуатационными расходами и устойчивостью к вибрации. Тем не менее, AGM и гель являются двумя совершенно разными типами батарей.
Иногда вы видите, что они называются VRLA (свинцово-кислотные аккумуляторы с регулирующим клапаном), потому что они имеют небольшой клапан, позволяющий выходить из газов, которые возникают во время зарядки.
Абсорбирующие батарейки из матового стекла являются наиболее популярными батареями VRLA, поскольку они могут работать в самых разных условиях. Электролит подвешен в тонком стекловолоконном мате, который расположен между свинцовыми пластинами. Это позволяет аккумулятору быть устойчивым к вибрации, что делает их отличным выбором для RV и других мобильных приложений.
Гелевая аккумуляторная батарея также может быть установлена в любой ориентации. Обычно их устанавливают по бокам для удобного размещения и подключения.
Гелиевый АКБ стоит дороже, чем затопленные свинцово-кислботные аккумуляторы, и они не служат так же долго. Но за эту дополнительную цену вы получаете роскошь, когда вам не нужно обслуживать батареи или иметь дело с тем большим количеством газа, которое выделяется на этапе зарядки. ИБП отлично совместимы с подобного рода аккумуляторами.
Параметры
Гелевые аккумуляторы являются самыми дорогими из аккумуляторов VRLA, но являются отличными кандидатами для проектов, которые требуют очень медленного глубокого разряда. Они также служат дольше при более высоких температурах, так что вы можете выбрать их, если вас беспокоит высокая температура окружающей среды в помещении, где находятся батареи.
Они также служат дольше при более высоких температурах, так что вы можете выбрать их, если вас беспокоит высокая температура окружающей среды в помещении, где находятся батареи.
Люди часто принимают гель за AGM, и это может повлиять на срок службы батареи. Гелевые аккумуляторы являются наиболее чувствительными из аккумуляторов VRLA, и очень важно, чтобы в вашем приложении использовались правильные параметры зарядки, когда у вас есть гелевые аккумуляторы, которые могут состоять из разных типов геля.
Срок службы
При сюблюдении всех условий эксплуатации и норм обслуживания, срок годности будет равен 5-7 годам.
Сферы применения
Аккумуляторы AGM используют специальный стеклянный коврик из тонких стеклянных волокон. Это разработано, чтобы поглотить электролиты между пластинами батареи.
Гелевые аккумуляторы , с другой стороны, используют специальный тип силикагеля, который удерживает электролиты вместе. Густая консистенция материала позволяет электронам свободно вытекать из пластин.
В этом посте мы сравниваем два типа батарей, чтобы понять, какой из них соответствует вашим потребностям. Эти две батареи классифицируются как свинцово-кислотные батареи с регулирующим клапаном (VRLA). Кислород, образующийся на положительных пластинах свинцово-кислотных батарей, поглощается отрицательными пластинами. В свою очередь, отрицательные пластины производят воду. Это помогает исключить тепло от химической реакции, производимой электролитами . Из-за этого пользователю не нужно поливать эти батареи, что делает их необслуживаемыми.
Преимущества и недостатки гелевых аккумуляторов
Гелевые аккумуляторы дороже, чем другие типы свинцово-кислотных аккумуляторов, поэтому они не идеальны за пределами небольшого количества конкретных солнечных приложений (в основном, с очень жарким климатом). Технология затмила другие типы батарей, которые были разработаны совсем недавно.
Плюсы и минусы
Рассмотрим гелевый аккумулятор, его плюсы и минусы с точки зрения практической пользы:
Плюсы батарей:
- Лучше всего подходит для применений с глубоким циклом, и их срок службы обычно составляет от 500 до 5000 циклов
- Бесплатная поддержка
- Поэтому минимальная коррозия совместима с чувствительным электронным оборудованием
- Прочный и виброустойчивый
- Очень безопасно, так как меньше риск ожогов серной кислотой
- Самая низкая цена за месяц (стоимость / месяцы жизни)
- Самая низкая цена за цикл (стоимость / жизненные циклы)
Минусы:
- Высокая начальная стоимость
- В случае перезарядки вода не может быть пополнена.

- Требуются специальные зарядные устройства и регуляторы.
- Горячие температуры могут отрицательно повлиять на кислоту, она может сильно повредить гель и может соскользнуть с пластин.
Чем отличается от обычного, от других видов
Аккумуляторы VRLA выпускаются в двух разных версиях: аккумуляторы AGM и гелевые аккумуляторы. В гелевой батарее определенные элементы – часто специфические смеси кремния – добавляются в кислоту батареи, превращая электролит в гелеобразное вещество, которое не может вытекать. Путем «сверления» каналов в геле газообразный кислород перемещается из положительной пластины в отрицательную пластину. Здесь он сталкивается с газообразным водородом и рекомбинирует в воду, выделяя энергию. Гелевые аккумуляторы имеют отличную емкость, но слегка повышенная кислотостойкость делает их менее пригодными для использования в качестве стартовых аккумуляторов. Они обладают высокой устойчивостью к чрезмерно глубокому разряду, сохраняя функцию даже при разряде батареи до 20% от ее номинальной емкости.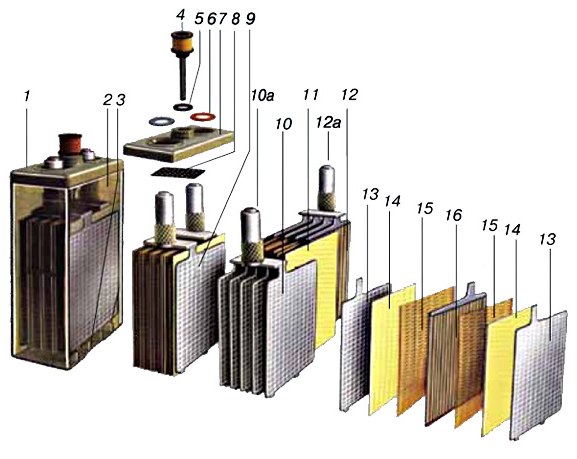
Обычный аккумулятор AGM сравнительно дешевле, чем gel аккумулятор но он имеет более длительный срок службы и при необходимости дает более мощный импульс. Эта батарея лучше всего работает в условиях высокой мощности, например, в спортивных автомобилях.
- Залитые свинцово-кислотные батареи являются наиболее экономически выгодным вариантом, но требуют регулярного технического обслуживания, когда герметичные свинцово-кислотные батареи (AGM и гель) стоят дороже, но не требуют регулярного технического обслуживания.
- Аккумуляторы AGM противостоят вибрации и могут выдерживать более высокие скорости зарядки / разрядки, а гелевые аккумуляторы могут выдерживать высокие температуры и лучше всего работают при медленном и глубоком разряде миносового контакта.
Аккумуляторы бывают разных форм и размеров. В солнечной промышленности для наших целей хорошо работают две батареи: свинцово-кислотные и литиевые, хоть они и могут существенно отличаться.
Как ведет себя при минусовых температурах
При низких (ниже 30 градусов) гель начинает хуже проводить ток и отдавать энергию. При резком нагреве может наблюдаться деструкция гелевой структуры, которая снижает срок службы аккумулятора.
Как обслуживать гелевый аккумулятор
Обслуживание гелевых аккумуляторов это восстановлению объема геля-электролита и заряда батареи. Несмотря на то, что поставщики не делают особенный упор на то, что в гелевых батареях происходит полная регенерация газов и они не поступают в атмосферу, утечка всё-таки присутствует. После использования батарею нужно правильно утилизировать.
Зарядное устройство
Хорошее зарядное устройство, допустим, Auto Welle AW05-1204, поддерживает заряд в несколько стадий, каждая из которых активируется в автоматическом режиме. Мультистудийный заряд позволяет держаться оптимальных параметров, которые зависят от заряда аккумулятора. Повышенная точность выходных параметров позвоялет обеспечить 100% заряд.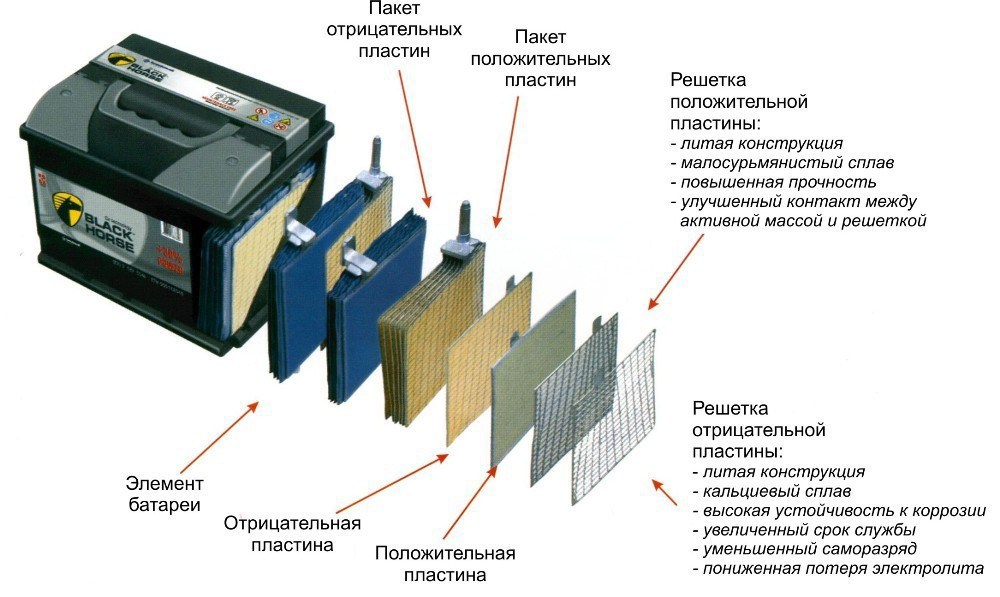 Простые ЗУ работают в 2-3 этапа, в дорогих приборах заряд может производится в 5 и больше этапов.
Простые ЗУ работают в 2-3 этапа, в дорогих приборах заряд может производится в 5 и больше этапов.
Особенности зарядки
Низкокачественная зарядка аккумулятора может нести для него опасность. Например, превышение тока зарядки может привести к “усыханию” аккумулятора. По стандарту, гелевые АКБ считаются самодостаточными (не обслуживаются), так как держат воду в своих капсулах. Тем не менее при повышенном токе заряда могут проходить испарения через клапаны защиты. Отработанный аккумулятор сильно теряет свои характеристики.
Проверка работоспособности
Рекомендуется выполнить тестовый запуск в объеме 30-40 процентов от планируемой нагрузки. Чтобы убедиться в рациональность выбора нагрузки для теста, лучше обратиться к инструкции и уточнить данные там.
Замена электролита
Замена электролита производится только в мастерских и профессиональных сервисных центрах. Самостоятельная замена, которая часто кажется пользователям легкой и незначительной, может окончиться взрывом аккумулятора и травмой.
Заключение
Аккумуляторы AGM превосходят типы гелей в отношении долговечности, долговечности и зарядки. Они также дешевле и работают в разных погодных условиях.
Гелевые батареи из-за их гелеобразного состава имеют меньший процент утечки по сравнению с батареями AGM.
принцип работы аккумуляторной батареи, устройство АКБ автомобиля, типы устройств
Независимые элементы питания сейчас стали одними из наиболее востребованных устройств, изобретённых людьми. Конструкция большинства гаджетов и их назначение часто предполагает отсутствие непрерывного доступа к электросети, поэтому и стали необходимыми такие устройства, как аккумуляторы. Они дают возможность пользоваться нужными приборами в любых требуемых условиях.
Что называют аккумулятором
Аккумулятором в самом общем значении этого понятия называется техническое приспособление, которое используется для накопления какого-либо вида энергии с целью её последующей равномерной отдачи в течение достаточно длительного периода времени (в отличие от конденсатора, который отдаёт накопленный заряд моментально).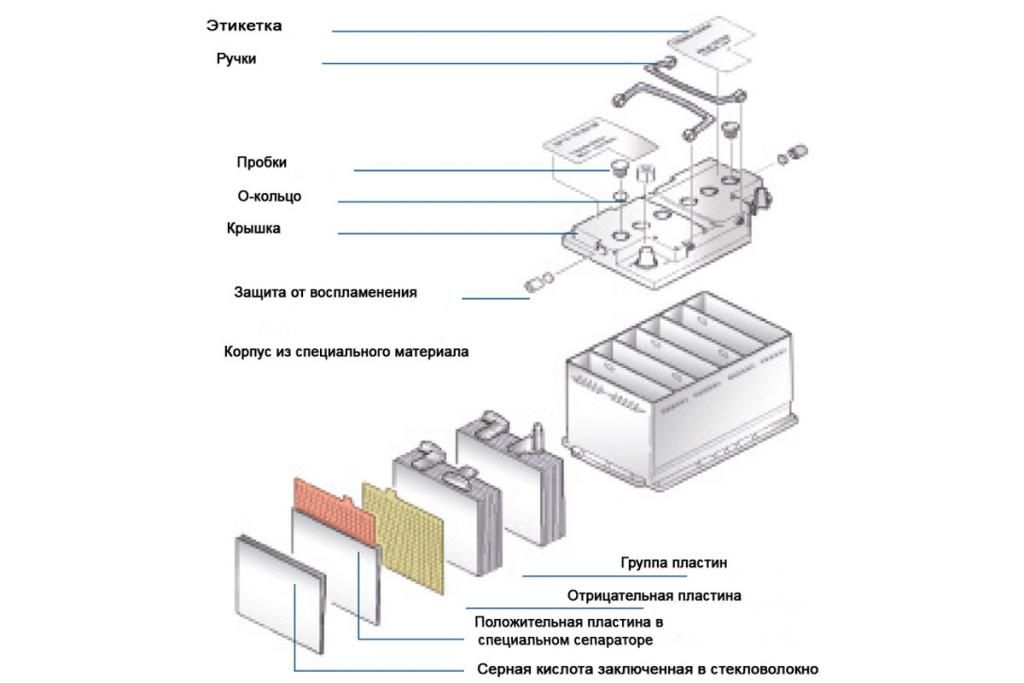 Конденсатор сохраняет непосредственно электрический заряд, в отличие от аккумулятора, который при зарядке преобразует электрическую энергию в энергию химической реакции, а когда будет работать под нагрузкой, превратит накопленную химическую энергию в электрическую.
Конденсатор сохраняет непосредственно электрический заряд, в отличие от аккумулятора, который при зарядке преобразует электрическую энергию в энергию химической реакции, а когда будет работать под нагрузкой, превратит накопленную химическую энергию в электрическую.
Принцип работы аккумуляторной батареи заключается в том, что постоянно происходит химическая реакция между жидкостью-электролитом и металлическими пластинами-электродами. Единичные аккумуляторы очень слабы и не могут давать ток, достаточный для работы большинства устройств. Поэтому чаще всего они объединяются в аккумуляторные батареи, в которых используется последовательное или параллельное соединение отдельных элементов питания.
Разряд элемента питания
Конструкция подобных источников питания предполагает наличие двух клемм: плюса и минуса. Их работа происходит таким образом: при отсутствии нагрузки электрическая цепь разомкнута, а при подключении к полюсам какого-либо устройства цепь замыкается и начинается разрядка АКБ. Ток разряда, протекающий по батарее в таких условиях, возникает за счёт перемещения между электродами ионов: анионов и катионов.
Ток разряда, протекающий по батарее в таких условиях, возникает за счёт перемещения между электродами ионов: анионов и катионов.
Более подробно процесс разрядки батареи удобнее всего будет рассмотреть на конкретном примере. Катод (положительный электрод в источнике тока) состоит из гидрата закиси никеля, в который для улучшения проводимости добавляется графитовый порошок.
Для изготовления анода (отрицательного электрода) в батареях такого типа применяются железные сетки с губчатым кадмием. Электролитом в таком устройстве будет смесь гидроксидов калия и лития. Оксид-гидроксид никеля в таком щелочном источнике питания вступает в химическое взаимодействие с атомами кадмия и молекулами воды. В результате такой реакции образуются гидроксиды кадмия и лития, а также выделяется электроэнергия.
Цикл заряда батареи
Для начала зарядки от клемм аккумулятора необходимо отключить нагрузку. На свободные клеммы батареи подаётся постоянный ток со значением напряжения большим, чем выходное напряжение заряжаемого устройства.
При осуществлении зарядки следует строго соблюдать полярность, то есть должны совпадать положительные и отрицательные контакты батареи и зарядного устройства. Важно учитывать, что устройство для зарядки необходимо выбирать с большей мощностью, чем сам аккумулятор, для того, чтобы преодолевать сопротивление оставшейся в нём энергии и производить электрический ток с направлением, противоположным току разряда. В результате обратимые химические реакции, протекающие в АКБ, поменяют своё направление.
Для рассмотрения примера можно взять также никель-кадмиевую батарею. В реакцию вступают гидроксиды кадмия и никеля, образовавшиеся при цикле разряда. Продуктами этой реакции будут оксид-гидроксид никеля, вода и восстановленный кадмий.
Из всего вышесказанного следует, что во время рабочего цикла меняется только химический состав электродов. Электролит лишь создаёт требуемую для протекания реакций среду. С течением времени он может испаряться, что не самым лучшим образом скажется на продолжительности работы батареи. Рассмотренный принцип работы верен для любого типа аккумуляторов, будет изменяться только химический состав электродов и электролита.
С течением времени он может испаряться, что не самым лучшим образом скажется на продолжительности работы батареи. Рассмотренный принцип работы верен для любого типа аккумуляторов, будет изменяться только химический состав электродов и электролита.
Типы соединения аккумуляторов
Отдельные аккумулирующие элементы позволяют получать малые напряжение и силу тока. Например, чаще всего значение напряжения будет находиться в пределах 1−2 вольта. Для работы большинства устройств таких значений явно недостаточно. Чтобы повысить получаемое напряжение или силу тока, нужно устроить соединение аккумуляторов в батарею. Нужно подробнее остановиться на описании этих способов.
Параллельное соединение
Для соединения аккумулирующих элементов в батарею или нескольких АКБ требуется соединять их положительные клеммы с положительными, а отрицательные с отрицательными. К нагрузке присоединяются соединённые выводы всех элементов. При таком способе соединения напряжение в цепи будет таким же, как у каждой батареи по отдельности (если использовать батареи с одинаковым напряжением). А ёмкость станет равна сумме ёмкостей всех входящих в батарею элементов. Соответственно, вырастет и сила тока, которую такое устройство будет способно давать за определённый период до полной разрядки.
А ёмкость станет равна сумме ёмкостей всех входящих в батарею элементов. Соответственно, вырастет и сила тока, которую такое устройство будет способно давать за определённый период до полной разрядки.
Последовательный способ
При использовании последовательного способа соединения АКБ следует связывать разнополярные контакты. Положительную клемму одного устройства соединяют с отрицательной клеммой другого, а электрическая схема подключается к свободным контактам первой и последней батарей. Итоговое выходное напряжение при применении такого вида соединения будет равняться сумме выходных напряжений всех задействованных источников электрического тока.
Например, чтобы получить АКБ с выходным напряжением двенадцать вольт, следует соединить последовательно четыре источника с напряжением три вольта или десяток аккумуляторов с выходным напряжением 1,2 вольта. Общая ёмкость собранных при помощи последовательного соединения АКБ будет равна ёмкости каждого аккумулятора по отдельности, то есть не изменится.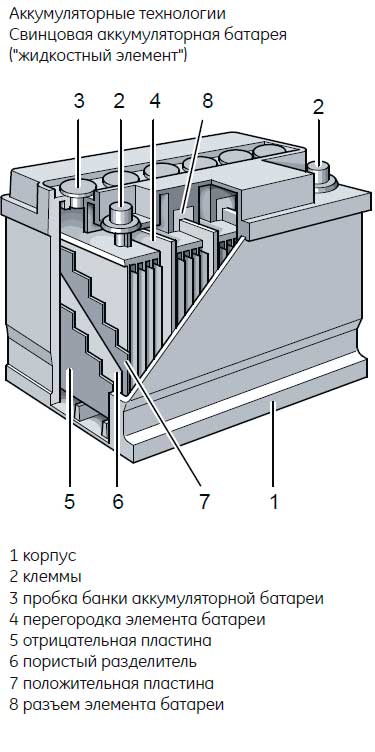
Типы источников тока
АКБ различаются по своему предназначению, характеристикам, тому как устроен аккумулятор и материалам, используемым при их изготовлении. На сегодняшний день в мире производится более трёх десятков типов различных аккумуляторов, основное различие между которыми заключается в химическом составе электродов, а также используемым видом электролита. Так, к примеру, в группу литий-ионных аккумуляторов входит двенадцать различных моделей. Наиболее популярными из всех производимых являются следующие типы:
- свинцово-кислотные;
- литиевые;
- никель-кадмиевые.
На них приходится значительная часть рынка элементов питания. Для лучшего представления о том, из каких материалов могут изготавливаться современные аккумуляторы стоит привести их полный список:
- железо;
- свинец;
- титан;
- литий;
- кадмий;
- кобальт;
- никель;
- цинк;
- ванадий;
- серебро;
- алюминий;
- целый ряд прочих металлов, которые, правда, используются крайне редко.

Применение при производстве различных материалов оказывает значительное влияние на итоговые эксплуатационные показатели и, как следствие, на область возможного использования. Например, литий-ионные АКБ часто устанавливаются в мобильные компьютеры и другие гаджеты.
В то время как никель-кадмиевые аккумуляторы в основном используются как альтернатива простым одноразовым батарейкам. В теории аккумуляторные батареи любого типа могут сочетаться с любым устройством. Дело лишь в целесообразности и себестоимости производства.
Основные характеристики
Выше были рассмотрены материалы, применяющиеся при изготовлении перезаряжаемых элементов питания, основные принципы их работы и способы соединения. Теперь можно перейти к их эксплуатационным качествам. Важнейшими эксплуатационными характеристиками являются:
- Плотность энергии АКБ. Этот показатель равен отношению полного количества электроэнергии, которую аккумулятор способен отдать, к его массе или объёму.

- Ёмкостью называют максимальный отдаваемый аккумулятором заряд во течение цикла разрядки, до достижения минимального значения напряжения на клеммах. В метрической системе такая величина выражается в кулонах (Кл), но в повседневной жизни гораздо чаще применяется внесистемная единица ампер-час (Ah) или, для слабых элементов питания миллиампер-час. Также в некоторых случаях может использоваться показатель, называемый энергетической ёмкостью. Он выражается в джоулях (система СИ) или в ватт-часах. Ёмкость показывает прибор какой мощности и в течение какого времени может питаться от конкретной АКБ.
- Температурный режим — диапазон значений температуры окружающей среды, в котором производитель рекомендует использование этого аккумулятора. При значительном отклонении от рекомендуемого изготовителем диапазона эксплуатационных температур, сильно возрастает вероятность того, что источник питания придёт в негодность. Это можно объяснить влиянием пониженных и повышенных температур на скорость течения химических реакций, а также на изменение давления внутри батареи.

- Саморазрядом АКБ называют потерю заряда, происходящую в заряженной батарее, при условии отсутствия нагрузки, подключённой к контактам. Величина этого показателя определяется, в основном, конструкцией батареи. Она может со временем возрастать из-за нарушения изоляции межу электродами по целому ряду причин.
Все эти параметры аккумуляторных батарей предоставляют наибольший интерес для конечного пользователя.
Устройство электродов
В качестве примера можно использовать свинцово-кислотную батарею. Каждая ячейка такого аккумулятора содержит пару электродов и разделительные пластины, которые изготовляются из пористого материала, не вступающего в химическое взаимодействие с кислотой. Такие пластины призваны препятствовать короткому замыканию погруженных в электролит электродов, и называются сепараторами.
Электроды в таких аккумуляторах выполняются в виде плоских свинцовых решёток.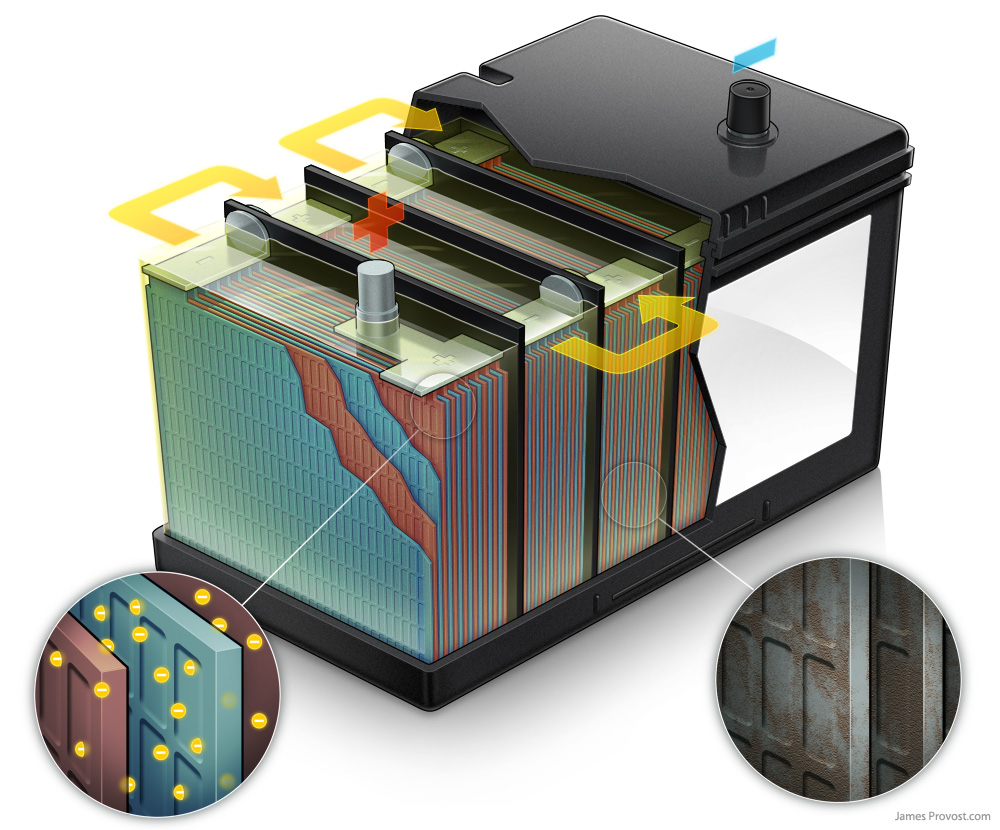 В ячейки таких решёток запрессовывается порошкообразная двуокись свинца (в пластинах-анодах) и металлический свинец в порошковой форме (в пластинах-катодах). Применение порошков обусловлено стремлением увеличить площадь поверхности раздела на границе электролит — электрод, что значительно повышает ёмкость такого источника тока.
В ячейки таких решёток запрессовывается порошкообразная двуокись свинца (в пластинах-анодах) и металлический свинец в порошковой форме (в пластинах-катодах). Применение порошков обусловлено стремлением увеличить площадь поверхности раздела на границе электролит — электрод, что значительно повышает ёмкость такого источника тока.
Имеются экспериментальные образцы аккумуляторов, в которых свинцовые решётки замешены электродами, состоящими из сплетённых нитей углеволокна, которые покрываются тончайшим свинцовым напылением. Такая технология позволяет использовать значительно меньше свинца за счёт распределения его по большой площади, что делает аккумуляторную батарею не только миниатюрнее и легче, но и повышает её эффективность. КПД выше, чем у традиционных, а время зарядки сильно снижено.
Проводящее вещество
Пластины электродов и сепараторов опущены в электролит, в качестве которого в свинцово-кислотных аккумуляторах используется серная кислота, разведённая дистиллированной водой.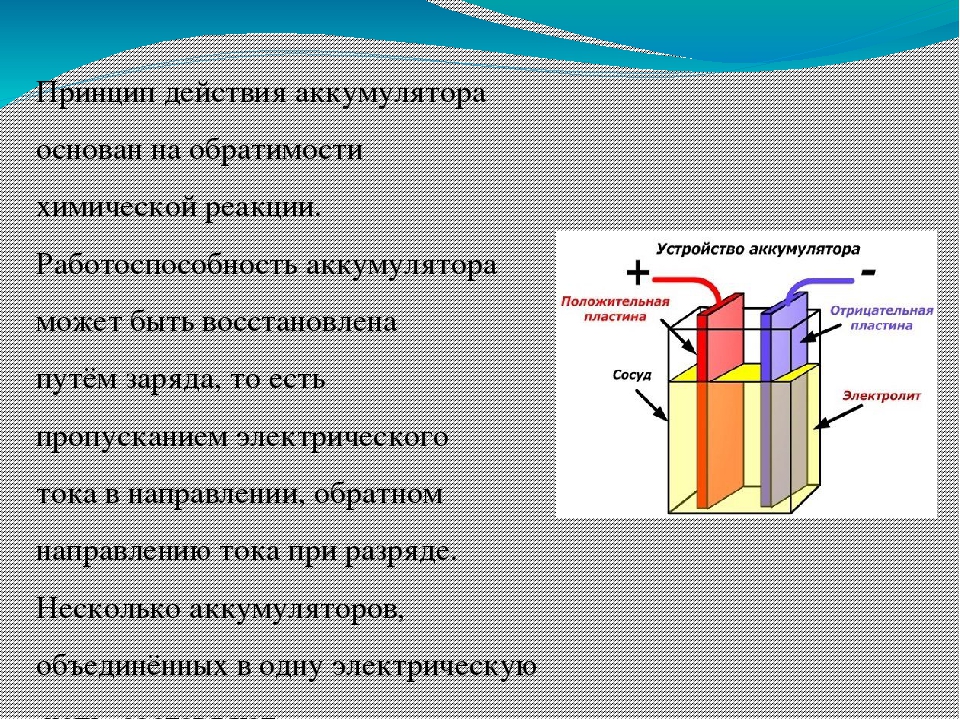 Такая вода применяется для приготовления раствора потому, что она не оказывает влияния на кислотность среды. Проводимость получаемого таким образом раствора зависит лишь от концентрации серной кислоты и комнатных условиях будет максимальной при значении плотности жидкости-электролита в 1,23 грамма на кубический сантиметр.
Такая вода применяется для приготовления раствора потому, что она не оказывает влияния на кислотность среды. Проводимость получаемого таким образом раствора зависит лишь от концентрации серной кислоты и комнатных условиях будет максимальной при значении плотности жидкости-электролита в 1,23 грамма на кубический сантиметр.
Проводимость электролита обратно пропорциональна внутреннему сопротивлению источника питания, и, соответственно, повышение проводимости снижает потери энергии и увеличивает КПД. Стоит отметить, что в областях холодного климата часто используют повышенные до 1,29−1,31 грамма на кубический сантиметр концентрации серной кислоты. Это делается для предотвращения замерзания электролита. Ведь образующийся лёд может повредить корпус аккумулятора.
В батареях, которые устанавливаются в бытовые источники бесперебойного питания, системы сигнализации и другие бытовые приборы, жидкий электролит иногда сгущается до состояния пасты раствором силиката натрия.
Но принцип работы АКБ остаётся тем же.
Области применения АКБ
Аккумуляторные батареи получили широчайшее распространение во всех видах технических устройств. Без них не обходится ни одно портативное электронное устройство: от наручных часов до ноутбуков. Даже в простых электрических фонарях производители предпочитают использовать встроенные АКБ вместо сменных элементов питания.
Не стали исключением и автомобили. В машинах привычных конструкций автомобильный аккумулятор используется для запуска двигателя и бесперебойного питания бортовой электрики и электроники. В набирающих всё большую популярность гибридных и электромобилях аккумуляторы играют ещё более важную роль. Причём в этом случае требования, предъявляемые к устройству АКБ автомобиля, ещё выше.
Крайне важны такие параметры: ток запуска, глубина разряда и максимальное количество циклов перезарядки, которое способен выдержать аккумулятор.
Можно смело утверждать, что современный образ жизни был бы невозможен без аккумуляторных батарей.
Принцип работы аккумулятора автомобиля и не только
АКБ окружают людей в их повседневной жизни буквально повсюду – в мелкой и крупной домашней технике, средствах связи, любимом автомобиле. Несмотря на это, многие не знают, каков принцип работы аккумулятора, и посему не умеют с ним обращаться. На самом деле есть один генеральный принцип, которому подчинена работа батарей всех видов. Это обратимые химические реакции, происходящие циклично. Во время разряда аккумуляторной батареи происходит превращение энергии химической в электрическую, что обеспечивает работу технического устройства, к которому подключен АКБ. Когда запас этой энергии будет исчерпан на определенный процент, производят зарядку аккумулятора. Во время нее также идут химические превращения, но уже с обратным эффектом. То есть поступление электрического тока вызывает накопление запасов химической энергии.
Отличают разные аккумуляторы между собой два аспекта – тип электролита и материал, из которого выполнены электроды. Основой для электролита выступают кислоты или щелочи, которые после разбавления водой или другими добавками приобретают вид готовой гомогенной смеси различной консистенции (жидкой либо гелевой). Вещество, выступающее электродом, способно изменять свойства готового изделия. Самыми распространенными являются литиевые, свинцовые и никель-кадмиевые батареи.
Об автомобильных аккумуляторах
Принцип работы стандартного автомобильного аккумулятора опирается на его конструкцию и не зависит от того, залит в него кислотный или щелочной электролит.
Внутри диэлектрического и нерастворимого серной кислотой корпуса из специального пластика помещаются шесть банок-батареек, последовательно прикрепленных друг к другу. В каждой из этих банок есть по несколько электродов с зарядами «плюс» и «минус», которые выглядят как отводящая ток решетка, смазанная специальной химически активной массой.
Чтобы решетки с разными знаками случайно не соприкоснулись и не закоротили, каждая из них погружена в разделитель из полиэтилена. Сами электроды сделаны обычно из свинца с разнообразными примесями.
Если быть точным, то таких свинцовых решеток бывает три вида:
- Малосурьмянистые. И аноды, и катоды сделаны из сплава свинец+сурьма и требуют мало обслуживающих процедур.
- Кальциевые. Здесь примесь, соответственно, кальций. Такие электроды вообще не нужно обслуживать.
- Гибридные. Один электрод, с минусом, делается из кальциевого сплава, а положительный содержит сурьму.
Можно с уверенностью утверждать, что свинцово-кислотный — самый востребованный и распространенный вид аккумулятора для авто. Принцип работы свинцового аккумулятора основывается на активном взаимодействии серной кислоты с диоксидом свинца.
Когда батарея эксплуатируется, то есть нужна электрическая энергия, на катоде свинец окисляется, а его диоксид на аноде, напротив, участвует в восстановительной реакции. При зарядке, как нетрудно догадаться, взаимодействия идут в обратную сторону.
При зарядке, как нетрудно догадаться, взаимодействия идут в обратную сторону.
Это все происходит за счет кислоты в электролите, часть ее распадается, соответственно, концентрация падает. Именно этим обусловлена необходимость периодически обновлять жидкость в батарее.
С гелевыми аккумуляторами такого не случается. Состояние электролита в них не позволяет ему испаряться, если, конечно, не перегреть АКБ во время подзарядки. Как правильно заряжать гелевые аккумуляторы, читайте здесь →
Именно благодаря отсутствию необходимости периодически восполнять запасы активного вещества батареи с желеобразным электролитом относят к категории необслуживаемых. Еще одно их преимущество в том, что гель не отсоединяется от электрических контактов, а значит, невозможны внезапные сбои и замыкания.
Как устроен литий-ионный аккумулятор?
Его конструкция не отличается сложностью: анод из пористого углерода, литиевый катод, пластина-сепаратор между ними и проводник тока – вещество-электролит. Во время разрядки ионы отделяются от анода и движутся на литий по электролиту, минуя сепаратор. Во время питания батареи все происходит с точностью до наоборот – литий отдает ионы, углерод принимает. Так и происходит процесс ионного круговорота между разнозарядными электродами литий-ионной батареи.
Во время разрядки ионы отделяются от анода и движутся на литий по электролиту, минуя сепаратор. Во время питания батареи все происходит с точностью до наоборот – литий отдает ионы, углерод принимает. Так и происходит процесс ионного круговорота между разнозарядными электродами литий-ионной батареи.
Точный состав катода может отличаться в конкретной модели или у определенного производителя АКБ. Дело в том, что многие фирмы тестируют разнообразные типы литиевых соединений для того чтобы изменять показатели устройств по своему усмотрению.
Впрочем, очевидно – улучшая одни характеристики, неизбежно приходится жертвовать другими. Чаще всего литий-ионные АКБ с повышенной емкостью, заботой об эксплуатирующих его людях и природной среде оказываются чрезмерно дорогостоящими или требуют слишком много внимания.
Но чего не отнять у батарей с литием, что составляет их принципиальную разницу с другими типами аккумуляторов, так это низкий уровень саморазряда.
Li-Pol аккумуляторные батареи
Литий-полимерные — это следующий этап развития литий-ионных АКБ. Принципиальная разница понятна из названия — в качестве электролита начинает использоваться полимерное соединение. Из-за прочности существующих в нем химических связей такой аккумулятор становится максимально безопасным, неправильная эксплуатация может сломать его самого, но не нанести вред владельцу, как это бывало с литиевыми АКБ с жидким наполнителем. Полимерный неопасно перегревать или протыкать острым предметом, в то время как жидкостной элемент уже давно бы взорвался.
Принципиальная разница понятна из названия — в качестве электролита начинает использоваться полимерное соединение. Из-за прочности существующих в нем химических связей такой аккумулятор становится максимально безопасным, неправильная эксплуатация может сломать его самого, но не нанести вред владельцу, как это бывало с литиевыми АКБ с жидким наполнителем. Полимерный неопасно перегревать или протыкать острым предметом, в то время как жидкостной элемент уже давно бы взорвался.
Еще один огромный плюс Li-Pol батарей — их огромная проводимость. Из-за того, что в процессе реакций на анодах и катодах батарея приобретает свойства хорошего полупроводника, она способна передавать ток, в разы превышающий ее собственную электроемкость.
Щелочные батареи
Методика функционирования щелочного аккумулятора основывается на химических превращениях в щелочной среде. Именно поэтому для электродов таких АКБ применяют соединения металлов, которые активно взаимодействуют именно со щелочами.
Гидроокись никеля на электроде с положительным зарядом превращается в гидрат его закиси из-за череды реакций со свободными ионами в электролите. На катоде в это же время идут похожие взаимодействия, но только с образованием гидрата окиси железа. Между только что создавшимися веществами образуется разница в потенциалах, за счет которой и выделяется электроэнергия. В процессе подзарядки реакции те же самые, только в обратном порядке, вещества восстанавливаются до исходных.
На катоде в это же время идут похожие взаимодействия, но только с образованием гидрата окиси железа. Между только что создавшимися веществами образуется разница в потенциалах, за счет которой и выделяется электроэнергия. В процессе подзарядки реакции те же самые, только в обратном порядке, вещества восстанавливаются до исходных.
Ni-Cd аккумулятор
Батареи никель-кадмиевого типа обычно применяют для некрупной техники, например, для шуруповерта. Принцип их устройства и работы схож с автомобильным АКБ, только в гораздо меньших масштабах – те же последовательно соединенные несколько маленьких батареек, совместно вырабатывающих нужные электрические показатели, а внутри них – уже знакомые аноды, катоды, пластины сепараторов и жидкий электролит.
Специфические характеристики, присущие только этому типу аккумуляторов, обеспечивают именно химические свойства никеля и кадмия. Они же накладывают и обязательство быть осторожным, особенно при утилизации. Это вызвано тем, что кадмий – довольно токсичный элемент.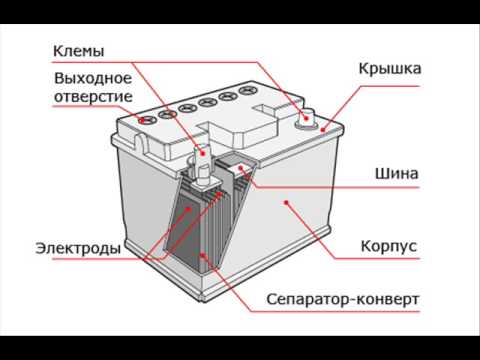
При аккуратной же эксплуатации шуруповертов с такими АКБ приборы гарантированно будут работать долгое время на высокой мощности, в любых погодных и температурных условиях. К тому же их можно очень быстро заряжать.
Ni-MH аккумулятор
По своему устройству и механизму работы никель-металл-гидридные батареи очень похожи на кадмиевые и были изобретены практически сразу после них. Основное отличие состоит в материале, из которого изготовлен отрицательный электрод.
В аккумуляторах типа Ni-MH он состоит из особого справа металлов, которые абсорбируют водород. Часть из них реагируют с ионами электролита с выделением тепловой энергии, другая часть – с ее поглощением, в результате чего возможно безопасное и экологически безвредное использование такого устройства.
Как работает зарядное устройство для АКБ?
ЗУ для аккумулятора обычно состоит из выпрямителя и трансформатора и создает ток с постоянным напряжением около 14 вольт. Также хорошие приборы содержат элементы, которые следят за напряжением на питаемом аккумуляторе и в нужный момент выключают зарядку.
По ходу процесса работы зарядного устройства для автомобильного аккумулятора или для любого другого подаваемый им ток сам собой падает. Вызвано это тем, что в заряжающемся АКБ увеличивается сопротивление, и он больше не пропускает ток с большим напряжением. Если в зарядке есть измеритель, то он фиксирует тот момент, когда в батарее достигнуто напряжение в 12В, после чего ее можно отключать от сети.
АКБ – вещь не такая сложная, как может показаться. Ее устройство легко понять, к тому же, принцип работы одинаков для разных видов. Знать его владельцу аккумулятора хоть в машине, хоть в настенных часах, очень полезно – это поможет поступать правильно на всех этапах – выбора, обслуживания и утилизации батарейки.
Аккумуляторная батарея: устройство, принцип работы, типы
Мы не представляем жизни без них. Они окружают нас повсюду. Лежат у людей в карманах, висят дома на стенах, установлены в каждом автомобиле и общественном транспорте, даже стационарные компьютеры не работают без них, не говоря уже о ноутбуках. Человечество в окружении этих элементов под названием аккумуляторы. Но несмотря на такое разнообразие источников энергии, единицы знают, как они устроены и как ими правильно пользоваться. В этой статье рассмотрены некоторые виды аккумуляторных батарей, применяемых в большинстве сферах человеческой жизни.
Человечество в окружении этих элементов под названием аккумуляторы. Но несмотря на такое разнообразие источников энергии, единицы знают, как они устроены и как ими правильно пользоваться. В этой статье рассмотрены некоторые виды аккумуляторных батарей, применяемых в большинстве сферах человеческой жизни.
История
Впервые свет увидел аккумулятор в 1859 году. Изобретенный блестящим физиком и профессором имя которого Луи́ Гасто́н Планте́. Это имя широко известно в узких кругах. Человечество уже на протяжении 160 лет пользуется этим изобретением, которое серьезно облегчает жизнь каждого человека. Начиная от часов на руках и заканчивая сложными аппаратами поддерживающими жизнь в больницах.
С каждым годом электромобили сильнее заполняют улицы городов. Самый дорогой элемент такого транспорта — аккумуляторная батарея. Работали над созданием и усовершенствованием батарей ученые умы, такие как Томас Эдисон, Камилл Фор, Пейкер, и другие. Подобные исследования продолжаются по сегодняшний день.
Обзор автомобильных аккумуляторов
Сурьмянистый АКБ
Название «Сурьмянистый» происходит из того факта, что в этом источнике питания большое количество сурьмы (Sb) – это вещество, которое придает свинцу твердость. Устройство батареи основано на сплаве сурьмы со свинцом (5-15% Sb), из которого изготовляют пластины применяемые. Когда в АКБ напряжение достигает 12 В — происходит бурная активизация процесса электролиза благодаря сурьме. В процессе выделяются водород и кислород. При такой работе понижается уровень электролита из которого начинают выступать пластины электродов. Как результат — частая доливка воды в аккумулятор. Это устаревший вид батарей, который уже не применяют, кроме старой аппаратуры. Современные АКБ содержат сурьму, но в меньшем количестве.
Малосурьмянистые АКБ
Это аккумуляторы идентичные описанным выше, но содержащие меньше пяти процентов сурьмы. Это сделали для меньшего испарения вода, в результате – проблема частой доливки воды уходит. Еще было достигнуто уменьшение уровня саморазряда батареи при простоях. Данный вид батарей принято называть необслуживаемыми, но через полгода лучше проверять уровень дистиллированной воды, т.к. в ходе химической реакции она испаряется.
Еще было достигнуто уменьшение уровня саморазряда батареи при простоях. Данный вид батарей принято называть необслуживаемыми, но через полгода лучше проверять уровень дистиллированной воды, т.к. в ходе химической реакции она испаряется.
Важно! Клеммы аккумуляторов «плюс» и «минус» изготавливают разной толщины. Преследовалась цель не дать клиенту перепутать контакты местами и сделать «короткое замыкание» в электрике автомобиля.
Модернизация вызвала повышение уровня стабильности батареи при нестабильности в сети автомобиля. Данный вид батареи по стабильности стоит на первом месте среди других АКБ.
Кальциевый АКБ
Устройство аккумулятора этого типа отличается тем, что сурьму заменили кальцием, что привело к еще меньшему испарению воды, которое стремится к нулю. Обозначение Са/Са на корпусе свидетельствует, что это кальциевый аккумулятор причем Са расположен в решетках как положительных так и отрицательных электродов.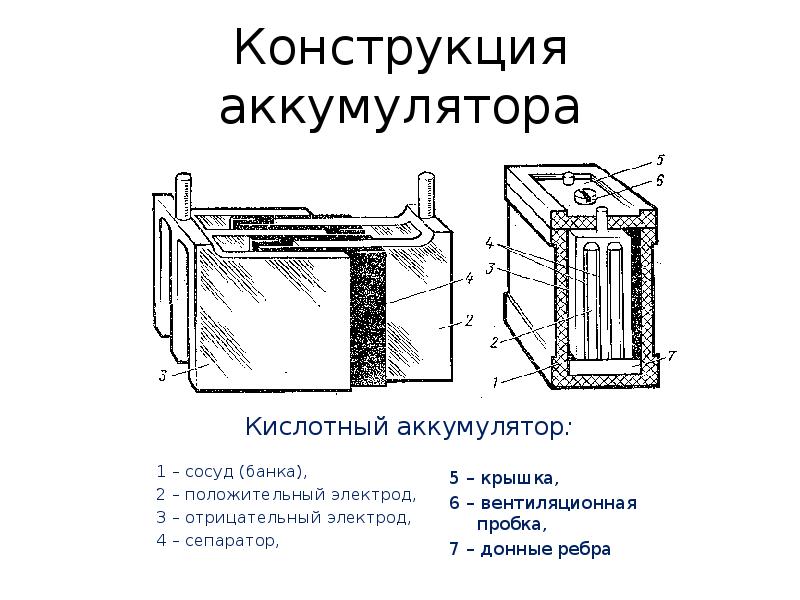 Если сравнить такой накопитель с сурьмянистым, то мы заметим, что саморазряд батареи с кальцием на семьдесят процентов понизился. Еще увеличилось напряжение с 12 вольт до 16.
Если сравнить такой накопитель с сурьмянистым, то мы заметим, что саморазряд батареи с кальцием на семьдесят процентов понизился. Еще увеличилось напряжение с 12 вольт до 16.
Гелиевые АКБ
Гелиевые аккумуляторы разработали, чтобы уйти от опасности вытекания электролита, который токсичен для человека. При повреждении этого источника энергии химический состав не вытекает как в других АКБ из-за вязкой структуры электролита. Преимущества таких АКБ положение установки, их можно устанавливать под углом, но меру знать тоже нужно. Еще такие аккумуляторы лучше других выдерживают вибрацию и способны до полной разрядки выдавать большой ток. Гелиевые батареи не боятся полной разрядки и способны восстанавливаться. Такие накопители лучше ставить на исправную машину в плане стабильности бортовой электрики, такой как генератор и др.
Принцип работы свинцово-кислотного АКБ
Это распространенные источники энергии, применяемые для механических транспортных средств. В первую очередь используются для заводки автомобиля и питания всей бортовой электрики.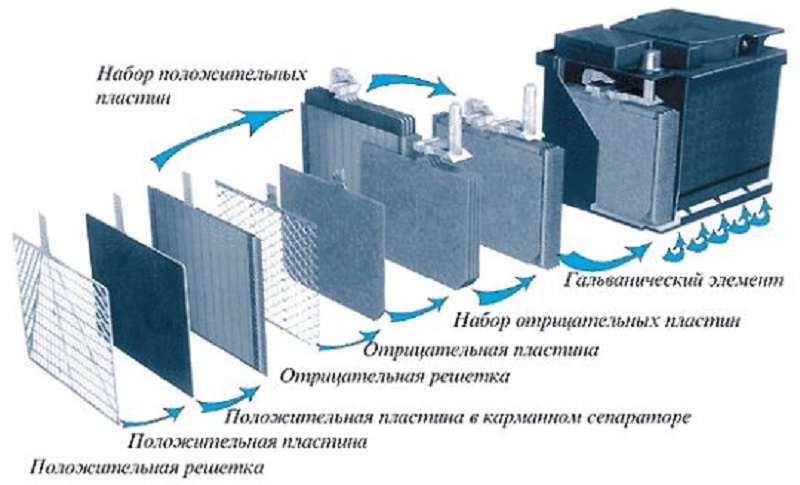
Как работает аккумулятор? Принцип выглядит следующим образом: в сосуд с серной кислотой помещены свинец и диоксид свинца. В спокойном состоянии процесс не протекает, но как только к электродам подключается нагрузки происходит электрохимический процесс взаимодействия серной кислоты с оксидом свинца, который окисляется до сульфата свинца. Больше 60 химический реакций протекает во время этого процесса. Формула выглядит так:
Принцип работы литий-ионного аккумулятора
Литий-ионные батареи зарекомендовали себя на мировом рынке лучшие накопители для современной техники, такой как смартфоны, ноутбуки, электромобили и другие виды домашней и производственной техники. В 1991 году впервые была выпущена литий-ионная батарея.
Напряжение такого источника составляет 3.7 В, около 800 циклов разряда/заряда способна выдержать это изобретение. Саморазряд составляет 2% в месяц. Работать такие элементы способны на температуре от -20 °C до +60 °C.
Принцип действия основан на электрохимической реакции лития при внедрении в кристаллическую решетку других материалов с образованием химической связи. Еще основной особенностью таких батарей является то, что они почти на 100% без эффекта памяти. Для определения этого факта проводили множество экспериментов и определили, что эффект памяти есть, но он настолько незначительный, что принято считать его нулевым.
Еще основной особенностью таких батарей является то, что они почти на 100% без эффекта памяти. Для определения этого факта проводили множество экспериментов и определили, что эффект памяти есть, но он настолько незначительный, что принято считать его нулевым.
Формула:
Совет! Для водителей, которые желают быстро запускать свой автомобиль на морозе. За несколько минут до запуска двигателя включите ближний свет фар или другой потребитель. При этих действиях батарея «просыпается» и приходит в рабочее состояние. Были проведены эксперименты и установлено, что этот метод работает на практике.
Отличие Li-Pol, щелочных аккумуляторов от Ni-Cd и Ni-Mh.
Ni-Cd Никель-кадмиевые аккумуляторы
Данный вид аккумуляторов широко применяли несколько лет назад для различного инструмента. Такие источники в своей структуре содержат кадмий, который является тяжелым металлом и токсичен, но хорошо ведет себя на морозе и имеет не высокую стоимость.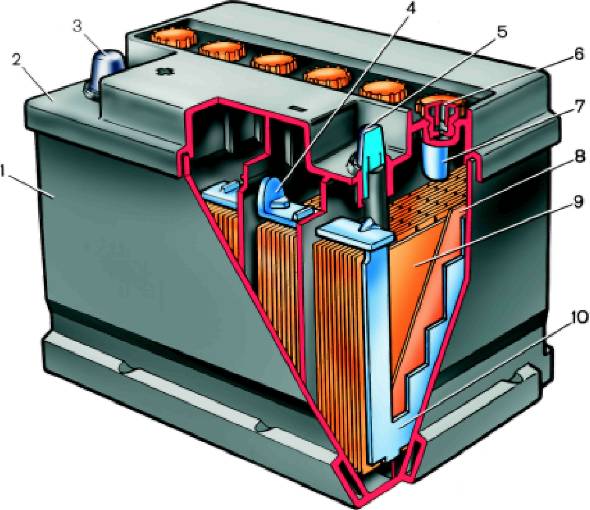
Новые модели аккумуляторов раньше приходят в негодность, чем батареи выпущенные 20 лет назад. Но уровень технических характеристик присущий современным решениям намного выше, чем у их предшественников.
Ni-MH Никель-металлогидридные аккумуляторы
Такие батареи претерпели некоторые изменения по сравнению с Ni-Cd Никель-кадмиевыми. Избавились от токсичных металлов, стали легче по весу и теперь можно не боятся причинить вред окружающей среде при ликвидации таких аккумуляторов. Еще удалось повысить энергоемкость и уменьшить эффект памяти.
Li-Pol Литий-полимерный аккумуляторы
Вид этих аккумуляторов — улучшенная модернизация литий-ионных. Электролит был заменен полимерными материалами. Такие батареи установлены в смартфонах, планшетах, ноутбуках, цифровой фототехнике и др. Особенность таких источников энергии состоит в форме изготовления, она может быть очень тонкой, что позволяет поместить батарею в любой корпус. Главное преимущество литий-полимерных элементов питания в том, что они не имеют эффекта памяти и энергоемкие.
Щелочные аккумуляторы.
Широкое применение щелочные аккумуляторы нашли в бытовой технике. Известные модели таких батарей — тип ААА и АА. Они установлены в:
- детских игрушках
- портативных приборах
- карманных фонарях
- фото, видео аппаратуре
- аудио магнитофонах, плеерах и пр.
Щелочной электролит впервые нашел применение в химически активных источниках тока благодаря Вальдемару Джангнеру в 1899 году. С этого времени ученые разных стран вовлечены в разработку щелочных источников питания.
Принцип действия аккумуляторной батареи таков: при работе щелочного элемента происходит химическая реакция, при которой цинк окислившись выделяет гидроксид цинка, далее последний распадается на оксид цинка и воду. При этом происходит восстановление оксида марганца на катоде. Формула выглядит следующим образом:
| Таблица сравнения 4-х видов АКБ | ||||
| Вид аккумулятора | Ni-Cd | Ni-Mh | Щелочные АКБ | Li-Pol |
| Работа при низких температурах | + | + | + | — быстро теряет емкость |
| Цена | низкая | средняя | средняя | Высокая |
| Быстрая зарядка | + | + | — | + |
| Кол-во циклов разряда-заряда | 1000 | 300-500 | 300 | 1000-2000 |
| Токсичность | + | — | — | — |
| Эффект памяти | + | низкий | + | — |
| Саморазрядка | + | + | — | — |
Обычный аккумулятор оказывается сложной и в то же время простой вещью, если разобраться с ней. Прежде чем выбрать для авто элемент питания, стоит изучить нюансы, которые в последствии могут сыграют весомую роль в вашей жизни.
Как работает аккумулятор и 3 способа его испортить
Одно из самых полезных электронных устройств, доступных нам, также является одним из самых распространенных. Современные батареи используются во многих из наших любимых технологий, что можно почти простить за то, что вы не тратите время на изучение их работы.
Но теперь для вас настало время расширить свою базу знаний за счет понимания того, как работает смартфон в вашем кармане, какие типы аккумуляторов распространены и что вы можете сделать, чтобы продлить срок их службы.
Краткая история батарей
Алессандро Вольта продемонстрировал первую работающую электромагнитную батарею в 1800 году.Его стопка медных и цинковых пластин, разделенных пропитанными рассолом бумажными дисками, вырабатывала стабильное напряжение в течение «разумного» периода времени. Это было известно как гальваническая батарея и стало предшественником поколения экспериментов с батарейным питанием.
В 1836 году Джон Фредерик Дэниелл стандартизировал конструкцию батареи.Медный горшок, наполненный раствором медного купороса, погруженный в неглазурованный глиняный сосуд, наполненный серной кислотой, и цинковый электрод стали де-факто стандартом аккумуляторов, распространенным в бесчисленных электрических телеграфных сетях.
Перенесемся в Оксфордский университет, 1979 год.Джон Гуденаф и Коичи Мидзусима продемонстрировали работающий перезаряжаемый элемент с диапазоном 4 В, в котором оксид лития-кобальта использовался в качестве положительного электрода и металлического лития в качестве отрицательного. Предшественник литиевого элемента в том виде, в каком мы его знаем, родился, но был коммерциализирован только в 1991 году Sony и Asahi Kasei в своих портативных электронных устройствах.
Что такое современный аккумулятор?
Мы используем термин современная батарея для описания электрохимических элементов, которые питают наши портативные технологические устройства.Батареи делятся на две общие категории:
- Одноразовые: одноразовые батарейки с электродами, которые необратимо меняются во время использования.
- Аккумуляторные: многоразовые батареи с электродами, восстанавливаемыми обратным током.
В большинстве современных портативных электронных устройств используется литиевая батарея, наиболее распространенной из которых является литий-ионный ( Li-ion ) элемент. Вы также можете встретить литий-полимерный ( Li-Po ) элемент, который имеет такой же электрохимический состав и общий химический состав, что и его аналог, но стоит дороже в производстве и имеет более низкую плотность энергии.
Тем не менее, Li-Po аккумуляторы по-прежнему популярны из-за их легкого веса, гибкости конструкции и улучшенных рабочих характеристик при более высоких и низких температурах, с чем Li-ion может бороться.
Литий-ионные батареи обычно содержат интеркалированное соединение лития, такое как оксид лития-кобальта (LiCoO 2 ) в качестве одного электрода, графит в качестве второго и органический растворитель в качестве электролита.Это соединение используется из-за его высокой плотности энергии и медленной потери заряда, когда он не используется, а также из-за того, что не требуется циклическое переключение памяти для продления срока службы батареи.
Все литиевые батареи содержат температурный коэффициент давления.Это отказоустойчивый переключатель или датчик, предназначенный для предотвращения перегрева батареи в экстремальных условиях или чрезмерного использования — процесса, который обычно делает батарею бесполезной из-за необратимого повреждения химических соединений, которые делают возможным процесс заряда / разряда.
Процесс зарядки
Литиевые батареи стали предпочтительными для портативных технологий благодаря их высокой плотности энергии и перезаряжаемым свойствам.
Во время процесса зарядки ионы лития перемещаются через электролит от положительного электрода из оксида лития-кобальта к отрицательному электроду из графита.При разряде или использовании ионы возвращаются через электролит, от отрицательного к положительному. Этот процесс происходит при относительно высоком напряжении — 3,7 вольт по сравнению с щелочной батареей AA при 1,5 вольт — вот почему литиевые батареи стали предпочтительным портативным источником питания для многих потребительских электронных устройств.
Литиевые батареи также входят в состав более крупных аккумуляторных блоков, таких как аккумулятор для ноутбука.Эти аккумуляторные блоки содержат ряд литий-ионных элементов, связанных в один более крупный компонент, и будут содержать ряд дополнительных компонентов:
- Датчик температуры : Датчик, отслеживающий температуру внутри упаковки, чтобы обеспечить безопасность и долговечность ячеек.
- Регулятор напряжения : Датчик и схема для контроля и регулирования выхода / емкости каждой ячейки внутри блока.
- Состояние заряда аккумулятора : Датчик, информирующий операционную систему о текущем состоянии заряда (например, 47% заряда)
- Разъем : Комплектный разъем для ноутбука, зависит от марки.
Литиевые батареи могут выполнить тысячи циклов заряда / разряда, прежде чем качество элемента начнет действительно ухудшаться, но есть несколько способов испортить батарею, потенциально подвергая себя опасности.
Обслуживание батарей
Положительный электрод, который есть в большинстве литиевых батарей, LiCoO 2 , может представлять ряд опасностей в случае повреждения элемента.В отличие от ряда других вариантов батарей, использование горючего компаунда под давлением может привести к экстремальным результатам. Чтобы смягчить это, элементы литиевых батарей подвергаются ряду тестов на безопасность, многие из которых более строгие, чем их аналоги на кислотной основе.
Тепло
Было несколько случаев воспламенения литиевых батарей в условиях экстремальной жары.Батареи под воздействием тепла в сочетании с любым дополнительным, неожиданным давлением или коротким замыканием могут «взорваться», оставив разрушенный аккумулятор и, чаще всего, поврежденный элемент портативной техники.
Каждая литиевая батарея имеет встроенный сепаратор внутри элемента.Это различает положительный и отрицательный электроды в процессе заряда / разряда. Если этот разделитель будет перфорирован или поврежден, существует вероятность контакта электродов. Это приводит к быстрому нагреву аккумулятора, что может привести к взрыву.
Батарея имеет вентиляционный механизм, чтобы предотвратить такое возникновение, но, в конечном счете, из-за природы удаляемого химического соединения, вероятность взрывной реакции все еще сохраняется из-за тепла, выделяемого химической реакцией.
Номинальные значения разрядки
Литиевые батареи предпочитают частичный разряд, а не «глубокий» или «полный».У них нет зарядной памяти, поэтому частичный разряд не повлияет на будущую производительность.
Однако «глубокая» разрядка i.е. полный разряд батареи приведет к падению напряжения литиевой батареи и может привести к необратимому повреждению батареи.
Процесс старения
Литиевые батареи стареют.Предполагается, что их максимальный срок службы составляет от 2 до 4 лет в зависимости от количества циклов заряда / разряда. Это не означает, что вам следует отслеживать количество раз, когда вы используете батарею, поскольку это было бы довольно сложно. Но отказ от использования новой батареи и оставление ее на полке не продлит срок службы батареи — батареи все равно прослужат те же 2-4 года.
Также стоит проверить, когда была произведена батарея, при покупке нового портативного технического продукта.Если он простаивал на складе в течение года, срок службы батареи уже истощился. Свяжитесь с производителем продукта и по возможности попросите новую батарею.
Существуют современные приложения для управления батареями, которые заявляют, что могут со временем обратить вспять текущую приемлемую деградацию ячеек, например, batteryOS, продукт, который будет запущен в феврале 2015 года.
Li-Air
В литиевых батареях следующего поколения будет использоваться химический состав литий-воздух, обеспечивающий чрезвычайно высокую плотность энергии во все более легких конструкциях.Литий-воздушные батареи получают преимущество в плотности энергии по сравнению с традиционными аналогами за счет использования большого количества кислорода для индукции тока, вместо того, чтобы хранить необходимый химический окислитель внутри.
К сожалению, до того, как коммерчески жизнеспособный продукт Li-Air появится в наших портативных устройствах, все еще необходимы исследования в ряде ключевых областей.
Помогло ли это вам понять батареи в ваших портативных устройствах? Дайте нам знать, что вы думаете ниже!
Кредиты на изображения: Батареи через Wikimedia Commons, Voltaic Pile через Wikimedia Commons, Литий-ионные батареи через Wikimedia Commons, Литий-полимерные батареи через Wikimedia Commons, 3GS со сломанной батареей через Wikimedia Commons, Пустая батарея через Pixabay, Плотность энергии батареи через Wikimedia Commons
Как разблокировать секретную кнопку на вашем iPhone с помощью обратного нажатия
Знаете ли вы, что на вашем iPhone есть скрытая кнопка, к которой можно получить доступ, нажав ее спину? Вот как им пользоваться.
Об авторе
Гэвин Филлипс
(Опубликовано 614 статей)
Гэвин — младший редактор отдела Windows and Technology Explained, регулярный участник Really Useful Podcast и редактор дочернего сайта MakeUseOf, посвященного криптографии, Blocks Decoded.У него есть степень бакалавра (с отличием) в области современного письма с использованием методов цифрового искусства, разграбленных на холмах Девона, а также более десяти лет профессионального писательского опыта. Он любит много пить чая, настольные игры и футбол.
Ещё от Gavin Phillips
Подпишитесь на нашу рассылку новостей
Подпишитесь на нашу рассылку, чтобы получать технические советы, обзоры, бесплатные электронные книги и эксклюзивные предложения!
Еще один шаг…!
Подтвердите свой адрес электронной почты в только что отправленном вам электронном письме.
Как работает Power Bank »Электронные заметки
Энергобанки
работают, используя сложную электронику для управления зарядом от зарядного устройства, хранением его в аккумуляторе и последующей зарядкой других устройств.
Power Banks Включает:
Что такое Power Bank
Как работает power bank
Как использовать power bank
Как купить лучший внешний аккумулятор
Внешний аккумулятор для беспроводной зарядки
Powerbank — это не просто аккумулятор: в них используется сложная электронная схема для управления зарядкой и последующей зарядкой других устройств.
Чтобы гарантировать, что величина заряда аккумулятора известна, чтобы они не перезаряжались, чтобы они заряжались с правильной скоростью, а также для управления зарядкой портативных устройств, специально разработанные интегральные схемы и модули обеспечивают все требуется интеллект.
Основы работы с аккумулятором
Если посмотреть, как работает внешний аккумулятор, это, по сути, аккумулятор, питание на который обычно подается от зарядного устройства USB с питанием от сети.Он сохраняется, а затем передается заряжаемому устройству по мере необходимости.
Для облегчения этой операции внешний аккумулятор состоит не только из самой батареи, но и из сложной электроники, которая управляет всеми этими операциями.
Работа типичного блока питания
Технология батареи блока питания
Хотя управление зарядкой и разрядкой аккумулятора является ключевым моментом в работе внешнего аккумулятора, также используется технология аккумуляторов.
Используются две основные технологии:
- Литий-ионный: Литий-ионный обеспечивает высокую удельную мощность и не проявляет так называемого эффекта памяти (когда аккумуляторы со временем становится все труднее заряжать).Литий-ионные аккумуляторы значительно дешевле.
- Литий-полимерный: Литий-полимерные батареи обычно более прочные и гибкие, особенно когда речь идет о размере и форме их конструкции, и они, как правило, служат дольше. Они также легкие, имеют низкий профиль и меньше подвержены утечке электролита.
Другое оборудование, предметы и гаджеты:
Беспроводная зарядка
Умные колонки
Bluetooth-динамики
Зарядные устройства USB
Энергобанки
Электронные книги
Светодиодные лампы
Пульты для ТВ
ВЭБ-камера
Вернуться в меню электронных устройств.. .
Как работают батареи
Как работают батареи
Батареи все
над местом — в наших машинах,
наши ПК,
ноутбуки,
портативный MP3
игроки и сотовый
телефоны. Батарея — это, по сути, банка с химикатами, которые
производят электроны. Химические реакции с образованием электронов
называется электрохимический
Реакция .В этой статье вы узнаете все об аккумуляторах — от базовых
концепция в действии с фактической химией, происходящей внутри батареи, чтобы
что ждет в будущем аккумуляторы и возможные источники энергии, которые
мог бы их заменить!
Если вы посмотрите на любой
аккумулятор, вы заметите, что в нем два
терминалы .
Один вывод отмечен знаком (+) или положительным, а другой отмечен
(-) или отрицательный. В ячейке AA, C или D (обычный фонарик
батареи), концы батареи — клеммы.В большой машине
аккумулятор, есть два тяжелых вывода, которые действуют как выводы.
Электронов
собираем на минусовой клемме АКБ. Если вы подключите
провод между отрицательной и положительной клеммами, электроны будут
течь от отрицательного к положительному выводу так быстро, как они могут
(и очень быстро изнашивает аккумулятор — это тоже имеет тенденцию
опасно, особенно с большими батареями, так что это не то
вы хотите делать). Обычно вы подключаете какой-то тип нагрузки
к батарее с помощью провода.Нагрузка может быть чем-то вроде
легкий
лампочка, мотор
или электронная схема, такая как радио.
Внутри батареи
Сама по себе химическая реакция производит электроны. Скорость
производство электронов этой химической реакцией (внутренняя батарея
сопротивление )
контролирует, сколько электронов может течь между клеммами. Электроны
течь от аккумулятора в провод и должна идти от отрицательного
к положительной клемме, чтобы произошла химическая реакция.
Поэтому аккумулятор может простоять год на полке и при этом иметь
много энергии — если электроны не текут от отрицательного к
положительный вывод, химическая реакция не происходит.Как только вы подключите провод, начинается реакция.
Первая батарея была создана
Алессандро Вольта в 1800 году. Чтобы создать свою батарею, он сделал стек
чередование слоев цинка, промокательной бумаги, смоченной соленой водой, и
серебро, вот так:
Это расположение
был известен как вольт
свая .
Верхний и нижний слои сваи должны быть из разных металлов, т.к.
показано. Если прикрепить проволоку к верху и низу стопки, вы
может измерять напряжение и ток от сваи.Куча может быть
сложены так высоко, как вам нравится, и каждый слой будет увеличивать напряжение
на фиксированную сумму.
В 1800-х годах
до изобретения электрического генератора (генератор был
изобретен и усовершенствован до 1870-х годов), модель Daniell
ячейка
(который также известен под тремя другими названиями — «клетка Ворона»
из-за типичной формы цинкового электрода «сила тяжести
ячейка «, потому что сила тяжести разделяет два сульфата, а
«мокрая ячейка» в отличие от современной «сухой ячейки»
потому что он использует жидкости для электролитов), было чрезвычайно распространено
для управления телеграфом и дверными звонками.Клетка Даниэля — мокрая
ячейка, состоящая из медных и цинковых пластин и меди и цинка
сульфаты.
Чтобы сделать Даниэля
ячейки медная пластина помещается на дно стеклянной банки. Медь
На тарелку наливают раствор сульфата, чтобы заполнить банку наполовину. затем
в банку подвешивают цинковую пластину, как показано на рисунке, и раствор сульфата цинка
очень осторожно налил в банку. Медный купорос плотнее, чем
сульфат цинка, поэтому сульфат цинка «плавает» на поверхности
сульфат меди. Очевидно, такая компоновка работает не очень хорошо.
в фонарике, но на стационарном работает нормально
приложения .Если у вас есть доступ к сульфату цинка и сульфату меди, вы можете попробовать
сделать свою собственную ячейку Даниэля.
Можно ли использовать кровь для питания
батареи?
Аккумуляторы
являются практически необходимыми устройствами, но представляют собой целый ряд
проблемы. Со временем у них могут возникнуть проблемы с удержанием заряда. Некоторые
перестать работать вообще. Другие перегреваются, протекают или даже взрываются.
Они также жесткие и иногда громоздкие. Тогда как насчет того, чтобы вместо
ваш стандартный AA или литий-ионный,
гибкий, невероятно тонкий аккумулятор, который может питаться кровью
или пот?
Похоже на
улучшение, правое
Группа
ученые из Политехнического института Ренсселера утверждают, что они создали
именно такой аккумулятор, в котором используются природные электролиты
в жидкостях организма.Результаты исследования, подробно изложенные в Авг.
13, 2007, выпуск Известий Национальной Академии
Науки, вызывают некоторый интерес как часть нового урожая
«биобатареи»
которые вытекают из телесных жидкостей или других органических соединений. (ИРЦ
команда утверждает, что их кровь могла протекать даже через слезы или мочу.)
Батареи нет
толщиной с бумагу; это по сути это
бумага. По крайней мере, 90 процентов батареи сделано из целлюлозы,
из которой состоит традиционная бумага и другие бумажные изделия [источник:
RPI]. Согласовано
углеродные нанотрубки
составляют остальные 10 процентов, придают бумаге ее проводящие свойства
а также сделать его черным. Нанотрубки запечатлены в самом
ткань бумаги, создавая так называемый нанокомпозит
бумага .
Один из авторов статьи сказал, что аккумулятор «выглядит, ощущается
и весит как бумага »[источник: RPI].
С помощью
нанотехнологии, малый размер батареи, гибкость и
восполнение источника электролита — то есть, пока вы едите —
сделать его идеальным для медицинских приложений.При использовании аккумулятора вдали
из человеческого тела, ученые пропитали бумагу ионным
жидкость
(соль в жидкой форме), которая обеспечивает электролиты.
Батарея
конструкция, похожая на бумагу, придает ей значительную гибкость. RPI
Исследовательская группа считает, что в будущем аккумулятор может быть
напечатанные на длинных листах, которые затем можно было разрезать на маленькие,
батареи нестандартной формы. В нанокомпозитной бумаге могут быть проделаны отверстия.
в нем или быть вырезанным в необычные формы и продолжать функционировать.Несколько
листы могут быть соединены вместе для питания медицинских имплантатов, таких как
кардиостимуляторы, искусственное сердце
или передовое протезирование. Аккумулятор легко поместится под кожу
не вызывая дискомфорта.
Поскольку ионный
используемая жидкость не замерзает и не испаряется, как вода, аккумулятор может
работать в широком диапазоне температур: от -100 градусов
По Фаренгейту до 300 градусов по Фаренгейту. Его термостойкость
и малый вес означают, что производители автомобилей и самолетов
— оба из них требуют легких и прочных материалов — могут появиться
звонит.
Исследователи
за батареей утверждают, что их устройство уникально, потому что оно может
действовать «как аккумулятор высокой энергии и как мощный
суперконденсатор »[источник: RPI].
Суперконденсаторы допускают большие и быстрые выбросы энергии, потенциально
расширение и без того широкого спектра приложений.
Аккумулятор, который считается
экологически чистый из-за отсутствия химикатов и высокого
содержание целлюлозы, было объявлено летом 2007 г., но может быть
лет, прежде чем он будет готов за долгое время сойти с производственных линий.
листы.Исследовательская группа RPI заявляет, что пока они
пытаясь повысить эффективность батареи и найти лучшее
способ производства.
Как работают батареи | dummies.com
- Программирование
- Электроника
- Как работают батареи
Часть электроники Для детей Для чайников Шпаргалка
Вы когда-нибудь смешивали уксус с пищевой содой, чтобы создать вулкан для проекта научной выставки? Пузырьки, которые вы видите, — это результат химической реакции.Эта реакция очень похожа на работу батарейки . Однако реакция происходит внутри батареи, скрытой от глаз отсеком для батареи. Эта реакция создает электрическую энергию, которую батарея подает в цепи.
Обычная батарея, например, AA или C, имеет корпус или контейнер. Внутри корпуса залита смесь катода и , состоящая из заземленного диоксида марганца и проводников, несущих естественный электрический заряд. Далее идет сепаратор .Эта бумага предохраняет катод от контакта с анодом, несущим отрицательный заряд. Анод и электролит (гидроксид калия) находятся внутри каждой батареи. Штырь, обычно сделанный из латуни, образует коллектор отрицательного тока и находится в центре корпуса батареи.
Каждая батарея имеет элемент, содержащий три компонента: два электрода и электролит между ними. Электролит представляет собой раствор гидроксида калия в воде.Электролит — это среда для движения ионов внутри элемента и переносит символический ток внутри батареи.
Положительная и отрицательная клеммы аккумулятора подключены к двум различным типам металлических пластин, известных как электроды , , которые погружены в химикаты внутри аккумулятора. Химические вещества вступают в реакцию с металлами, в результате чего избыточные электроны накапливаются на отрицательном электроде (металлическая пластина, подключенная к отрицательной клемме аккумулятора) и вызывая нехватку электронов на положительном электроде (металлическая пластина, подключенная к положительной клемме аккумулятора).
Батарейки для фонарей или меньшие по размеру, обычно маркированные A, AA, C или D, имеют выводы, встроенные в концы батарей. Вот почему батарейный отсек вашего фонарика имеет знаки + и -, что упрощает установку батарей в правильном направлении. У более крупных аккумуляторов, таких как автомобильные, есть клеммы, выходящие из аккумулятора. (Обычно они выглядят как большие винтовые вершины.)
Разница в количестве электронов между положительной и отрицательной клеммами создает силу, известную как напряжение . Эта сила хочет выровнять команды, так сказать, выталкивая лишние электроны от отрицательного электрода к положительному. Но химические вещества внутри батареи действуют как преграда и препятствуют перемещению электронов между электродами. Если существует альтернативный путь, который позволяет электронам свободно перемещаться от отрицательного электрода к положительному, сила (напряжение) будет успешно толкать электроны по этому пути.
Когда вы подключаете батарею к цепи, вы обеспечиваете альтернативный путь для электронов.Таким образом, избыточные электроны уходят из батареи через отрицательный вывод через цепь и обратно в батарею через положительный вывод. Этот поток электронов — это электрический ток, который передает энергию в вашу цепь.
Когда электроды соединяются через цепь, например, клеммы внутри фонарика или в вашем автомобиле, химические вещества в электролите начинают реагировать.
По мере того, как электроны проходят через цепь, химические вещества внутри батареи продолжают реагировать с металлами, избыточные электроны продолжают накапливаться на отрицательном электроде, а электроны продолжают течь, пытаясь уравновесить ситуацию — пока есть полный путь для текущий.Если вы держите батарею подключенной к цепи в течение длительного времени, в конечном итоге все химические вещества внутри батареи израсходуются, и батарея умирает (она больше не поставляет электрическую энергию).
Электролит окисляет цинк на аноде. Смесь диоксида марганца / углерода катода реагирует с окисленным цинком с образованием электричества. Взаимодействие между цинком и электролитом постепенно замедляет действие элемента и снижает его напряжение.
Коллектор представляет собой латунный штифт в середине ячейки, который проводит электричество во внешнюю цепь.
Обратите внимание, что два электрода в каждой батарее сделаны из двух разных материалов, оба из которых должны быть электрическими проводниками. Один из материалов отдает электроны, а другой их принимает, в результате чего ток течет.
Об авторе книги
Кэтлин Шейми — инженер-электрик и писатель в области высоких технологий с обширным инженерным и консультационным опытом в области медицинской электроники, обработки речи и телекоммуникаций.
.


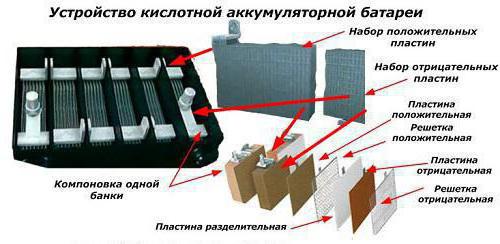



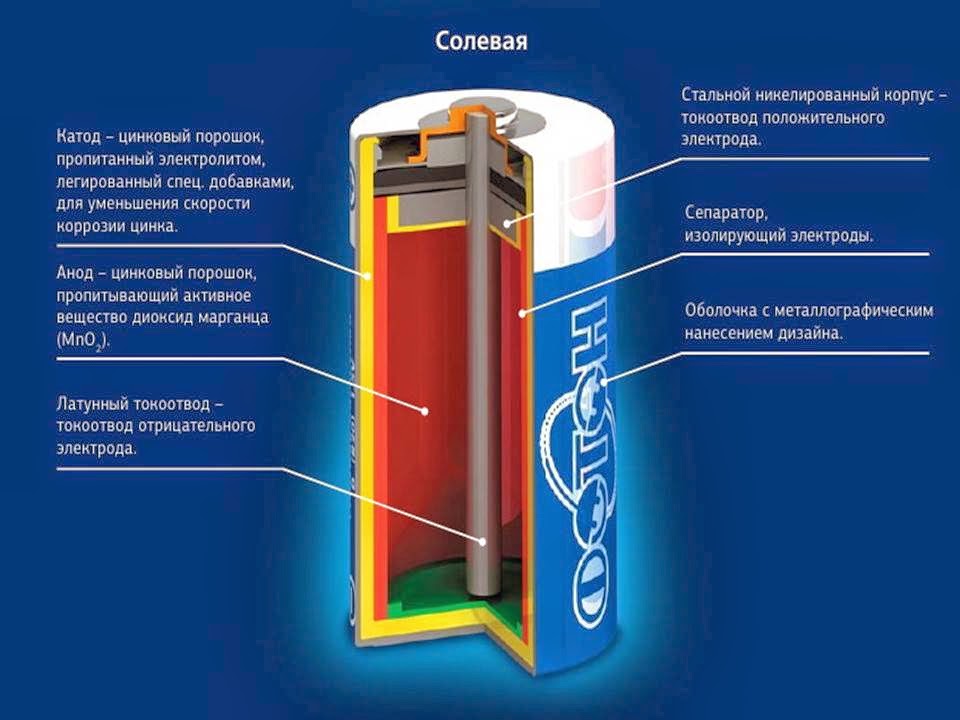
 Но принцип работы АКБ остаётся тем же.
Но принцип работы АКБ остаётся тем же. Можно смело утверждать, что современный образ жизни был бы невозможен без аккумуляторных батарей.
Можно смело утверждать, что современный образ жизни был бы невозможен без аккумуляторных батарей.